1. 서 론
기존 고온 세라믹의 한계를 극복하고, 2000 °C 이상의 초고온 환경에서 응용 가능한 재료로써 초고온 세라믹 스(ultra-high temperature ceramics, UHTCs)가 있다. 초 고온 세라믹스는 주기율표의 3족에서 5족에 해당하는 전 이 금속을 포함하는 붕화물, 질화물 또는 탄화물계 세 라믹스로 약 3000 °C 이상의 높은 녹는점을 갖는다.1,2) 이와 같은 특성으로 인해 초고온 세라믹스는 우수한 고 온 물성과 부품 경량화를 동시에 필요로 하는 항공 우주 분야에서 각광 받고 있다. 그 중에서도 tantalum carbide (TaC)는 가장 높은 녹는점(~3950 °C)을 갖고 있고 우수 한 열충격 저항성과 고온 침식에 대한 내성을 갖고 있 어서 UHTCs 분야에서 잠재적 가능성이 높다. 하지만 TaC는 일반적인 세라믹 재료와 마찬가지로 취성 파괴 거 동을 보이는 한계가 있다. 한편, 탄소섬유강화 복합재료 (carbon-carbon composite, C/C)는 고온에서 높은 강도와 파괴 인성을 갖고 있어서 가장 신뢰도가 높은 소재이나 내산화 거동이나 내마모 특성이 부족하여 이를 보완하 기 위하여 C/C에 TaC를 증착시키는 연구가 활발히 진 행되고 있다.3-6) 이 때, TaC 코팅은 C/C를 습한 산소를 포함하는 고온의 공기로부터의 산화를 억제할 뿐만 아 니라 초고속 입자로부터의 삭마를 억제하는 두 가지 효 과를 기대할 수 있다.
일반적인 TaC 코팅 방법 중 화학기상증착법(chemical vapor deposition, CVD)은 가장 치밀하고 균일하게 막을 형성할 수 있다는 점과 TaC의 합성과 복합체에서의 코 팅이 동시에 일어나기 때문에 간단한 공정으로 진행할 수 있어서 주목받고 있다. 그러나 CVD 법은 여러 실 험 변수들의 영향을 전체적으로 분석할 수 있는 열역학 분석이 필수적이고 반응기 내부의 유체 흐름에 따른 영 향이 크기 때문에 전산유체(computational fluid dynamics, CFD) 해석이 중요하다. 이를 통하여 반응기 내부의 기 상 및 고상 반응을 예상하고 치구의 모양이나 시편의 위 치를 정함으로써 더 균일한 코팅이 가능하다.7-9)
본 연구에서는 TaC 증착에 따른 열역학 해석을 상용 소프트웨어인 FactSage6.2를 통하여 수행하였다. TaCl5- C3H6-H2 계에서 TaC 코팅 층을 효율적으로 얻기 위하 여 온도, 압력 및 조성을 변수로 하여 얻어지는 증착상 인 C, TaC와 Ta2C의 상대적인 몰 비를 예측하였고 동 시에 가장 이상적인 TaC 상을 효과적으로 얻을 수 있 는 조건을 열역학적인 관점에서 추론하였고 이를 실험 적으로 확인하였다.
2. 실험 방법
2.1. 열역학 계산
열역학 평형 계산은 상용 소프트웨어인 FactSage 6.2 프로그램(thermofact/CRCT>T-thchnologies)을 사용하 였는데 여기서 m 화학종의 기상과 s 화학종의 고상이 혼재한 경우의 Gibbs 자유에너지는 다음과 같이 표현될 수 있다.(1)
위 식에서 은 가스 종들을 형성하는 자유에너지, 은 고체 종들을 형성하는 자유에너지, 는 기체 상 의 몰수, 은 고체 상의 몰수, 그리고 Ng 는 기체 종의 총 몰수이다. 위의 식을 이용하여 특정 압력, 온도, 조 성에서의 자유에너지 값을 계산함으로써 해당 조건에서 의 안정한 상과 그 양을 구하였으며, 같은 계산을 반복 적으로 수행함으로써 증착상에 대한 열역학 상태도를 도 출할 수 있었다.8) 계산에 사용된 총 54개의 화학종(45 개의 기상 종과 9개의 고상 종) 내에서 진행되었으며, 해 당 화학종을 Table 1에 정리하였다.
Table 1
Chemical species to calculate thermodynamic equilibrium including 45 gas species and 9 solid species.
열역학 계산 범위는 일반적으로 증착에 사용되는 조 건3-6,9-11)인 압력 10~500 Torr, 온도 1100~1400 °C로 진 행하였다. 증착된 고상의 농도를 기준으로 전체의 0.1 mol%가 되는 점을 경계로 하여 상평형도를 도시하였고 조성은 Ta와 C의 비율을 변수로 압력과 온도에 따른 증 착상의 영역을 표시하였다.
2.2. 증착 공정
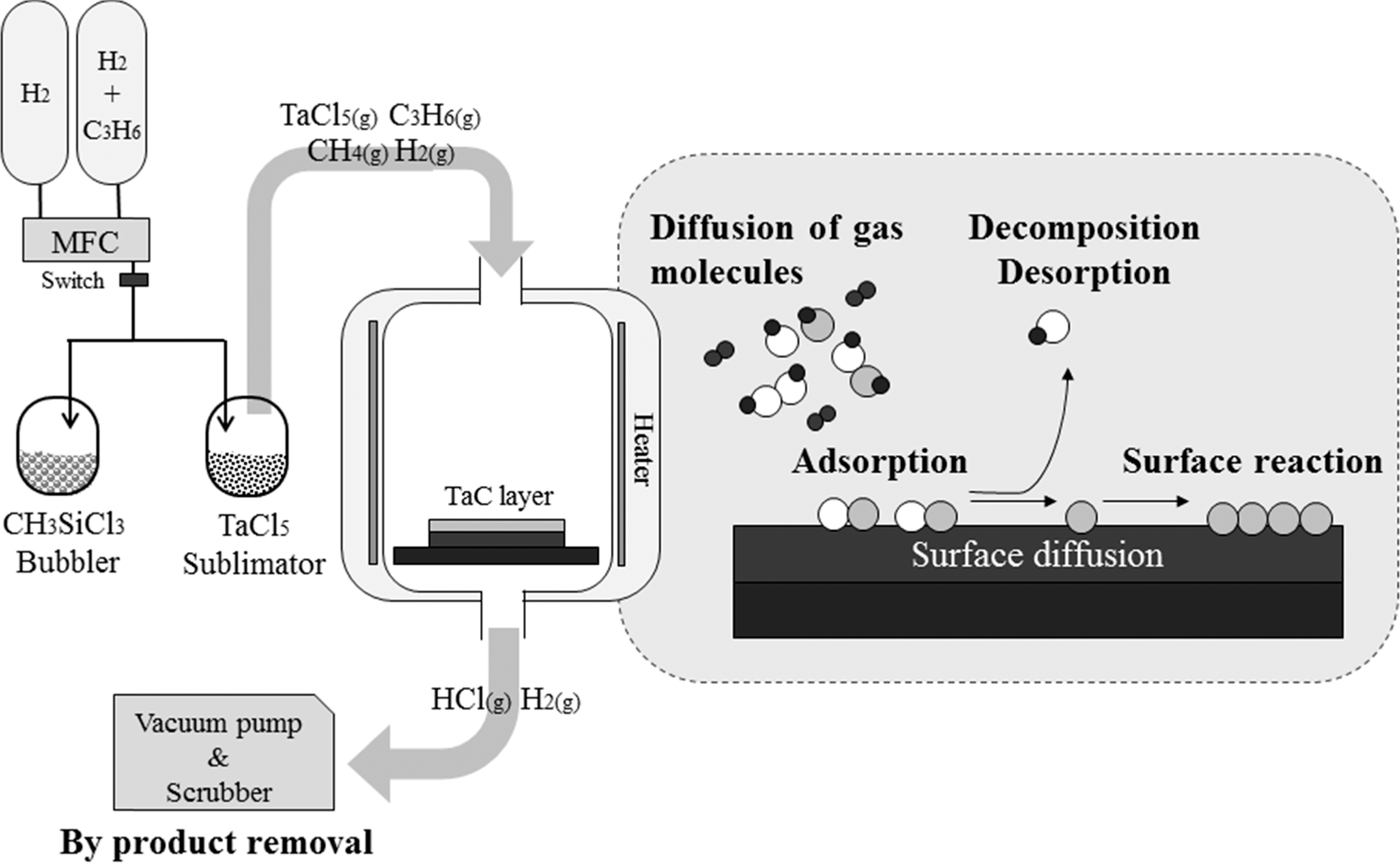
TaC의 증착 공정에 사용된 반응기는 수직형 반응기로 국내 제작(Thermvac Co., Ltd., Korea)되었으며 vertical type의 hot-wall CVD 반응기에 SiC를 증착할 수 있는 MTS(methyl-trichlorosilane, CH3SiCl3) 버블러와 고상의 TaCl5 분말을 승화시켜 TaC를 증착할 수 있는 기화기가 구비된 장치를 사용하였다. Fig. 1에 해당 장비의 모식 도를 나타내었다. 기판으로는 탄소섬유강화 탄소복합재(C/ C composite, Daeyang Industries Co., Ltd., Korea)를 사용하였는데 카본과 TaC 코팅층과의 열팽창 계수의 차 이가 커서 중간층인 탄화규소 층을 20에서 50 um 정도 형성한6,7) 후 TaC 공정을 진행하였다.
Ta의 원료인 TaCl5(H.C. Stark, GmbH, 99.5 %) 500 g 를 승화기에 넣고 약 185 °C의 온도로 가열한 후, H2와 C3H6가 9 : 1로 혼합된 가스를 캐리어 가스로 사용하여 증착 챔버 내로 공급되었다. 증착에 사용된 가스의 유 량은 mass flow meter를 통하여 500 sccm으로 고정하 였고 증착 완료 후 잔류된 TaCl5의 양을 확인하여 소모 량으로부터 Ta와 C의 비율을 확인하였다.
증착된 코팅 층의 상을 확인하기 위해서 X-ray diffraction( XRD, Rigaku D/MAX-2500PC)이 수행되었고, 추가적으로 코팅 층을 구성하고 있는 성분을 확인하기 위해 energy dispersive spectrometer(EDS, Oxford INCA penta FET X-3)을 사용하였다. 코팅 층의 외형은 FESEM( SEM, JEOL JSM-6701F)을 통하여 관찰하였다.
3. 결과 및 고찰
3.1. TaCl5-C3H6-H2 계와 TaCl5-CH4-H2 계에서 상 평형도
TaCl5-C3H6-H2 계에서 조성은 3종의 가스 농도에 의 해 결정되는데, H2와 C3H6가 9 : 1로 혼합된 가스를 캐 리어 가스로 TaCl5를 승화시키면 H/C 비는 8로 고정되 고, TaCl5의 양은 승화기의 온도를 조절함으로써 변화될 수 있다. 이 때 일어나는 화학 반응은 다음과 같다.(2)
이와 같은 화학 반응을 고려하여 온도, 압력 변화에 따 른 해당 계에서의 열역학 상태도를 Fig. 2에 나타내었 다. 증착온도를 1100 °C에서 1400 °C까지 100 °C 간격으 로 도시하면 나타나는 고상은 TaC, Ta2C와 C 상이며 두 상의 공존 영역까지 총 4개의 영역을 확인할 수 있다. 온도가 상승할수록 빨간색 선으로 표현 된 TaC와 Ta2C 의 공존 영역이 넓어지는 것을 확인할 수 있고 압력의 경우에는 압력이 높아질수록 TaC 단일 상 영역이 넓어 진다. 한편, Ta/C의 경우에는 Ta/C가 1에 가까울수록 TaC의 양이 많아지며 단일 상을 얻을 확률이 높아짐을 확인할 수 있다. 따라서 TaCl5-C3H6-H2 계에서 TaC 단 일상을 증착하기 위해서는 1100 °C 나 1200 °C 정도의 공정 온도에서 100 torr 이상의 압력으로 Ta/C의 양을 1에 가깝게 유지하는 것이 TaC를 증착하는데 더 효과 적인 조건임을 알 수 있다.
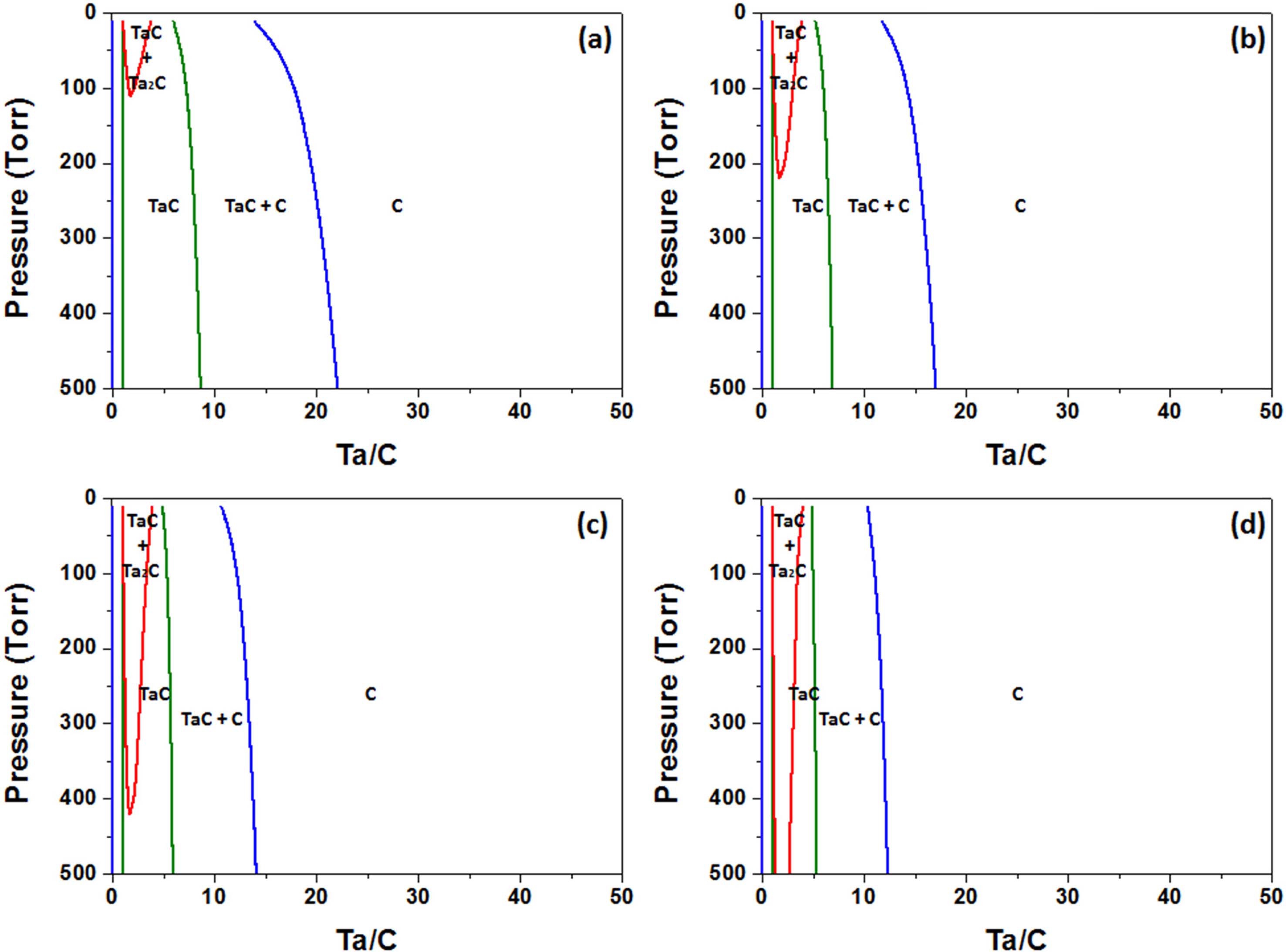
Fig. 2
Isothermal sections at (a) 1100 °C, (b) 1200 °C, (c) 1300 °C and (d) 1400 °C of phase diagram of TaCl5-C3H6-H2 system where H/C = 8.
마찬가지로 TaCl5-CH4-H2 계에서도 조성은 3종의 가 스 농도에 의해 결정되는데, H/C 비는 42로 고정하고, TaCl5의 양을 변화시키면서 열역학 계산을 진행하였다. 이 때 일어나는 화학 반응은 다음과 같이 묘사될 수 있다.(3)
이와 같은 화학 반응을 고려하여 각각 1100 °C에서 1400 °C까지 100 °C 간격으로 상태도를 나타내면 Fig. 3 과 같다. 생성되는 고상은 TaC, Ta2C와 C 뿐만 아니라 Ta 상까지 생성되어 4 종류의 고상이 생성되고 두 상의 공존 영역까지 총 6 개의 영역으로 나뉘어지는 것을 확 인할 수 있다. H/C가 커지면서 Ta 금속이 석출되는 영 역이 존재하며 Ta/C가 1에서 5까지 변화하는 동안 여러 가지 석출 상의 변화가 나타난다. 특히, 저온에서는 Ta 석출 영역이 저압으로 한정되지만 1300 °C 이상에서는 전 압력에 걸쳐서 Ta가 Ta2C와 공존하는 영역이 나타나게 된다. 반면에 TaC 단일 상은 1100 °C에서 가장 넓은 석 출 영역을 보여주며 온도가 상승할수록 그 영역이 좁아 지는 것을 확인할 수 있다. 그러나 1100 °C의 경우에도 Ta/C가 40을 넘어서야만 단일 상을 얻을 수 있고 이것 은 값비싼 원료인 TaCl5의 상당 량이 증착되지 못하고 소모되는 것을 의미하므로 현실적으로 바람직한 조건이 라고 볼 수 없다.
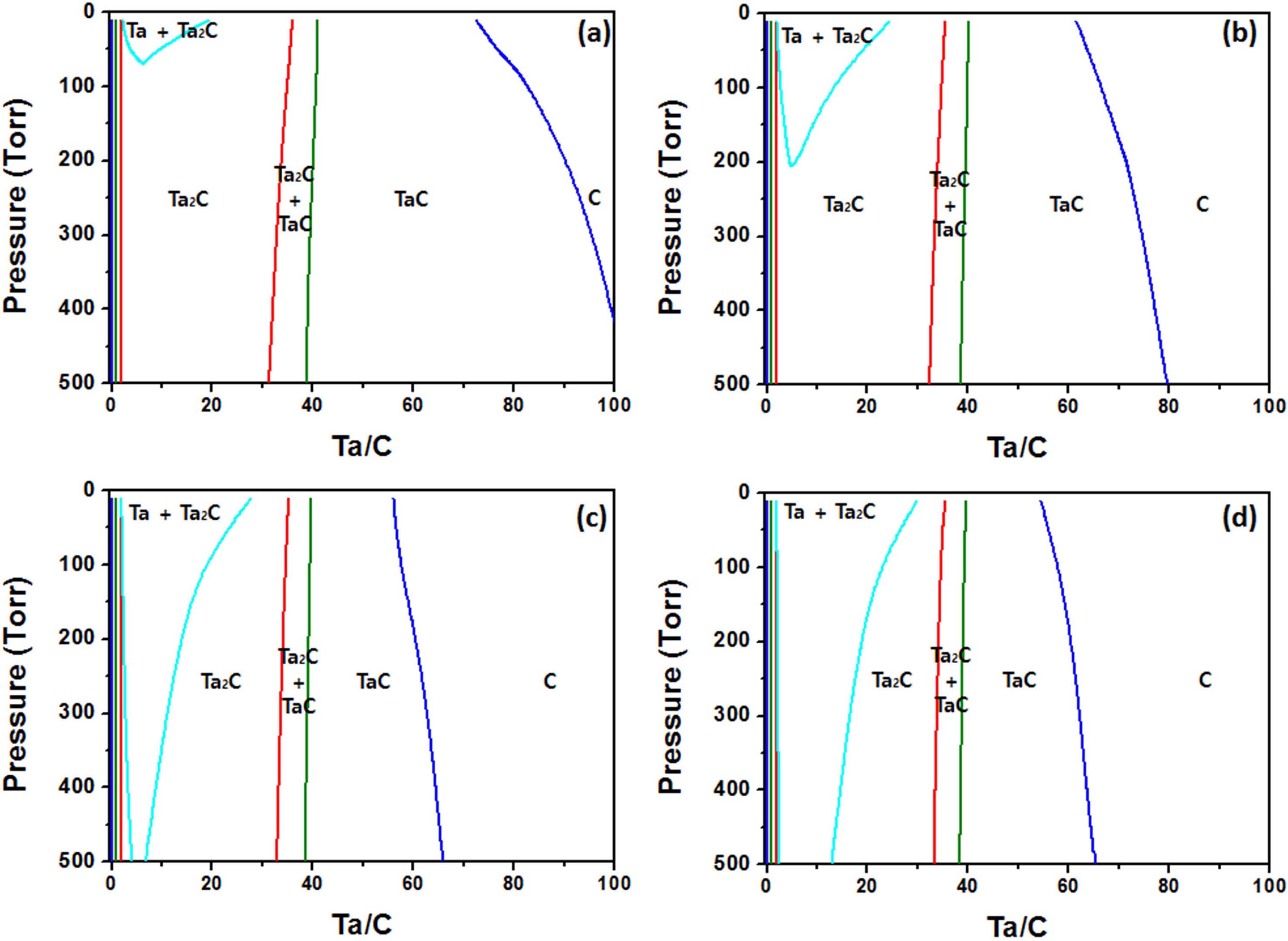
Fig. 3
Isothermal sections at (a) 1100 °C, (b) 1200 °C, (c) 1300 °C and (d) 1400 °C of phase diagram of TaCl5-CH4-H2 system where H/C = 42.
반응기 내부의 hot zone 형성과 온도 구배를 고려하 여 두 계를 1200 °C에서 비교하였다. 1200 °C에서 계산된 Fig. 2(b)와 Fig. 3(b)의 두 상태도를 비교해보면, Fig. 2(b)가 더 낮은 Ta/C 구간에서 TaC 상을 형성하는 것을 확인할 수 있다. 이를 통해 더 적은 TaCl5의 공급으로 TaC 상을 형성할 수 있음을 예측할 수 있다. 또한 Fig. 2(b)는 4 개의 영역(C, TaC+C, TaC, TaC+Ta2C)으로 증 착 구간이 나뉘어 지지만 Fig. 3(b)의 경우는 총 6 개의 영역(C, TaC+C, TaC, TaC+Ta2C, Ta2C, Ta+Ta2C)으로 나뉜다. 이를 고려하면 C3H6와 H2의 혼합가스를 이용하 여 TaCl5를 승화시키는 방법이 단일 상 형성에 더 효과 적임을 확인할 수 있고 이 연구에서는 TaCl5-C3H6-H2 계 에서 공정을 진행하였다.
3.2. 수소의 영향
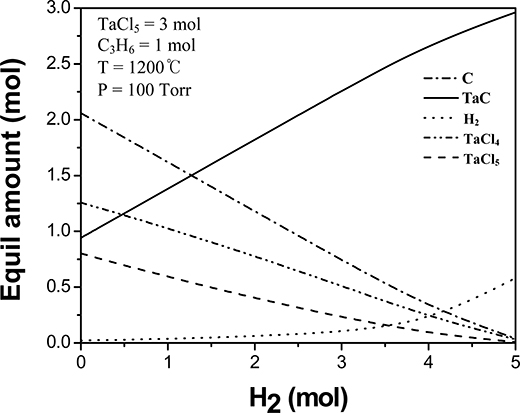
수소 가스는 단순히 운반 가스가 아니라 실질적으로 TaCl5와 화학적으로 반응하여 Ta를 공급하는 중요한 요 소이다. 따라서 수소 가스의 농도에 따라 화학 반응에 어떠한 영향을 주는지를 Factsage 프로그램을 통해 계산 하여 Fig. 4에 도시하였다. TaCl5와 C3H6를 각각 3 몰과 1 몰씩을 넣고(Ta/C = 1), 1200 °C, 100 Torr에서 공급하 는 수소 가스의 양을 늘리면서 계산한 결과이다. C와 TaC는 고체로 석출되고, H2, TaCl4, TaCl5는 가스 상으 로 존재한다. 수소 가스의 몰수가 0일 때를 보면, 수소 가 없이 소량의 TaC가 형성되는 것을 확인할 수 있다. 그러나 TaCl4와 TaCl5는 기상으로 존재하고 대부분의 C 는 탄소로 석출되므로 수소의 양을 늘림으로써 TaC의 석 출량을 증가시킬 수 있다. 즉, 5 몰 이상의 수소를 공급 함으로써 TaC의 석출량을 100%에 가깝게 만들 수 있다.
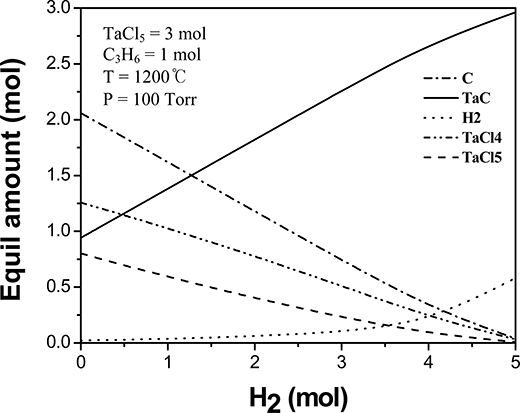
Fig. 4
Effect of hydrogen addition on TaC formation where 3 moles of TaCl5 and 1 mole of C3H6 exist in a closed system.
한편, TaCl5가 3 몰이 들어있는 닫힌 계에 1 몰의 수 소와 프로필렌 혼합가스가 존재할 때, 수소와 프로필렌 의 비가 TaC의 석출량에 미치는 영향을 Fig. 5에 도시 하였다. C는 C3H6의 분해과정에서 생성되며, TaC를 형 성하기 위한 C3H6와 H2의 적정 비율을 전산 열역학 계 산을 통해 예측하였다. H2와 C3H6의 비율을 변화시키면 서 석출되는 상의 변화를 보면, 수소가 100 % 일 때에 는 석출되는 상이 형성되지 않았기 때문에 0~95 % 까 지 범위에서 계산을 수행하였다. H2의 몰분율이 약 88 % 이상 일 때, TaC가 더 우세하게 석출되는 것을 확인할 수 있다. 이로 부터 H2와 C3H6 간의 혼합가스의 몰비는 9 : 1로 정하였다.
3.3. TaC의 증착
열역학 계산 결과를 기반으로 1200 °C, 100 Torr에서 H2와 C3H6가 9 : 1로 혼합된 가스를 2 시간 동안 흘리 면서 TaC를 증착하였다. 증착 후 TaCl5의 소모량으로부 터 계산된 Ta/C는 0.5이었다. XRD를 사용하여 디스크 시 편 위에 증착된 결정상의 회절 패턴을 Fig. 6에 나타내 었다. XRD 피크들은 JCPDS 카드의 No. 00-035-0801의 TaC 상과 No. 03-065-0360의 SiC 상에 잘 부합하고 있 음을 확인할 수 있었고, 미반응의 C 또는 Ta2C, Ta와 같은 고체 상들은 관찰되지 않았다.
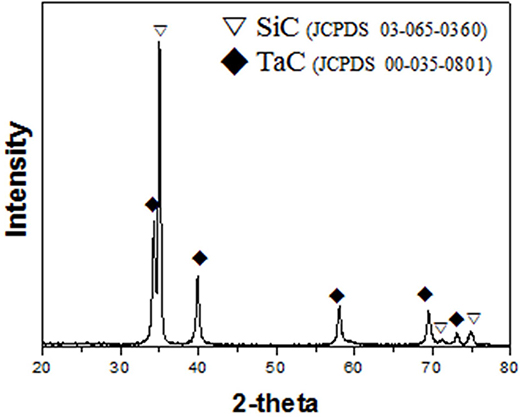
Fig. 6
XRD pattern of the film deposited at 1200 °C, 100 Torr with TaCl5-saturated mixed gas(H2: C3H6= 9 : 1).
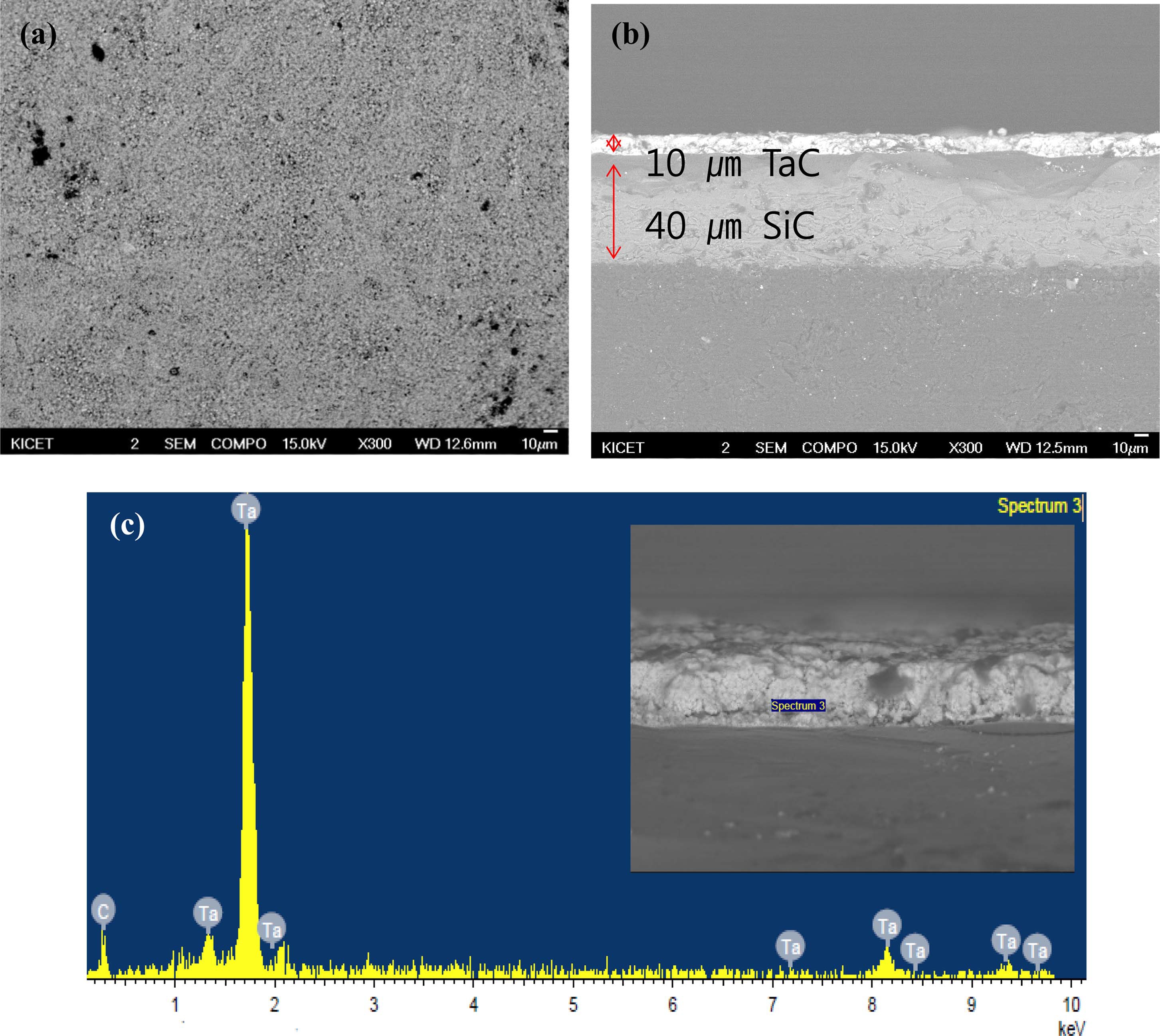
증착된 시편의 표면과 TaC 층과 SiC 층의 두께를 확 인하기 위하여 FE-SEM으로 표면과 단면을 각각 Fig. 7 에 나타내었다. Fig. 7(a)에서 TaC가 C/C 표면에 전체 적으로 고르게 증착된 것을 확인할 수 있다. Fig. 7(b) 의 단면 사진에서 TaC는 10 μm, SiC는 40 μm의 두께 로 증착되었음을 확인할 수 있다. 또한 코팅 층의 구성 원소를 Fig. 7(c)로부터 확인할 수 있듯이 Ta와 C로 구 성되어 있다. 이로부터 열역학 분석으로 예측하였듯이 CVD를 통하여 성공적으로 TaC 층을 형성할 수 있음을 확인하였다.