1.서 론
천이금속 질화물인 CrN는 경도가 높고 열적 안정성이 우수하며, 높은 내식성과 내마모성을 가지고 있어 기계 부품의 부식과 마모를 방지하기 위한 보호막으로 적용 되고 있다.1,2) 또한 CrN는 GaN와 격자정합을 이루므로 광전소자의 제작에 이용되었고,3) 훌륭한 전기적 성질을 가지고 있어 Li 전지의 전극으로 사용되었다.4) 최근에는 CrN 박막을 고온 태양 에너지 흡수체, 슈퍼 커패시터, 연료전지용 맴브레인 등에 적용하기 위한 연구가 이루어 졌다.5-7)
일반적으로 CrN 박막은 반응성 RF 스퍼터링 또는 DC 스퍼터링 방법으로 제작되고 있다.4-10) 스퍼터링 방법으 로 제작되는 CrN 박막은 플라즈마 가스 중 N2의 분압 에 따라 Cr (N), Cr2N, Cr2N/CrN 및 CrN과 같이 다양 한 상이 관찰되었다.2) 이와 같은 CrN 박막 성분의 불 균질성은 기계적, 전기적, 광학적 성질에 영향을 가져와 소재의 응용을 제약하게 된다. 한편 단일상의 CrN 박막 을 얻기 위해 스퍼터링된 Cr 박막을 NH3 및 N2 분위 기에서의 질화 반응이 적용되었다. 그러나 질화 반응으 로 제작된 CrN 박막에서도 다양한 상의 형성이 보고되 었다.8) 또한 Cr 박막을 NH3 분위기에서 질화 반응시켰 을 때 CrN와 Cr2O3가 함께 형성되며,9) 그 원인으로 스 퍼터링 중 O2의 오염에 의한 영향이 보고되었다.10)
이 연구에서는 DC 스퍼터링 방법으로 O가 첨가된 Cr 박막을 사파이어 기판위에 증착하고 NH3 분위기에서 질 화 반응시켜 CrN 박막을 제작하였다. 질화 반응 조건이 CrN 박막의 구조적 특성에 미치는 영향을 X선 회절(Xray diffraction, XRD)과 X선 광전자분광(X-ray photoelectron spectroscopy, XPS)법으로 분석하여 조사하였다.
2. 실험방법
DC 스퍼터링 방법으로 사파이어(α-Al2O3) 기판 위에 O 가 첨가된 Cr 박막을 성장시켰다. 이를 위해 c-면의 사 파이어 기판을 에탄올과 아세톤으로 각각 5분 동안 초 음파 세척하고 건조시켜 스퍼터링 장치(DaON-1000D, VTS)의 기판 지지대에 부착하였다. 지름이 6 인치인 Cr 타겟(99.99 %, LTS Inc.)을 기판에 대해 30°로 기울여 20 cm 아래쪽에 설치하였다. 진공 챔버의 진공도가 3.0 × 10-6 Torr에 도달하면 Ar (99.999 %)을 30 sccm으로 주 입하고, 자동 밸브를 작동시켜 5.0 × 10-3 Torr의 진공을 유지하면서 O2를 3 sccm 첨가하였다. 스퍼터링 동안 DC 출력은 300W를 유지하였고, 기판을 200°C로 가열하면 서 5 rpm으로 회전시켰다. Cr 박막의 증착 속도는 0.6 μm/h이었고, 2시간 동안 1.2 μm 두께로 증착시켰다.
증착된 Cr 박막을 석영판에 얹어 수평형 3단 전기로 에 위치시키고 진공 배기한 후, 고순도 N2 (99.999 %) 가 스를 1000 sccm으로 주입하면서 10°C/min으로 승온시켰 다. 설정 온도에 도달하면 운송 가스인 N2 1000 sccm과 고순도 NH3 (99.999 %) 가스 300 sccm을 함께 주입하 면서 질화 반응시켰다. 질화 반응 온도와 시간은 각각 300~900°C와 10~240분 범위에서 변화시켰다. 질화 반응 이 종료되면 전기로의 전원을 차단하고 300°C까지 NH3 를 주입하였고, 이후에는 N2를 주입하면서 상온까지 냉 각시켰다.
박막의 결정 구조는 Cu 타겟을 사용하는 XRD 장치 (Rigaku D/MAX 2500U)로 분석하였다. X-선관의 가속 전압과 전류는 각각 40 kV와 100 mA로 일정하게 하고, 분당 4°씩 0.02°의 step으로 측정하였다. 박막의 구성 성 분은 XPS장치(ULVAC, PHI 5000)로 분석하였다. Al-kα (1486.6 eV) 선을 15 kV로 가속시켜 시료 표면에 100μm 크기로 조사하였다. 반원구형 분석기를 이용하여 얻어진 스펙트럼으로 구성 원소의 조성과 화학적 결합상태를 확 인하였다. 이를 위해 시료 표면에서의 survey scan 스펙 트럼과 Cr2p, O1s, 및 N1s에 대해 narrow scan 스펙트 럼을 측정하였다. 또한, 깊이 방향으로 Ar 이온 스퍼터 에칭하면서 Cr2p, O1s, 및 N1s 및 A l 2s에 대한 narrow scan 스펙트럼을 순차적으로 측정하여 구성 원소의 depth profile을 얻었다.
3. 결과 및 고찰
Fig. 1은 DC 스퍼터링 방법으로 제조한 (a) as-deposit Cr 박막과 NH3 분위기에서 1시간 동안 (b) 500°C, (c) 600°C, 및 (d) 900°C에서 질화 처리된 박막의 XRD 패 턴을 나타낸 것이다. 각 회절선의 위치를 비교하기 위 해 회절 강도를 자연대수 값으로 나타냈다. 모든 시료 에서 사파이어 기판의 (006) 회절이 41.59°에서 나타났 다(JCPDS #46-1212). Fig. 1의 회절선에 대해 JCPDS 카드의 bcc Cr (■; #85-1336), rhombohedral Cr2O3 (◆; 38-1479), hexagonal Cr2N (▲; #35-0803), fcc CrN (●; #76-2494)를 참조하여 표시하였다. 우선 as-deposit 시료 에서는 Cr의 (110) 회절이 검출되었다. 500°C에서는 Cr (110) 회절과 함께 CrN의 (111)과 Cr2N의 (002) 회절이 나타났다. 600°C에서는 CrN의 (111), Cr2N의 (002)와 (111) 및 Cr2O3의 (110) 회절이 나타났다. 900°C에서는 Cr2O3 (110) 회절 강도가 감소하고 CrN의 (111)과 (200) 회절 이 주되게 나타났다. 이때 CrN의 격자상수는 0.4145 nm 로서 JCPDS (#76-2494)의 a0=0.414 nm와 잘 일치했다. 이로부터 O가 첨가된 Cr 박막은 NH3 분위기에서의 질 화 반응으로 500°C에서 CrN와 Cr2N가 형성되고 600°C 의 온도에서 Cr2O3를 형성한 후 900°C 이상의 온도에 서 CrN로 전환되는 것을 알 수 있었다.
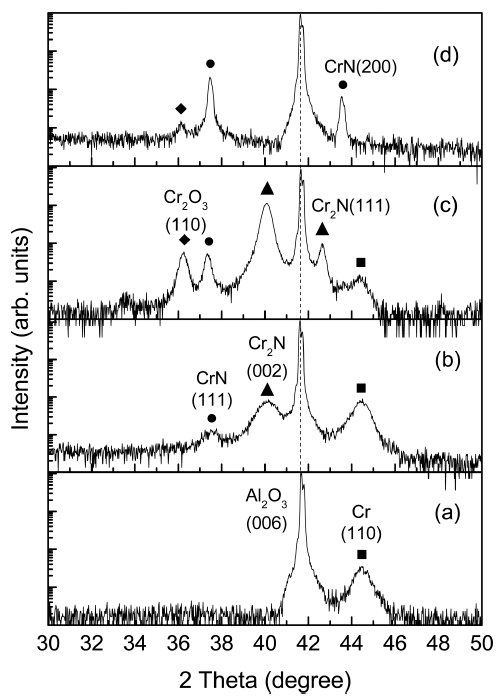
Fig. 1
XRD patterns for Cr films, (a) as-deposited and nitrided at (b) 500°C, (c) 600°C and (d) 900°C.
Fig. 2는 Fig. 1의 시료들에 대한 XPS survey 스펙트 럼을 나타낸 것이다. XPS 스펙트럼은 N, O 및 Cr과 관 련된 피크들로 이루어졌다. Fig. 1 (a)에 보인 as-deposit Cr의 경우 결합 에너지 530.8 eV 부근에서 O1s 피크가 관찰되었다. 한편, 질화 온도가 증가함에 따라 396.8 eV 부근의 N1s 피크 강도가 증가하고 O1s 피크 강도는 감 소하였다. 이것은 Fig. 1의 XRD 패턴에서 질화 온도에 따라 CrN (111)의 강도가 증가하고 Cr2O3 (110)의 강도 가 감소한 것과 같은 경향이다.
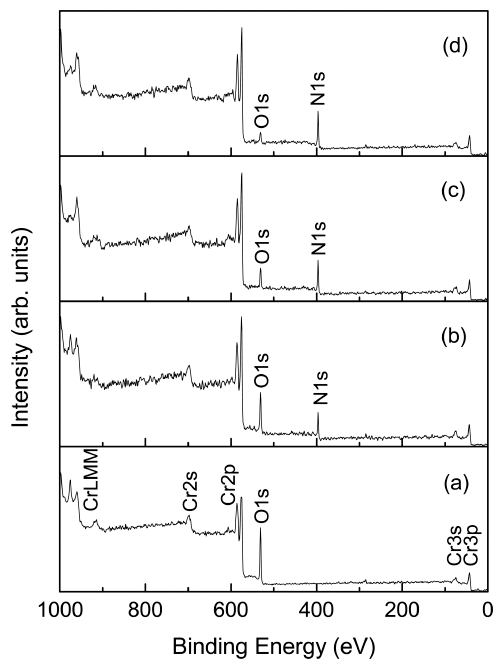
Fig. 2
XPS survey spectra for Cr films, (a) as-deposited and nitrided at (b) 500°C, (c) 600°C and (d) 900°C.
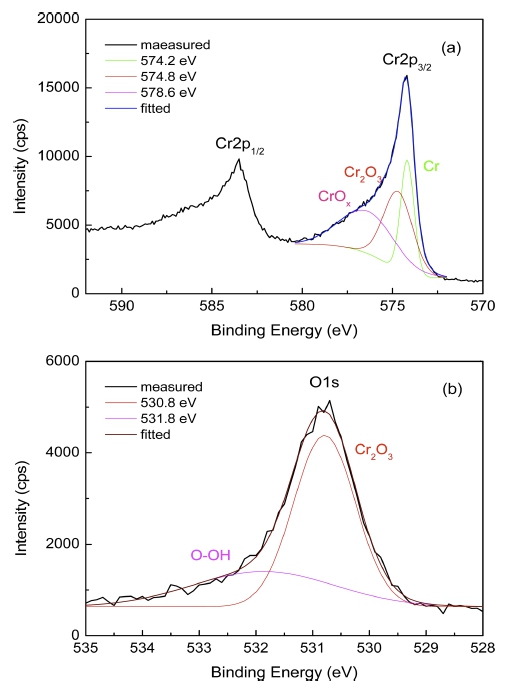
Fig. 3은 as-deposit Cr 박막 표면에서 측정된 (a) Cr2p와 (b) O1s에 대한 XPS narrow scan 스펙트럼이다. 우선 Fig. 3(a)에서 as-deposit Cr 박막의 Cr2p 피크는 spin-orbit splitting에 의해 Cr2p1/2 (583.5 eV)와 Cr2p3/2 (574.2 eV) 피크로 분리되었으며, 그 간격이 9.3 eV로서 문헌에 주어진 값 9.4 eV와 잘 일치했다.11) Cr2p3/2 피크 는 결합 에너지의 최대값이 각각 574.2 eV, 574.8 eV 및 576.8 eV인 세 개의 피크로 분해되었다. 574.2 eV와 576.8 eV에서의 피크는 금속 Cr과 Cr2O3 결합에 해당한다.12) 한편, 금속 Cr으로부터 +0.6 eV 위치에서의 피크는 Cr 의 산화물로서 CrO2 또는 CrOx (x<1.5) 결합에 의한 것 이다.13,14) O1s는 최대값이 각각 530.8 eV와 532.8 eV인 두 개의 피크로 분해되었다. 이들은 각각 Cr2O3와 O- (OH)에 해당한다.13) as-deposit 박막의 Cr과 O의 농도는 각각 78%와 22 %이었다.
Fig. 4는 (a) as-deposit 박막과 (b) 500°C, (c) 600°C 및 (d) 900°C에서 1시간 동안 질화 처리된 박막의 XPS depth profile을 나타낸 것이다. 표면과 기판 경계 부근 을 제외하고 박막 두께 전체적으로 Cr과 O의 농도가 각 각 77 %와 23 %로 균일하게 유지되었다. 500°C에서 질 화 처리된 시료 표면에서 N의 농도가 30 %이었고, 400 nm 두께까지 O의 농도보다 높았으며, 기판과의 경계까 지 서서히 감소하였다. 600°C에서 처리된 시료는 표면 으로부터 90 nm까지 O가 N으로 치환된 CrN 층이 형 성되었다. 이 영역에서 Cr과 N의 농도비는 3:2이었다. 약 180 nm부터 기판까지는 Cr:O:N의 비가 3:1:1을 유지하 였다. 또한 질화 온도 900°C에서는 CrN 층의 두께가 640 nm이었고, 시료 전체에 걸쳐 N의 농도가 O의 농도 보다 높았다.
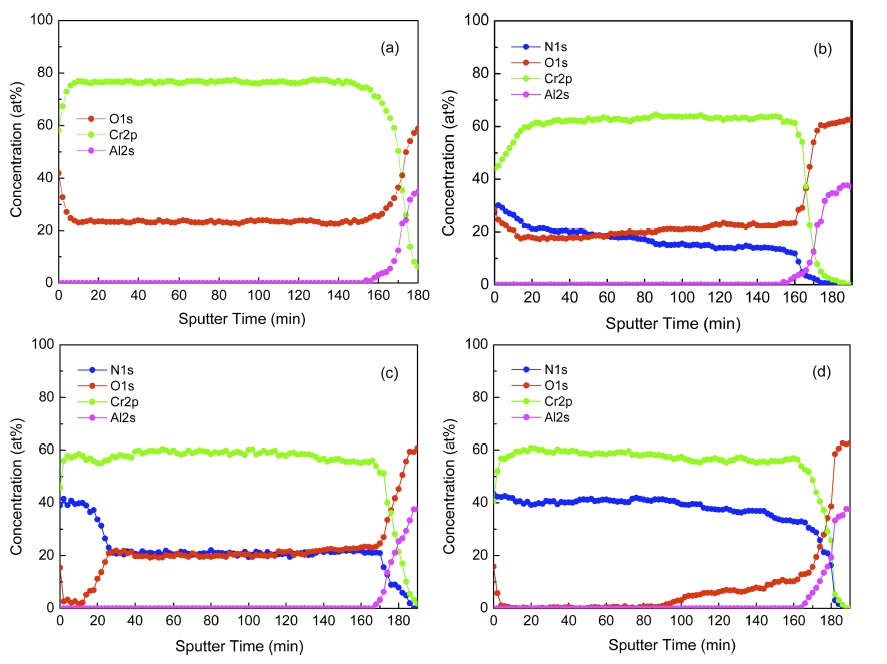
Fig. 4
Sputter depth profile of Cr films, (a) as-deposited and nitrided at (b) 500°C, (c) 600°C and (d) 900°C.
Fig. 5는 800°C에서 질화 시간이 서로 다른 시료의 depth profile을 나타낸 것이다. O가 N으로 치환된 CrN 층의 두께는 질화 시간이 10분일 때 343 nm에서 240분 일 때 510 nm로 증가하였다. CrN 층에서 Cr과 N의 농 도는 각각 60%와 40 %를 유지하였고, 기판과의 경계까 지 N의 농도는 감소하고 O의 농도는 증가하였다. 한편, 표면으로부터 약 1,000 nm 위치에서의 Cr, N, O의 농도 비는 5:3:2 정도이었다. 이와 같이 NH3 분위기에서의 질 화 반응으로 Cr 박막은 O가 N으로 치환된 영역에서는 CrN과 Cr2N 등의 질화물이 분포하고, 그 아래 영역에 는 CrxNyOz 화합물이 분포하게 될 것으로 추정된다.12)
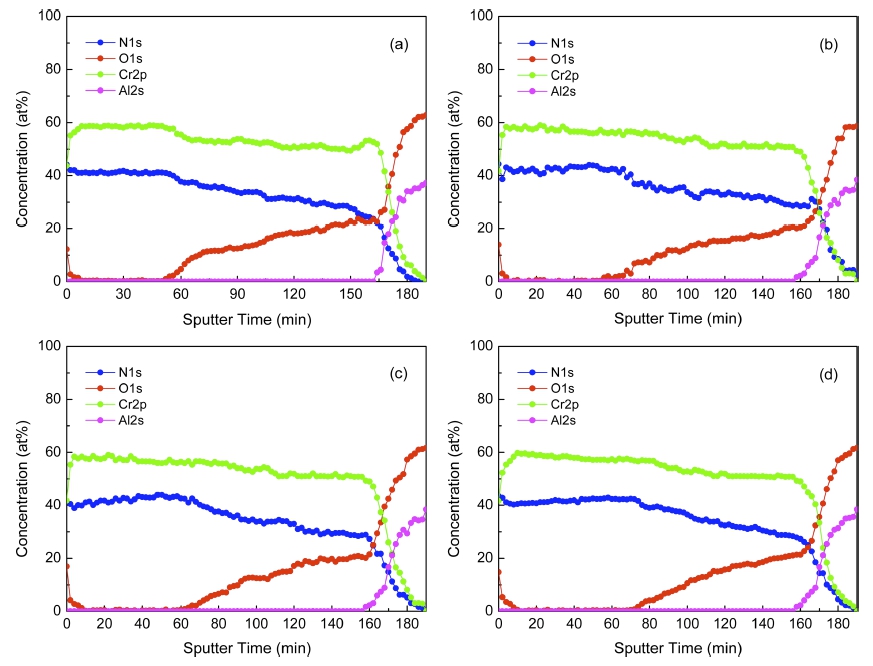
Fig. 5
Sputter depth profile of Cr films nitrided at 800°C for (a) 10 min, (b) 30 min, (c) 60 min and (d) 240 min.
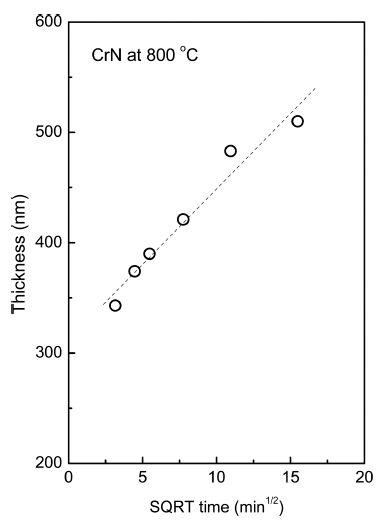
Fig. 6은 800°C에서 형성된 CrN 층의 두께(x)를 시간 (t)의 제곱근에 대해 나타낸 것이다. 질화 반응 초기 단 계 이후에 CrN 층의 두께는 질화 시간의 제곱근에 비 례하였다. 이것은 Deal과 Grove의 모델15) 즉, SiO2 열 산화막 성장 초기에 반응 제어에 의해 빠르게 성장하는 단계와 O가 산화막을 가로질러 확산 이동하는 속도 제 어에 의해 포물선 관계를 보이는 단계로 이루어지는 것 과 잘 비교된다. 즉, 확산에 의한 성장 속도의 제어 단 계에서 산화층의 두께는 시간의 제곱근에 비례한다. 이 러한 모델이 TiN의 산화 반응과16), GaOOH의 질화 반 응을 해석하는데 적용되었다.17)
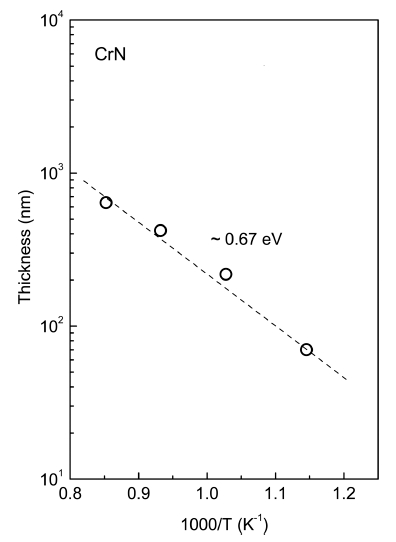
Fig. 7은 800°C에서의 질화 반응으로 형성된 CrN 층 의 두께를 온도에 대해 Arrhenius plot한 것이다. 물질 의 생성 량과 직접적으로 관계하는 CrN 층의 두께는 온 도에 대해 지수함수적으로 증가하였다. ln(x) = -(EA/kB) (1/T) 관계의 기울기로부터 CrN 생성에 필요한 활성화 에너지 EA를 구할 수 있으며, 그 값은 0.69 eV이었다.
Fig. 8은 Fig. 1의 XRD 패턴에서 CrN (111)과 Cr2 O3 (110)의 회절 강도 비와 Fig. 2의 XPS 스펙트럼에서 N1s 와 O1s 피크 강도 비, 즉 산화물에 대한 질화물의 생 성 비(IN/IO)를 온도에 대해 Arrhenius plot한 것이다. Cr2O3 가 생성되기 전인 600°C보다 낮은 온도 영역에서는 XPS 의 IN/IO가, 600°C 이상의 온도 영역에서는 XRD의 IN/IO 가 서로 같은 기울기를 보였다. 그림의 기울기로부터 구 해진 활성화 에너지는 0.69 eV로서, Fig. 7에서 구한 활 성화 에너지와 같았다.
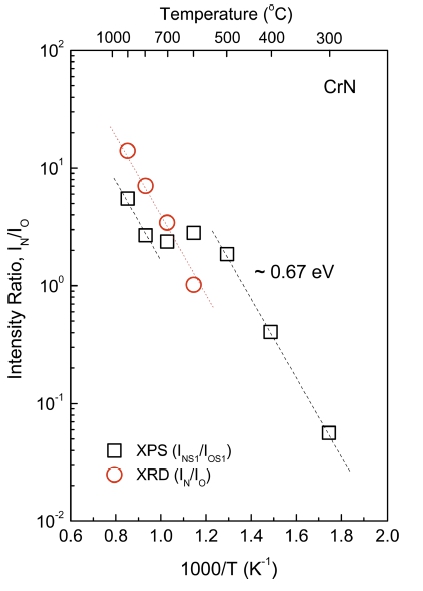
Fig. 8
Temperature dependence of intensity ratios for nitrides to oxides from XRD (IN/IO) and XPS (IN1s/IO1s).
온도에 따른 두께 증가는 물질 생성량과 관계하며, XRD 패턴에서 회절 강도와 XPS 스펙트럼 발광 강도 는 해당하는 물질의 량에 직접적으로 비례한다.18,19) 따 라서 Fig. 7과 Fig. 8에서의 활성화 에너지는 Cr 내에 존재하는 O를 N으로 치환하고 CrN를 생성하는데 필요 한 것이다. CrN의 생성열은 1.22 eV이고,2) CrN에서 N 의 자기 확산에 필요한 활성화 에너지는 2.8 eV로 보고 되었다.1) Buijinsters 등9)은 NH3 분위기에서 Cr의 질화 반응에 있어 Cr2N과 Cr 내에서 N의 확산 속도가 CrN 생성에 영향을 미친다고 하였다. Mayr 등20)은 Cr2N과 Cr 내에서 N의 확산에 필요한 활성화 에너지가 각각 2.68 eV와 2.79 eV로 보고하였다. 따라서 이 연구에서 실 험적으로 구해진 CrN의 생성에 필요한 활성화 에너지가 선행 연구와 커다란 차이가 있음을 알 수 있다. 이것은 CrN의 생성과정이 서로 다르기 때문이라 여겨진다. Jimenez 등16)은 Ti와 TiN의 플라즈마 산화에 필요한 활성화 에 너지가 TiN의 열산화에 필요한 활성화 에너지 2 eV 보 다 적은 0.7 eV임을 보고하였다. 이것은 TiO2를 통한 O 의 확산 속도제어 단계에서는 N의 out-diffusion이 Ti의 산화를 제한하지 않기 때문이다. 즉, O-N 교환에 있어 상호작용이 존재하지 않기 때문에 확산이 보다 용이하 게 이루어지므로 활성화 에너지가 작은 값을 갖는다. 그 러나 Russell 등8)에 의하면 NH3 분위기에서 Cr 박막의 급속 질화에 있어 Cr2N과 CrN 형성이 낮은 온도에서는 Cr의 확산에 의해 이루어지고, 높은 온도에서는 N의 확 산이 지배적으로 작용하여 높은 활성화 에너지를 필요 로 하게 된다. 특히, CrN 내에 O가 높은 농도로 분포 하는 것은 O의 확산 속도가 CrN의 성장 속도보다 느 리기 때문이며, 850°C 이상의 온도에서 O가 충분한 이 동성과 용해도를 갖추어 CrN 내에서 균질하게 분포하게 된다. 따라서 본 연구에서 CrN 생성에 필요한 활성화 에 너지가 작은 값을 보인 것은 TiN의 산화에 대한 Jimenez 등16)의 해석과 같이 CrN 층의 형성이 N과 O의 동시 확 산으로 이루어지기 때문이라 여겨진다. 즉, Cr 박막 내 에 첨가된 O의 out-diffusion과 N의 in-diffusion이 동시 에 진행되는 상호 확산 과정으로 CrN가 형성되기 때문 에 활성화 에너지가 작은 값을 갖는다. 그러나 이와 같 은 추정은 N 또는 O 원자 마커를 적용한 추가 실험을 통해 질화 메커니즘이 확인될 수 있을 것이다.
4.결 론
DC 스퍼터링 방법으로 O가 첨가된 Cr 박막을 제작 하고 NH3 분위기에서 질화 반응시켜 구조적 특성을 조 사하여 다음과 같은 결론을 얻었다.
1. As-deposit Cr 박막 전체에 걸쳐 Cr과 O의 원자 농도 비율이 각각 77 %와 23 %로 구성되었다. Asdeposit Cr 박막은 질화 반응으로 500°C에서 Cr 질 화물 (CrN, Cr2N)을 형성하고 600°C에서 Cr 산화 물(Cr2O3)을 형성하며, 900°C보다 높은 온도에서 중 간물질인 Cr2N과 Cr2O3가 소멸되고 CrN가 주되게 생성된다.
2. 600°C에서 처리된 시료는 표면으로부터 90 nm까지 O가 N으로 치환된 CrN 층이 형성되었고, 900°C에 서 CrN 층의 두께는 640 nm이었다. 800°C에서 CrN 층의 두께는 질화 시간이 10분일 때 343 nm 에서 240분일 때 510 nm로 증가하였다. CrN 층에 서 Cr과 N의 농도는 각각 60 %와 40 %이었다.
3. CrN의 생성은 속도제어 단계에서의 N과 O의 동시 확산으로 이루어진다. 질화 반응에 의해 표면으로부 터 O와 N이 상호 치환된 영역에서는 CrN과 Cr2N 질화물이 분포하고, 그 아래 영역에는 CrxNyOz 화 합물로 형성된다.
4. 질화 반응으로 형성되는 CrN 층의 두께는 시간의 제곱근에 비례하였고, 온도에 대해서는 지수함수적 으로 증가하였다. 온도에 따른 CrN 층의 두께, CrN (111)과 Cr2O3 (110)의 XRD 강도 비와 XPS의 N1s 와 O1s 피크 강도 비 등 산화물에 대한 질화물의 생성비(IN/IO)의 변화로부터 구한 활성화 에너지는 0.69 eV이었다.