1. 서 론
최근 휴대용 전자기기, 컴퓨터, 전기자동차 및 대용량 에너지 저장장치에 대한 관심이 폭발적으로 증가하는 가 운데 에너지 저장원으로 주로 사용되던 리튬 이온 전지에 대한 수요가 급증하고 있다. 기존 석유 에너지 기반 에너 지 패러다임의 변화, 2050 탄소 중립 및 글로벌 기후변화 협약 등 에너지 자원을 둘러싼 국제적인 흐름은 급격하게 변화하고 있으며 친환경적인 에너지 저장 장치에 대한 수 요는 2030년 3,000 GWh를 돌파하여 2019년 198 GWh 대 비 17배 이상 폭발적으로 성장할 것으로 전망된다. 하지 만, 리튬의 원자재로 사용되는 리튬 카보네이트는 분포는 지역적으로 편중되어 있으며 차세대 에너지 디바이스 시 장에서 수급적으로 많은 한계를 지니고 있다. 급증하는 수 요와 부족한 공급의 불균형으로 인하여 리튬을 대체할 금 속으로써 지구상에 많이 분포하고 비교적 저렴하며 화학 적 특성이 비슷한 나트륨을 이용한 나트륨 이온 전지가 유 력한 대체 에너지 저장원으로써 활발한 연구가 진행되고 있다.1-3)
나트륨 이온은 리튬이온보다 반경이 약 55 % 더 커서 호스트 재료에 가역적으로 삽입되고 탈리되는 것을 더 어 렵게 만든다. 더 큰 크기의 나트륨 이온의 느린 반응속도 는 낮은 에너지 밀도와 부족한 사이클 안정성을 초래한다. 기존 리튬 기반 시스템에서 음극재로써 널리 사용된 흑연 은 리튬/나트륨 이온반경 차이에 의한 삽입/탈리 비가역성 이 한계를 보였으며 하드카본은 흡탈착 반응 기반 낮은 가 역용량(<300 mAh g-1) 및 전류 속도에 따른 나트륨 덴드라 이트 형성 등의 안전성 문제를 야기할 수 있다. 나트륨 이 온 전지의 관심이 높아지면서 양극 소재의 개발은 발달하 였지만 음극 소재의 개발은 높은 에너지 밀도와 훌륭한 사 이클 안정성을 확보하기 위해 여전히 더 많은 투자가 필요 하다.4-6) 특히나, 넓은 전압 범위와 우수한 율속 특성, 저렴 한 재료 안에서의 넓은 가역적 용량과 함께 적절한 음극 재료의 개발은 나트륨 이온 전지 상업화를 위해 매우 시급 하다. 추후 차세대 중대형 전지용 나트륨이차전지 개발 시 양극-음극 불균형 안정성 문제를 해소하기 위한 나트륨 음극 설계가 반드시 필요한 상황이다.7-9)
현재까지 나트륨 이온 전지를 위한 음극 물질 연구는 층상구조로 이루어진 전이금속 산화물, 금속 황화물 화합 물 등이 2차원 결정 구조에서 기인하는 높은 나트륨 저장 용량과 낮은 산화환원전위를 가지며 더 좋은 전기화학적 가역성, 그리고 충방전반응에서 금속 산화물보다 더 긴 사 이클 수명 등의 우수한 전기적 특성을 기반으로 주목을 받 고 있다.5,8) 그 중 주석과 안티몬를 기반으로 한 전이금속 황화물은 전하 저장을 위한 반응 사이트를 제공하고 전자 와 이온을 수송 및 전해질 확산을 촉진하는 등의 효과를 바탕으로 전기화학 반응 중에 연속적인 전환-합금화 전기 화학 반응 메커니즘을 통해 나트륨 이온을 수용할 수 있으 므로 높은 가역적 이론용량을 가질 수 있다고 보고되고 있 다.10-12) 이러한 전이금속 황화물계 물질은 전기화학 반응 중에 나트륨과 반응하여 큰 부피 팽창을 야기하고 이는 용 량 감퇴의 주된 원인이 되어 부피팽창이 억제된 음극 물질 을 개발하는 것은 필수적이다.13-15) 본 연구에서는 전이금 속 황화물계 물질의 전이금속 후보군으로써 주석과 안티 몬의 비율을 조절함과 동시에 그래핀 옥사이드 위에 고르 게 분포되도록 수열합성을 통해 복합화 시킴으로써 반응 중 야기되는 부피팽창을 최소화하고 최적화된 황화물 조 성을 통하여 차세대 나트륨 이차전지 음극 소재로써의 가 능성을 평가하였다.
2. 실험 및 분석 방법
본 연구에서는 주석-안티몬 황화물과 복합화하기 위한 그래핀 옥사이드(graphene oxide, GO)를 기존 Hummers method를 이용하여 합성하였다. 1.0 g 흑연 분말과, 50 ml 황산을 바깥이 얼음으로 둘러싸인 비커에서 교반하였다. 3.0 g의 Potassium Permanganate (KMnO4)을 앞의 용액에 넣고 상온에서 2시간동안 교반하였다. 그 후, 200 ml의 DI Water를 천천히 넣고 2시간동안 초음파 처리 후 20 ml의 Hydrogen peroxide를 천천히 첨가하였다. 44 ml의 HCl을 500 ml DI Water에 천천히 넣었다. 원심분리기를 이용하 여 6,000 rpm으로 5분간 원심분리를 실시 후 포집한 GO를 희석된 HCl 용액과 DI water을 이용하여 중성이 될 때까지 세척하였으며, 최종적으로 동결건조를 진행하였다. 주석- 안티몬 황화물계 나노복합체(SnSbS nanocomposites)를 합 성하기 위하여 화학양론적 비율 8:2 및 6:4로 각각 SnCl4- 5H2O 및 SbCl3를 각각 GO 50 mg이 분산된 에탄올 80 ml에 넣고 1시간 교반 뒤 10분간 초음파 처리를 하였다. 상기 용 액에 C2H5NS (0.006 mol)를 넣고 추가로 1시간 교반 이후 160 °C, 15시간 수열 합성을 진행하였다. 수열 합성 이후 생성된 화합물을 에탄올 및 DI water를 이용하여 반복적 으로 원심 분리를 실시하였으며, 동결 건조 이후 포집한 화합물을 표면 유기물 제거 및 결정성 증대를 위한 질소 분위기 하에서 500 °C, 2시간동안 환원 열처리를 실시하 였다. 주석-안티몬 비율에 따라 8:2 및 6:4를 각각 SnSbS-1 및 SnSbS-2로 명명하였다. 물리적 특성과 구조 변화에 대 한 분석을 위하여 X선 회절분석(X-ray diffraction, XRD, BRUKER, D8 Advance A25 X-ray diffractometer)를 이용하 여 10 ≤ 2θ ≤ 80°의 각도 범위에서 λ = 0.15418 nm의 파장 으로 결정 구조를 확인하였다. 주사전자현미경(scanning electron microscopy, SEM, JEOL, JSM-7610F)과 투과전자 현미경(transmission electron microscopy, TEM, FEI, TF30 ST)을 이용하여 주석-안티몬 황화물계 나노복합체의 미 세구조와 형태를 분석하였다. 25~900 °C까지 10 °C/min의 속도로 승온시켜 산화 분위기에서 열 중량 분석(thermogravimetric analysis, TGA, TA, Q600/Q200)를 진행하여 환 원된 그래핀 옥사이드(rGO)의 양을 분석하였다.
전극 슬러리는 SnSbS : Super P : CMC를 75 : 17 : 8의 중 량비로 용매는 DI water로 균일하게 혼합하여 제조하였다. 만든 슬러리를 닥터블레이드법(150 μm)으로 Cu 호일에 도포하고 진공 오븐에서 50 °C에서 건조하였다. 전해질은 1 M NaPF6 농도의 EC/DEC (ethylene carbonate/diethylene carbonate), Glass fiber (GF-D) 분리막, 1~1.3 mg/cm2 활물 질이 로딩된 직경 12 mm 전극, 반쪽 셀(half cell) 테스트를 위하여 직경 14 mm의 Na metal (99.9 %, Merck)를 상대 전 극으로 사용하여 CR2032 코인 셀을 조립하였다. 반쪽 셀 (half cell) 테스트를 위한 상대 전극으로 Na metal (99.9 %, Merck)를 직경 14 mm로 Cut-off 전압범위는 0.01~2.5 V (vs Na/Na+)로 Cyclic voltammetry를 VSP-3e (BioLogic) 수 행하였으며, 에너지 저장 성능 평가는 전압 범위 0.01~2.5 V (vs Na/Na+)에서 100~5,000 mA g-1의 전류밀도 범위에서 충방전 평가(charging-discharging test)를 통해 평가하였다.
3. 결과 및 고찰
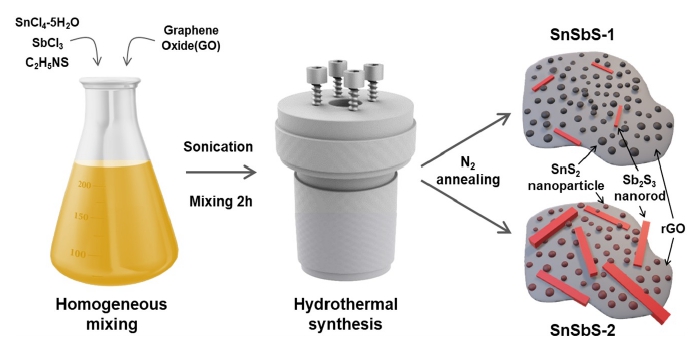
본 연구에서는 간단한 수열합성법과 환원 열처리를 통 하여 주석-안티몬 황화물 나노복합체를 제조하였으며 실 험에 대한 간단한 모식도는 Fig. 1에 나타내었다. 주석-안 티몬 황화물은 낮은 전기전도도를 가지므로 이를 극복하 기 위해 그래핀 옥사이드를 복합화시켰으며 주석 및 안티 몬 전구체의 비율을 화학양론적으로 각각 8:2 및 6:4 비율 로 맞추어 합성을 진행하였다. 수열합성 전 단계에서 화합 물의 완전한 균일성을 위하여 그래핀 옥사이드와 전구체 간의 혼합과 분산을 진행한 후에 수열합성을 진행하였다. 이후 준비된 전극 재료들을 추가적인 환원 열처리를 통하 여 전극재 표면의 유기물 제거 및 그래핀 옥사이드의 환원 을 유도함으로써 최종적으로 전극 물질을 제조하였다.
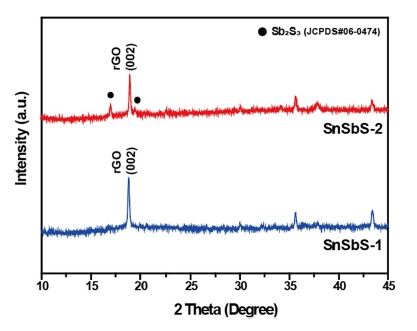
합성된 전극재의 결정 구조 및 rGO의 함유량을 정확히 판단하기 위하여 Fig. 2와 같이 XRD 및 TGA를 진행하였 다. Fig. 2(a)의 XRD 결과, 두 전극재 모두 hexagonal SnS2 및 Sb2S3로 구성된 복합체가 형성되었으며, 합성 단계에 서 주석 대비 안티몬의 비율이 더 낮았던 SnSbS-1가 더 적 은 Sb2S3를 포함하고 있음을 확인할 수 있다. 주석-안티몬 황화물에 있어서 물질 간 고용될 수 있는 한계가 있으며 안티몬의 비율이 높아짐에 따라 많은 양의 Sb2S3가 높은 결정성을 띄며 많은 양이 함유되어 있음을 알 수 있다. Fig. 2(b)의 TGA 분석을 통하여 rGO의 최종 비율은 각각 19.19 % 및 16.64 %로 초기 의도한 그래핀 옥사이드의 분율(10 wt%)을 상회하는 것을 확인하였으며 이는 화학양론적으 로 설계한 주석-안티몬 황화물이 전부 수열 합성 반응에 참여하여 화합물을 형성하지 못 하였다고 판단된다. Fig. 2(c)는 열처리 이후 rGO의 환원 정도를 확인하기 위한 라 만 분석 결과를 나타낸다. D 밴드는 그래핀 옥사이드의 sp2 도메인의 크기와 관련이 있으며 1,350 cm-1에 위치하는 반 면 G 밴드는 sp2 C 원자의 E2g 포논의 1차 산란에서 발생하 며 1,600 cm-1에 위치한다. 합성 직후 SnSbS-1 및 SnSbS-2 의 D 밴드와 G 밴드의 강도 비율(ID/IG)은 각각 1.21 및 1.22 였으며, 환원 열처리 이후 각각 1.28 및 1.31로 증가함을 알 수 있다. D/G 밴드 비율의 증가는 sp2 링의 결함이 더욱 형 성되었음을 나타내며, 그래핀 옥사이드의 탄소 원자가 환 원 후 더 높은 결함 농도로 무질서하게 배열함을 나타낸 다. 이를 통해 두 샘플 모두 열처리 이후 그래핀 옥사이드 의 환원이 일어났음을 알 수 있다.
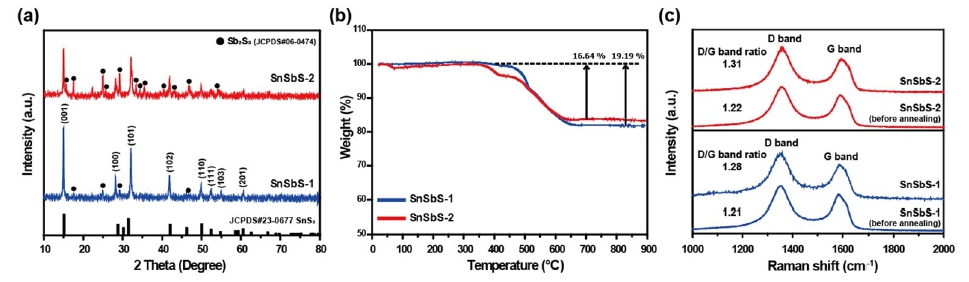
Fig. 2
(a) X-ray powder diffraction patterns (10~80°), (b) TGA curves and (c) Raman spectra of tin antimony sulfide nanocomposites.
주석-안티몬 황화물의 미세구조를 각각 저배율 Fig. 3(a, b) 및 고배율 Fig. 3(c, d)에서 분석하였다. SnSbS-1 샘 플의 경우, 환원된 그래핀 옥사이드의 표면 위에 많은 양 의 SnS2 입자들이 분포되어 있으며 Sb2S3의 입자는 XRD 상에서 작은 강도 세기로 관찰되지만 SEM 상에서는 명확 하게 구분하기는 어려워 작은 입자 형태로 혼재되어 있을 것으로 판단된다. 반면에 SnSbS-2 샘플의 경우, 5 μm 수준 의 매우 큰 각진 입자들이 나노복합체 표면에 불균일하게 분포되어 있음을 알 수 있다. 이러한 큰 입자들은 XRD 결 과에서 관찰되었던 큰 결정성을 가지는 Sb2S3 입자들로 판단되며 주석-안티몬 간의 고용 한계를 벗어나는 합성 초기 비율에 따라 화합물을 형성하지 못하고 물리적으로 섞여 있는 복합체를 형성한 것으로 판단되며 앞선 XRD의 결과와 부합한다.

Fig. 3
SEM images of tin antimony sulfide nanocomposites; (a, b) the low magnification, and (c, d) the high magnification of SnSbS-1, and SnSbS-2, respectively.
입자의 표면 형상 뿐만 아니라 rGO와의 결합 및 분포를 더욱 명확하게 관찰하기 위하여 TEM 분석을 Fig. 4와 같 이 진행하였다. Fig. 4(a, b)를 통하여 rGO 표면 위에 hexagonal 형태의 50 nm 크기 수준 SnS2 나노 입자들이 고르게 분포되어 있음을 알 수 있다. Fig. 4(c)의 링 형태의 SAED 패턴을 통하여 SnS2 나노 입자들로 인하여 각각의 결정을 이루며 집합한 다결정 형태로 존재하고 있으며 각각 (100), (110) 및 (023) 면지수에 부합되는 면간 거리를 나타 냄을 보여준다. Fig. 4(d)는 SbSnS-1 입자의 EDS mapping 결과를 보여주며 고르게 Sn, Sb, S 원소들이 고르게 분포 되어 있음을 다시 한 번 보여준다. Fig. 4(e-f)는 SnSbS-2 입 자의 미세구조를 나타내며 SEM에서 관찰되었던 수 μm 크기 수준의 각진 형태의 Sb2S3 입자와 SnS2 나노 입자가 혼재되어 관찰되며, 단결정상의 여러 입자들이 뭉쳐 보이 는 SAED 패턴을 Fig. 4(g)를 통하여 확인할 수 있다. Fig. 4(h)의 EDS 결과, 입자 전체에 Sn, Sb, S가 분포되어 있는 것으로 관찰되나 Sb2S3 입자가 있는 곳에서 Sb가 비교적 으로 강한 신호를 나타내고 있음을 확인할 수 있으며 이는 Sn과 일부 고용된 Sb는 그래핀 옥사이드 표면 위에 SnS2 나노 입자의 결정 구조 안에 존재하며, 고용 한계를 벗어 난 Sb가 Sb2S3를 형성하여 이차상을 형성함으로써 복합체 를 만든 것으로 사료되며 앞선 XRD 및 SEM의 결과와 부 합된다.

Fig. 4
TEM images of tin antimony sulfide nanocomposites; (a, e) the low magnification, (b, f) the high magnification, (c, g) SAED pattern and (d, h) elemental distribution of SnSbS-1, and SnSbS-2, respectively.
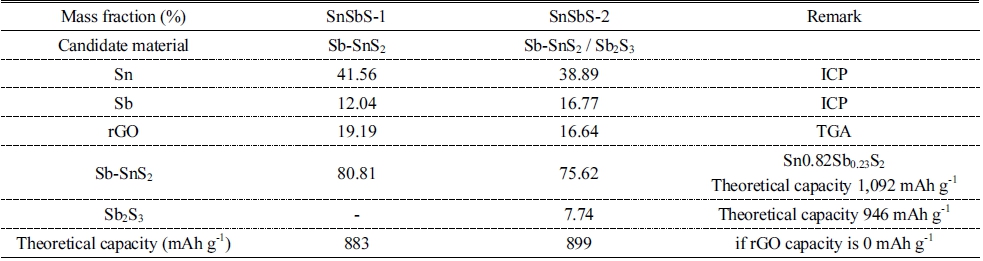
전기화학 테스트를 진행하기에 앞서 SnSbS-1 및 SnSbS- 2 샘플의 원소 분석에 따른 물질 구성비 및 이론 용량을 Table 1에 정리하였다. 후보 물질로써 rGO 위에 성장한 Sb 가 고용된 SnS2 입자(Sb-SnS2)와 5 μm 크기의 Sb2S3을 고 려하였다. 유도 결합 플라즈마 발광 분석법(ICP-OES)을 통하여 얻어낸 Sn 및 Sb의 비율은 초기 합성 단계에서 넣 어준 화학양론 비율(SnSbS-1, 8:2; SnSbS-2, 6:4)을 정확하 게 따르지는 않았지만 경향성 있는 결과를 보였으며 이는 앞서 말한 주석-안티몬 간의 고용 한계에서 기인하였을 것으로 판단된다. TGA 분석을 통한 그래핀 옥사이드의 비율과 ICP-OES 분석을 통하여 얻어낸 Sn 및 Sb의 비율을 통하여 SnSbS-1 샘플의 후보 물질인 Sb-SnS2의 최종 조성 이 Sn0.82Sb0.23S2로 구성되어 있으며, 이를 통해 SnSbS-2 샘 플이 7.74 wt%의 Sb2S3를 함유하고 있을 것으로 판단된다. 환원된 그래핀 옥사이드의 전기화학적 용량을 고려하지 않는다면 SnSbS-1, 2 샘플 각각 883, 899 mAh g-1의 이론용 량을 가질 것으로 사료된다.
충방전 과정동안 나타나는 SbSnS 입자들의 전기화학적 반응을 확인하기 위하여 Cyclic voltammogram test를 Fig. 5와 같이 진행하였다. 방전과정동안 전지의 전압이 0.8 V 이상일 때 SbSnS 입자들과 나트륨 이온 사이에서 일어나 는 주요 반응은 Sn 및 Sb 나노 입자와 비정질상의Na2S가 생성되는 전환 반응이며 이는 Fig. 5(a, b)에서 모두 동일하 게 나타난다. 0.56 V에서 일어나는SEI층 형성 이후, Sn과 Sb 금속과 Na 이온은 각각 합금화 반응을 거쳐 Na3.75Sn 및 Na3Sb합금을 형성한다. SnSbS-2 입자의 경우, 입자 사이 즈가 큰 Sb2S3에 기인하는 SnSbS-1 입자와 다른 방전 반응 을 가지며 이는 Fig. 5(b)의 0.13 V영역의 반응과 대응한 다. 전반적인 반응 전위의 위치는 SnSbS-1와 SnSbS-2 샘 플이 유사하지만 0.79 V 영역에서 나타나는 충전 반응이 SnSbS-2의 경우에 더 지배적으로 나타나며 이는 합금화 되었던 Na3.75Sn 및 Na3Sb이 다시 금속으로 전환되는 반응 을 의미하며 첫 사이클 이후 비가역적인 반응으로 전환되 는 것을 확인할 수 있다. SnSbS-1의 경우, 모든 합금상이 Sn금속 상으로 가역적으로 변환되고, 반응 전위의 영역으 로 봤을 때 더 나아가 Na2S은 Sulfur로 전환될 것으로 판단 된다.16) 이러한 연속적인 전환-합금화 반응은 사이클이 지속됨에 따라서도 가역적인 반응을 가지게 되며 충전 과 정에서 형성된 최종 SnSbS2상은 비정질화될 것으로 사료 된다. 주석-안티몬 황화물 나노복합체의 전기화학적 특성 을 평가하기 위하여 다양한 충방전 속도에서 수명 테스트 를 진행하였으며 이를 Fig. 6에 나타내었다. 모든 전기화 학 테스트의 무게는 그래핀 옥사이드를 포함하는 전체 전 극재 무게를 기준으로 나타내었다. Fig. 6(a)를 통해 SnSbS-1 및 SnSbS-2는 100 mA g-1의 충방전 속도에서 770 mAh g-1 및 498 mAh g-1의 초기 용량을 나타내었다. SnSbS-2의 경우, 복합체 안에 혼재하는 큰 입자 크기를 가 지는 Sb2S3의 존재로 인하여 제한적인 나트륨 이온의 이 용만이 가능하여 전기화학 반응을 유도하지 못하여 낮은 가역 용량을 보이는 것으로 판단된다. 이에 반해 SnSbS-1 은 50 nm 급 작은 SnS2 나노 입자들이 rGO 표면 위에 고르 게 분포되어 있어 전해질 상에서 많은 양의 나트륨 이온과 의 반응을 할 수 있는 넓은 표면적을 보유하고 있으며, 작 은 입자 크기로 인하여 입자 내부로의 나트륨 이온 확산도 가능하여 이론용량에 준하는 매우 높은 가역용량을 나타 내고 있음을 알 수 있다. Fig. 6(b)에서 SnSbS 나노복합체 샘플들의 충방전 속도에 따른 율속 특성 평가를 위해 전류 속도를 100, 200, 500, 1,000, 2,000, 5,000 mA g-1의 단계별 로 증가시켜가며 진행하였으며 SnSbS-1 샘플이 모든 전 류 속도에서 매우 우수한 가역 용량을 나타내었다. rGO 복합화로 인하여 5,000 mA g-1 테스트 시 500 mAh g-1의 높 은 용량을 보이며 100 mA g-1 테스트 시 초기 용량 대비 60 % 수준의 매우 우수한 율속 특성을 보였다. 전류를 다시 100 mA g-1로 감소하였을 때 샘플 전부 가역 용량으로 회 복하였으며 SnSbS-2는 역시 비슷한 양상을 보였지만 여 전히 용량이 낮게 나오는 것을 확인할 수 있었다. Fig. 6(c, d)를 통하여 주석-안티몬 황화물 복합체의 전기화학 반응 영역을 확인하였으며, 초기 사이클에서 음극 표면에 안정 적으로 SEI 층을 형성하고 이후 연속된 두번째, 다섯 번째, 열 번째 cycle 모두 방전 곡선이 겹치는 것을 통해 가역적 으로 충방전이 이루어지고 있다는 것을 통하여 초기 용량 수준의 안정적인 반응 거동을 보이는 것으로 확인되었다. 500 mA g-1의 높은 충방전 속도에서 장기 수명 테스트를 진행하였으며 마찬가지로 SnSbS-2의 경우, 200사이클 이 후 초기 용량 대비 50 % 수준의 낮은 용량을 유지하고 있 는 반면 SnSbS-1은 71.2 %의 높은 용량을 유지하고 있음 을 알 수 있다. Fig. 7은 전기화학 테스트 이후 셀을 분리하 여 전극 표면을 측정한 XRD이며 전극 결정 구조의 변화 를 측정함으로써 전기화학 결과와의 연관성을 추적해보 고자 하였다. XRD 결과, 19°에서 환원된 그래핀 옥사이드 가 관찰되었으며 이는 SnSbS-1 및 SnSbS-2 전극 모두 동 일하게 관찰되었다. 나노입자로 존재하는 SnS2 입자는 반 응 중 가역적으로 반응에 참여함으로써 연속적인 변환-합 금 반응을 거치며 비정질화 되어 피크의 세기가 약해졌을 것으로 생각된다. 17°영역에서 피크가 관찰되었으며 이 는 SnSbS-2 샘플에 존재하는 큰 입자 사이즈를 가지고 있 는 Sb2S3이 전기화학 반응 중 참여하지 못 하였으며 이러 한 미반응 Sb2S3 입자의 존재로 최종적으로 전기화학 용 량에 기인하지 못하여 낮은 성능 및 사이클 안정성을 나타 냈을 것으로 판단된다.
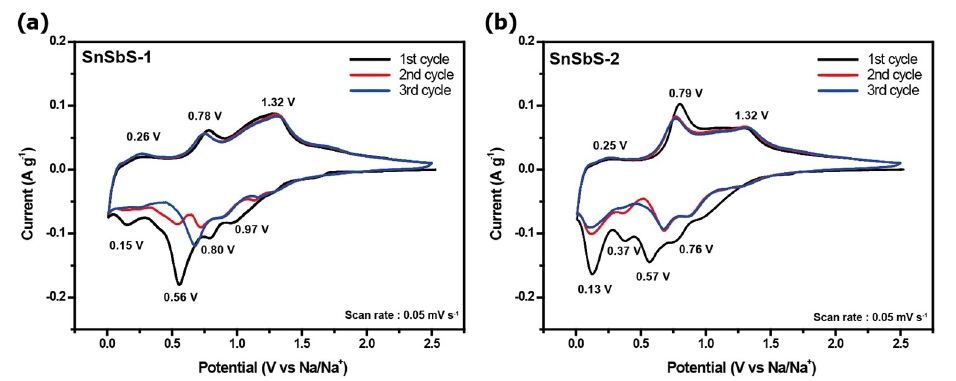
Fig. 5
Cyclic voltammetry for initial two cycles at the scan rate of 0.1 mV s-1 ranging from 0.01 to 2.50 V of (a) SnSbS-1, and (b) SnSbS-2.
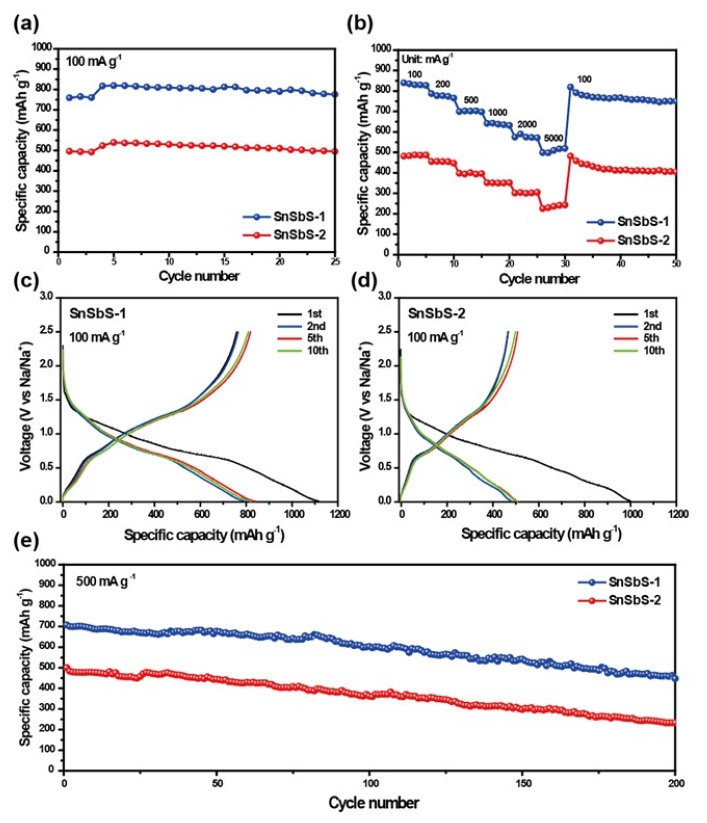
Fig. 6
(a) Cycling performance of tin antimony sulfide nanocomposites at 100 mA g-1, (b) rate performance of tin antimony sulfide nanocomposites at various current densities from 100 to 5,000 mA g-1, galvanostatic charge/discharge curves at 100 mA g-1 of the (c) SnSbS-1 and (d) SnSbS-2, (e) long-term cycling performance of tin antimony sulfide nanocomposites at 500 mA g-1.
4. 결 론
본 연구에서는 주석-안티몬 황화물 음극 조성 설계에 따 른 나트륨이온전지용 음극으로써의 전기화학적 에너지 저장 성능을 분석하기 위하여 수열 합성법 및 환원 열처리 를 도입하였고 그래핀 옥사이드 표면 위에 나노 복합체가 균일하게 성장한 나노복합체를 성공적으로 제조하였다. 최적화된 SnSbS-1은SnSbS-2와 비교하여, 우수한 충방전 용량과 안정적인 수명 특성을 보이며, 100 mA g-1의 충방 전 속도에서 770 mAh g-1의 방전 용량과 5,000 mA g-1 테스 트 시 500 mAh g-1의 방전 용량으로 반응에 지속적으로 참 여하는 가역적인 특성을 나타냈다. 특히, 500 mA g-1부터 전류밀도 하에서 200 사이클 동안 71.2 %의 향상된 방전 용량 유지율을 나타냈다. 이렇게 전기화학적 에너지 저장 성능 및 사이클 안정성이 향상된 이유는 합성 과정에서 주 석-안티몬 비율의 최적화로 인하여 고용 한계를 벗어나지 않는 주석-안티몬 황화물의 조성 제어를 통한 작은 입자 사이즈와 그래핀 옥사이드 복합화에 따른 전기화학 반응 시 부피 팽창 억제에서 기인하였을 것으로 판단된다. 본 연구를 통하여 나트륨이온전지용 음극 소재로써 주석-안 티몬 황화물 나노복합체의 전기화학적 성능을 평가하였 으며 이를 통해 중대형 에너지 저장원으로써의 가능성을 확인하였다.