1. 서 론
정형외과 및 치과의 중요한 금속 생체재료가 되기 위 해서는 우수한 생체적합성 및 체액 내 부식성, 높은 기 계적 강도 및 피로 저항성, 낮은 탄성 계수와 같은 특 성을 가져야 한다.1) 임플란트 산업에서 최근 몇 년 동 안 금, 스테인리스 강, Ti, Co-Cr 합금, Ni-Ti 합금과 같 은 금속재료를 사용하고 있다.2) 그 중 스테인리스 강은 최대 연성을 가지고 Co-Cr 합금은 내마모성이 가장 우 수한 장점을 가지고 있지만 Co, Cr, Ni과 같은 금속 이 온은 인체에 부작용을 끼칠 수 있다.3) 금속 생체재료 산 업에서 대표적인 재료는 cp-Ti 와 Ti-6Al-4V 합금으로 치과용 임플란트, 인공관절, 본 플레이트 등에 많이 사 용되는 금속재료이다.4) Ti-6Al-4V 합금은 이식 가능한 구 성요소 및 장치에 도입된 최초의 Ti 생체재료 중 하나 였다.
그러나 많은 연구에 의해 Al 이온과 V 이온이 점진 적으로 방출되면 국소적인 조직 이상 반응과 면역 반응 을 일으킬 수 있음이 확인되었다. 원소 V는 동물의 조 직에 심각한 반응을 일으키는 것으로 밝혀졌으며, Al은 신경계 장애 및 알츠하이머병과 관련될 수 있다.5) 한편 낮은 탄성계수는 뼈와 임플란트 사이의 더 효과적인 응 력 전달을 유도하고 불균형 응력 분포로 발생하는 응력 차폐 현상을 예방한다.6) 임플란트 장치 및 정형외과에 뼈 플레이트 등으로 많이 사용되는 스테인리스 강과 Co- Cr 합금의 탄성계수 값은 190 GPa 및 210 GPa 이고 Ti-6Al-4V 합금의 탄성계수 값은 약 110 GPa 이다. 비 록 Ti 및 Ti 합금의 탄성계수가 스테인리스 강 및 Co- Cr 합금보다 낮지만, 여전히 인체 뼈의 탄성계수 값인 15 ~ 30 GPa 보다 높게 나타난다.7) 이러한 문제를 해결 하기 위해 많은 새로운 Ti 합금, 특히 단일 β-Ti 합금 이 개발되었으나, 불행하게도 대부분의 β-타입 Ti 합금 의 탄성계수는 60 ~ 80 GPa 정도이며 이는 경조직 대 체물(hard tissue replacement: HTR)의 요구 사항과는 거리가 멀다.8)
또한 금속 생체재료, 예를 들어 스테인리스강 및 Co- Cr 합금 등과 같이 자화율이 현저히 높은 경우 자기공 명영상(MRI) 장비의 강한 자기장에 자화되어 재료에 열 이 발생하고 이미지에 인공물이 발생하게 된다.9) 발생된 인공물은 임플란트 주변의 장기 및 조직 이미지 왜곡을 유발하여 정확한 진단을 방해하고 인공물에 의해 방해 받는 영역은 임플란트의 자화율과 크게 관련이 있다. 인 공물의 생성은 자화율을 낮추면 같이 감소된다.10) 순수 한 Ti와 Ti 합금 및 Ti-6Al-4V 합금은 광범위한 인공물 이 발생하여 임플란트에 인접한 이미지의 품질을 크게 저하시킨다.11) 이상에 보고된 문제들을 해결하기 위해 다 양한 금속재료를 이용한 연구들이 진행되고 있는데 특 히 Zr 기반 생체재료가 큰 주목을 받고 있다. Zr은 본 래 핵연료의 피복재로 사용되는 유일한 재료로 알려져 있지만,12) Zr 및 Zr 합금은 낮은 탄성계수 값을 갖기 때 문에 생체역학적 이점으로 간주되며 Ti 및 Ti 합금에 비 해 인체 뼈의 응력 차폐 현상을 최소화한다.13) 또한 높 은 기계적 강도, 높은 파괴 인성 및 우수한 내식성을 나 타낸다.14) 추가적으로 Zr의 경우 임플란트 재료와 주변 조직 사이의 골 임플란트 접촉이 Ti 보다 우수한 것으 로 나타났고 부식으로 생성되는 ZrO2는 TiO2보다 독성 이 적기 때문에 인체조직이 더 잘 성장한다.15) Zr 합금 의 자화율은 cp-Ti 합금의 약 절반이고 스테인리스 강 의 30분의 1 내지 60분의 1이며 더 낮출 수도 있다.16) 이처럼 Zr 합금은 자화율이 낮아 MRI 진단을 방해하는 인공물의 영향을 덜 받는다. 이를 바탕으로 Zr 관련 생 체재료의 연구가 진행되고 있지만 아직까지 Zr에 대한 연구는 많이 부족한 실정이다. 원소 간의 복잡한 상호 작용으로 인해 Zr 삼원계 합금에 초점을 맞춘 연구는 거 의 없으며 기계적 특성 및 탄성계수, 내식성과 자화율 에 대한 체계적인 조사가 이루어지지 않았다. 기존 연 구에서 Zr-7Cu 합금은 금속간화합물인 Zr2Cu 상을 형성 하여 강도 값이 우수하고 저 탄성계수와 저 자화율 값 을 갖는 것으로 조사되었다. Sn은 독성이 거의 없고 내 화학성이 우수한 원소로 자화율 값이 현저히 낮으며, Sn 첨가시 생기는 금속간화합물에 의해 발생하는 기계적 강 도 값 증가와 탄성계수 변화, 자화율 값 감소를 위해 선 택되었다. 따라서 본 연구에서는 Zr을 기반으로 하는 Zr- 7Cu-xSn (x = 1, 5, 10, 15 mass%) 합금을 새롭게 설 계 및 제작하였으며 미세조직을 관찰하고 탄성계수와 자 화율 특성을 평가하였다.
2. 실험 방법
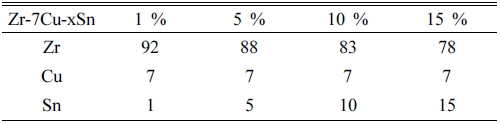
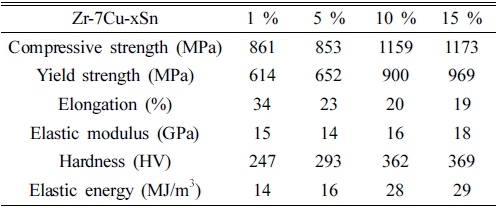
본 연구에 사용된 재료의 합금조성은 Table 1과 같 다. 각 합금들은 순수 지르코늄(99.9 mass%), 무산소 동 (99.9 mass%) 그리고 주석(99.99 mass%)을 합금의 원료 로 사용하였다. Zr-7Cu-xSn 합금은 각각 4개의 150 g 양을 진공아크용해로를 사용하여 아르곤 가스 분위기에 서 용해하였다. 진공도는 5.1 × 10-5 Torr를 유지했으며 잉 곳들은 분리를 방지하기 위해 6회씩 뒤집기와 재용해를 진행하였다.
저융점 금속인 주석은 함께 용해하지 않고 Zr-Cu 합 금을 높은 에너지의 아크를 이용하여 4,000 °C 부근에서 1차 합금을 만들고, Sn을 추가 장입하여 낮은 에너지의 아크를 이용하여 2,500 ~ 3,000 °C 에서 2차 용해합금으 로 지름 13mm×70mm 길이의 원통형의 잉곳을 제작하 였다. 시편은 저속 다이아몬드 쏘(wafering blade, USA) 를 사용하여 정밀하게 절단하였다. 합금의 미세조직은 10 mm × 10 mm의 크기로 절단된 Zr-7Cu-xSn의 시편을 #220에서 #4000의 그릿이 있는 SiC 에머리 페이퍼를 사 용하여 연마를 실시하였고, 다이아몬드 서스펜스 1 mm를 사용하여 미세연마를 실시하였다. 그 후 콜로이달 실리 카 현탁액으로 진동연마를 실시하였으며 화학적 에칭은 증류수 45mL, 질산 45 mL, 불산 10 mL (Dist water 45 mL + Nitric acid 45 mL + Hydrofluoric acid 10 mL) 를 이용하여 약 3초간 에칭을 진행하였다. 준비된 4개 의 시편을 광학현미경(OM, Zess: Axio Vert. Al)과 주 사전자현미경(SEM, Seron: AIS2000C)를 이용하여 미세 조직을 관찰하였다. 시험편의 결정상 구조의 변화를 관 찰하기 위해 X선 회절계 3D 고분해능(high resolution X-Ray diffractometer: PANalytical EMPyrean)를 사용하 여 20°에서 80°까지 0.02°의 스캔간격에 유지시간 1초의 조건으로 2θ 스캔을 수행하였다. 압축 시험은 시편의 기 계적 특성, 압축 강도, 항복 강도 및 탄성 계수를 측정 하기 위해 범용 시험기(MTDI: Minos-100S)를 사용하여 수행하였다. 압축 시험편은 3 mm× 3 mm× 6 mm의 크기 로 와이어 절단으로 준비되었다. 시험은 응력-변형 곡선 을 얻기 위해 실온에서 1 mm/min의 초기 변형률로 수 행되었다. 합금의 경도는 미세조직에 관찰된 시험편을 사 용하였으며 비커스 경도 시험기(Shimadzu: HMV-G21, JAP)를 사용하여 19.61 N 하중 하에서 유지시간 5 s 조 건으로 측정하였다. 임플란트에 활용되는 금속 생체재료 는 낮은 탄성계수 값이 필요하며 탄성 에너지의 공식은 다음과 같이 식 (1)로 표현할 수 있다.
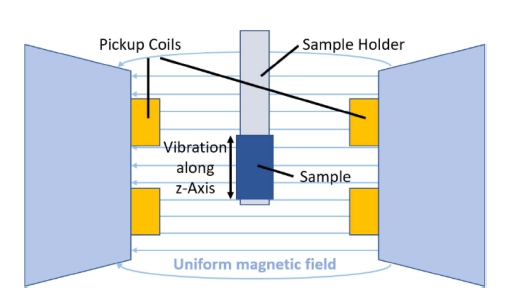
여기서 δe는 탄성 에너지, σy는 항복강도, εe는 탄성변 형, E는 탄성계수이다. 자기적특성 평가는 상온에서 초 전도양자간섭장치(superconducting quantum interference device: SQUID MOMS XL7)을 사용하여 측정하였고 Fig. 1에 개략도를 나타내었다. 자화율 측정 시험편은 3 mm× 3 mm × 1 mm의 크기로 와이어 절단으로 준비되었 다. 시편의 두께는 1mm를 넘지 않게 하였는데, 이는 두 께가 1mm를 넘어가게 되면 무게가 증가하게 되고 자성 이 센 시료의 경우에는 최적의 자화 감도인 ~ 10-4 emu 를 넘어가기 때문에 정확한 측정이 어려워지기 때문이 다. 시편 자화 (M) 및 적용된 자기장 (H)을 통해 자기 이력곡선을 얻어 자화율을 측정하였다. 적용된 자기장의 범위는 임상 MRI 검출에 사용되는 자기장 범위와 일치 하는 -30,000 Oe ~ 30,000 Oe로 설정하였다. 설계된 Zr- 7Cu-xSn 합금의 부식특성평가를 위해 전기화학분극장 치(ZIVE sp1)를 사용하여 측정하였다. 37 °C의 식염수 (saline)를 전해질로 사용하여 인체 환경과 유사하게 부 식 테스트를 진행하였다. 부식 측정을 위한 시편은 에 폭시를 사용하여 구리선에 연결하고 콜드 마운팅(cold mounting) 하였다. 표면은 에머리 페이퍼 4000 그릿까지 사용하여 연마하였다. 실리콘 씰링을 통해 0.25 cm2 면 적의 정사각형 표면을 전해질과 접촉하게 했다. 기준전 극으로는 포화 칼로멜 전극(SCE), 상대 전극으로는 백 금선을 사용하였다. 잠재적 편광 측정은 1 mV/s의 스캔 속도로 -1.5 V ~ 1 V에서 수행되었다.
3. 결과 및 고찰
3.1. 미세조직
Fig. 2와 Fig. 3은 Zr-7Cu-xSn 합금의 광학현미경사진 과 주사전자현미경사진이다. Cu와 Sn을 첨가한 시편에 서 α-Zr 상 및 진회색상인 Zr2Cu 금속간화합물이 관찰 되었다. 계면 주변에서 원형모양인 Zr2Cu 상은 온도가 낮 아짐에 따라 Zr 및 Cu의 용해도가 감소하여 형성되는 석출상과 820 °C 미만의 온도에서 형성되는 공석상으로 분류할 수 있고 온도가 낮아질수록 Cu 원자가 입계 영 역으로 확산되어 Zr2Cu 상을 형성한다.

Fig. 2
Optical microscopy (OM) Microstructure of the Zr-7Cu-xSn alloys: (a) Zr-7Cu-1Sn, (b) Zr-7Cu-5Sn, (c) Zr-7Cu-10Sn, and (d) Zr-7Cu-15Sn.

Fig. 3
Scanning electron microscopy (SEM) Microstructure of the Zr-7Cu-xSn alloys: (a) Zr-7Cu-1Sn, (b) Zr-7Cu-5Sn, (c) Zr-7Cu- 10Sn, and (d) Zr-7Cu-15Sn.
기지 내 라멜라 층상조직이 나타나는데 이는 α-Zr + Zr2Cu의 공정조직으로 판단되며 Fig. 3에서 확인할 수 있다. Sn 함량이 증가함에 따라 구형입자가 약 40 ~ 250 μm인 판상모양의 금속간화합물이 10 wt% 이상부터 관 찰되었으며 크기와 양이 증가하였다. 동시에 기지 영역 과 Zr2Cu 상의 부피분율은 감소하였다. Zr - Sn 상태도 에 따라 온도가 낮아지면서 기지와 Zr2Cu 상에서 Sn 의 고용도가 감소하고 Zr4Sn 상이 석출된 것으로 판단 된다.17)
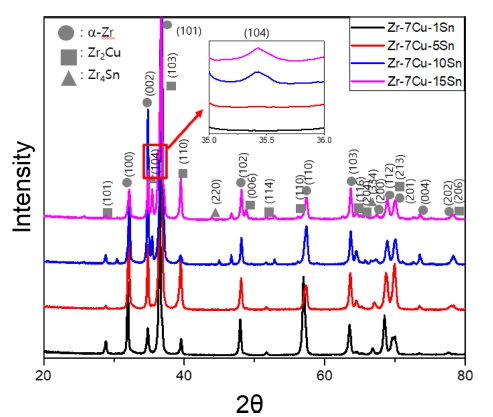
Fig. 4에서는 Zr-7Cu-xSn 합금의 XRD 패턴을 보여 준다. 주 회절피크의 분석은 JCPDS를 참고하였다. 36° 부근에서 α-Zr의 높은 회절피크인 (101)을 확인하였고 Zr2Cu 상의 주요 피크인 (103), (110), (213) 피크도 확 인하였다. Sn 함량이 10 wt% 이상부터 Zr4Sn의 피크 (220), (104), (334)를 확인하였다.
3.2. 기계적 특성
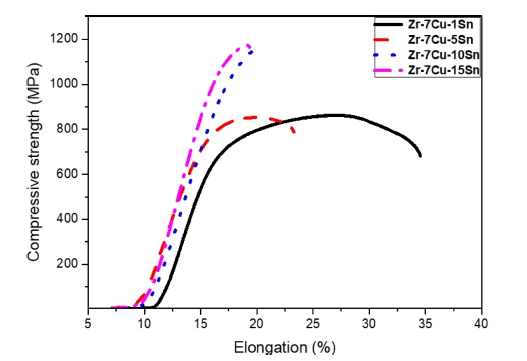
기계적 성질을 조사하기 위해 압축시험을 통한 Zr- 7Cu-xSn 합금의 응력-변형률 곡선이 Fig. 5에 나타냈다 . Cu와 Sn으로 구성된 지르코늄 합금에서 압축강도와 항복강도는 Sn 함량이 증가함에 따라 증가하고 연성은 감소한다. 이것은 고용강화 효과로 볼 수 있으며, 미세 구조 관찰에서 이미 논의된 바와 같이 기지인 α-Zr에 비해 상대적으로 경한 Zr2Cu 공정상의 증가에 따른 결 과이고 Zr2Cu는 전체적으로 균일하게 분포되어 2상 강 화 효과를 나타낸다. 고용강화 효과에 더해, 삼원계 합 금의 강도는 Zr2Cu 상과 함께 증가하였다. 응력-변형률 곡선에 따른 기계적 성질 값들은 Table 2에 나타내었 다. Sn 함량이 1 ~ 5wt%인 합금의 압축강도 값의 평 균인 약 856 MPa과 비교해 10 ~ 15 wt%인 합금의 압 축강도 값의 평균은 약 1,166 MPa로 상승하였으며 이 는 Sn 함량이 10 wt% 이상부터 Zr4Sn 상이 나타나며 2상 강화 효과 및 석출 강화로 인해 더욱 증가한 것으 로 판단된다. 반면에 합금의 연성은 강도 값이 증가할 수록 감소하였다.
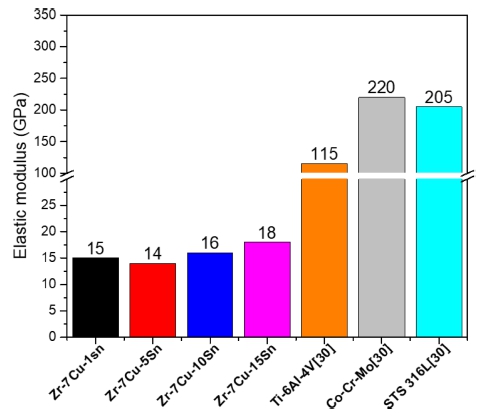
합금의 항복강도는 614 ~ 969 MPa 범위 이내이고 최 대압축강도는 861 ~ 1,173 MPa로 Ti 합금과 같은 대부 분 금속 생체재료와 비교해 비슷하거나 높다.18) 일반적 으로 낮은 탄성계수 값은 금속 생체재료의 필수 요소이 다. Zr-7Cu-xSn 합금의 탄성계수 값은 상용화되고 있는 대표적인 금속 생체재료들과 비교해 현저히 낮은 탄성 계수를 갖고 있으며 Fig. 6에 나타내었다. 탄성계수는 화 학 조성과 미세 구조의 영향을 받기 때문에 Zr-7Cu 합 금의 탄성계수(20 GPa)19) 보다 감소시킬 수 있었다.20) 식 (1)에 따르면 탄성 에너지가 계산될 수 있으며 14 ~ 29 MJ/m3로 Ti 기반 생체재료보다 높다.20) 따라서 Zr- 7Cu-xSn 합금은 상용 생체재료보다 더 높은 변형을 견 딜 수 있다.
3.3. 자기적 특성
Zr-7Cu-xSn 합금의 자화율은 Fig. 7(a)의 자화곡선을 통해 데이터의 선형 피팅에서 자화율 값을 얻었고 Fig. 7(b)에 나타내었다. 인체조직의 자화율은 37 °C에서 조직 의 주요 구성요소인 물의 질량 자화율 -9.07 × 10-6 또 는 체적 자화율이 -9.05 × 10-8인 물 값의 ± 20% 이내 인 -11 × 10-6~ -7 × 10-6 이다.21-22) 또한 혈액 세포는 자 화율에 기여하는데, 탈산소화된 혈액 세포(-6.52 × 10-6)는 산소화된 적혈구(-9.19 × 10-6)와 비교해 상자성이 더 크 다.21,23,24) 따라서 일반적으로 생물학적 조직은 상자성과 반자성의 특성을 가진다. 반자성체와 상자성체 재료는 자 기장이 존재할 때만 민감도를 보이는 특성 때문에 비자 성체라 할 수 있는데, Zr은 외부 자기장에 영향을 받지 않으면 불규칙적이게 되는 전형적인 상자성체이다. 이에 반해 Cu는 반자성체 재료이기 때문에 약한 자성 특성 을 가진다.
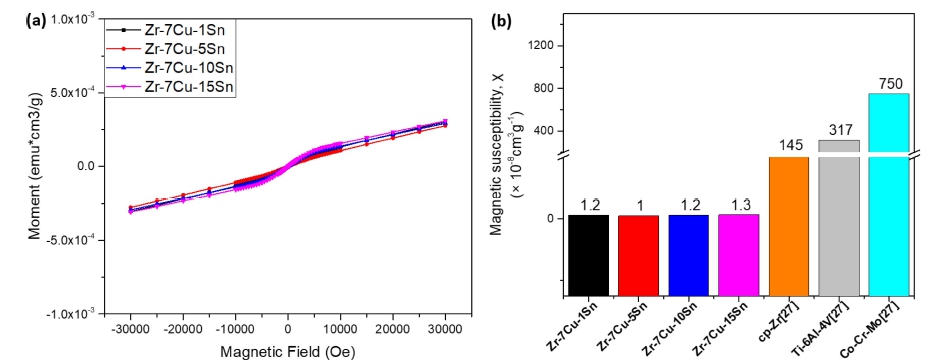
Fig. 7
Magnetic characteristic o f Zr-7Cu-xSn a lloys: (a) The magnetization of applied magnetic f ield for Z r-7Cu-xSn ( x = 1 , 5, 10, 15 wt%) and (b) Magnetic susceptibilities of Zr-7Cu-xSn and conventional implant materials.
Sn은 상자성체 재료이며 자화율 값이 0.03×10-6 cm3g-1 로 상당히 낮은 자성특성을 가지고 있다. Zr-7Cu-xSn 합 금의 평균 자화율 값은 약 1.17 × 10-8 cm3g-1 이다. 아 쉽게도 Sn 함량변화에 따른 경향성은 없는 것으로 판단 된다. 그러나 대표적인 금속 생체재료인 Ti-6Al-4V 합금 의 자화율 값 3.487 × 10-6 cm3g-1, cp-Zr 자화율 값25) 1.455 × 10-6 cm3g-1과 비교해 그 수치가 생체조직에 가 까운 현저히 낮은 자화율 값을 가짐으로써 Sn 첨가의 영 향은 확연히 나타났다. 이는 영상진단 시 방해가 되는 인공물을 억제할 수 있는 새로운 금속 생체재료로 기대 할 수 있다.
3.4. 전기화학적 부식 특성
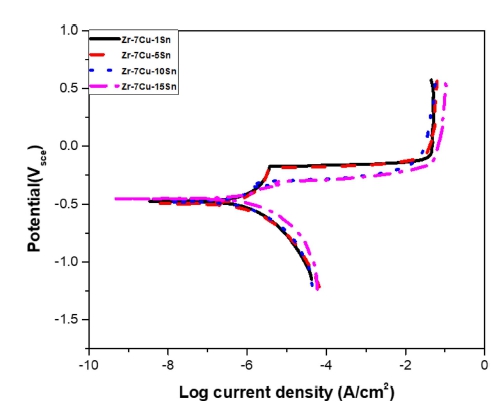
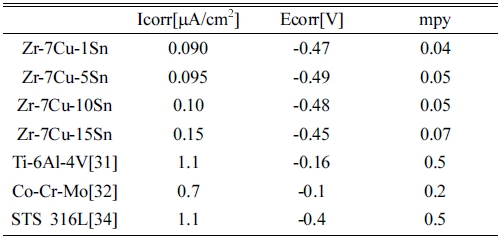
Fig. 8은 Zr-7Cu-xSn 합금을 37 °C의 생리 식염수에서 측정한 분극실험 곡선이다. 부식 전류 밀도(Icorr) 및 부 식 전위(Ecorr)은 타펠 외삽법에 의해 결정되었다. 각 평 균값들은 Table 3에 나타냈다. 일반적으로 부식 전류 밀 도가 낮고 합금의 자기 부식 전위가 높을수록 내식성이 좋다. 특히 부식 전류 밀도는 합금의 내식성을 판단하 는 데 중요한 척도이다. Sn 함량이 증가함에 따라 부식 전류밀도 Icorr 값은 약간 증가하였다. 그러나 순수 Zr 의 Icorr 값26)인 0.182μA/cm2, Ti-6Al-4V의 Icorr 값 1.1 μA/cm2과 Co-Cr-Mo의 Icorr 값 0.7μA/cm2 비해 Zr- 7Cu-xSn 합금은 낮은 부식전류밀도 값을 가진다. Zr- 7Cu-xSn 합금 모두 전위 값이 증가함에 따라 -0.15 V 이상의 영역에서 전류밀도 값이 증가하지 않고 10-1 A/ cm3 근처에서 유지하는 형태를 나타냈다. 이는 분극시 험 중 용액과 금속표면이 접촉하여 금속표면에 부식을 일으키는 양극반응에 의해 형성되는 부식생성물이 표면 에 산화물 형태로 쌓여 전류차단으로 양극반응을 방해 하기 때문으로 판단된다.27,28) 유럽의 표준 의료 응용 분 야에 따르면 금속 임플란트의 부식 속도는 1mpy 미만 이어야 한다.32) Zr-7Cu-xSn 합금의 평균 mpy 값은 0.05로 표준 의료 분야에 적합하며 상용 금속생체재료 의 평균 mpy 값인 0.4 보다 낮은 값을 가진다. 분극실 험 후 표면을 광학현미경으로 관찰한 이미지를 Fig. 9 에 나타냈다. 전체적으로 금속간화합물들인 Zr2Cu와 Zr4Sn 상들이 부식이 많이 된 것을 확인할 수 있고 기지와 비 교하여 우선 부식영역으로 작용한다.28) 10 wt% 부터 는 Zr4Sn이 나타나면서 우선 부식영역인 금속간화합물 의 영역이 넓어져 부식속도에도 영향을 미친 것으로 판 단된다.
4. 결 론
본 연구에서는 금속 생체재료로써 큰 사용 가치가 있 는 재료인 지르코늄기 3원계 합금을 설계 및 제작하여 다음과 같은 결론을 이끌어냈다.
1) Zr-7Cu-xSn 합금에서 Zr2Cu, Zr4Sn의 금속간화합물 을 확인하였으며 Zr2Cu 상은 입계를 따라 분포하고 있 다. Sn 함량이 증가함에 따라 Zr4Sn 상의 부피분율이 증 가하고 Zr2Cu 부피분율은 감소하였다.
2) Sn 함량이 증가함에 따라 판상모양의 금속간화합물 이 증가하였다. 또한 압축강도는 증가하였으나 연성은 감 소하였다. 지르코늄 3원계 합금의 탄성계수 값은 14 ~ 18 GPa이며, 이는 인체 뼈의 탄성계수 값(15 ~ 30 GPa)과 비 슷한 값을 가진다. 따라서 응력차폐효과를 극복할 수 있 는 생체재료로 활용될 수 있다.
3) Zr-7Cu-xSn 합금의 부식속도 mpy 값의 평균은 0.05로 대표적인 금속 생체재료인 Ti-6Al-4V 합금의 mpy 값인 0.5 보다 낮은 부식속도를 가져 높은 부식특성을 가진다.
4) 지르코늄 합금의 자화율 평균값은 Zr-7Cu-xSn 합 금(1.2 × 10-8 cm3g-1)로 Ti-6Al-4V 합금의 자화율 값(3.4 × 10-6 cm3g-1)보다 낮은 자화율을 가진다. 따라서 자기 공명영상(MRI) 진단에 용이한 생체재료로 활용될 수 있다.
5) 기계적, 자기적, 전기화학적 특성을 종합적으로 분 석한 결과, Sn의 조성에 따라 기계적 특성이 향상되고 부식특성은 감소하며, 자화율은 미소한 변화를 나타내었 다. 결과적으로 본 연구에서는 Zr-7Cu-10Sn 합금이 최 적의 특성을 나타내었다.