1. 서 론
최근 몇 년 동안 나노 재료는 벌크 재료와는 다른 독특한 광학 및 전자 ‧ 전기적 특성으로 인해 큰 관심을 끌고 있으며 전자소자, 광학소자, 센서 등 다양한 분야에서 응용이 기대되고 있다. 일부 금속 산화물에서 나노와이어, 나노로드, 나노튜브, 나노벨트와 같은 다양한 형태의 일차원 나노구조가 합성되고 있다. 이러한 길쭉한 결정 형태의 일차원 금속 산화물 나노구조는 고성능의 소형화된 나노소자를 개발하는 데 큰 도움이 된다.
일차원 금속 산화물 나노구조는 양자 효과 및 높은 종횡비와 같은 특징으로 인해 차세대 광전자 소자의 새로운 빌딩 블록으로 기대되고 있으며, 다이오드, 전계 효과 트랜지스터, 광검출기, 센서, 태양 전지 등에 활용될 것이다. 실제로 ZnO, SnO2, In2O3, MgO를 포함하는 금속 산화물의 일차원 나노구조를 이용하여 높은 효율을 갖는 에너지 하베스팅 및 변환소자, 발광 및 수광 소자를 개발하고 있다.
금속 산화물 중에서도 MgO 나노구조는 자외선(UV) 광검출기로 사용되며, 광촉매 활성이 우수하여 UV 광 조사하에서 메틸 오렌지 및 메틸렌 블루 염료의 분해에도 활용되고 있다.1,2) 환경 및 생의학 분야에도 응용 가능성이 높아 암세포에 대해 독성을 나타내어 암 치료에 활용될 수 있고, 요오드와 혼합하여 방부제로도 사용된다.3-5) MgO 나노구조는 폐수 처리에도 사용되며 중금속 이온의 제거 능력도 뛰어나다.6-8) 또한, 자기 센서에도 사용되는 등 스핀트로닉스 분야에서도 그 중요성이 증가하고 있다.9,10)
표면적이 넓고 표면 화학 반응이 뛰어난 MgO 나노구조를 합성하기 위해 에어로젤,11) 열 증발,12) 화학 기상 증착,13) 레이저 어블레이션,14) 졸-겔,15) 수열 합성법16) 등의 다양한 합성 방법을 사용하고 있다. 이 중에서도 열증발법은 공정이 용이하고 제조 비용이 저렴한 합성법이다. 열증발법을 이용한 금속 산화물 나노구조의 합성 과정에서는 합성 공정 중의 분위기 가스 내의 산소 농도도 나노구조의 형상에 영향을 주는 중요한 공정 변수이다. ZnO 분말에 다양한 탄소 소재 분말을 혼합한 원료를 열증발시켜 ZnO 나노구조를 합성한 연구 결과에 의하면, 큰 비표면적을 가진 활성탄소를 사용할 경우에는 표면활성도가 높기 때문에 높은 환원성 분위기가 형성되어 낮은 온도에서도 ZnO를 Zn으로 환원시키는 반응을 촉진해 여러 형태의 ZnO 나노구조를 용이하게 합성하였다.17) 따라서 비표면적이 큰 활성탄소는 적은 양으로도 산소 농도의 제어가 가능하여 열증발법으로 다양한 산화물 나노구조를 합성하는 데 매우 유용할 것이다. 한편, 나노구조의 특성은 형상에 따라 변할 수 있기 때문에 여러 응용 분야에 활용하기 위해 다양한 형상의 MgO 나노구조를 합성하려는 연구가 활발히 진행되고 있다.
본 논문에서는 대기 분위기의 단순한 조건에서 열증발법을 이용한 MgO 나노구조의 합성을 보고하며, 특히 다공성이기 때문에 비표면적이 큰 활성탄소를 원료 분말에 혼합함으로써 합성 공정 중의 산소 농도를 효과적으로 제어하여 여러 가지 형상의 일차원 MgO 나노구조를 합성할 수 있음을 보고한다.
2. 실험방법
MgO 나노구조를 제조하기 위하여 박스형 전기로를 사용하였다. 원료 분말로는 Mg 분말 0.5 g과 활성탄소 분말 0.1 g을 혼합한 분말을 사용하였다. 원료 분말을 알루미나 도가니에 넣고 박스형 전기로의 중앙에 놓았다. 그다음 전기로의 온도를 5 °C/min의 속도로 공정 온도까지 올리고, 공정 온도에서 1시간 동안 유지하였다. 그 후 전기로의 전원을 끄고 상온까지 냉각하였다. 공정 온도가 생성물의 성장에 미치는 영향을 살펴보기 위하여 700 °C, 850 °C, 1,000 °C, 1,100 °C로 공정온도를 변화시켜 실험을 수행하였다.
생성물의 형상은 전계방출형 주사전자현미경(FE-SEM, JSM-IT800, JEOL)으로 관찰하였고, 생성물의 구성 성분은 에너지 분산 X선 분광분석기(EDS, Ultim Max 100, Oxford)를 이용하여 분석하였다. X선 회절 분석기(XRD, X’pert PRO MPD, PANalytical)를 사용하여 생성물의 결정구조를 분석하였고, 푸리에 변환 적외선 분광기(FTIR, Nicolet iS10, Thermo-Fisher-Scientific)를 사용하여 생성된 물질을 확인하였다.
3. 결과 및 고찰
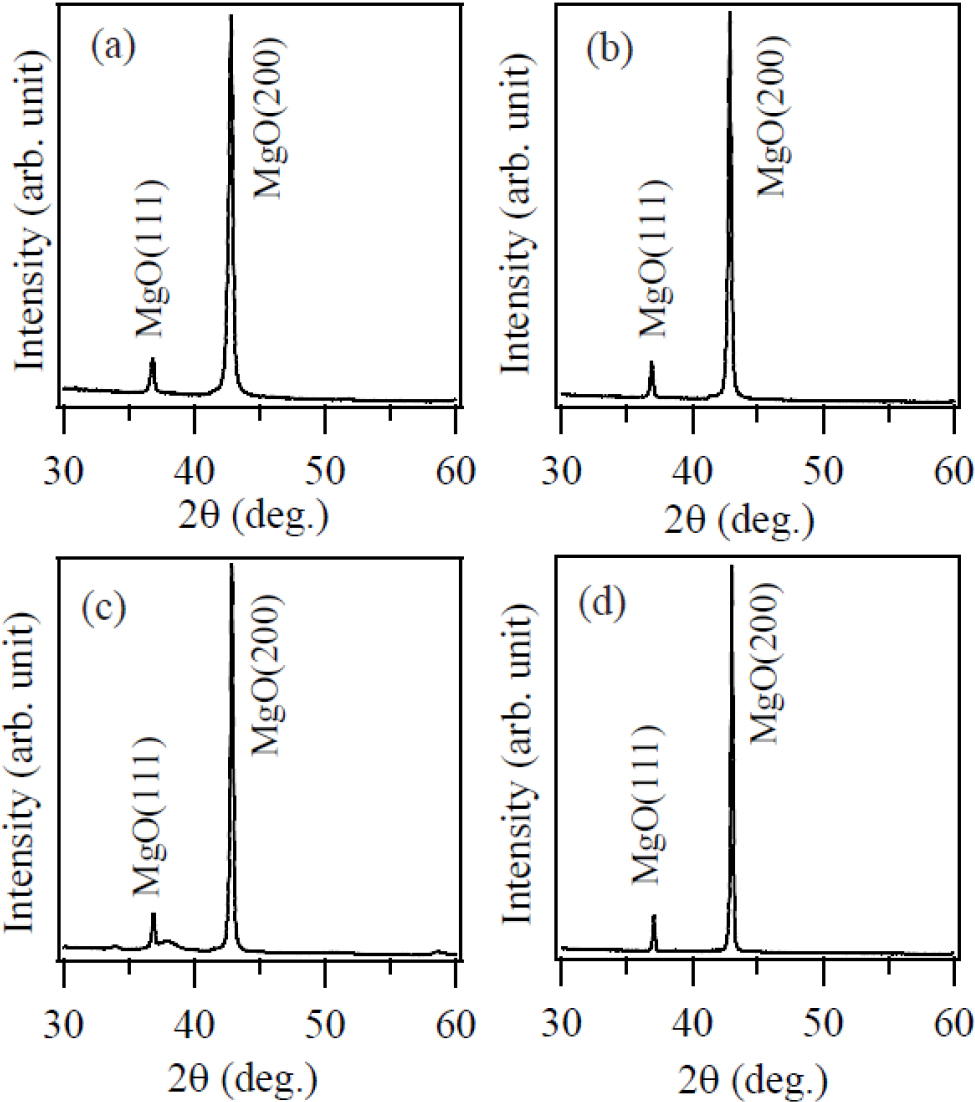
X선 회절(XRD)을 이용하여 생성물의 결정구조를 확인하였다. Fig. 1은 700 °C, 850 °C, 1,000 °C, 1,100 °C에서 생성된 생성물의 XRD 회절 패턴을 나타낸다. 관찰된 XRD 회절 패턴은 격자상수가 4.21Å인 입방정 결정구조를 갖는 MgO 결정의 회절 패턴과 잘 일치하였다. 2θ 회절각인 36.9°, 42.9°에서 나타난 회절 피크는 MgO의 결정면 (111), (200)에 해당한다. 불순물과 미반응 Mg와 관련된 회절 피크가 관찰되지 않았다는 분석 결과는 생성물이 순도가 높은 MgO임을 나타낸다.
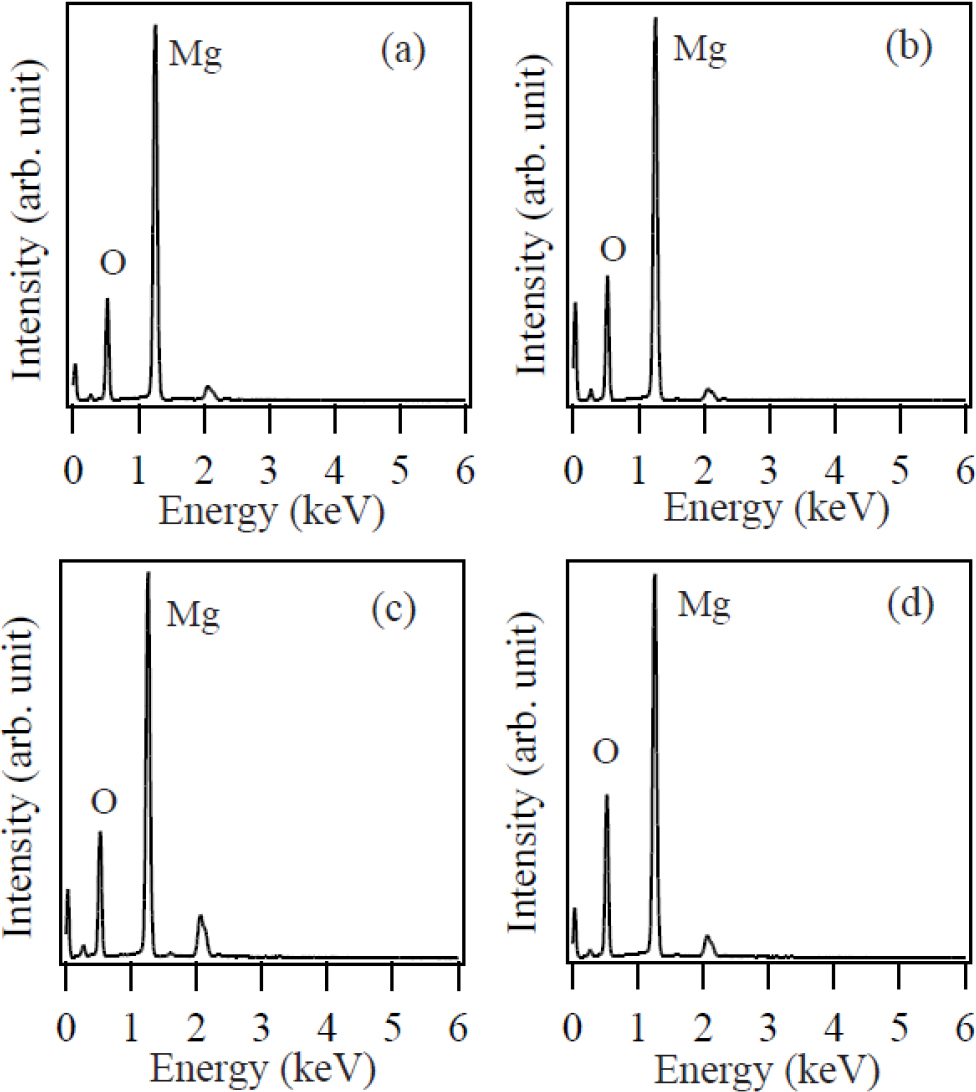
생성물의 구성 원소를 EDS를 이용하여 분석하였다. Fig. 2는 700 °C, 850 °C, 1,000 °C, 1,100 °C에서 생성된 생성물의 EDS 스펙트럼을 나타낸다. EDS 스펙트럼에서 Mg와 O를 제외한 다른 불순물과 관련된 피크는 관찰되지 않았다. 이로부터 생성물은 불순물이 없이 Mg와 O로만 구성되었음을 알 수 있었다. Mg와 O의 원자비는 약 1:1을 나타내었다.
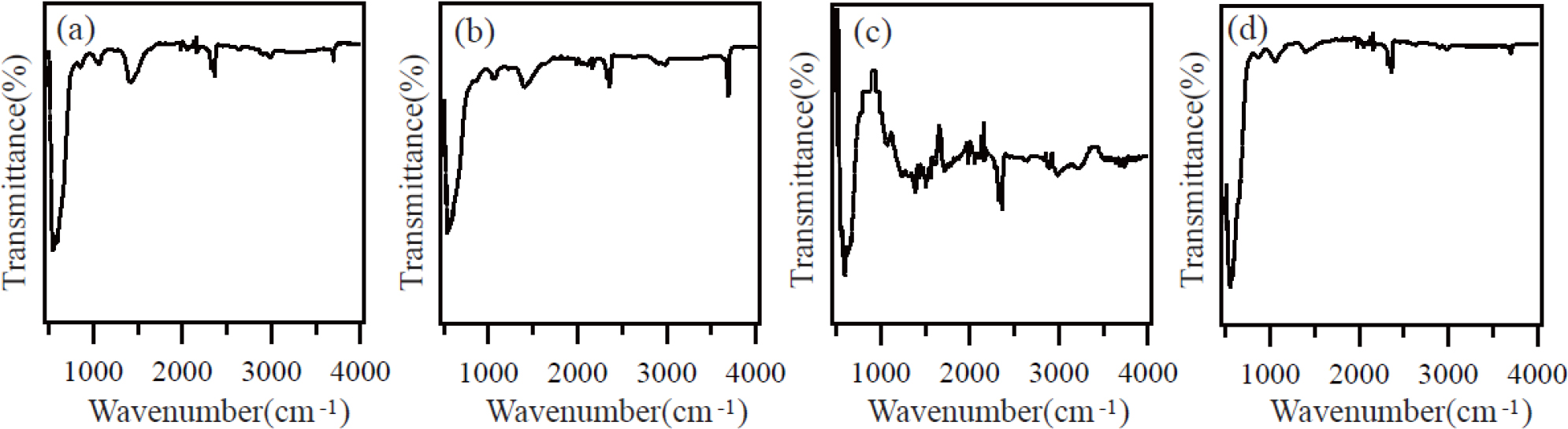
Fig. 3은 700 °C, 850 °C, 1,000 °C, 1,100 °C에서 생성된 생성물의 FTIR 스펙트럼을 나타낸다. 모든 생성물에 대해 550-580 cm-1 범위의 파수에서 흡수 피크들이 관찰되었다. 이 피크들은 Mg-O 결합의 신축 진동에 의한 흡수 피크로 생성물이 MgO임을 나타낸다.18,19)
생성물의 형상을 SEM으로 관찰하였다. Fig. 4는 700 °C, 850 °C, 1,000 °C, 1,100 °C에서 생성된 생성물의 SEM 이미지를 나타낸다. 700 °C에서 생성된 MgO에서 MgO 나노와이어의 성장이 관찰되었다. 나노와이어의 직경은 길이 방향에 대하여 변함없이 일정하였다. 나노와이어의 직경은 40~200 nm 범위의 크기를 가졌으며 길이는 수 µm부터 수십 µm의 크기를 나타내었다. 공정 온도에서의 유지 시간이 1시간이었기 때문에 결정핵이 생성된 시점에 따라 성장할 수 있는 시간이 다르게 되어 나노와이어의 직경에 차이가 생기게 되었다. 한편, 나노와이어의 표면은 매우 매끄러웠다. 850 °C에서 생성된 MgO에서는 성장 방향으로 폭이 점점 작아지는 형상의 일차원 나노구조가 관찰되었다. SEM 이미지로부터 알 수 있듯이 대부분의 일차원 나노구조는 두께가 매우 얇은 벨트 형상의 나노구조였다. 나노벨트의 확대 사진을 Fig. 5(a)에 나타내었다. 반투명할 정도로 두께가 매우 얇음을 알 수 있다. 나노벨트의 폭은 밑면이 약 2.3 µm이며 길이 방향에 따라 점점 줄어들어 300 nm까지 감소하였다. 나노벨트의 표면은 매우 매끄럽고 평탄하였다. 1,000 °C의 조건에서는 벨트 형상이 아닌 와이어 형상을 가진 MgO 결정이 관찰되었다. 그러나 850 °C의 조건에서 성장한 나노벨트와 같이, 성장할수록 와이어의 직경이 점점 감소하는 양상을 보인다. 850 °C에서 성장한 나노벨트와 비교하기 위하여 확대한 SEM 이미지를 Fig. 5(b)에 나타내었다. 1,000 °C에서 성장한 MgO 와이어는 마이크로-미터 크기를 나타내며, 밑면의 직경은 약 1.2 µm이며 성장 방향을 따라서 600 nm까지 감소하였다. 길이는 약 10 µm를 나타내었다. 1,100 °C의 온도에서는 나노와이어가 관찰되었으나 표면이 거칠고 길이 방향을 따라서 매듭들이 관찰되었다. 나노와이어의 직경은 150~350 nm의 크기를 가지고 있었으며 길이는 십수 µm의 크기를 나타내었다. 거친 표면을 가진 MgO 나노구조가 촉매의 효과를 높인다고 알려져 있기 때문에 거친 표면을 가진 MgO 나노구조의 합성에 관한 관심이 높아지고 있다. 들쭉날쭉한 또는 매듭 모양을 한 MgO 나노와이어는 관찰하기가 어려운 일차원 형상으로 다양한 응용이 기대된다.
공정 온도가 700 °C에서 850 °C, 1,000 °C, 1,100 °C로 증가함에 따라 MgO 나노구조는 성장 방향을 따라 직경의 변화가 없고 표면이 매끄러운 와이어 형상에서 성장 방향으로 폭이 점점 좁아지는 벨트 형상으로, 그리고 성장 방향을 따라 점점 가늘어지는 와이어 형상으로 1,100 °C의 고온에서는 직경의 변화는 없으나 표면에 매듭 모양을 한 와이어 형상으로 변하였다. 공정 온도에 따라 다양한 형상의 MgO 나노구조가 성장하였다.
온도에 따른 MgO 나노구조의 형상 변화는 성장 물질의 농도와 흡착 원자의 확산 속도(거리)와 연관이 있을 것으로 생각된다. 낮은 온도인 700 °C의 경우에는 형성되는 MgO 증기의 농도가 낮아 MgO 결정핵의 표면에 흡착한 MgO 분자가 먼 거리까지 확산이 가능하여 표면 확산을 통하여 와이어 형상으로 성장하였을 것으로 생각된다. 또한 낮은 온도에서는 산소와 반응하지 못한 Mg 또는 MgOx (x < 1) 증기의 농도가 MgO 증기의 농도보다 높을 것이며 MgO 결정핵의 표면에서는 MgO 분자보다 Mg 원자의 확산 속도가 빠르기 때문에 폭은 좁고 길이가 매우 긴 와이어 형상으로 성장하였을 것으로 추론된다. 온도가 850 °C로 증가함에 따라 Mg보다 확산 속도가 느린 MgO 증기의 농도가 증가하고 MgO 결정핵의 표면에 흡착한 MgO 분자의 표면 확산 속도가 느리기 때문에 결정의 폭 방향으로의 성장도 증가하게 된다. 또한 Mg 원료 분말의 표면에서 생성된 MgO 결정핵에서는 원료 분말 표면에서의 MgO 증기 농도가 높기 때문에 결정의 윗부분보다는 밑부분에서 폭 방향으로의 성장이 가장 빠르게 일어나게 되어 결정이 성장하면서 길이 방향으로 폭이 점점 가늘어지는 양상이 나타난다. 한편, 입방정 결정구조를 가진 MgO 결정에서 (200) 결정면이 가장 낮은 표면에너지를 가지고 있기 때문에 MgO 결정의 측면성장(lateral growth)이 강화되면서 (200) 결정면과 평행한 폭 방향으로 결정 성장 속도가 증가하여 벨트 형상의 결정으로 성장한 것으로 추론된다. 온도가 1,000 °C로 증가하게 되면 결정 표면에 흡착된 MgO 분자의 확산 속도도 증가하고, MgO 증기의 농도도 크게 증가하기 때문에 결정면에 대해 수직 방향으로의 성장(vertical growth)이 강화되어 벨트 형상이 아닌 와이어 형상으로 바뀌며, 또한 길이 방향으로의 와이어 폭의 차이도 줄어들게 된다. Liang et al.20)의 연구 결과에서도 ZnS 분말을 열증발시켜 생성된 ZnS 나노구조에서 ZnS 증기 농도의 차이로 인해 나노벨트와 나노시트 등의 측면 성장 속도가 증가하여 생성된 나노구조로부터 수직 성장 속도가 증가하여 생성된 나노로드로 형상이 변하였다. 또한, 열증발법을 이용한 CdS 일차원 나노구조의 성장에 관한 Kar and Chaudhuri21)의 연구 결과에서도 성장 온도가 증가할수록 나노구조의 형상이 나노선에서 나노벨트로 다시 나노로드로 변하였다. 이 연구 결과는 MgO 나노구조의 형상 변화에 미치는 성장 온도의 영향에 관한 본 실험의 결과와 매우 유사하다. 온도가 1,100 °C로 더욱 증가하면 결정 표면에서의 MgO 분자의 확산 속도가 더욱 크게 증가하여 폭은 좁고 길이 방향으로의 폭도 균일하며 길이는 수 µm 크기를 가진 와이어 형상으로 성장하였다. 그러나 와이어의 표면이 거칠며 마치 매듭들로 연결된 형상을 보인다. 1,100 °C에서 성장한 매듭 형상의 와이어와 700 °C에서 성장한 표면이 매끄러운 와이어와는 성장 거동이 다르다는 것을 알 수 있다. Sheela22)의 보고에 의하면, Zn과 Mg 같은 저융점 금속의 경우에는 생성된 나노입자들이 방향성 결합(orientation-attachment)을 함으로써 나노와이어를 형성할 수 있다고 하였다. 나노입자들의 방향성 결합으로 나노와이어의 성장이 일어날 경우, 나노와이어의 표면이 구불구불하게 된다고 한다. 따라서 본 실험의 1,100 °C 조건에서 생성된 MgO 나노와이어도 MgO 나노입자들의 방향성 결합을 통해 성장하여 마치 매듭들로 연결된 형상이 된 것으로 추론된다.
Fig. 5는 850 °C에서 성장한 벨트 형상과 1,000 °C에서 성장한 와이어 형상의 결정을 비교한 SEM 이미지이다. 두 결정 모두, 결정이 성장하면서 폭이 점점 작아지는 형상을 나타내고 있으나 850 °C에서 성장한 일차원 나노구조의 성장 방향으로의 결정 폭의 차이가 1,000 °C에서 성장한 일차원 나노구조의 결정 폭의 차이보다 크다는 사실을 알 수 있다. 또한, 850 °C에서 성장한 일차원 나노구조는 벨트 형상을 나타내고 있기 때문에 폭 방향으로의 측면 성장 양식이 강화되었음을 알 수 있다.
Fig. 6은 700 °C와 1,100 °C에서 생성된 나노와이어를 비교한 SEM 이미지이다. SEM 이미지로부터 두 조건에서 성장한 나노와이어의 성장 거동이 다르다는 것을 알 수 있다. 700 °C에서 성장한 나노와이어는 매끈한 표면을 가지고 있다. 이는 Mg의 표면 확산을 통해 성장하였기 때문이라고 추론되며, 1,100 °C에서 성장한 나노와이어는 매듭으로 연결된 형상을 나타내고 있다. 이는 나노입자들이 결합하여 성장한 것으로 추론된다. 특히, 매듭 형상을 한 나노와이어는 비표면적이 매우 크다는 것을 고려할 때 활용 범위가 넓다.
모든 공정 온도에서 성장한 일차원 나노구조들의 끝부분에는 촉매로 생각되는 구형의 입자가 관찰되지 않았기 때문에 일차원 나노구조들은 기상-고상 성장기구(vapor-solid growth mechanism)에 따라 성장하였다고 판단된다.
4. 결 론
Mg와 활성탄소의 혼합 분말을 대기압의 공기 분위기에서 열증발시킴으로써 일차원 MgO 나노구조를 합성하였다. 일차원 MgO 나노구조의 형상은 합성 온도에 따라 크게 변하였다. 합성 온도가 증가함에 따라 나노구조의 형상이 나노와이어에서 성장 방향에 따라 폭이 줄어드는 나노벨트, 성장하면서 폭이 감소하는 와이어, 매듭이 연결된 형태의 나노와이어로 변하였다. 나노구조의 형상 변화는 합성 온도에 따른 성장물질의 농도와 결정핵 표면에 흡착된 원자의 확산 속도(거리)의 변화로 설명할 수 있었다. MgO 나노구조들은 입방정 결정구조를 가지고 있었고, 높은 순도를 나타내었다. 나노구조는 기상-고상 성장기구에 의해 성장하였다고 판단된다. Mg와 활성탄소를 혼합한 분말의 열증발을 이용한 MgO 나노구조의 합성 공정에서 MgO 나노구조의 형상에 미치는 합성 온도의 중요한 역할과 온도 변화에 따른 나노구조의 성장 메커니즘의 변화에 대해 이해하였다. 본 연구 결과는 더욱 다양한 형상의 MgO 나노구조를 합성하는 데 기여를 할 것으로 기대된다.