1. 서 론
LED(Light Emitting Diode)를 이용한 백색 발광 방식 중에서 pc-LED(phosphor converted Light Emitting Diode) 는 저전력, 높은 효율, 긴 수명시간 등의 특징으로 인하 여 차세대 디스플레이의 광원이나 조명 장치로써 많이 응용되고 있다.1,2) 통상적으로 백색 LED를 제작할 때는 InGaN의 청색 LED 칩 위에 황색의 YAG:Ce 형광체를 도포하는 방법이 주로 사용된다. 하지만 청색과 황색의 두 가지 색으로는 가시광 영역인 적색을 표현 할 수가 없기 때문에, 이 조합에 의한 백색 LED는 연색성이 낮 고 색재현 범위가 좁으며 색온도가 높다는 문제를 가지 고 있다.3-5) 이러한 단점을 극복하기 위한 방안으로 산 화물, 산질화물, 그리고 질화물 계열의 모체 조성에 Eu2+ 이 첨가 된 Sr2Si5N8:Eu2+, CaAlSiN3:Eu2+ 등의 적색형광 체가 개발 되었다.6,7) 그러나, 질화물계열의 형광체를 합 성하기 위해서는 고온 및 고압이 필요한 것으로 알려져 있어, 이는 대량합성이나 제조의 경제성 면에서 큰 문 제가 되고, 또한 희토류 금속 성분인 고가의 Eu2+을 활 성제로 사용하기 때문에 형광체의 가격이 높아질 수 밖 에 없다. 게다가 Eu2+이 첨가된 질화물 적색형광체는 넓 은 밴드형의 발광 스펙트럼을 나타내므로 사람의 눈이 감지할 수 없는 650 nm 보다 긴 장파장 영역의 빛은 손 실로 이어지며 녹색 및 황색 영역의 발광에 대해서 재 흡수가 일어나서 광 효율을 저하시킨다는 단점이 있다.8)
최근에 이러한 문제점을 극복할 수 있는 발광물질로써 A2MF6:Mn4+(A = Na, K and M = Si, Ti 등)의 불화물계 형광체들에 대해서 합성 및 디스플레이 응용을 위한 연 구들이 활발하게 수행되어 왔다.9-11) Mn4+ 이온을 활성제 로 하는 형광체에서 발광 중심파장은 모체 조성에 따라 의존한다. 예로서, 불화물계 형광체들은 630 nm 주위의 적색 발광파장을 나타내며 산화물 모체들에서는 보다 장 파장 영역(605-720 nm)에서 심적색의 발광을 하는 것으 로 알려져 있다.12-13) Mn4+ 활성 K2TiF6 적색형광체는 360 nm 부근과 450 nm 부근에 두 가지 넓은 밴드형의 흡수 스펙트럼을 가지며 중심파장이 635 nm이고 반치폭 (FWHM < 10 nm)이 매우 좁은 발광 스펙트럼을 나타낸 다. 이에 따라 450 nm 청색 LED 칩에 응용이 가능하며 적색 영역에서 반치폭이 좁은 발광특성으로 인하여, 이 형광체를 이용하여 제조되는 백색 LED는 넓은 색재현 범위와 낮은 색온도를 구현할 수 있다. 현재까지 보고된 불화물 적색형광체의 대표적인 합성방법으로 불산을 이 용한 실리콘 산화물의 식각방법과14) 불산 용액 하에서 결 정화하는 방법15,16) 등이 알려져 있다. 최근 Chen17) 등 이 양이온 교환반응을 이용하는 새로운 합성 방법으로 K2TiF6:Mn4+ 형광체를 합성하여 양자효율 98 %, 높은 CRI(Ra = 81) 및 낮은 색온도(3556K)를 구현했다는 보고 가 있었지만, 합성에 있어서는 여전히 다루기 어려운 불 산을 사용한다는 점이 문제로 남는다. 불산은 끓는 점 이 19.5 °C로 휘발성이 강하고 강력한 자극성을 갖는 물 질이고 이러한 자극성은 인체에 노출시 심각한 위해를 초래한다. 저 농도의 불산(수 ppm)이라도 인체에 중독될 경우 눈과 호흡기, 위장 등에 자극에 의한 염증이 생기 고, 고 농도의 불산에 누출이 되면 뼈 조직에 침투하거 나 칼슘 이온과 결합하는 등 인체에 치명적인 문제를 유 발하기 때문에 최근 산업적으로 불산 사용이 기피되고 있다.18)
이에 따라 본 연구에서는 취급이 기피되는 불산 사용 없이 합성하는 방법을 고안하여 K2TiF6:Mn4+ 불화물 형 광체의 합성을 시도하였다. 일반적으로 용액반응을 이용 하여 합성 시 사용되는 HF와 TiO2를 대신하여 NH5F2 와 TiF4를 사용하였다. 정량분석을 통해 첨가된 망간의 양과 실제 형광체에 함유되는 망간의 양을 비교하였으 며 망간 첨가량을 변화시키면서 최적의 활성제 농도를 조사하였다. 온도 변화에 따른 발광특성과 잔광시간을 측 정하였다. 또한 합성된 적색형광체와 상용의 녹색형광체 를 혼합해 청색 LED 칩에 도포하여 백색 LED를 제조 하여 전계 발광 특성을 조사하였다.
2. 실험 방법
TiF4, NH5F2, KF 또는 KHF2 그리고 K2MnF6 분말을 이용하여 고안된 간단한 침전반응을 이용하여 K2TiF6:Mn4+ 형광체를 합성했다. 먼저 TiF4(Aldrich, 99.9 %) 분말 4.2 mmol과 NH5F2(Aldrich, 99 %) 분말 0.1 mmol을 증류수 2 ml에 첨가하고 30분 동안 교반하여 TiF4/NH5F2 용액 을 만들었다(A 용액이라 칭함). 이와는 별도로 KHF2 (Alfa Aeser 99 %) 또는 KF(Aldrich, 99 %) 분말 4.2 mmol, 그리고 K2MnF6 분말을 정해진 망간의 몰 비(1.5- 10.5 mol%)만큼 칭량하여 폴리프로필렌 비이커(Nalgene) 에 담았다. 그리고 위에서 제조된 A용액을 상기 용기에 가한 후 20시간 교반시켰다. 다음으로 진공여과기를 이 용해 형성되는 침전물과 여액을 분리시키고 소량의 에 탄올을 이용해 침전물을 3회 세정하였다. 얻은 침전물을 70 °C 진공오븐에서 3시간 동안 건조하여 K2TiF6:Mn4+ 형 광체를 수득하였다. 형광체를 합성할 때 활성제의 원료 로 사용되는 K2MnF6 분말은 KHF2와 불산으로 이루어진 용액에 KMnO4를 용해시키고 환원제로 과산화수소(H2O2) 를 조금씩 천천히 가하여 생성되는 침전물을 여과 및 건 조시켜 얻는 Bode의 방법을 이용해 제조하였다.19)
합성된 형광체의 결정구조는 JADE software를 이용하 여 X선 회절분석법(XRD)을 이용하여 분석하였으며, 측 정 장비는 Rigaku D/MAX-2200으로 40 kV와 40 mA의 측정 조건을 적용하였다. 형광체의 입자 형상을 관찰하 기 위해 TERACAN사의 전계 방사형 주사전자현미경 (Field-emission scanning electron microscope, FE-SEM) Mira 3 LMU FEG 모델을 이용하였으며, 각각의 원소 분포를 관찰하기 위하여 에너지 분산형 분석기(Energy dispersive spectroscopy) Bruker Quantax 200 모델을 이용하였다. 또한, 형광체에 함유된 Mn4+의 함유량 분 석을 위하여 ICP-AES(Thermo scientific iCAP 7400) system을 이용하였다. 형광체의 발광 특성은 제논(Xe) 램 프를 사용한 PSI photoluminescence system을 이용하여 측정하였고, 온도 의존 특성을 평가하기 위해 자체 제 작한 승온 장비를 이용하였다. 제조된 형광체를 형광체 변환 LED로 제작하여 전계 발광 특성을 조사하였다. 녹 색과 적색 형광체의 비율을 6 : 4로 고정하고 에폭시 (Dowhitech Co., EG6301A)와 경화제(EG6301B)가 1 : 1 의 부피비로 혼합한 결합 수지를 청색 LED 칩 위에 봉 지하였고 160 °C에서 12시간 동안 소성시켜 백색 LED 칩을 제작하여 적분구 내에서 관찰하였다.
3. 결과 및 고찰
고안된 합성공정에서는 불산 사용을 배제시키기 위해 서 불산을 대신하여 NH5F2를 물에 용해시켜 용액으로 제 조하여 반응용액으로 사용하였다. 활성제 원료로 첨가되 는 K2MnF6가 물과 만나면 실온에서도 KF, HF 및 MnO2 로 가수분해가 일어나게 되어 불화물 모체 성분에 도핑 될 수 없다. 식(1)에 K2MnF6와 물이 만나서 일어나는 가수분해 반응식을 나타내었다.
이러한 K2MnF6의 가수분해를 방지하기 위해서는 반응 시에 용액에 F− 이온이 일정 농도 이상으로 존재하게 함 으로써 공통이온 효과로 인하여 K2MnF6의 가수분해 반 응을 억제시킬 수 있기 때문에 NH5F2를 첨가하였다.20) 실제로 K2MnF6를 각기 증류수와 0.1 M NH5F2 수용액 에 넣고 1시간 경과 후에 비교하였을 때, 증류수에서는 K2MnF6의 가수분해가 일어나 검정색의 MnO2 침전물을 형성하였으나 NH5F2 수용액에서는 가수분해 반응 없이 황색의 K2MnF6 그대로 유지됨을 알 수 있었다.
불산을 사용하지 않는 침전반응으로 합성되는 K2TiF6: Mn4+ 형광체에 대해 첨가되는 Mn4+의 양과 실제 형광 체에 함유되는 Mn4+ 양에 차이가 있을 수 있으므로 정 량분석을 수행하여 Mn4+의 함유량을 분석하여 Table 1 에 나타내었다. 4.5, 6, 7.5, 9 및 10.5 mol%의 Mn4+이 첨가되어 합성된 형광체의 경우에 실제 Mn4+ 함유량은 각기 4, 5.6, 6.9, 8.2 및 9.5 mol%이다. 즉, 실험된 전체 농도범위에서 Mn4+의 첨가량에 대해 실제로는 대략 92 %의 Mn4+이 형광체에 함유된다는 것을 나타낸다. 이는 K2TiF6 성분이 수용액에서 약간의 용해성을 가지기 때문 으로, 불산을 사용하여 같은 형광체를 합성하는 경우에 도 유사한 경향을 나타내는 것으로 알려져 있다. 반응 으로 형성되는 침전물과 분리되는 여액에서 Mn과 Ti의 함량을 비교해보면, 여액으로 빠져나가는 Ti의 양은 평 균 7 %이었고 Mn4+의 양은 평균 10 %로 평가되었다. 실 제 Mn4+의 첨가량에 대해 형광체에의 실제 함유량은 약 92 %를 나타내므로, 최대 발광강도를 나타내는 6.9 mol% Mn4+을 형광체에 함유되도록 하기 위해서는 여분의 Mn4+ 이온 첨가가 필요하여 7.5 mol%의 Mn이 첨가되어야 하 는 것으로 계산된다. 상기의 서술에서, 용액반응에서는 모 체 성분인 Ti와 활성제인 Mn의 용해도가 각각의 농도 에서 약간씩 다르다는 문제가 있기 때문에, 이후 서술 에서는 형광체에서의 Mn 농도를 최초 첨가량 기준으로 하여 표기하였다.
Table 1.
ICP analysis results for the Mn4+ content in the synthesized K2TiF6:Mn4+ phosphors.
| Additive Mn4+ amount (mol%) | 4.5 | 6 | 7.5 | 9 | 10.5 |
|---|---|---|---|---|---|
| Mn4+ amount contained in K2TiF6:Mn4+ (mol%) | 4 | 5.6 | 6.9 | 8.2 | 9.5 |
첨가되는 Mn4+의 농도를 1.5-10.5 mol% 사이에서 변 화시키며 합성된 K2TiF6:Mn4+ 형광체들에 대한 X-선 회 절패턴을 Fig. 1에 나타내었다. 그리고 불화물 형광체의 일반적인 합성법인 불산을 이용하여 합성된 형광체에 대 한 회절패턴도 제시하였다. K2TiF6:Mn4+ 형광체들의 X- 선 회절패턴들은 불산에서 제조된 Fig. 1(f)에 제시된 회 절패턴과 일치하는 것을 알 수 있다. 즉, Mn4+의 함량 이나 불산 사용유무에 관계없이, 합성된 모든 형광체 분 말이 불순물 상 없이 JCPDS #00-008-0488의 X-선 회 절패턴과 정확히 일치함으로써 형광체들이 단일상으로 얻 어졌음을 확인할 수 있다. Mn4+의 공급원으로 사용된 K2MnF6에 의한 X-선 회절피크가 관찰되지 않기 때문에 Mn4+이 모체에 잘 치환되었음을 알 수 있다. Chen 등 은 모체인 K2TiF6가 결정학적으로 육방정계(Hexagonal system)의 결정 구조로 단위 격자의 격자상수가 a = 4.67 Å, b = 5.74 Å이고, p-3ml의 공간군에 해당하며 한 개의 Ti4+ 이온이 6개의 F− 이온에 의해 둘러싸여 있는 구조 임을 보고하였다.17) K2TiF6 모체 결정에서 Mn4+ 양이온 이 치환되는 자리로 K+ 자리와 Ti4+ 자리를 고려할 수 있으나, Mn4+ 이온의 반지름(0.052 nm)이 Ti4+의 반지름 (0.064 nm)과 크기가 비슷하며, 같은 전이금속 이온으로 동일한 원자가 상태를 가지기 때문에 K+(0.133 nm) 자 리가 아니라 Ti4+ 자리에 치환이 일어난다고 보아야 한다.
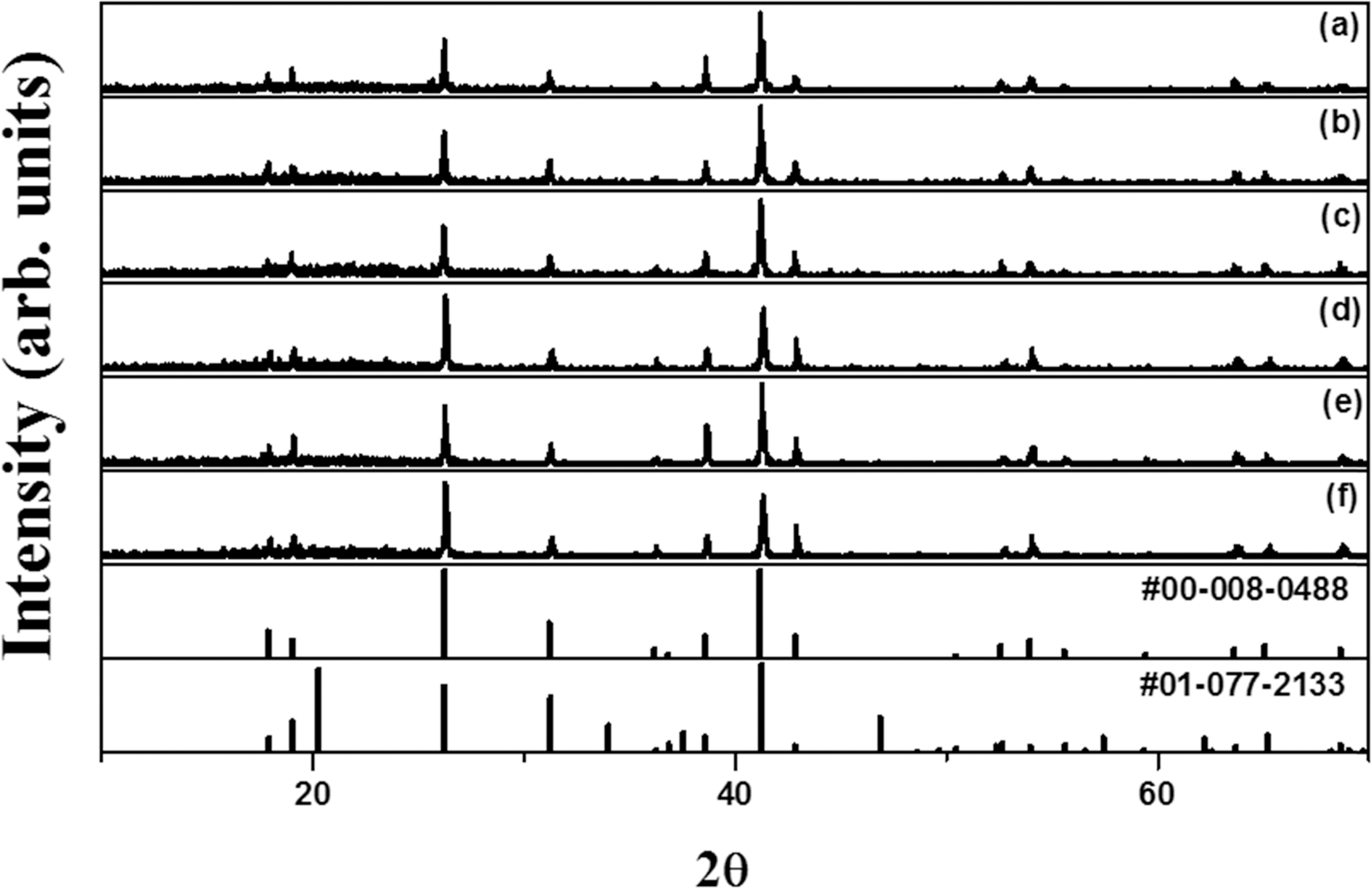
Fig. 1.
XRD patterns of the K2TiF6:Mn4+ phosphors synthesized with HF-free (a-e) and HF solution (f).
Fig. 2에 합성방법에 따른 K2TiF6:Mn4+ 형광체 분말들 의 형상을 비교하기 위하여 측정된 SEM 사진을 제시 하였다. NH5F2를 사용하여 합성된 Fig. 2(a)의 경우에 5- 30 μm로 입자크기에 있어서는 입자들 간에 상당한 차이 가 있으나 전체적으로 매끈한 표면 상태를 보여주고 있 다. 이와는 다르게 불산을 사용하여 합성된 형광체에서 는 Fig. 2(b)에서와 같이 입자크기 면에서는 약 30 μm 의 큰 입자들로 상대적으로 크고 비교적 균일하다. 하 지만 입자형상 면에서는 일정한 다면체의 형태를 보여 주지만, 표면 상태를 보면 입자에 따라 매우 거친 표면 상태를 나타내는 것이 관찰된다. 이러한 현상은 불산에 서 형광체가 합성될 때, 일부 형광체 입자의 표면에서 강한 산성 용액에 의한 화학적 식각작용이 일어나기 때 문인 것으로 보고되고 있다.21) 한편, Fig. 2(c-f)는 NH5F2 를 사용하여 합성된 K2TiF6:Mn4+ 형광체에 대한 EDS (Energy Dispersive Spectroscopy) 사진 결과로서 K, Ti, Mn 과 F의 모든 원소들이 각 입자의 전 영역에 걸쳐 뭉쳐져 있지 않고 고르게 분포되어 있음을 보여 주는 것 으로, 고안된 합성법에 따른 K2TiF6:Mn4+ 형광체 제조 시에 각 조성 성분들이 균일하게 분포한다는 것을 시사 한다.

Fig. 2.
SEM images of the K2TiF6:Mn4+ phosphors synthesized with HF-free (a) and HF solution (b) and EDS mapping results of K2TiF6: 0.075Mn4+ sample (c-f).
합성방법에 따른 K2TiF6:Mn4+ 형광체들의 흡수 및 발 광 스펙트럼을 비교해서 Fig. 3에 나타내었다. Mn4+ 활 성제의 흡수 및 발광원리는 d3의 Tanabe-Sugano diagram 을 통해 서술이 가능하다.22) 먼저 바닥상태 4A2 에너지 준위에 있는 전자가 외부의 에너지를 받아 4T1, 4T2의 에 너지 준위로 들뜨게 되고(spin-allowed transition), 이러 한 전자들은 비복사 전이(non-radiative transition)을 통해 2Eg의 에너지 준위로 낮아지게 된다. 이 전자 상태로부 터 다시 복사 전이(radiative transition)가 일어나면서 4A2 바닥상태로 돌아오면서 에너지 방출이 일어나는데, 이 때 방출하는 에너지가 Mn4+의 발광 스펙트럼으로 나타나게 된다. Mn4+ 이온을 활성제로 하는 형광체에서 산화물계 형광체인 SrTiO3:Mn4+의 발광은 중심파장이 723 nm 이 고 불화물계 형광체 Na2SiF6:Mn4+ 의 발광 중심파장은 617 nm로, Mn4+ 활성제는 모체 조성에 의존하여 발광파 장이 변화된다.23) 이것은 Mn4+의 발광이 Tanabe-Sugano diagram에서 확인할 수 있는 것처럼 주위 이온의 결정 장(crystal field)에 의한 2Eg→4A2 전이의 에너지 차이 가 크지 않으므로 결정장 보다는 공유성(covalency)에 의 한 차이에서 기인하는 것으로 유추된다. 불화물과 산화 물에서 F− 이온이 상대적으로 높은 이온성을 가져 구름 퍼짐효과(nephelauxetic effect)가 크지 않아 단파장에서의 발광을 초래하는 반면에 O2− 이온은 F− 이온보다 상대 적으로 강한 공유성으로 인하여 구름퍼짐효과가 강해서 적색이동(red shift)을 유도하여 상대적으로 장파장 영역 에서 발광하게 되는 것으로 설명된다. Fig. 3에서 볼 수 있는 바와 같이, 불화물계인 K2TiF6:Mn4+ 형광체는 580- 660 nm 영역 사이에 반치폭이 매우 좁고 중심파장이 635 nm인 적색 발광을 하게 된다.24) 한편, 이 형광체의 흡 수 스펙트럼은 2개의 넓은 띠 형태의 흡수 피크들로 구 성되어 있음을 볼 수 있다. 360 nm 파장 부근의 흡수 밴 드는 4A2→4T1에 의한 흡수이며 465 nm 부근의 밴드는 4A2→4T2에 의한 흡수에 기인한다. K2TiF6:Mn4+ 형광체 의 발광 스펙트럼은 3개의 매우 좁은 발광피크(620, 635 및 652 nm)들로 구성되어 있음을 볼 수 있는데, 이는 전 형적인 Mn4+ 이온의 2Eg→4A2 전이로부터 기인되는 발 광이다. 합성방법에 따른 발광강도를 비교해보면, 불산 대 신 NH5F2를 사용하여 합성하더라도 형광체의 발광강도가 불산을 사용한 경우에 비교하여 약 80 % 이상의 상대 발 광강도를 나타내면서 발광 및 흡수 스펙트럼은 패턴에 있어 아무런 차이를 보이지 않는다. 발광강도에서의 그 러한 차이는 NH5F2를 사용해 합성된 경우에 불산 사용 의 경우보다 각 입자들의 입자크기가 불균일하고 특히 상대적으로 입자크기가 작기 때문인 것으로 생각된다. 이 로부터 아직 불산을 사용한 합성에 비해 발광강도를 개 선시켜야 하는 문제점이 있지만 고안된 방법에 따라 불 산의 사용 없이 K2TiF6:Mn4+ 적색형광체를 합성할 수 있 음이 명백하다.
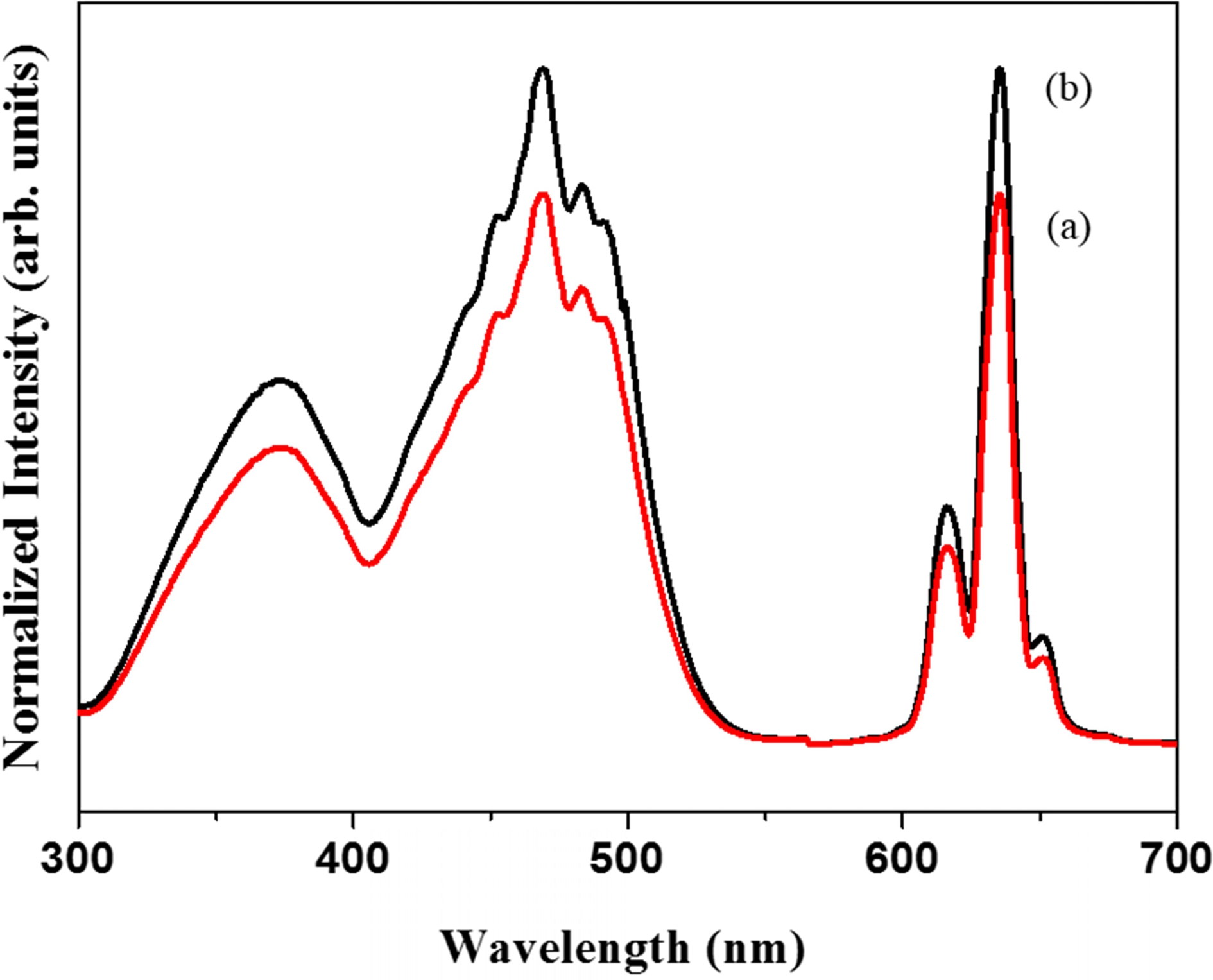
Fig. 3.
Excitation and emission spectra of the K2TiF6:0.075Mn4+ phosphor (a) synthesized with HF-free and the K2TiF6:0.09Mn4+ synthesized with HF solution (b).
K2TiF6:Mn4+ 형광체의 합성을 위해서 K+의 원료로는 KF와 KHF2를 고려할 수 있다. 이 두 종류의 원료에 대 해 형광체의 합성과 발광강도에 미치는 영향을 비교하 였다. Fig. 4에 K+ 원료에 따라 합성된 형광체의 발광 스펙트럼을 제시하였고, 얻어진 형광체 분말들의 사진을 비교하여 나타내었다. 발광 스펙트럼에서 K+ 원료에 따 른 (a)와 (b)를 비교하여 보면 스펙트럼의 패턴에는 차 이가 없지만 발광강도에서는 큰 차이를 보이고 있음을 알 수 있다. 이것은 KF와 KHF2가 용해됨으로써 반응 용액에서 F− 이온의 농도 차이를 유발하기 때문인 것으 로 볼 수 있다. KF를 사용하는 경우에 K2TiF6 합성을 위해 KF와 TiF4가 2:1의 당량비로 유지되어야 함으로 생 성되는 형광체 성분을 제외하고 용액 속에 F− 이온이 남 아 있지 않게 된다. 하지만 KHF2 원료의 경우에는 KHF2 와 TiF4가 2:1의 당량비로 합성될 때 형광체로 침전되고 나서도 여분의 F− 이온이 용액에 남아있게 됨으로써, 이 에 따라 F− 이온의 공통이온효과에 의해 K2MnF6의 가 수분해를 방지할 수 있어 결과적으로 높은 발광강도를 나타내는 것으로 해석할 수 있다. 합성된 형광체 분말 의 사진을 비교해 보더라도 KF를 사용한 (c)의 경우 어 두운 황색을 나타내지만, KHF2를 사용한 (d)의 경우에 는 훨씬 밝은 황색을 보여준다. 이는 KF를 원료로 사 용 시에 일부의 K2MnF6가 가수분해되어 MnO2로 침전 화되기 때문에 발생하는 것으로 볼 수 있다. 즉, K2TiF6:Mn4+ 형광체의 합성을 위해서 K+ 원료는 KHF2가 적합 하며 침전반응에 의해 불화물 형광체를 합성할 때 반응 용액에 여분의 F− 이온을 존재하게 함으로써 활성제 원 료인 K2MnF6의 가수분해를 막는 것이 매우 중요하다는 것을 알 수 있다.
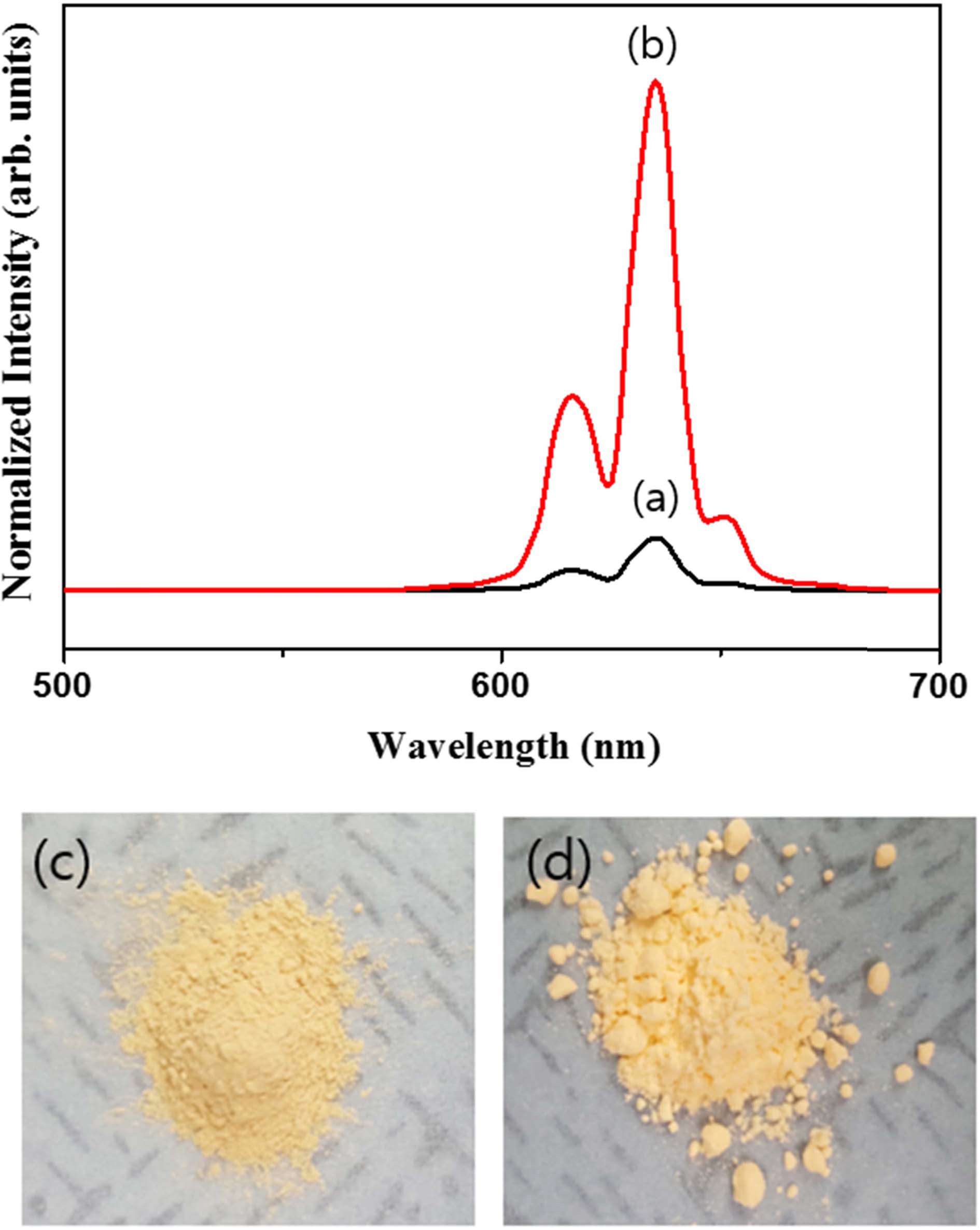
Fig. 4.
PL emission spectra and body colors of the K2TiF6:0.015Mn4+ phosphors synthesized using KHF2 (b, d) or KF (a, c) as a K+ source.
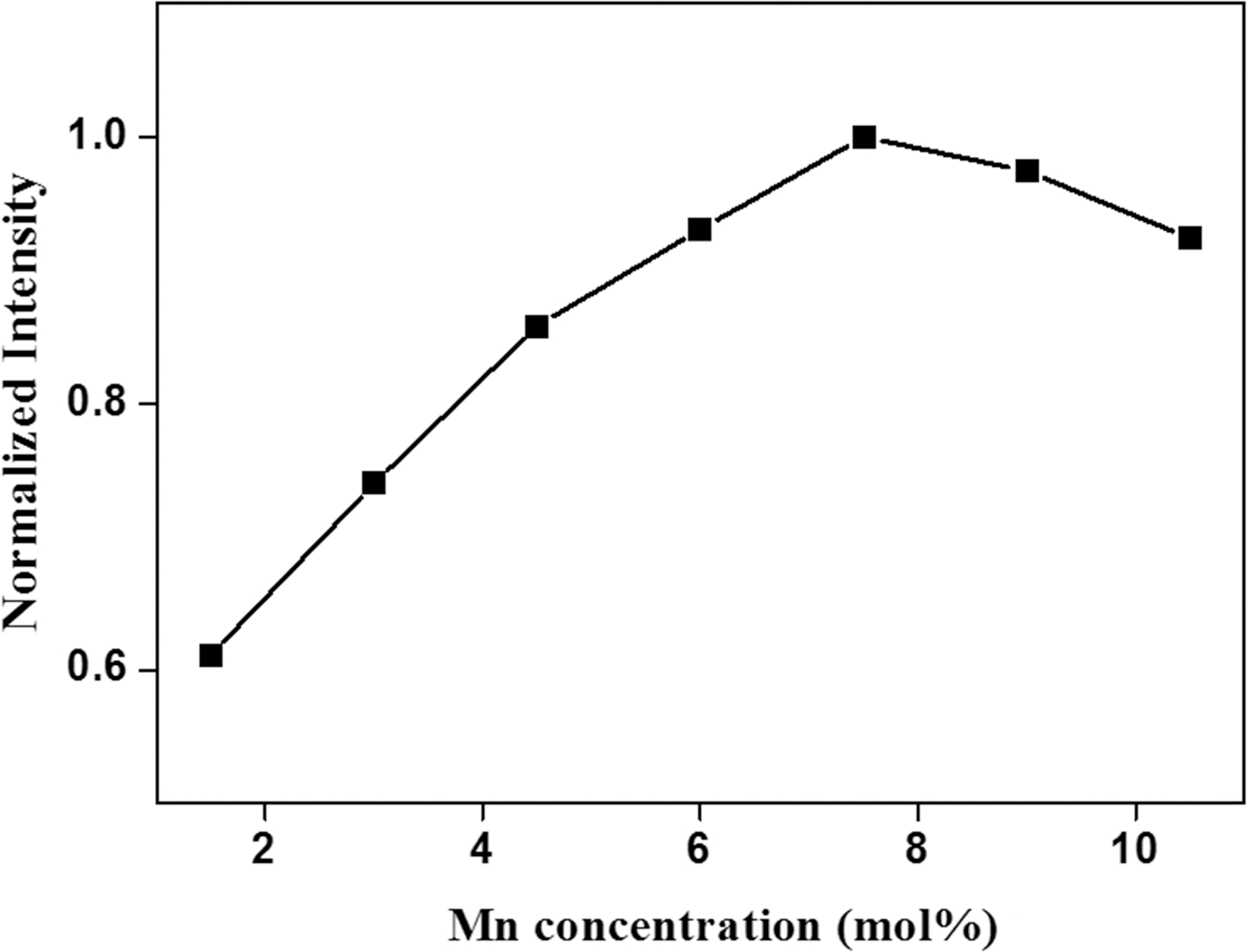
형광체에서 실제 발광을 하는 성분은 활성제이다. 제 조되는 형광체에서 최대의 발광강도를 나타내게 되는 활 성제의 농도를 최적화하는 것이 중요하다. Fig. 5는 Mn4+ 의 첨가량을 변화시키면서 제조된 K2TiF6:Mn4+ 형광체들 의 발광강도 변화를 보여준다. Mn4+의 첨가량이 1.5 mol% 부터 7.5 mol%까지 증가함에 따라 형광체의 발광강도는 활성제 함량의 증가와 함께 지속적으로 증가하다가 더 높은 첨가량인 9 mol%와 10.5 mol%에서는 오히려 발광 강도가 감소하는 현상을 보인다. 이로부터 Mn4+ 이온의 최적 첨가량은 7.5 mol%이며, 이 첨가량보다 더 증가하 면 형광체의 발광강도가 감소하게 되는 농도소광(concentration quenching) 현상이 일어난다는 것을 알 수 있다.
Fig. 6에 제조된 K2TiF6:Mn4+ 형광체에 대한 온도 증 가에 따른 발광 스펙트럼의 변화와 함께 발광강도 변화 를 제시하였다. Fig. 6(a)의 발광 스펙트럼을 보면 주위 의 온도가 증가함에 따라 주 발광피크인 635 nm와 652 nm의 강도는 점진적으로 감소하고, 620 nm의 발광피크 는 점점 증가하는 현상을 나타낸다. 이런 현상이 나타 나는 이유는 Mn4+의 제로 포논 라인(ZPL)의 진동에 의 한 효과 때문인 것으로 보고되었다.24) 한편, 온도 증가 에 따라 발광피크의 강도는 변화하더라도, 색좌표에서 약 간의 청색 이동(blue-shift)만을 나타낸다는 것을 관찰할 수 있다(Fig. 6(a) inset). 한편, K2TiF6:Mn4+ 형광체는 고온 영역에서 형광체의 발광강도가 저하되는 열화문제 를 가지고 있는 것으로 알려져 있다. 이러한 특성을 알 아보기 위해서 가장 대표적인 불화물 형광체인 K2TiF6:Mn4+과 K2TiF6:Mn4+ 형광체의 온도 의존성을 비교하였 다. 실온으로부터 190 °C까지 온도를 증가시키면서 측정 된 K2TiF6:Mn4+ 형광체와 상용의 K2SiF6:Mn4+ 형광체의 발광강도 변화를 Fig. 6(b)에 제시하였다. K2TiF6:Mn4+ 형광체는 150 °C까지는 K2SiF6:Mn4+ 형광체와 같이 발광 강도에 있어 감소현상이 거의 나타나지 않는다. 하지만 150 °C이상의 높은 온도 영역에서는 K2SiF6:Mn4+ 형광체 가 약한 발광강도 저하 현상을 나타내는데 반하여, K2TiF6:Mn4+ 형광체는 발광강도가 상대적으로 급격히 감소한다 는 것을 볼 수 있다. 이는 K2TiF6:Mn4+ 형광체의 일반 적인 특징으로 궁극적으로 150 °C이상의 높은 온도 영 역에서의 온도의존성의 개선이 필요한 것으로 보인다.
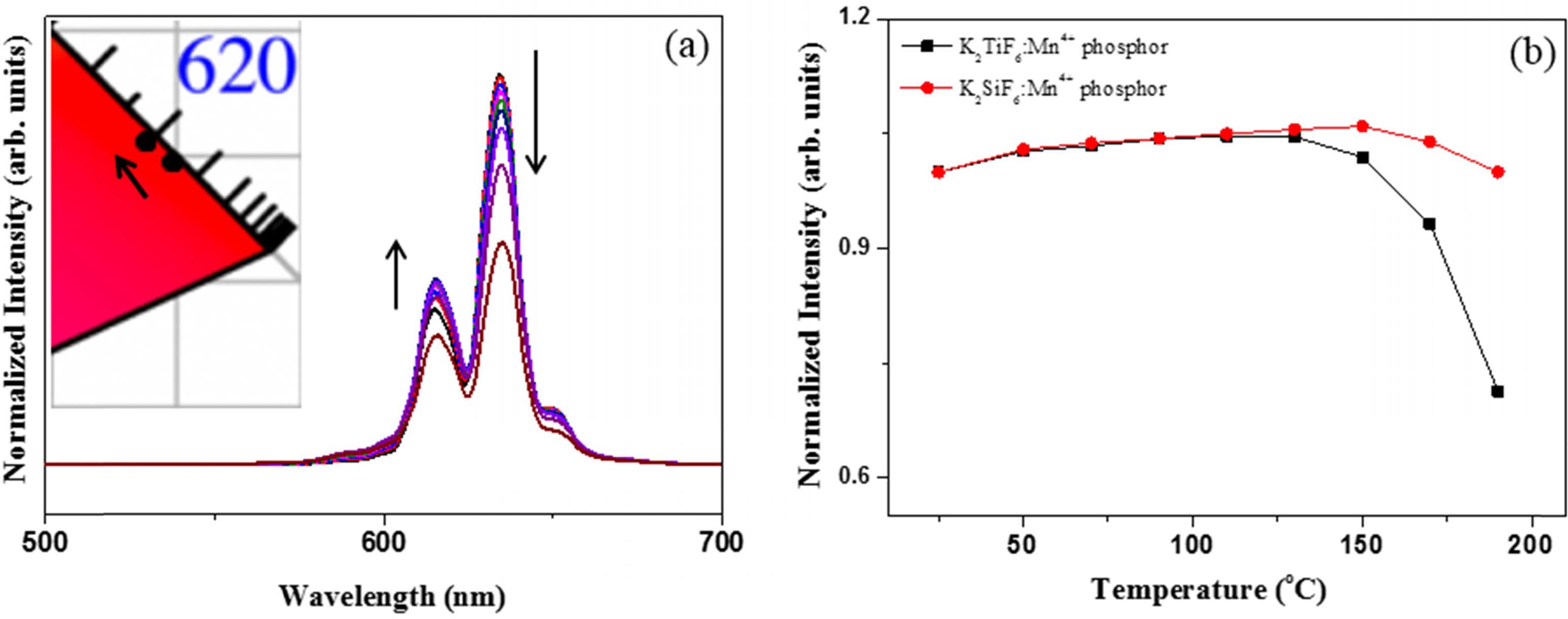
Fig. 6.
Changes in the emission peaks and the color coordinates of the K2TiF6:0.075Mn4+ phosphor (a) and temperature dependence of the synthesized K2TiF6:Mn4+ and the commercial K2SiF6:Mn4+ phosphors (b).
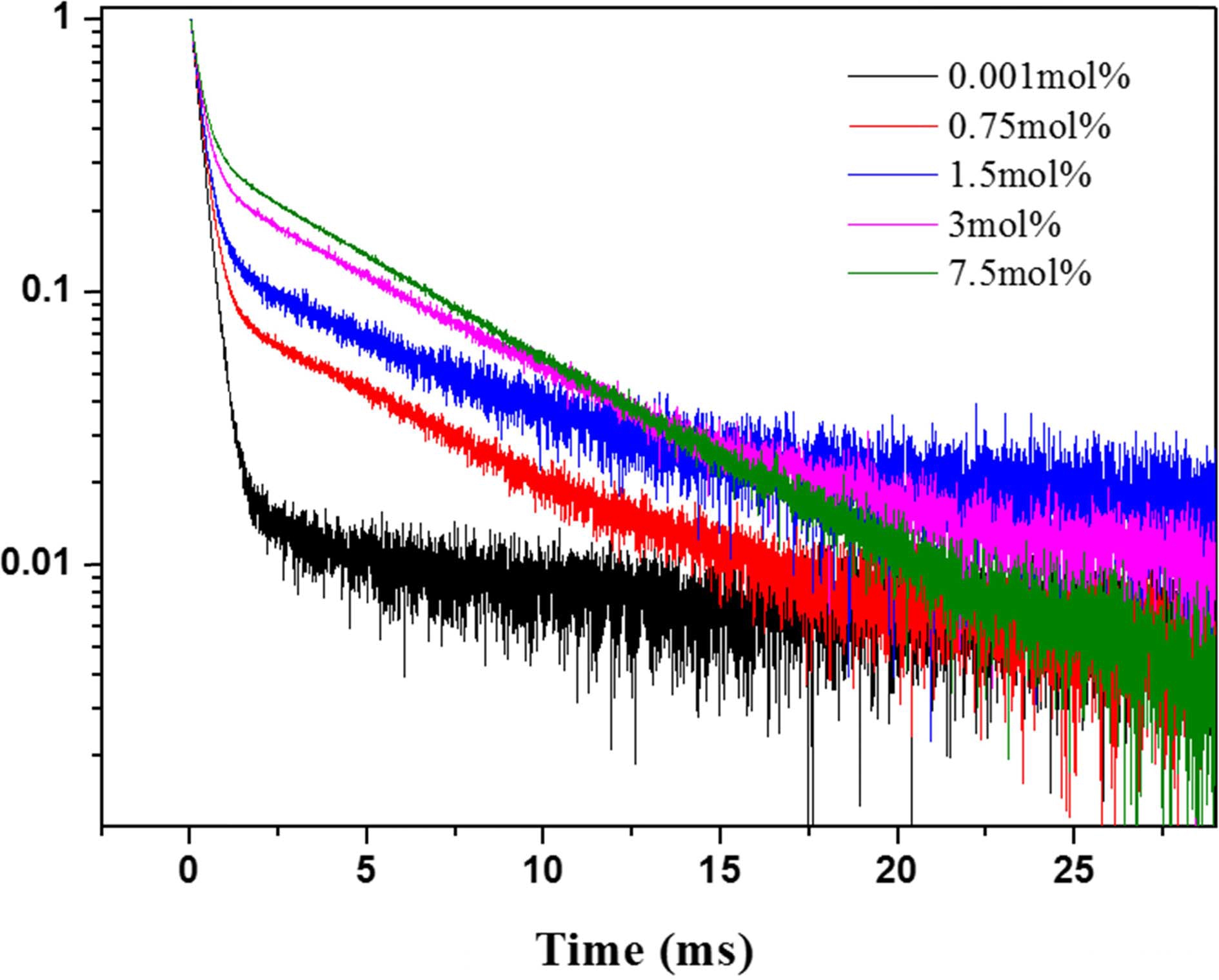
Fig. 7에 Mn4+의 첨가량 변화에 따른 K2TiF6:Mn4+ 형 광체에 대한 잔광곡선을 측정하여 결과를 나타내었다. 형 광체의 잔광시간은 특히 디스플레이 응용을 위해서는 중 요한 요소로 알려져 있다. 잔광시간이 길면 영상을 표 현함에 있어 잔상과 같은 문제를 유발하기 때문이다. 측 정된 결과를 보면 첨가된 Mn4+의 범위에서 형광체의 잔 광시간(τ1/10)이 Mn4+의 증가와 함께 증가하며 최대의 발 광강도를 나타내는 7.5 mol%의 Mn4+ 첨가량에서 6.7 ms 의 잔광시간을 나타내는 것으로 평가되었다. 이는 디스플 레이의 응용을 위해서는 조금 긴 편이기는 하지만 Zn2SiO4: Mn2+ 녹색형광체(~8 ms)와 같은 Mn2+ 활성제 형광체와 비교하여 거의 유사한 잔광시간인 것으로 평가된다.
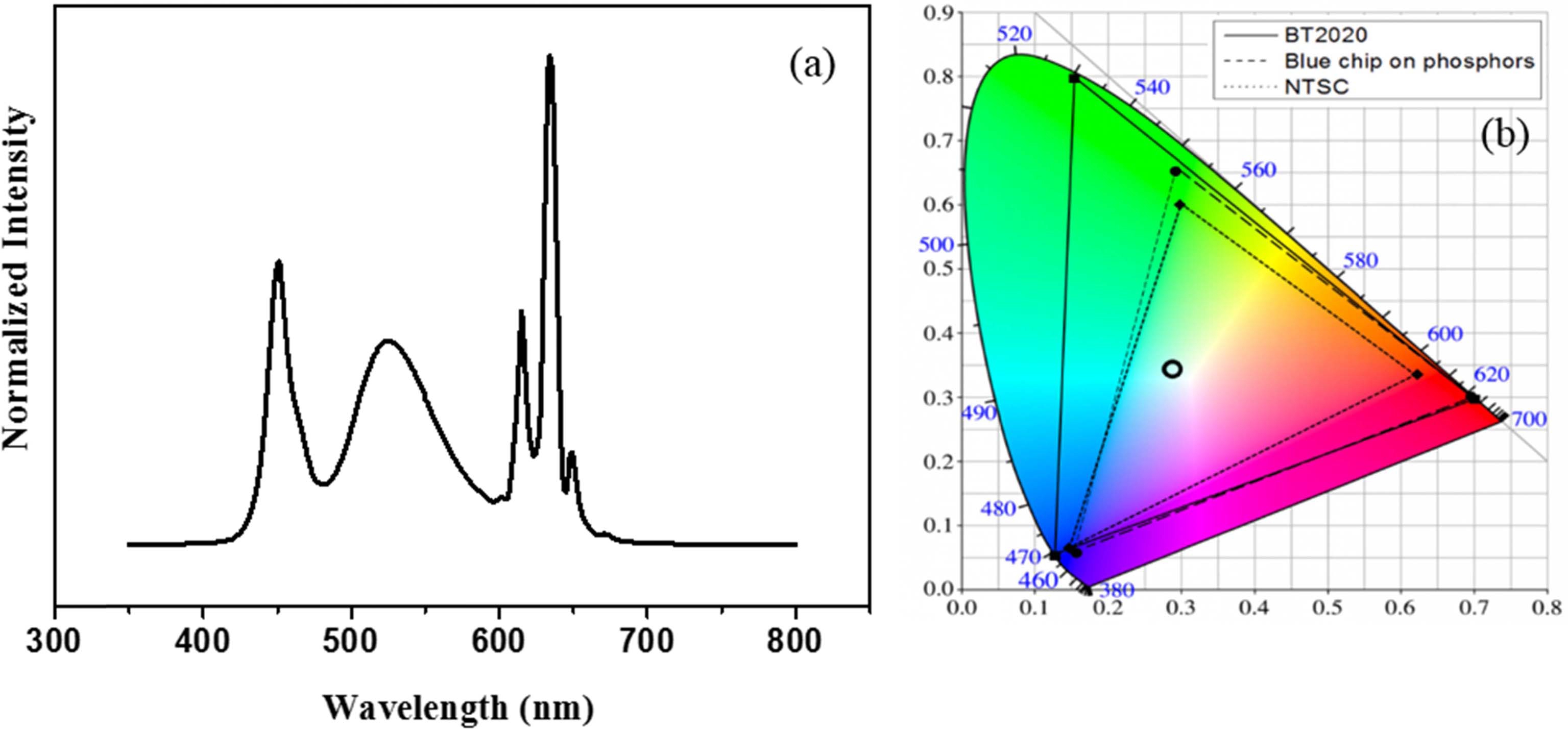
합성된 K2TiF6:Mn4+ 형광체에 대해 백색 LED로의 응 용성을 조사하기 위하여, 합성된 K2TiF6:Mn4+ 적색형광 체를 상용의 SrSiO4:Eu2+ 녹색형광체와 함께 450 nm 청 색 LED 칩과 결합시켜 pc-WLED를 제작하여 측정된 전 계 발광 스펙트럼을 Fig. 8에 제시하였다. Fig. 8(a)에서 볼 수 있는 것처럼, 제작된 pc-WLED는 기존의 청색 LED칩과 YAG:Ce 황색형광체의 결합 방식보다 적색 영 역의 발광이 크게 강화됨을 알 수 있다. 또한, Fig. 8(b) 에서 제작된 백색 LED에 대해 적색 영역이 강화되어 색 온도가 낮은 백색의 색좌표를 가진다는 것을 확인할 수 있고, 각 구성 성분에 의해 만들어지는 색재현 범위를 보면 NTSC 기준 색재현율이 133.7 %로 매우 넓어지는 것이 확인된다.25) 결과적으로 본 실험에서 고안된 제조 방법을 이용하여 적색형광체를 합성함으로써 고색재현이 가능한 pc-WLED 를 제조할 수 있음을 알 수 있다.
4. 결 론
불산 사용 없이 NH5F2를 이용하는 고안된 침전방법으 로 Mn4+가 치환된 K2TiF6 적색형광체를 상온에서의 반 응으로 합성하였고 반응조건들이 최적화되었다. 활성제 원 료로 사용되는 K2MnF6가 반응 중에 가수분해되는 것을 억제시켜 K2TiF6:Mn4+ 형광체를 얻기 위하여, 반응용액 에 NH5F2의 존재가 필요하며 K+의 원료로써 KHF2를 사 용하는 것이 효과적이었다. 고안된 합성방법에 따른 K2TiF6:Mn4+ 형광체에서 Mn4+ 활성제의 최적 첨가량은 7.5 mol% 이었다. 합성된 형광체는 불산을 사용하여 제조되는 형 광체에 비교하여 발광강도의 개선이 필요하지만 적색영 역에서 매우 우수한 발광특성을 보였다. 또한, 합성된 K2TiF6:Mn4+ 형광체와 상용의 녹색형광체 및 청색 LED 칩과의 결합을 통하여 제작되는 pc-WLED가 색온도가 낮 은 백색 발광과 넓은 색재현범위를 나타낼 수 있음을 확 인하였다.