1.서 론
최근 반도체 광촉매의 주요소재로서 사용되는 TiO2는 무독성이며 화학적 안정성과 내부식성 및 내구성이 높 을 뿐 아니라, 광촉매 반응시 TiO2의 낮은 가전대 (~ 2.9 eV vs. NHE)로부터 생성되는 정공들은 높은 산화특성 을 나타내는 것으로 알려져 있다.1) 따라서 광여기된 정 공들은 직접 유기오염물질들을 산화시켜 분해할 수 있 을 뿐 아니라 물과 반응하여 강력한 산화특성을 갖는 수 산화라디칼(OH•)을 생성시키기 때문에 고효율의 광활성 재료로서 많이 사용되고 있다.
그러나 TiO2 광촉매는 여러 장점에도 불구하고 비교 적 넓은 밴드갭 에너지(3.2 eV)를 나타내기 때문에 단지 태양광의 약 4 %에 해당되는 자외선 영역의 빛에 대해 서만 반응할 수 있으며, 태양광의 대부분을 차지하는 적 외선 영역에서는 광반응의 활용이 어렵다는 단점이 나 타난다. 또한 광촉매 표면에서 광여기에 의해 생성된 전 자와 정공들이 빠르게 재결합되어 소멸되기 때문에 광 반응에 참여할 전하들의 양이 감소되어 광촉매 효율을 저하시키는 단점들도 나타나므로 다양한 적용 분야로의 활용에 제약을 받고 있다. 따라서 최근 TiO2 광촉매의 활용도를 높이기 위해 전하들의 재결합을 방지하는 방 법과 낮은 양자효율을 개선시키기 위한 다양한 연구가 진행되고 있다. 예를 들면, 밴드 갭 에너지 폭이 좁은 반도체 입자와 TiO2와의 이중 접합을 이용하여 TiO2 표 면에서 광여기된 전자와 정공들의 재결합을 방지하는 방 법과,2,3) TiO2 결정 내부로 질소(N), 보론(B)과 같은 원 소들을 도핑하여 TiO2의 흡광능력의 향상시키는 방법 등 이 있으며,4,5) 특히 B를 TiO2 결정 내부로 도핑 시켰을 경우는 광촉매의 광학적 특성의 변화에 의해 가시광의 흡광 능력이 향상될 뿐 아니라 광여기된 전자와 정공의 재결합이 방지되어 광촉매의 전하이동 효율이 현저히 개 선되었다는 연구도 보고되고 있다.6)
따라서 본 연구에서는 가시광 영역의 흡광능력과 전하 이동 반응의 효율성을 향상시킨 고효율 TiO2 광촉매를 제조하는 것을 목적으로 보론(boron)이 도핑 된 TiO2 결 정을 제조한 후, 보론도핑에 의해 나타나는 TiO2 광촉 매의 결정형태와 광촉매 특성 변화에 대해 조사하였다. 이 를 위해 보론이 도핑된 TiO2 광촉매 시편은 TiO2 형성 과 보론도핑을 한 번에 간단하고 경제적으로 합성할 수 있는 장점이 있는 plasma electrolytic oxidation (PEO) 방식을 통해 제조했으며, 광촉매 효율은 광 전기화학 반 응과 rhodamine B 염료의 분해반응을 통해 조사했다.
2. 실험 방법
2.1. B 도핑된 TiO2 제조
본 실험에서 사용되는 boron이 도핑된 TiO2 피막을 제 조하기 위해 3 × 4 c m2 크기의 티타늄 sheet (commercial grade, 99.6 wt%)를 탈지와 수세 등을 통해 전처리를 실 시한 후, 수용액에서의 양극산화 반응을 이용한 plasma electrolytic oxidation (PEO) 방식으로 Ti 표면상에 TiO2 피막을 형성시켰다. 이때 TiO2 광촉매를 제조하기 위해 서 0.5M H2SO4 용액을 사용하였으며, 보론도핑된 TiO2 광촉매를 제조하기 위해 0.5M H2SO4 용액에 0.2, 0.4, 0.6, 0.8 그리고 1.0M H3BO3를 첨가한 혼합용액을 전 해액으로 사용하였으며, 180 V의 정전압을 20min 동안 인가하여 TiO2 피막을 제조하였다. 이 과정에서 직류 전 원공급장치(DC power supply)에 의해 조절되는 2극관의 유리 전해조를 사용하였다. PEO 방식에 의해 보론이 도 핑된 TiO2 산화 피막이 형성되는 과정은, 전해조 내부 의 티타늄 양극(anode) 시편에 180 V의 정전압이 인가 되기 시작하면 전해액 내부의 티타늄 시편 표면에서는 국부적으로 플라즈마 방전 현상이 발생되면서 TiO2 피 막이 생성되며 성장하게 된다. 이때 생성되는 TiO2 피 막의 형상과 조직은 전해액 성분의 이온들에 의해 영향 을 받게 되며, 보론이 첨가된 전해액을 사용할 경우 전 해액으로부터 보론이온들은 TiO2 피막 내부로 침투하여 피막내에 존재하게 된다
2.2. TiO2 광촉매 피막의 특성조사
PEO 방식으로 제조된 TiO2 피막과, 보론도핑된 TiO2 산화피막의 피막 형상과 표면특성은 FE-SEM (Philips XL30 ESEM-FEG)을 통하여 관찰하였으며, TiO2 산화 피막의 결정구조는 X-선 회절분석기(Phillips, Model PW1710)를 사용하여 조사하였다. 또한 제조된 광 촉 매의 표면조성과 결합상태 특성은 X-ray photoelectron spectroscopy (XPS, PHI 5700)를 사용하여 조사했다. TiO2와 보론도핑된 TiO2 광촉매의 활성에 대한 특성 조 사는 광조사에 의한 광전류의 변화반응을 통하여 조사 했으며, 이를 위해 potentiostat (CHI600E, USA)와 3극 계(three-electrode system) 셀을 이용했다. 이때 셀의 기 준전극과 상대전극으로는 Hg/Hg2SO4와 백금전극을 사용 했으며, 3극계 셀의 내부는 석영 유리로 된 튜브로 연 결하고, 외부에서 공급되는 광원이 광촉매 표면에 도달 될 수 있도록 하였다. 외부에서 공급되는 광원으로는 LED 광원(LED illuminator, B&B Opto)을 이용하였으며 내부필터를 이용하여 400 nm 이하의 광원은 제거된 상 태로 사용하고, 또한 전기화학적 실험을 위한 전해액으 로는 0.5 M K2SO4 용액을 사용했다.
2.3. 염료분해 효율 조사
TiO2 피막의 광촉매 반응효율은 염료의 분해 효율을 통 해 평가하였으며, 염료로는 rhodamine B를 사용하였다. rhodamine B 염료의 분해 반응은 0.038 μM rhodamine B 용액(pH 4.88)을 사용하여 광 조사시간에 따른 염료분해 효율을 조사하였다. 또한 반응 용액으로부터 6 0 c m 위 에 100W의 고압 수은등을 장치한 후 조사 시간에 따 른 TiO2의 광촉매 반응을 측정하였다. 반응시간에 따른 rhodamine B의 분해 농도의 관찰은 자외선 분광 광도 계(Unicam 8700)를 사용하여 554 nm에서의 흡광도의 변 화를 측정하였다.
3. 결과 및 고찰
3.1. 보론도핑된 TiO2 산화피막의 표면특성
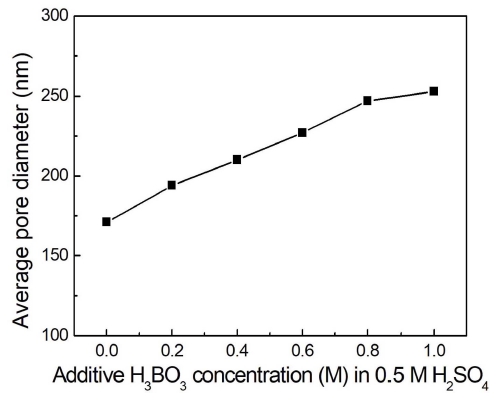
Fig. 1은 plasma electrolytic oxidation (PEO) 방식을 통해 180 V의 양극전압을 20 min 인가하여 Ti sheet 시 편 표면에 생성된 TiO2와 보론이 도핑된 TiO2 산화의 표 면조직을 나타낸 사진이다. 이때 TiO2 광촉매를 제조하 기 위해서 0.5 M H2SO4 용액을 사용하였으며, 보론이 도핑된 TiO2 광촉매를 제조하기 위해 0.5 M H2SO4 용 액에 0.2, 0.4, 0.6, 0.8 그리고 1.0 M H3BO3를 첨가한 혼합용액을 전해액으로 사용하였다. PEO 방식을 통해 TiO2 양극 산화 피막을 제조할 경우, 양극(anode)의 티 타늄(Ti) 시편 표면에서는 국부적인 플라스마 현상과 더 불어 기공형상의 TiO2 피막이 생성되면서 성장하게 되 며 이때 전해액 성분의 보론이온들은 TiO2 피막 내부 로 침투하여 피막내에 존재하게 된다. 따라서 고농도의 H3BO3 용액이 혼합된 전해액에서 형성된 TiO2 피막일 수록, 전해액에서 존재하는 보론원소 성분들이 PEO 과 정 중에 산화피막 내부로 도핑되는 양이 많아지기 때문 에 TiO2 양극 산화 피막 내부에는 많은 양의 보론이 첨 가되어 있음을 예상할 수 있다. Fig. 1(a)는 H3BO3 용 액이 첨가되지 않은 0.5 M H2SO4 전해액에서 생성된 TiO2의 표면조직을 나타냈으며, TiO2 산화피막은 기공 (pore)을 포함하는 셀(cell) 구조를 보여주고 있다. 또한 H3BO3 용액이 혼합된 전해액에서 형성된 TiO2 피막 Fig. 1(b) - (f)의 경우에도 표면구조는 0.5 M H2SO4 전해액 에서 생성된 피막의 표면 조직과 비슷한 셀 구조로 형 성되었으며, H3BO3 용액 첨가에 의해서 산화피막의 표 면 조직의 형상은 크게 변화하지 않았다. 그러나 Fig. 1(b) - (f)에서 보듯이 고농도의 H3BO3 용액이 혼합된 전 해액에서 형성된 TiO2 피막일수록, 산화피막 표면에서 생 성된 기공과 셀조직의 크기는 점차적으로 증가하는 경 향을 나타내고 있으며, 이러한 TiO2 표면 셀조직에서의 기공(pore)크기의 변화는 Fig. 2에 나타냈다. Fig. 2에서 0.5 M H2SO4 전해액에서 생성된 TiO2 피막의 경우 셀 구조의 기공직경 크기는 평균적으로 172 nm로 나타났으 며, 0.5 M H2SO4 전해액에 0.2 M H3BO3가 첨가된 혼 합용액에서 생성된 산화피막 표면의 기공의 평균직경 크 기는 195 nm로 측정되었다. 또한 고농도의 H3BO3가 첨 가된 혼합용액에서 제조된 산화피막일수록 기공의 크기 는 증가하였으며 1.0 M H3BO3가 첨가된 혼합용액의 경 우 산화피막의 기공의 평균 직경은 253 nm로 나타났다 . 따라서 0.5 M H2SO4의 용액액에 H3BO3 용액을 첨가 한 혼합 전해액을 사용할 경우, 산화피막의 표면 셀조 직의 형상은 크게 변하지 않으나 셀조직과 기공크기는 증가하며, 혼합한 H3BO3 용액의 농도가 높을수록 이러 한 경향도 증가하는 것으로 나타났다.
3.2. TiO2 양극산화피막의 결정구조
Fig. 3은 H3BO3가 첨가된 0.5 M H2SO4 혼합용액에서, PEO 방식으로 보론이 도핑된 TiO2 산화피막의 광촉매 를 제조한 후, 이때 생성된 TiO2 광촉매의 결정구조를 XRD 측정결과를 분석하여 조사한 결과이다. Fig. 3의 결 과에서는 0.5 M H2SO4 전해액에서 제조된 TiO2 광촉 매의 결정구조와, 0.5 M H2SO4 전해액에 H3BO3가 첨 가된 혼합용액에서 제조되어 보론이 도핑된 TiO2 광촉 매와의 결정구조는 큰 차이가 나타나지 않았다. Fig. 3 의 XRD 분석 결과로부터, 대부분 양극산화 TiO2 피막 에서는 anatase 결정조직(JCPDS No. 21-1272)의 (101), (103), (004), (200), (105), (211)면을 나타내는 회절 피 크가 25.28°, 36.95°, 37.80°, 48.05°, 53.89°, 그리고 55.06°에서 나타났으며, rutile 결정(JCPDS No. 21-1276) 의 (110)면을 나타내는 회절 피크는 27.45°에서 나타났 다. 또한 산화 피막 층인 TiO2 광촉매의 결정 피크 이 외에도, 피막내부의 기저층에 존재하는 티타늄 금속에 의 해 티타늄의 회절피크도 동시에 나타났으며, 보론과 관 련된 특별한 화합물의 형태는 관찰되지 않았다. 따라서 Fig. 3의 XRD 측정결과를 통하여, PEO 방식에 의해 제 조된 TiO2 광촉매의 경우, 전해액의 종류와 관계없이 대 부분 anatase 결정과 약간의 rutile 결정이 혼합된 형태 로 생성됨을 알 수 있었다.
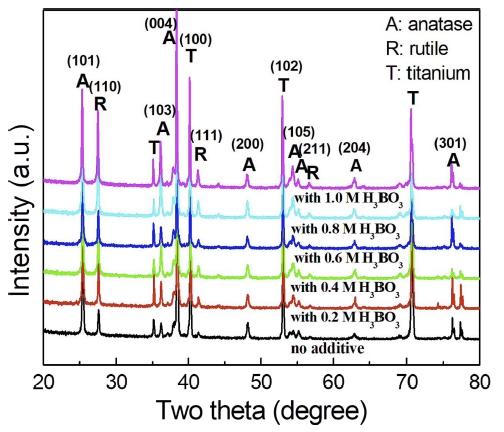
Fig. 3
XRD patterns of the anodic TiO2 layer synthesized by PEO process at 180 V in 0.5 M H2SO4 with different concentrations of H3BO3 additives.
또한 전해액 중의 보론이온들이 TiO2 결정 내부에 도 핑되어 존재할 경우 TiO2 결정의 물리적 변화에 영향을 미치게 되며, 이러한 현상에 대해 자세히 관찰하기 위 하여, anatase 결정의 (101)과 (200) XRD 피크의 변화 거동을 조사하고 그 결과를 Fig. 4에 나타냈다. 이를 통 하여 TiO2 산화피막의87 anatase 결정에서 격자상수의 변 화와 결정크기와 같은 물리적 특성의 변화를 분석했으 며, Fig. 4의 결과에서, 보론이 많이 첨가된 전해액에서 제조된 TiO2 산화피막 일수록 anatase 조직의 (101)와 (200) 피크중앙이 점차로 2θ 크기가 감소하는 방향으로 이동하고 있는 것으로 나타났다. 이러한 현상의 원인은 아래 식의 Bragg 법칙에 의해 설명될 수 있으며,
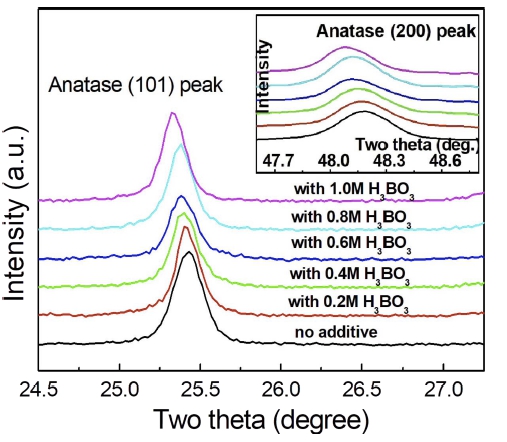
Fig. 4
The shift of (101) and (200) anatase XRD peaks for the TiO2 layers synthesized by PEO process at 180 V in 0.5 M H2SO4 with different concentrations of H3BO3.
이때 d(hkl)은 결정의 면간 거리이며, θ는 회절각 그리 고 λ는 X-ray의 파장(Cu, Kα: 0.1541 nm)을 나타낸다.
따라서 Fig. 4에서 보여 지듯, (101)와 (200) 면의 XRD 피크 중앙이 점차로 2θ의 크기가 감소하는 방향 으로 이동되는 것은, anatase 결정격자(tetragonal phase) 의 (101)와 (200) 면간 거리가 증가하는 현상을 나타내 는 것으로서, 이것은 높은 농도의 H3BO3가 첨가된 혼 합용액에서 제조된 TiO2 광촉매일수록 표면부에서 인장 응력의 증가, 또는 anatase 단위 셀의 격자상수가 증가 하는 것을 의미한다. 이와 같이 다양한 농도의 B 이온 이 첨가된 전해액을 통하여 TiO2 광촉매를 제조할 경 우, 전해액에 첨가된 보론이온 농도가 TiO2 결정구조의 물리적 특성에 영향을 미치는 것으로 나타났다. TiO2 산 화피막내 anatase 결정의 (101)와 (200)면의 XRD 피크 분석을 통해 평균 결정크기를 조사하기 위해서 Scherrer 방정식을 이용했으며, anatase (101) 피크의 FWHM (full width at half maximum)을 사용하여 나타난 결과 는 Table 1에 나타냈다.
Table 1
Structural parameters of the TiO2 anatase photocatalyst synthesized by PEO process at 180 V in 0.5 M H2SO4 electrolyte with different concentrations of H3BO3.
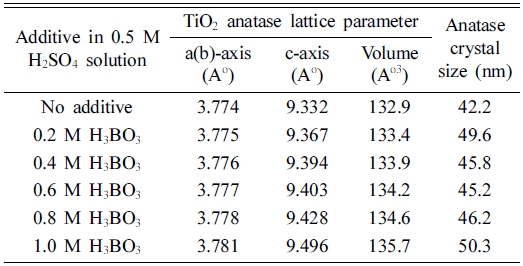 |
Table 1의 결과에서 보론이 첨가되지 않은 0.5M H2SO4 전해액에서 제조된 TiO2 광촉매의 anatase 결정격자는 a 축이 3.774 A° , c축이 9.332 A°으로 나타나 격자의 부피는 132.9 A°3으로 나타났다. 그러나 보론이온이 많 이 첨가된 황산전해액에서 제조된 TiO2 광촉매 일수록 anatase 격자상수는 점차 증가하여 단위 셀의 부피크기 는 132.9 A°3에서 135.7 A°3으로 증가되어 2.1% 증가 한 것으로 나타났다. 이것은 전기화학적 방식인 PEO 방 법으로 TiO2 광촉매를 형상시키는 과정에서 용액 중에 존재하는 보론이온이 TiO2 결정내부로 침투해 들어가 며, 이때 침투된 보론이온은 침입형과 치환형의 형태로 TiO2 내부에서 존재하게 된다. 그러나 B3+의 반지름은 0.023 nm로서, Ti4+ (IV)의 반지름인 0.068 nm와 O2- 의 반지름인 0.140 nm와 비교하면 너무 작기 때문에 대 부분은 칩입형으로 존재하고 있는 것으로 보고되고 있 다.7-9) 따라서 보론이온이 많이 첨가된 혼합 전해액에서 제조된 TiO2 광촉매일수록, 용액속에 존재하는 보론이온 이 TiO2 결정내부로 많이 침투하여 침입형 상태로 존재 하기 때문에, TiO2 격자는 점차 팽창하게 되고 이로 인 해 격자상수와 결정의 크기가 증가하는 것으로 판단된다.
또한 본 연구에서 PEO 방법으로 생성된 anatase 결정 의 크기를 비교하여 보면, 보론이 첨가되지 않은 anatase 결정의 크기는 42.2 nm로 나타났으나 보론이 첨가된 anatase 결정의 크기는 47.75 ± 2.55 nm로 나타났다. 따 라서 PEO 방식에 의해 생성된 anatase 결정의 크기는, 보론이온이 도핑된 anatase의 경우, 보론이 도핑 되지 않 은 경우에 비해 anatase 결정의 크기는 증가하였으나, 일 단 보론이 도핑된 anatase 결정의 크기는 보론의 도핑 첨 가량과는 직접적인 선형관계를 나타내지는 않았다. 이것 은 본 연구에서 제조한 TiO2의 경우, 결정의 생성과 성 장은 Ti 표면에서 발생되는 순간적인 전기 에너지인 micro arc에 의해 영향을 받기 때문에, TiO2 생성과정의 표면상태와 인가되는 전압과 전류의 상태는 매우 중요 한 변수로 작용하게 된다. 따라서 보론이 많이 첨가된 황산 전해액은 용액의 전도성에 영향을 주기 때문에 TiO2 생성과정에서 표면에 전기적 arc spark의 발생을 촉진시 키며 이로 인해 TiO2 결정이 성장된 것으로 사료된다. 그러나 전해액에 일정량 이상의 보론이 첨가된 경우는, TiO2 표면에서 변화되는 전압과 전류 상태가 TiO2 결정 성장에 더 큰 영향을 미치기 때문에 TiO2 결정크기가 다 소 불규칙적으로 나타난 것으로 사료된다.
3.3. TiO2 산화피막의 XPS 분석
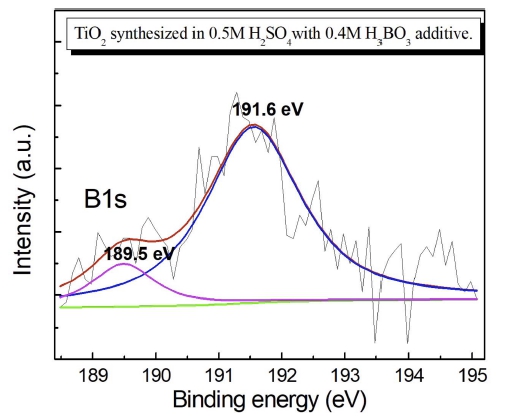
PEO 방식을 통해 제조된 TiO2와 보론이 도핑된 TiO2 광촉매 표면의 화학적 결합상태를 관찰하기 위하여 XPS 분석을 실시했으며 그 결과를 Fig. 5, 6 그리고 7에 나 타냈다. Fig. 5는 TiO2 광촉매 표면의 XPS survey spectrum을 나타내며, TiO2 결정의 주 원소성분인 Ti와 O 원소에 의해 Ti 2p와 O 1s 피크가 나타났으며, TiO2 피막의 오염에 의한 C 1s 피크가 나타났다. 그러나 도 핑된 B 원소의 화학적 결합상태를 조사하기 위한 자 세한 spectrum은 Fig. 6에 나타냈다. Fig. 6의 B 1s의 chemical state 변화 결과는 높은 농도의 H3BO3 용액이 첨가된 전해액에서 제조된 시편의 경우, XPS의 B1s 에 너지 피크가 점차 선명하게 나타나는 것을 보여준다. 이 때의 B1s 에너지 피크의 중심은 약 191.5 – 192 eV 사 이에서 존재했다.
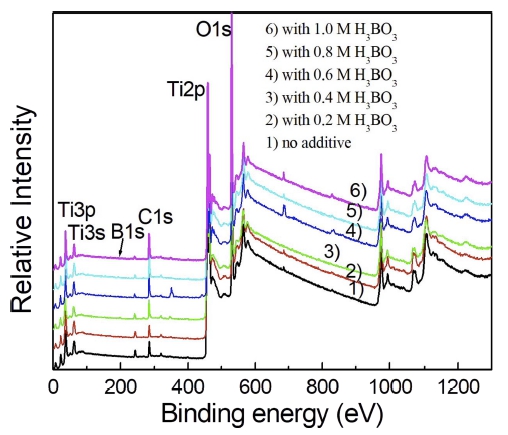
Fig. 5
XPS survey spectrum of anodic TiO2 surface synthesized at 180 V in 0.5 M H2SO4 with different concentrations of H3BO3 additives.
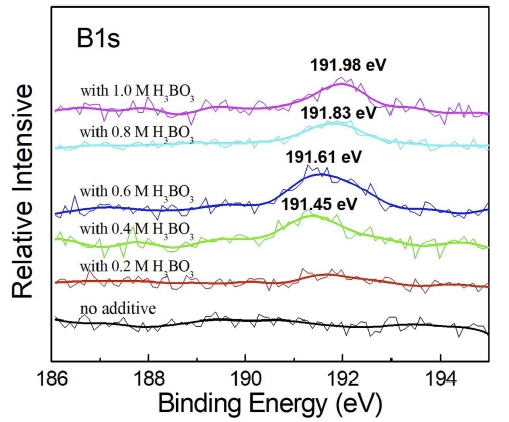
Fig. 6
B1s core peak for TiO2 surface synthesized at 180 V in 0.5 M H2SO4 with different concentrations of H3BO3 additives.
따라서 Fig. 6의 결과에서, H3BO3와 H2SO4의 혼합용 액에서 제조된 TiO2 산화피막은 PEO 과정중에 혼합 전 해액에 존재하는 보론이온들이 TiO2 산화피막으로 침투 되어 보론이 도핑된 산화피막이 형성되었음을 나타내고 있다. 또한 첨가된 H3BO3의 농도가 높은 조성의 혼합 전해액에서 제조된 산화피막일수록, B 1s 에너지 피크 중심은 191.45 eV에서 191.98 eV로 점차 높은 에너지 방향으로 이동하는 것을 나타내고 있다. 이것은 도핑된 보론원자들이 TiO2 결정 내부에서 화학적 결합방식의 변 화와 관련이 있는 것으로 사료된다. Fig. 7는 0.5 M H2SO4 용액에 0.4 M H3BO3이 첨가된 혼합용액에서 제 조된 TiO2 피막 표면의 화학적 결합 상태를 분석한 결 과이다. B 1s peak를 세밀하게 분석하기 위해 XPSPEAK 4.1 프로그램을 사용하였으며, B 1s 피크는 189.5 그리 고 191.6 eV에서 피크들이 분리되어 나타났다. 일반적 으로 보론이 도핑된 TiO2 결정에서 나타나는 B 1s 피 크는 기본적으로는 2가지 형태에 의해 영향을 받는 것 으로 알려져 있다.
첫번째는 TiB2 형태에서 기인되는 B-Ti bond이며 이 것은 B가 TiO2 내부에서 주로 치환형으로 존재할 때 나 타나며 187.5 eV의 피크에 해당된다. 다른 하나는 B2O3 또는 H3BO3 형태에서 나타나는 B-O bond이며 이것은 B가 TiO2내부로 주로 침입형으로 존재할 경우 나타나며 193.0 eV의 B 1s 에너지 피크에 해당되는 것으로 알려 져 왔다.10-13) 그러나 많은 연구결과에서 TiO2 내부에서 보론이 도핑되는 환경차이에 의해 B 1s 에너지 피크는 187.5 - 193.0 eV 사이에서 이동이 될 수가 있으며, 특 히 Lu 등은 보론이 도핑된 TiO2 표면에서 190.3 eV 이 하의 B 1s 피크가 나타나는 경우는 O-Ti-B bond와 일 치하는 치환형으로 보론이 존재하기 때문이며, 191.6 eV 이상의 B1s 피크는 보론이 TiO2 내부에서 침입형으로 존재할 경우 나타나는 에너지 피크라고 보고하였다.7) 따 라서 Fig. 7의 결과에서 0.5 M H2SO4 용액에 0.4M H3BO3가 첨가된 용액에서 제조된 TiO2 피막표면의 경 우, B 1s의 분리된 피크에서 189.5 eV의 피크는 B 이 온이 O 원소와 치환하여 O-Ti-B 결합 시 나타나는 에 너지 피크를 나타내며, 191.6 eV 피크는 B 이온이 TiO2 결정내에 침입형으로 존재하는 것을 나타내고 있으므 로,14) TiO2 산화피막에는 전해액에서 존재하는 B 이온 이 TiO2 결정 내부로 도핑된 후 치환형과 침입형의 두 가지 형태로 존재하고 있음을 시사하고 있다. 그러나 Fig. 6과 7의 결과를 통해, B 이온의 농도가 높은 혼합 전 해액에서 제조된 TiO2 피막의 경우 B 1s의 중심 피크 가 주로 191 – 193 eV 사이에서 나타났으며, 이것은 B 이온이 TiO2 결정내부에서 치환형보다는 대부분이 침입 형의 형태로 존재하고 있는 것을 나타내고 있다. 또한 TiO2 결정내부에서 존재하는 B 이온 형태가 치환형 일 경우 TiO2 단위격자의 크기는 감소하며, 침입형으로 존 재할 경우 TiO2 격자의 크기는 증가하게 된다. 따라서 Fig. 6과 7의 결과에서 보여주듯이, TiO2 결정내부에 존 재하는 B 이온의 대부분은 침입형의 형태이고, XRD 분 석을 통한 결정격자의 측정 결과(Table 1)에서 TiO2의 격 자 크기가 증가하는 결과와 잘 일치하는 것으로 나타났다.
3.4. 광 전기화학적 특성 분석
PEO 방식에 의해 제조된 TiO2 산화피막의 광반응 효 율을 조사하기 위해 TiO2 산화피막의 표면에 가시광을 조사한 후 가시광에 의해 여기 되는 광전자의 거동을 조 사했다. 이를 위해 가시광의 조사에 의해 TiO2 피막의 표면에서 발생되는 광전류를 측정하고 그 결과를 Fig. 8 에 나타냈다. Fig. 8에서 보여지는 광전류 측정 방법은 광이 차단된 어두운 상태를 유지한 후 정전류 전압(open circuit potential) 상태에서 가시광을 조사(light on) 하거 나 제거(light off) 했을 경우 변화되는 광전류를 측정한 결과이며, 실험방법에 대한 자세한 내용은 이미 보고된 바 있다.15,16) Fig. 8의 경우, 정전류 상태에서 가시광을 조사한 후 약 30초 경과하는 동안 순간적으로 상승했던 광전류가 서서히 감소하게 되며 이때 0.5 M H2SO4 전 해액에서 PEO 방식으로 생성된 TiO2 산화피막의 경우 Fig. 8(a)에서 보여지듯이, 안정화된 상태의 양극 광전류 는 23.5 μA/cm2으로 나타났다. 그러나 0.5M H2SO4 전 해액에 0.2, 0.4, 0.6, 0.8 그리고 1.0M H3BO3 용액이 첨가된 혼합용액에서 제조된 보론이 도핑된 TiO2 산화 피막의 경우는 37.1, 41.5, 47.9, 50.6 그리고 53.0 μA/ cm2의 양극 광전류가 생성되었다. 따라서 순수한 TiO2 산 화피막에 비해 보론이 도핑된 TiO2의 경우 양극 광전류 가 높게 생성되었으며, TiO2 산화피막 내부로 도핑되는 보론의 양이 많을수록 생성되는 광전류의 크기도 증가 하는 것으로 나타났다. 이와 같이 광촉매 표면에서 광 조사에 의해 나타나는 광전류의 크기는, 광촉매 반응에 의한 전자와 정공쌍의 생성과정, 전자와 정공의 이동효 율 그리고 전자와 정공의 분리되어 나타나는 반응효율 에 크게 의존되는 것으로 알려져 있다.16) 따라서 Fig. 8 에서 가시광을 조사할 경우 생성되는 광전류의 크기가 크게 나타날수록, TiO2 산화피막 표면에서 광여기에 의 해 많은 전자들이 발생되고, 전기화학 셀의 상대 전극 인 백금전극까지의 전자이동이 효율적이라는 것을 의미 한다. 따라서 Fig. 8의 결과를 통해 0.5 M H2SO4 용액 에 1.0 M H3BO3가 첨가된 혼합용액에서 제조된 TiO2 산화피막의 경우가 광반응 효율이 가장 높기 때문에, 광 촉매로 사용하기 위한 반응효율도 가장 높을 것으로 예 상할 수 있다.
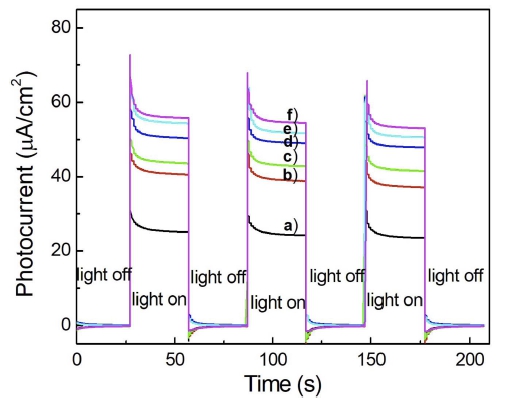
Fig. 8
Photocurrent responses of anodic TiO2 photocatalysts synthesized by PEO process at 180 V in 0.5 M H2SO4 solution containing (a) no additive, (b) 0.2 M H3BO3, (c) 0.4 M H3BO3, (d) 0.6 M H3BO3, (e) 0.8 M H3BO3 and (f)1.0 M H3BO3. The photocurrent of catalysts was measured in 0.5 M K2SO4 solution under the visible light impulse irradiation.
3.5. 염료분해 반응
Fig. 9는 제조된 TiO2 광촉매를 이용하여 rhodamine B 염료의 분해효율을 측정한 결과를 나타냈으며 Co는 초 기의 rhodamine B 염료의 농도를, Ct는 일정시간 광촉 매 분해반응에 의해 변화된 염료의 농도를 나타낸다. Fig. 9(a)는 0.5 M H2SO4 전해액에서 제조되어 보론이온이 도핑되지 않은 TiO2 산화피막의 경우, 300 min의 광촉 매 반응시간 후 Ct/Co는 0.228로 나타났다. 그러나 Fig. 9(b) - (f)와 같이 0.5 M H2SO4 전해액에 0.2, 0.4, 0.6, 0.8, 1.0 M의 H3BO3 용액이 첨가된 혼합용액에서 제조 된 피막의 경우, Ct/Co 비율은 0.180, 0.141, 0.113, 0.080 그리고 0.065로 나타났으며, TiO2 산화피막 내부로 보론 이온의 도핑량이 증가될수록 Ct/Co 비율은 감소하며 염 료의 분해율이 증가하는 것으로 나타났다. Fig. 9의 결 과로부터 광촉매 반응에 의한 rhodamine B 염료의 분 해효율 η (%)은 식 (2)을 통해 나타낼 수 있다.17)
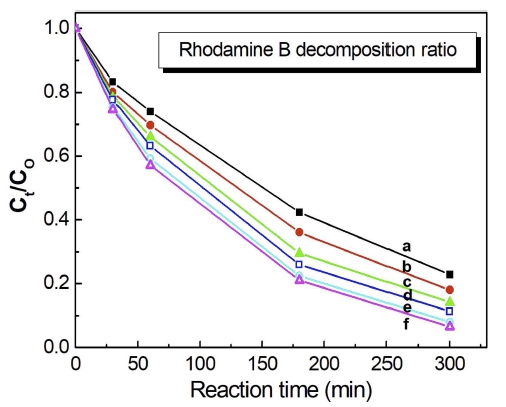
Fig. 9
Photocatalytic decomposition efficiency of dye (rhodamine B) on TiO2 layer synthesized by PEO process at 180 V in 0.5 M H2SO4 solution containing (a) no additive, (b) 0.2 M H3BO3, (c) 0.4 M H3BO3, (d) 0.6 M H3BO3, (e) 0.8 M H3BO3 and (f) 1.0 M H3BO3.
식 (2)에서 Co는 초기의 rhodamine B 염료의 농도이 며, Ct는 일정시간 염료분해 반응이 진행된 후의 변화된 염료농도이다. 또한 광촉매에 의한 rhodamine B 염료의 분해반응에 대한 중요한 변수인 반응상수를 측정했으며 이때 TiO2 광촉매의 반응상수는 1차식을 이용하고 반응 시간과 염료농도의 변화를 통해 염료분해에 대한 반응 상수를 계산했다.18) 이 경우 rhodamine B 염료의 분해 반응시간에 따른 농도의 변화는 아래의 식 (3)으로 나 타내며, 이로부터 반응상수는 식 (4)에 의해 계산될 수 있다.
식 (3)과 (4)의 반응시간과 ln(Co/Ct)의 관계를 통해 염 료분해반응의 반응상수 k는 계산될 수 있으며, 그 결과 는 Table 2에 나타냈다.
Table 2
Rhodamine B degradation rates (h) and rate constants (k) of dye degradation on B doped anodic TiO2 layers evaluated from dye decomposition test for 300 min.
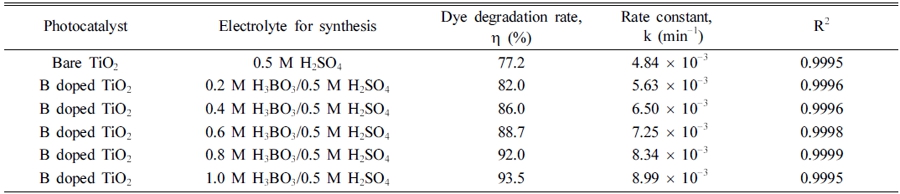 |
Table 2로부터 0.5 M H2SO4 전해액을 사용하여 제조 된 TiO2 산화피막의 경우, rhodamine B 분해반응의 반 응상수는 4.84 × 10−3/min으로 나타났으며, 0.5 M H2SO4 전해액에 0.2, 0.4, 0.6, 0.8, 1.0 M의 H3BO3가 첨가된 전해액에서 제조된 보론이 도핑된 TiO2 피막의 경우, 반 응상수는 4.84 × 10−3, 5.63 × 10−3, 6.50 × 10−3, 7.25 × 10−3, 8.34 × 10−3 그리고 8.99 × 10−3/min으로 나타나, H3BO3 용액의 농도가 높게 첨가된 혼합 전해액에서 제 조된 산화피막 일수록, 염료분해 반응 시 염료분해 효 율이 높게 나타나며 반응상수가 증가하는 것을 보여준 다. 이 결과는 H3BO3의 농도가 높은 조성의 전해액에 서 제조된 산화피막 일수록, TiO2 산화피막 내부에 도 핑되는 보론원자들이 증가할 뿐 아니라, 도핑된 보론원 자들이 TiO2 결정 내부에서 점차적으로 침입형의 위치 에서 존재하는 비율이 증가하고 있는것과 관련이 있는 것으로 사료된다. 이와 같이 TiO2 산화피막 내부에 도 핑된 보론원자들이 TiO2 결정내에서 존재하고 있는 형 태와 광촉매 반응효율과의 관계에 대해서는 Patel 등에 의해 보고된 바 있다.19) Patel 등은 도핑된 보론원자의 대부분이 TiO2 결정의 침입형 위치에서 존재하는 경우, 전 하이동 반응의 효율을 현저하게 증가시키는 장점이 있 으며, 반면에 도핑된 보론원자들이 TiO2 결정 내부에서 치환형과 침입형이 비슷한 비율로 같이 존재할 경우, 가 시광 영역에서의 광 흡수능력을 향상시키는 장점이 있 는 것으로 보고했다. 또한 광촉매 염료분해 결과를 통 해 두 경우를 비교한 결과, 침입형 위치로 보론이 존재 하는 경우가 침입형과 치환형 보론이 동시에 존재하는 경우에 비해 더 높은 분해효율을 나타냈다. 따라서 광 촉매 효율성에 기여하는 항목은 광흡수 능력보다는 광 여기된 전자와 정공의 재결합을 방지시켜 전하이동의 반 응을 향상시키는 요소가 더 중요하다고 보고했다.
따라서 본 연구에서와 같이 PEO 방식을 통해 제조 된 보론이 도핑된 TiO2 광촉매의 경우, 0.5 M H2SO4 전해액에 낮은 농도의 H3BO3가 첨가된 용액에서 제 조된 TiO2 산화피막에서는 도핑된 보론원자들은 대부 분은 침입형의 위치에서 존재하고 비교적 적은 양의 보론이 치환형 위치에서도 존재하고 있음을 보여주고 있 다. 이 경우 TiO2 결정의 전도띠 최소위치(conduction band minimum) 보다 낮은 영역에서 국부적인 불순물 에 너지띠가 형성되어 실제적으로 에너지 밴드갭이 감소되 는 효과가 나타나 광촉매 효율이 증가한 것으로 판단된 다.19) 또한 높은 농도의 H3BO3 용액이 첨가된 전해액 에서 제조된 TiO2 피막의 경우 침입형 위치를 차지하는 보론의 비율이 점차 증가하는 것으로 나타났다. 이와 같 이 TiO2 결정 내부에 침입형으로 존재하는 보론의 비율 이 높을 경우 에너지 밴드갭이 감소되는 효과가 나타나 지만 이때 형성되는 불순물 에너지띠의 위치는 치환형 과 침입형이 비슷하게 존재하는 경우에 비해 더 높은 위 치에서 형성되는 것으로 알려져 있다.6) 이 경우 새롭게 생성된 불순물 에너지 레벨은 가시광 영역에서의 흡광 능력의 개선효과 보다는 광여기에 의해 발생된 전자와 정공의 재결합 억제를 통한 전하이동반응을 현저하게 개 선시키기 때문에 광촉매 효율을 증가시키게 된다. 따라 서 PEO 방식을 통해 제조된 TiO2 광촉매의 염료분해 효 율과 반응상수는 TiO2 산화피막 내부로 도핑되는 보론 원자들이 많을수록, 도핑된 보론이 TiO2 결정내의 침입 형 위치로 존재하는 비율이 높아 질수록 점차 증가하는 것으로 나타났다.
4.결 론
광촉매 효율성을 향상시킨 고효율 TiO2 광촉매를 제 조하는 것을 목적으로 보론이 도핑된 TiO2 산화피막을 plasma electrolytic oxidation (PEO) 방식을 통해 제조했 으며, 이때 전해액으로는 0.5 M의 H2SO4과 다양한 농 도의 H3BO3 용액이 첨가된 혼합용액을 사용하였다. PEO 방식을 통해 제조된 TiO2 광촉매의 경우, XRD 측정결 과를 통해 전해액의 종류와 관계없이 대부분 anatase 결 정과 약간의 rutile 결정이 혼합된 형태로 조성되어 있 었다. 그러나 고농도의 H3BO3 첨가제가 혼합된 전해액 에서 형성된 TiO2 피막일수록, TiO2 산화 피막 내부에 는 많은 양의 보론이 도핑 되었으며 TiO2 anatase 단위 격자의 부피가 증가하는 것으로 나타났다. 이것은 용액 속에 존재하는 보론이온이 TiO2 결정내부로 침투하여 침 입형 상태로 존재하기 때문에 TiO2 격자는 점차 팽창하 게 되어 단위 격자의 부피가 증가한 것으로 판단된다.
XPS 분석 결과에서는 높은 농도의 H3BO3가 첨가된 전 해액에서 제조된 산화피막 일수록, B 1s 에너지 피크 중심이 191.45 eV에서 191.98 eV로 이동하였으며, 이 것은 도핑된 보론이온이 TiO2 결정내부에서 치환형 보 다는 대부분이 침입형의 형태로 존재하고 있는 것을 나 타냈다. 광전류 반응 결과에서도 TiO2 산화피막 내부로 도핑되는 보론의 양이 많을수록, 그리고 도핑된 보론이 TiO2 결정내의 침입형 위치로 존재하는 비율이 높아 질 수록 광촉매의 전하이동 반응이 개선되어 광여기에 의 해 생성되는 광전류의 크기가 증가하였으며, rhodamine B 염료의 분해효율과 분해반응 상수도 증가하는 경향을 나타냈다. 이것은 침입형 위치의 보론에 의해 TiO2 결 정내에서 형성된 불순물 에너지띠에 의해 TiO2 밴드갭 에너지가 감소되는 효과뿐 아니라 TiO2 표면에서 광여 기된 전자와 정공의 재결합이 억제되어 전하이동 반응 의 효과를 상승시켜 주기 때문에 전반적인 광촉매 효율 이 현저하게 증가된 것으로 사료된다.