1. 서 론
최근 차세대 에너지원인 각종 전지의 전극재료로 이용 되는 탄소 소재는 물리적, 화학적 유용성으로 인하여 다 양한 응용 연구가 진행되고 있다.1-4) 전극재료는 전기전 도성, 열전도성, 열 충격저항, 높은 비표면적 그리고 화 학적 안정성 등이 필수적으로 요구된다. 흑연은 상온에 서 높은 전기전도성과, 알루미늄, 구리, 철 등의 전도성 금속에 비해 현저히 낮은 열팽창율과 높은 열전도성으 로 인한 열 충격저항 등의 유용한 특성을 나타낸다.5-7) 그러나 천연흑연은 결정성은 뛰어난 반면, 비표면적이 매 우 낮고 고순도로 정재의 어려움이 있으며, 합성흑연은 약 2000 °C의 높은 온도에서 장시간의 흑연화 과정을 거 쳐야 하는 제조상의 어려움과 결정화도가 낮은 문제점 을 안고 있다.
따라서 인조흑연의 폭넓은 응용을 위해서는 흑연의 기 공모양과 분표, 비표면적과 결정화도를 인위적으로 조정 할 수 있는 합성 방법을 찾는 것이 필수적이다. 특히 탄 소가 흑연으로 결정화되는 과정은 매우 높은 온도와 불 활성 분위기를 요구한다는 점을 감안할 때, 탄소가 분 자차원에서 거동할 수 있는 나노 차원의 반응공간과 적 절한 촉매를 활용하는 방법이 해결책이 될 수 있다. 층 상 실리케이트의 층과 층 사이의 2차원 공간은 공기와 의 접촉이 어려운 불활성의 극한 분위기를 제공할 수 있 어서 나노 차원의 반응기로서 역할을 할 수 있으며, 특 히 흑연과 같은 층상화합물의 배향을 도울 수 있다.
또한 층상 실리케이트는 수열합성에 의해 대량 합성이 용이하며, 불산 또는 알칼리에 의해 용출된 실리카 폐 액은 다시 사용할 수 있는 장점이 있다. 특히 층상 실 리케이트는 높은 이온 교환능으로 인하여 층과 층 사이 의 2차원 공간은 유동적인 확장이 가능하여 다양한 크 기와 입체구조를 갖는 금속이온 혹은 유기물질을 층간 삽입시킬 수 있다. 일반적으로 흑연 제조에 이용되는 탄 소 원료로는 열처리에 의해 흑연화될 수 있는 통상의 유 기물이 이용될 수 있다. 하지만 나프타 열분해 공정의 부산물로써 다환족 탄화수소가 60 % 이상인 PFO을 이 용할 경우 거의 순수한 탄소 화합물로써 자원 재활용에 의미가 있다.
우리는 선행연구에서 다공성 층상탄소와 흑연을 제조 함에 있어서 층상 실리케이트 주형을 이용할 수 있음을 이미 보고한 바 있다8-10). 또한 Co가 탄소를 흑연으로 열 변환시키는 촉매로 작용할 수 있음을 보고하였다11). 여 기서 사용한 Co촉매는 고가의 Co-hexanoate를 이용하였 다. 그러나 본 연구에서는 Co(NO3)2·6H2O와 Ni(NO3)2· 6H2O와 같은 구하기 쉽고 값싼 시약을 이용하여 Co와 Ni를 magadiite 층간에 삽입하여 다공성 흑연을 제조하 고자 하였다. 또한 층간에 도입된 Co와 Ni의 양의 변 화에 따른 다공성 흑연의 물리적 성질을 XRD, SEM, EDS, N2 자동흡착장치를 이용하여 조사하였다.
2. 실험 방법
2.1 시약
Na-magadiite, H-magadiite 그리고 organo-magadiite 합성을 위해서 sodium silicate(Shin-hung, 38 %), H2SO4 (Oriental chemical, 99%), HCl(Oriental chemical, 37 %), dodecylamine(DDA, Junsei, 98 %), EtOH(Jin chemical, 95 %), NaOH(DC chemical, 98 %)를 사용하였으며, 촉매 원료로서 Co(NO3)2·6H2O(Aldrich, 98 %), Ni(NO3)2·6H2O (Aldrich, crystal)를 사용하였다. 흑연 전구체로 사용한 PFO(Honam petrochemical)는 평균분자량이 대략 8000 정도의 지방족과 방향족 탄화수소의 혼합물로서, 비점이 288 °C 이하인 탄화수소가 67 %이고, 288 °C 이상이 33 % 로 구성되며, 그 중 60 % 이상이 방향족화합물이었다. Magadiite 주형을 용출 제거하기 위해서 HF(DC chemical, 48 %)를 사용하였다.
2.2 Na-magadiite와 H-magadiite의 합성
Na-magadiite는 sodium silicate를 원료로 이용하는 Kwon et al.12,13)의 방법을 적용하였다. H2SO4 용액(10%) 250 ml 을 70-80 °C의 온도에서 잘 저어주면서, 여기에 sodium silicate 용액(38 %) 250 g을 pH 6-7에 도달할 때까지 서 서히 첨가하여 실리카를 침전시켰다. 여기에 증류수와 NaOH를 추가하여 SiO2: NaOH : H2O의 몰 비가 1 : 0.3 : 33.3이 되도록 조정한 후, stainless steel autoclave에 넣 고 160 °C에서 72h 동안 수열 반응시켰다. 반응물을 여 과한 후, 증류수로 3회 이상 세척하여 과잉으로 남아있 는 염과 알칼리를 제거하고 40 °C에서 건조하여 Namagadiite를 얻었다. 또한 magadiite의 층간에 유기물을 도입하기 위해 Na-magadiite의 Na+를 H+로 이온 교환하 여 H-magadiite를 제조하였다. Na-magadiite 40 g을 증류 수 500 ml에 분산시키고, 0.10 N-HCl 용액을 12h에 걸쳐 서서히 적가하여 pH가 1.9로 되도록 한 후, 12h 동안 유지하면서 더 이상의 pH 변화가 없으면 여과하고, 증 류수로 Cl−이온이 남지 않도록 완전히 씻어내고 40 °C에 서 건조하였다.
2.3 Co/magadiite, Co/DDA/magadiite Ni/DDA/ magadiite의 제조
Co/MA는 Na-magadiite의 Na 이온을 Co 이온으로 직 접 이온 교환하여 제조한 것이며, Co/DDA/MA와 Ni/ DDA/MA는 H-magadiite의 층간에 먼저 DDA를 층간 삽입한 후, DDA의 리간드적 성질을 이용하여 Co와 Ni 를 층간 도입하여 제조한 것이다. Co/MA 시료는 각각 6.3, 12.5 그리고 25.0 g의 Co(NO3)2·6H2O를 증류수 100 ml에 녹이고, 각각의 용액에 Na-magadiite 5 g씩 가하고 상온에서 교반하면서 20h 동안 유지한 후, 여과하고 증 류수로 세척한 후 80 °C에서 건조하여 얻었으며, 각각 Co/MA-1, Co/MA-2 그리고 Co/MA-3로 칭하였다.
Co/DDA/MA의 제조를 위해 먼저 10 g의 H-magadiite 를 0.5 M DDA-ETOH 용액 20 ml에 분산시키고, 50 °C 의 오븐에서 증발 건조하여 DDA가 층간 삽입된 DDA/ MA를 제조하였다.14-16) 에탄올 용액 100 ml에 Co(NO3)2· 6H2O을 각각 6.3 g과 12.5 g씩 녹이고, DDA/MA 5 g을 가하고 잘 교반하면서 5시간 동안 정치 후, 여과하고 80 °C에서 건조하였으며, 시료의 명칭을 Co/DDA/MA-1 과 -2로 칭하였다. 한편 흑연 결정화에 미치는 Ni의 촉 매효과를 Co와 비교하기위해 Ni의 몰수를 Co와 동일한 값이 되도록 Ni(NO3)2·6H2O를 취하고, Co/DDA/MA 제 조와 동일한 절차에 의해 Ni/DDA/MA를 제조하였다.
2.4 다공성 흑연의 합성
탄소 전구체인 PFO 30 g과 상기 제조된 Co/MA, Co/ DDA/MA 그리고 Ni/DDA/MA 시료 10 g을 교반기를 이 용하여 30 min 동안 혼합한 후, 상온에서 15h 동안 방 치하여 PFO의 자발적 층간 삽입을 유도하였다. 결과물 들을 알루미늄 보트에 넣고 tube furnace에서 3 l/min로 질소를 흘려주면서 900 °C에서 3h 동안 열분해 시켰다. 소 성된 시료를 24 %의 불산 용액에 6h 이상 분산시켜 실 리케이트 주형을 용출시키고, 여과, 세척, 건조하여 다공 성 흑연을 제조하였다.
2.5 특성 분석
XRD 분석은 X-ray powder diffractometer(Rigaku, D/ MAX-IIIB)를 이용하여 CuKα, 40 kV, 40 mA, Ni-filter 조건의 광원을 이용하여 1.5~60° 범위에서 0.02° 간격으 로 주사속도 4o/min로 측정되었다. 또한 scanning electron microscopes(Philips, XL 30S FEH, XL V.5.50)를 사용 하여 입자크기 및 형상을 관찰하였으며, 합성된 시료들 의 비표면적은 자동흡착장치(MicroMetrics, ASAP 2010) 를 사용하여 액체질소 온도(77 K)에서 질소가스 흡/탈착 자료로부터 구하였다. Energy dispersive X-ray spectrometer( EDS, Phoenix, EDAX V.3.)를 이용하여 시료의 화 학조성을 확인하였다.
3. 결과 및 고찰
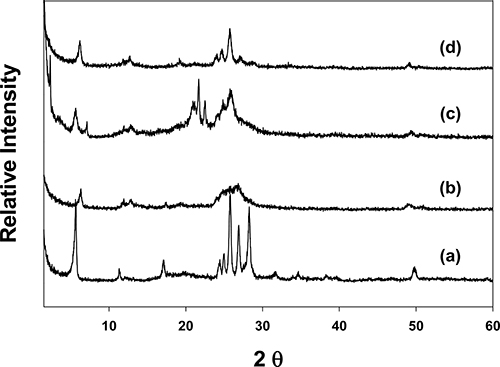
Fig. 1은 Na-magadiite와 DDA/MA, 그리고 CO2+가 층 간 삽입된 magadiite와 DDA/MA에 대한 XRD 피크를 나타낸 것이다. Fig. 1(a)는 Na-magadiite에 대한 피크로 써, d-spacing이 2.0 nm인 문헌 값17,18)과 잘 일치하는 전 형적인 결정 피크를 보여준다. CO2+를 이온교환으로 층 간 삽입시킨 Co/MA의 결정 구조를 보면 001면 피크의 세기가 작아짐과 동시에 CO2+ 이온의 층간 삽입에 의해 2θ의 값이 약간 오른쪽으로 이동함을 Fig. 1(b)에서 확 인할 수 있다. 이것은 수화 반경이 상대적으로 큰 CO2+ 이온이 CO2+ 이온으로 교환되면서 층간 간격이 약간 줄 었음을 보여준다. Fig. 1(c)는 DDA/MA의 피크로써 dspacing이 5.1 nm로 층간 간격이 크게 확장되었음을 보 여준다. 이것은 H-magadiite의 층 표면에 존재하는 Si- OH 그룹과 DDA간의 수소결합에 의해 DDA가 다량 층 간 삽입되었음을 보여준다. 그러나 Fig. 1(d)는 DDA/MA 를 CO2+ 이온이 녹아 있는 에탄올 용액으로 처리함으로 써 DDA의 일부가 용출됨으로 인하여 층간 간격이 다시 줄어들었음을 볼 수 있다.
Table 1은 CO2+와 Ni2+이온이 층간 삽입된 시료들의 EDS 분석 결과이다. Na-magadiite의 경우, 슬러리의 Co 함량을 변화시켜도 Co/MA에서 Co/Si 몰 비가 0.09로서 일정한 값을 나타내며, 이것은 용액 중 CO2+ 이온이 일 정 농도 이상이 되면 이온 교환될 수 있는 CO2+ 양이 포화 상태에 이름을 의미한다. 그러나 DDA/MA의 경우 슬러리의 CO2+ 농도가 증가하면 Co/DDA/MA에서 Co/Si 몰 비가 0.19에서 0.27로 두 배 이상 증가하였다. 또한 동일한 CO2+를 포함한 용액에서 Na-magadiite와 DDA/ MA를 처리할 경우, Co/Si 몰 비가 각각 0.08, 0.19로써 Co/DDA/MA가 Co/MA보다 두 배 이상 증가하였다. 또 한 동일한 Ni2+를 함유하는 용액에서 각각 처리했을 때, Ni/DDA/MA가 Ni/MA보다 Ni/Si 비가 0.05에서 0.18로 증가하였다. 이는 DDA/MA의 층간 간격이 DDA에 의 해 크게 확장되어 CO2+와 Ni2+의 침투를 용이하게 했을 뿐만 아니라, DDA가 배위자로 작용하여 CO2+와 Ni2+의 층간 삽입을 유도한 결과로 볼 수 있다.
Table 1
BET surface area of porous graphite prepared at various molar ratios of metal/Si in the presence of templates.
| Template | Molar ratio of metal/Si (EDS analysis) | BET Surface areas (m2/g) |
|---|---|---|
| Co/MA-1 | 0.09 | 400 |
| Co/MA-2 | 0.08 | 328 |
| Co/MA-3 | 0.09 | 373 |
| Ni/MA | 0.05 | 366 |
| Co/DDA/MA-1 | 0.19 | 477 |
| Co/DDA/MA-2 | 0.27 | 428 |
| Ni/DDA/MA | 0.18 | 477 |
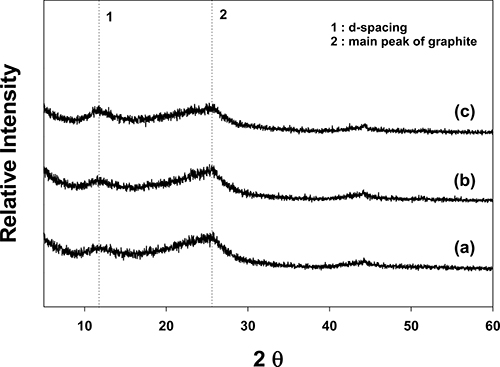
Fig. 2는 다양한 농도의 CO2+ 수용액에서 Na-magadiite 를 이온 교환시켜 제조한 Co/MA 주형에서 PFO를 탄 소 열 변환시킨 다공성 흑연의 XRD 피크를 보여준다. Co/Si 원자비와 무관하게 2θ = 26°에서 낮고 넓은 흑연 의 특성 피크가 나타나는 것으로 볼 때, 흑연의 결정구 조가 다소 무질서함을 보여준다. 그러나 2θ = 11° 부근에 서 약 0.7 nm의 d-spacing 값을 갖는 피크는 다공성 흑 연이 다소 무질서하지만 일정한 층간 간격을 갖고 있음 을 나타낸다. 또한 Fig. 3(a-c)에서처럼 흑연의 결정화를 나타내는 피크가 Co/Si 몰 비와 관계없이 일정하게 낮 은 이유는 이온 교환에 의해 층간 삽입될 수 있는 CO2+ 이온 양의 한계로 인하여 탄소 열 변환촉매로써 작용이 어려웠기 때문이다.
Fig. 3은 Co/Si 몰 비가 다른 Co/DDA/MA 주형으로 제조한 다공성 흑연의 XRD 피크를 나타낸 것이다. 2θ = 26o 부근의 흑연 고유의 피크가 뚜렷하게 증가할 뿐만 아니라, Co/Si 몰 비의 증가에 따라 증가하는 현상을 볼 수 있다. 이는 DDA의 전 처리 과정을 통하여 층간 거 리가 크게 확장된 DDA/MA의 층 사이에 많은 양의 CO2+ 이온이 충분히 층간 삽입되어 탄소가 흑연으로 열 변환과정에서 Co가 효과적인 촉매로 작용했음을 확인해 준다. 또한 2θ = 11° 부근에서 약 0.7 nm의 d-spacing 값 을 확인할 수 있는데 이는 박막들이 일정한 간격으로 서 로 포개어진 층상 구조의 다공성 흑연이 형성되었음을 보여준다.
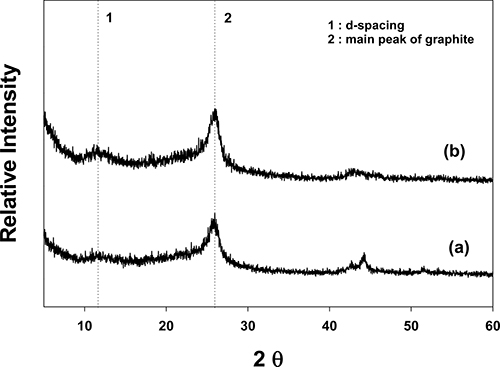
한편 Fig. 4는 Ni의 촉매효과를 보기위해 Ni/DDA/MA 주형을 이용하여 합성한 다공성 흑연의 XRD 피크를 Co/ DDA/MA와 비교해서 나타낸 것이다. Co/DDA/MA와 마 찬가지로 2θ = 26° 부근에서 흑연 고유의 피크가 뚜렷하 게 나타날 뿐만 아니라, 2θ = 11o에서 약 0.7 nm의 dspacing 값을 확인할 수 있다. 이는 Co뿐 아니라 Ni도 탄소-흑연 열 변환을 촉진시키는 촉매로써 작용함을 보 여 주며, Ni가 Co에 비해 구하기 쉽고 값이 싼 점을 고 려하면 매우 의미 있는 결과라 할 수 있다.
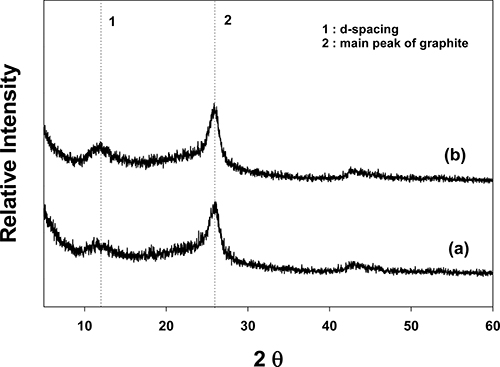
Fig. 4.
XRD patterns of porous graphite by Co/DDA/MA (a) and Ni/DDA/MA (b) with molar ratio of Co/Si and Ni/Si = 1.16.
Fig. 5는 DDA/MA 주형과 여기에 Co와 Ni를 층간 삽입한 주형으로 합성한 다공성 흑연의 SEM을 보여준 다. DDA/MA 주형 Fig. 5(a)의 경우, magadiite 고유의 장미꽃 형상을 유지하면서도 DDA의 층간 삽입으로 인 하여 엽들이 약간 팽창되었음을 보여준다. Co 촉매 Fig. 5(b)와 Ni 촉매 Fig. 5(c)를 이용하여 합성한 다공성 흑 연의 경우, DDA/MA에 비해 입자크기가 2~3 μm 정도 로 작아지지만, 개개의 엽들이 다발을 이루는 DDA/MA 의 형상을 그대로 유지하는 것으로 보아 주형의 효과가 잘 반영된 것으로 사료된다.
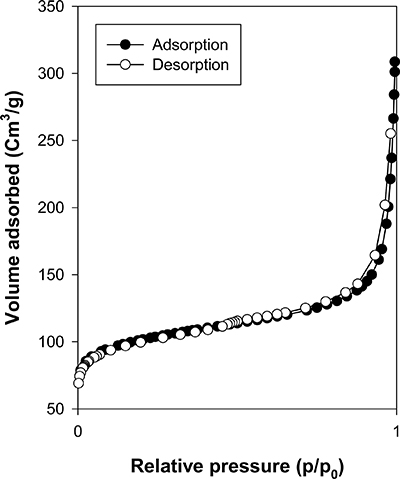
Fig. 6은 다공성 흑연의 전형적인 N2 흡탈착 등온선 으로써, Co/DDA/MA를 주형으로 합성한 다공성 흑연을 대표적으로 나타낸 것이다. 전형적인 II타입 유형의 흡 탈착 등온선을 보여주며, Table 1에 종합적으로 나타낸 비표면적은 328-477 m2/g의 큰 값을 보여주었다. 특히 DDA/MA 주형을 이용했을 때, 420 m2/g 이상의 큰 값 을 나타내는 것은 DDA에 의한 층간 거리 확장으로 상 대적으로 많은 양의 PFO가 층간 삽입된 결과로 볼 수 있다. 이것은 층상 실리케이트의 층간에서 탄소를 흑연 으로 열 변환시키고 주형을 제거함으로써 흑연의 비표 면적을 정량적으로 조절할 수 있음을 보여주는 매우 흥 미로운 결과로 볼 수 있다.
Fig. 7은 다공성 흑연의 TEM 사진으로써, 흑연의 층 상구조가 뚜렷하게 나타나며 magadiite 주형의 실리케이 트 층들이 있던 자리가 일정한 간격의 빈 공간을 형성 하고 있음을 잘 보여준다.
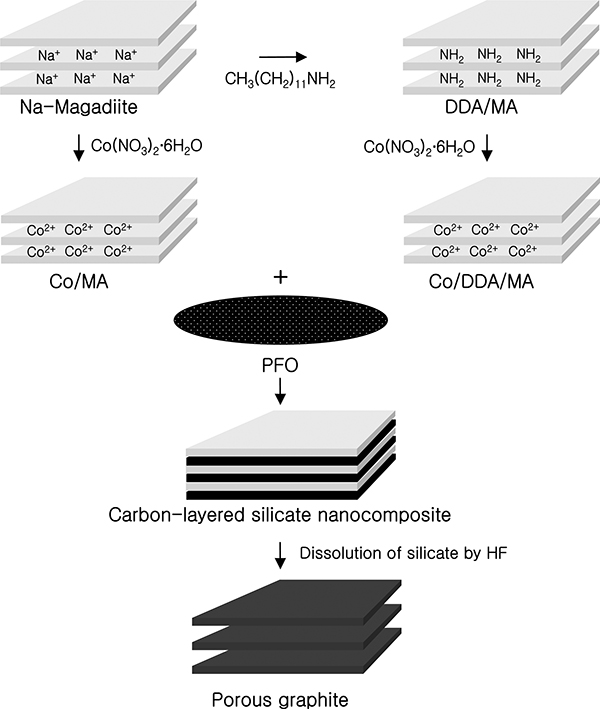
Fig. 8은 상기의 결과들의 토대로 하여 magadiite 주 형에 의한 다공성 흑연의 합성과정을 도식적으로 나타 낸 것이다. 전 처리에 의해 CO2+ 또는 Ni2+가 층간 삽 입된 magadiite 혹은 DDA/MA에 PFO를 혼합하게 되면 층간의 SiOH 그룹 혹은 DDA는 방향족 탄화수소와 같 은 유기물이 쉽게 층간 삽입될 수 있는 유기물 친화적 인 분위기를 형성한다. 열처리가 시작되면 온도 상승과 더불어 층밖에 존재하는 저비점의 탄화수소가 서서히 증 발하게 되면서 높은 분자량의 탄화수소가 추가적으로 층 내부로 스며들게 된다. 계속적인 열 변환이 일어나서 실 리케이트 층간에 탄소박막을 형성하게 된다. 불산 용액 으로 실리케이트 주형을 용출 제거하면 탄소만으로 이 루어진 다공성 층상 흑연을 얻게 된다.
4. 결 론
층간 거리가 유동적인 Na-magadiite를 CO2+로 직접 이 온교환 하거나 DDA를 층간 삽입하여 층간거리를 확장 시킨 DDA/MA에 CO2+ 혹은 Ni2+ 이온을 층간 삽입하고, 이를 주형으로 다공성 흑연을 합성한 결과 다음과 같은 결론을 얻었다.
1) DDA/MA를 주형으로 이용하였을 경우 CO2+ 혹은 N2+ 이온이 효과적으로 층간 삽입되었으며, 이것은 넓은 층간 거리와 층 내부의 아민기가 CO2+ 혹은 Ni2+ 이온 에 대한 배위자의 역할을 함으로써 층내 도입을 정량적 으로 조절할 수 있음을 보여주었다. 흑연의 결정화도는 층간 삽입된 Co와 Ni의 양에 뚜렷한 의존성을 보여주 어 Co와 Ni가 흑연결정화에 효과적인 촉매로서 작용할 수 있음을 확인해 주었다.
2) 합성된 다공성 흑연은 개개의 흑연 박막들이 일정 간격으로 적층된 층상 구조로써, 이는 magadiite가 효과 적인 주형으로 작용하였음으로 확인해 준다.
3) 다공성 흑연은 전형적인 II 타입 유형의 흡탈착 등 온선을 나타내었으며, 비표면적은 328-477 m2/g의 큰 값 을 보여주었다. 특히 DDA/MA 주형을 이용했을 때, 420 m2/g 이상의 큰 값을 나타내는 것은 DDA에 의한 층간 거리 확장으로 상대적으로 많은 양의 PFO가 층간 삽입 된 결과로 볼 수 있다.