1. 서 론
최근 화석연료의 남용에 따라 환경오염 문제가 극심 해지면서, 이를 대체할 수 있는 이차전지, 레독스 흐름 전지, 슈퍼커패시터 등의 에너지 저장 소자에 대한 수 요가 급증하고 있다.1,2) 이 중 슈퍼커패시터는 반 영구 적 수명, 높은 출력밀도, 빠른 충전 속도 및 낮은 작 동 온도 등의 장점을 가지고 있기 때문에 전기자동차, 휴대폰, 소형 전자소자 등의 첨단 산업 분야에 활용되 고 있다.3) 슈퍼커패시터는 구동원리에 따라 크게 faradiac 반응을 기반한 의사 커패시터(pseudocapacitor), 전하의 물리적 흡·탈착 반응을 기반한 전기 이중층 커패시터 (electric double layer capacitor), 두 가지 커패시터를 혼합한 하이브리드 커패시터(hybrid capacitor)로 구분된 다.4) 이 중 의사 커패시터는 전극, 전해질, 분리막으로 구성되어 있으며, 전극 표면에서 전극소재의 산화·환원 반 응을 통해 전하를 축적하는 거동이 일어나 이차전지와 유사한 특성을 나타낸다. 이러한 관점에서 의사 커패시 터는 우수한 정전용량의 장점을 가지지만 산화·환원 반 응에 필요한 이온 및 전자의 이동이 느리기 때문에 전 기 이중층 커패시터와 비교하여 낮은 안정성 및 느린 충 전속도를 갖는다.3,4)
의사 커패시터의 전극 소재로 주로 사용되는 것은 전 이 금속 화합물, 전도성 고분자, 탄소 복합소재 등이 사 용된다. 전이 금속 화합물은 높은 정전용량을 가지고 있 지만 낮은 이온/전기 전도도로 인한 느린 충방전 속도 와 낮은 안정성으로 이를 해결하고자 하는 연구가 활 발히 진행되고 있다.5) 전이 금속 화합물 중 전이 금속 수산화물(transition metal hydroxides, TMHs)은 높은 이론 용량, 저렴한 가격, 환경친화적, 합성 용이성 등 의 장점뿐만 아니라 결정학적으로 층상 구조를 이루고 있어 우수한 이온 확산 속도를 가지고 있다. 이러한 구 조적 특징으로 인해 높은 율속 특성을 나타내며, 구조 적 변화가 적어 우수한 사이클 안정성을 나타내어 의사 커패시터의 전극 소재로 다양한 연구가 진행되고 있다. 예를 들어, Ede 등은 solvethermal 방법을 이용하여 Ni/ Ni(OH)2 입자를 개발하여 이를 의사 커패시터 전극소재 로 활용하여 1mV/s의 스캔 속도에서 550F/g의 용량을 나타냈으며, Jiang 등은 자가조립법을 이용하여 꽃 형상 의 Ni(OH)2 입자를 개발하여 50mV/s의 스캔속도에서 697F/g의 용량을 나타내었다.6,7) 또한, He 등은 용액합성 법을 이용하여 중공 구조의 Ni(OH)2@PPy 입자를 개발 하였고, 전기화학 특성 평가 결과 1A/g의 전류밀도에서 934F/g의 용량을 나타내었다.8) 하지만, 아직까지 전이 금 속 수산화물의 나노 형상 제어 기술과 나노 형상에 따 른 의사 커패시터 특성에 대한 체계적인 연구는 미흡한 실정이다.
따라서, 본 연구에서는 수열합성법을 이용하여 전이 금 속 수산화물 중 NiCo(OH)2 소재의 나노 형상 제어 기 술을 개발하고, 이들의 형상학적 구조와 전기화학적 특 성간의 상관관계 규명을 수행하였다. NiCo(OH)2는 우수 한 정전용량(~2300F/g)을 가지고 있어 의사커패시터의 전 극소재로 연구가 진행되고 있으나, 그들의 낮은 전도도 및 응집성으로 인해 NiCo(OH)2 입자의 형상은 전기화 학적 특성에 큰 영향을 미친다. 따라서, 본 연구에서는 수열합성 중 urea 첨가제의 분해 반응을 이용하여 간단 하게 용액 내 pH를 제어하였고, NiCo(OH)2의 나노입자 를 판상, 바늘상, 바늘상이 응집된 구형 입자상으로 성 공적으로 제어하였다. 결과적으로, 의사 커패시터 전극 소 재로 합성한 NiCo(OH)2를 적용하여 평가하고, 전기화학 적 특성을 향상 시킬 수 있는 최적의 나노 구조를 갖 는 NiCo(OH)2 형상을 제안하였다.
2. 실험방법
Nickel cobalt hydroxide [NiCo(OH)2]가 담지된 Ni foam (Ni, 99.95%)를 제조하기 위하여 수열합성법을 활용 하였다. NiCo(OH)2 담지를 위한 Ni foam는 1 × 12 cm2 크기로 절삭한 후 사용하였다. 수열합성에 사용된 혼합 용 액은 0.2M nickel nitrate hexahydrate [Ni(NO3)2·6H2O, 98.5 %, Aldrich] 및 0.2M cobalt nitrate hexahydrate [Co(NO3)2·6H2O, 98.0%, Aldrich]를 20ml의 증류수에 3 시간동안 교반하였고, 그 후 NiCo(OH)2의 형상제어를 위 해서 각각 0.09, 0.18, 0.27M의 urea (CH4N2O, 99.5 %, Aldrich)를 첨가하여 용해시켰다. 첨가된 urea는 수열합 성 시 분해되어 암모니아를 형성하는 첨가제로 용액 내 pH를 조절하여 NiCo(OH)2 형상을 제어할 수 있으며, 각각의 첨가량에 따른 pH는 8.5, 8.7 및 9.0로 나타났 다. 그 후, 준비된 용액은 100 mL teflon lined stainless steel auto-clave에 옮겨 담은 후 절삭된 Ni foam를 용액 내에 1.5 cm만 담지되도록 위치시켰다. 수열합성 공정은 120 °C에서 12시간동안 진행되었으며, 수열합성 이후의 샘플들은 증류수를 이용하여 3회 세척한 후 건조 오븐 을 이용하여 80 °C에서 12시간동안 건조하였다. 또한, 합 성 전∙후의 무게를 측정하여 비교했을 때 샘플에 코팅 된 NiCo(OH)2 입자는 각각 13.1, 13.5, 14.4 wt%로 확인되었다. 건조가 끝난 NiCo(OH)2가 담지된 Ni foam 는 urea의 첨가량에 따라 각각 NCOH-U9, NCOH-U18, NCOH-U27로 언급될 것이다.
NiCo(OH)2가 담지된 Ni foam 샘플의 형상 및 구조는 전계 방사형 주사 전자 현미경(field emission scanning electron microscopy, FESEM, Nova NanoSEM 450)를 이용하여 분석하였고, 샘플의 성분은 X-선 분광 분석기 가 장착된 전계 방사형 주사전자 현미경(energy dispersive spectroscopy, EDS, Nova NanoSEM 450)을 이용하여 분석하였다. 또한, 제조한 샘플의 결정 구조는 X-ray diffraction (XRD, Rigaku Rint 2500)을 이용하여 1°/min 의 속도로 2θ = 10 - 90° 범위에서 측정하였으며, 화학 적 결합 상태는 X-ray photoelectron spectroscopy (XPS, ESCALAB 250)을 이용하여 분석하였다. NiCo(OH)2의 형상에 따른 샘플의 비표면적 분석을 위하여 brunaueremmet- teller (BET, Micromeritics ASAP2010)을 이용하 여 분석하였고, 분석 전 샘플의 이물질 및 흡착 물질을 제거하기 위해서 질소 분위기에서 350 °C로 전처리 하였 다. 전기화학적 분석은 potentiostat/galvanostat (CS310, Corrtest Instruments Corp.)를 이용하여 삼 전극 시스템 형태로 측정하였다. 삼 전극 시스템은 기준전극(Ag/AgCl saturated KCl), 상대전극(Pt wire) 및 작업전극(NCOHU9, NCOH-U18 및 NCOH-U27)로 구성하였고, 6M 수 산화 칼륨(potassium hydroxide, KOH) 전해질 내에서 측정하였다. 수산화 칼륨 전해질은 일반적으로 사용되는 의사커패시터의 전해질로 NiCo(OH)2 전극소재를 평가 하는데 주로 사용되는 전해질이다. 또한, 제조한 샘플의 전기화학적 거동은 순환전압전류법(cyclic voltammetry, CV)를 이용하여 0.0-0.4V 범위에서 1mV/s 속도로 측정 하였고, 에너지 저장 성능은 정전류 충방전법(galvanostatic charge-discharge test)을 이용하여 0.5, 0.7, 1.0, 1.5, 2.0, 3.0, 5.0, 10.0A/g의 전류밀도에서 0.0 - 0.4 V 범위로 측정하였다. 특히, 샘플의 전기화학적 안정성을 평가하기 위해 10.0 A/g의 고 전류밀도에서 5,000회 충∙방전 평 가를 수행하였다.
3. 결과 및 고찰
Fig. 1은 urea 첨가량에 따른 NiCo(OH)2가 담지된 Ni foam의 형상 변화에 대한 모식도이다. Ni foam 표면의 NiCo(OH)2 입자는 수열합성 과정 중 발생하는 urea의 분 해 및 Ni2+/Co2+ 이온의 환원 단계를 통해 형성된다. Urea의 분해는 용액 내에 OH- 이온을 형성시켜 Ni2+/ Co2+ 이온의 환원 속도를 제어하는 중요한 요소이다. Urea의 분해에 따른 OH- 이온의 형성 과정은 다음과 같 다[식 (1)-(2)].9,10)
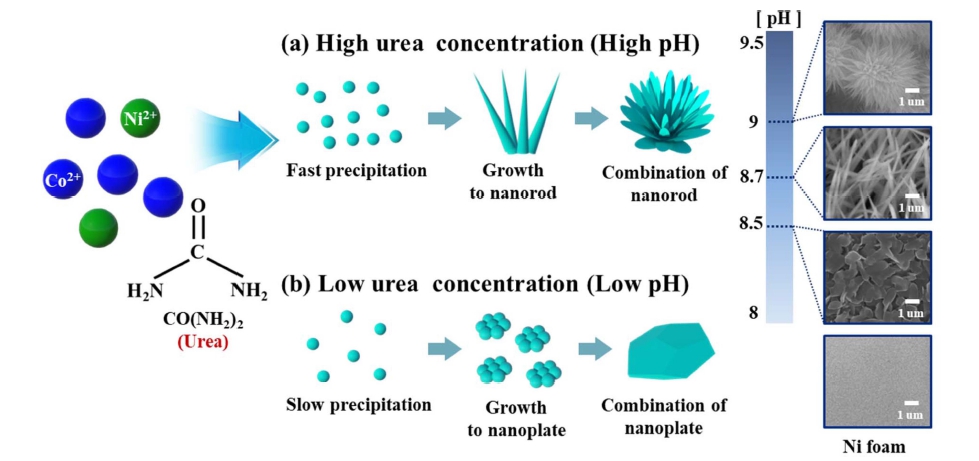
Fig. 1
Schematic illustration of the synthesis mechanism for the NiCo(OH)2 nanoparticles decorated on Ni faom.
Urea는 수용성 시약으로 NH3와 CO2로 분해된 후 NH3가 H2O와 반응하여 NH4+ 이온과 OH- 이온을 발생 시킨다. 그 후 용액 내 생성된 OH- 이온으로부터 Ni2+/ Co2+ 이온이 환원되어 NiCo(OH)2 입자를 형성한다. Ni2+ 및 Co2+의 환원 반응은 다음과 같다[식 (3)].9,10)
많은 양의 urea가 첨가되는 경우 용액 내 OH- 이온 농도는 급격히 증가하고 Ni2+/Co2+ 이온을 빠르게 환원 시켜 작은 NiCo(OH)2 입자가 형성된다[Fig. 1(a)]. 작은 NiCo(OH)2 입자는 높은 pH 내에서 바늘 형상으로 성 장하게 되며, 불안정한 표면적을 최소화하기 위해 응 집되고 Ni foam 표면에 담지된다.9,11) 반면에 적은 양 의 urea가 첨가되어 상대적으로 낮은 pH의 용액에서는 Ni2+/Co2+ 이온이 OH- 이온과 반응하여 환원되며, 느린 속도로 NiCo(OH)2 입자를 형성한다[Fig 1(b)]. 형성된 NiCo(OH)2는 점차 성장하여 판상 형태로 나타나며 Ni foam 표면에 담지된다.9,11) 이는 NiCo(OH)2의 핵 생성 및 성장 간의 관계로 설명되며, 생성된 NiCo(OH)2 입 자가 주어진 환경에서 안정적인 결정학적 구조를 가지 도록 성장되는 것이다. 결과적으로, urea의 첨가량을 조 절함으로써 Ni2+/Co2+ 이온과 OH- 이온의 반응 속도를 제어할 수 있고, 전기화학 커패시터에 유리한 구조적 특 성을 가지도록 NiCo(OH)2의 나노입자 형상을 제어할 수 있다.
Fig. 2는 각각 Ni foam, NCOH-U9, NCOH-U18 및 NCOH-U27의 저 배율[Fig. 2(a)-(d)] 및 고 배율[Fig. 2(e)-(h)]의 전계 방사형 주사전자 현미경 이미지를 나타 낸다. NiCo(OH)2 지지체로 사용된 Ni foam은 직경이 42.7 - 58.1 um의 Ni 골격 구조로 매끈한 표면 구조를 나타낸다[Fig. 2(a) 및 (e)]. NCOH-U9, NCOH-U18 및 NCOH-U27은 표면에 형성된 NiCo(OH)2 입자로 인 해 거친 표면이 나타나는 것을 확인할 수 있다[Fig. 2(b)- (d)]. 또한, 상대적으로 낮은 pH에서 합성된 NCOH-U9는 361.4 - 444.1 nm 직경을 갖는 판상 형태의 NiCo(OH)2 입 자가 형성된 것을 확인할 수 있는데, 이는 Ni2+ 및 Co2+ 이온이 OH- 이온과 느리게 반응하면서 NiCo(OH)2가 판 상 형태로 성장하였기 때문이다[Fig. 2(f)]. 반면에, 비교 적 높은 pH에서 합성된 NCOH-U18은 54.7 - 87.5 nm의 직경을 갖는 바늘 형상의 NiCo(OH)2가 확인되었다[Fig. 2(g)]. 이는 증가된 pH로부터 Ni2+ 및 Co2+ 이온이 OH- 이온과 빠르게 반응하면서 작은 NiCo(OH)2 입자 형성 되고 Ni foam 표면에서 바늘 형상으로 성장한 것이다. 또한, 가장 높은 pH에서 합성된 NCOH-U27의 경우 표 면에 31.3 - 48.9 nm 직경을 갖는 바늘 형상의 입자가 응 집되어 7.3 - 7.6 um 크기의 구 형태로 담지된 것을 확 인할 수 있다. 이러한 현상은 Ni2+ 및 Co2+ 이온과 OH- 이온의 빠른 속도로 반응하여 형성된 NiCo(OH)2 입자 가 불안정한 표면적을 감소시키기 위해 서로 응집된 것 이다. 따라서, urea의 첨가량에 따라 용액 내 pH를 조 절하고 Ni2+ 및 Co2+ 이온과 OH- 이온의 반응 속도를 제어함으로써 NiCo(OH)2 입자의 형태가 변화하는 것을 확인하였다.

Fig. 2
(a-d) Low-resolution and (e-h) high-resolution FESEM images of Ni foam, NCOH-U9, NCOH-U18, and NCOH-U27.
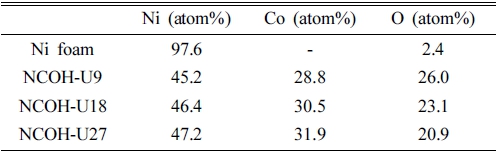
Fig. 3(a)-(d)는 Ni foam, NCOH-U9, NCOH-U18 및 NCOH-U27의 X-선 분광 분석 결과를 보여준다. 실험에 사용된 Ni foam은 금속 소재로 97.6 %의 Ni 성분과 공 기 중에서 산화로 인한 2.4%의 O 성분으로 구성되어 있다. NCOH-U9, NCOH-U18 및 NCOH-U27 샘플들은 표면에 형성된 NiCo(OH)2로부터 Ni, Co, O 성분이 검 출되었으며, 유사한 원소 함량비를 나타내는 것으로 보 아 NiCo(OH)2 입자가 잘 합성된 것으로 판단된다. 모 든 샘플의 원소 함량비는 Table 1에 나타내었다.

Fig. 3
SEM-EDS mapping images obtained from (a) Ni foam, (b) NCOH-U9, (c) NCOH-U18, and (d) NCOH-U27.
Fig. 4(a)는 Ni foam, NCOH-U9, NCOH-U18 및 NCOH-U27의 X-선 회절 패턴을 보여준다. 모든 샘플에 서 45.1°, 52.3° 및 77.4°의 2θ 값에서 강한 회절 패턴이 나타나며, 이는 Ni foam에 해당하는 face-centered cubic (fcc) 구조를 갖는 Ni 금속 상(JCPDS card No. 03-1051) 의 (111), (200) 및 (222)면을 의미한다.12) 또한, NCOHU9, NCOH-U18 및 NCOH-U27 샘플은 Ni foam상 이 외에 19.3°, 33.1°, 38.6°, 52.8° 및 59.1°의 2θ 값에서 회절패턴이 나타나는데, 이는 β-NiCo(OH)2 상(JCPDS No. 14-0117)의 (001), (100), (101), (102) 및 (110)면에 상 응한다.13,14) 특히, urea의 첨가량이 증가할수록 (100)면의 peak의 강도가 점차 증가하는 것을 확인할 수 있는데, 이 는 NiCo(OH)2 입자가 (100)면으로 성장하여 안정한 구 조의 바늘상을 형성한 이유로 판단된다. 그러나, NCOHU27의 경우 23.2° 및 34.9°의 2θ 값에서 rhombohedral 구조를 갖는 α-Ni(OH)2 상(JCPDS card No. 38-0715)의 (006) 및 (012)면에 상응하는 회절패턴이 추가로 관찰된 다.15) 이러한 이유는 증가된 urea의 함량으로 Ni2+/Co2+ 이온과 OH- 이온이 빠르게 반응하며 균일한 NiCo(OH)2 입자를 형성하지 못하고 일부분에서 α-NiOH2 입자가 형 성된 것으로 판단된다. α-NiOH2는 NiCo(OH)2보다 우수 한 안정성을 가지고 있으나, 전기적 특성이 NiCo(OH)2 보다 낮아 고 전류밀도에서의 전기화학적 특성을 감소 시킬 수 있다.
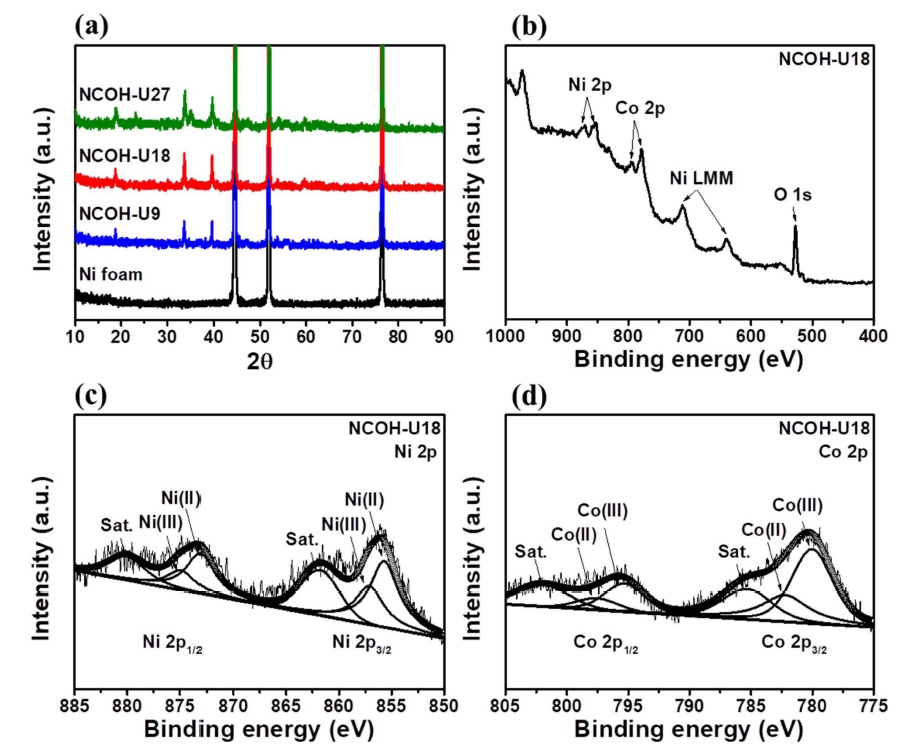
Fig. 4
(a) XRD results of Ni foam, NCOH-U9, NCOH-U18, and NCOH-U27, (b) XPS full spectrum consisting of (c) Ni 2p, (d) Co 2p obtained from NCOH-U18.
Fig. 4(b)-(d)는 NCOH-U18의 X-선 광전자 분광 스펙 트럼을 보여준다. 모든 스펙트럼의 결합에너지는 284.5 eV 의 C 1s를 기준으로 보정하였다. NCOH-U18의 전체 스 캔 범위의 스펙트럼에서 다른 성분 검출 없이 Ni 2p, Co 2p, O 1s 피크가 잘 형성된 것을 확인하였다[Fig. 4(b)]. Fig. 4(c)에서 나타낸 NCOH-U18의 Ni 2p core level은 Ni 2p3/2 및 Ni 2p1/2이 각각 세 개의 피크들로 이루어진 두 쌍의 doublet으로 보여진다. Ni 2p3/2 photo- electrons에서는 855.7 eV, 856.8 eV, 861.7 eV의 결합에너 지가, Ni 2p1/2 photoelectrons에서는 873.1 eV, 874.8 eV, 880.1 eV의 결합에너지에서 피크가 관찰되며, 이는 각각 Ni 성분과 관련된 Ni(II), Ni(III) 및 satellite 피크를 의 미한다.16) 또한, NCOH-U18의 Co 2p core level은 세 개의 피크들로 이루어진 두 쌍의 doublet으로 나타나는 Co 2p3/2 및 Co 2p1/2로 관찰되었다. Co 2p3/2 및 Co 2p1/2의 photoelectrons는 각각 Co(III) 상태를 의미하는 780.1 eV, 795.3 eV, Co(II) 상태를 의미하는 782.2 eV, 797. 6eV 및 satellite 피크를 의미하는 784.6 eV, 802.1 eV에서 나타난다.16) 결과적으로 NCOH-U18 전극은 X-선 회절 분석 및 X-선 광전자 분광법을 통해서 최적화된 결 정학적 및 형상학적 구조를 가진 바늘상의 NiCo(OH)2 입자가 Ni foam 표면에 잘 형성되었음을 확인할 수 있 었다.
Fig. 5는 질소 흡착 및 탈착 등온선을 이용하여 분석 한 샘플들의 비표면적 및 기공 부피 분석 결과이다. Ni foam은 낮은 비표면적으로 인해 질소 흡착 및 탈착 반 응이 정확하게 일어나지 않아 측정이 불가하였다. NCOHU9, NCOH-U18, NCOH-U27의 비표면적 및 기공 부피 는 각각 2.501m2 /g 및 0.023cm3 /g, 3.559 m2/g 및 0.304 cm3/g, 3.631 m2/g 및 0.311 cm3/g로 나타났다. 이는 urea 의 함량이 증가함에 따라 판상의 NiCo(OH)2 입자가 바 늘 형상으로 변화하면서 비표면적 및 기공 부피가 증가 한 것으로 판단된다. 샘플의 증가된 비표면적은 이온의 저장 공간을 개선시켜 높은 정전 용량을 구현할 수 있다.
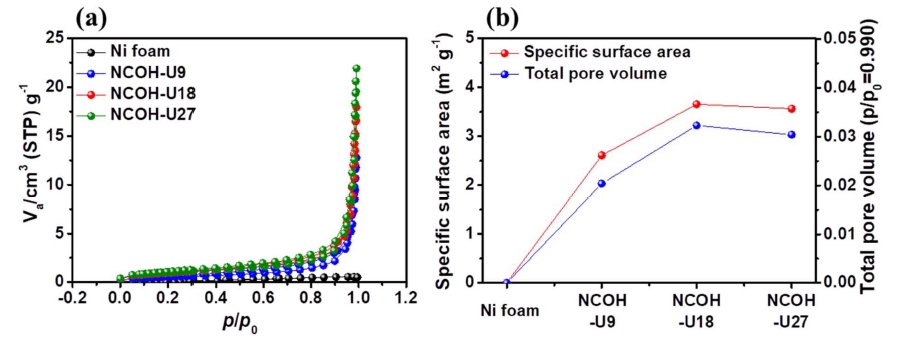
Fig. 5
(a) N2 adsorption/desorption isotherms and (b) specific surface area and total pore volume obtained from Ni foam, NCOH-U9, NCOH-U18, and NCOH-U27.
Fig. 6(a)는 제조한 샘플의 순환 전류-전압분석 결과를 나타낸다. 순환 전류-전압분석은 0 .0 - 0.4V (v s. A g/AgCl) 전압 범위 내에서 1mV/s의 주사 속도로 측정하였으며, 6M 수산화 칼륨 전해질 내에서 수행하였다. 모든 샘플 의 순환 전류-전압 곡선은 anodic 및 cathodic 반응에서 산화/환원 peak가 명확하게 나타나는 것으로 보아 전형 적인 의사 커패시터의 Faradaic 반응이 일어나는 것을 알 수 있다. NiCo(OH)2 입자의 산화/환원 반응은 다음 식 으로 설명할 수 있다[식 (4)-(5)].17)
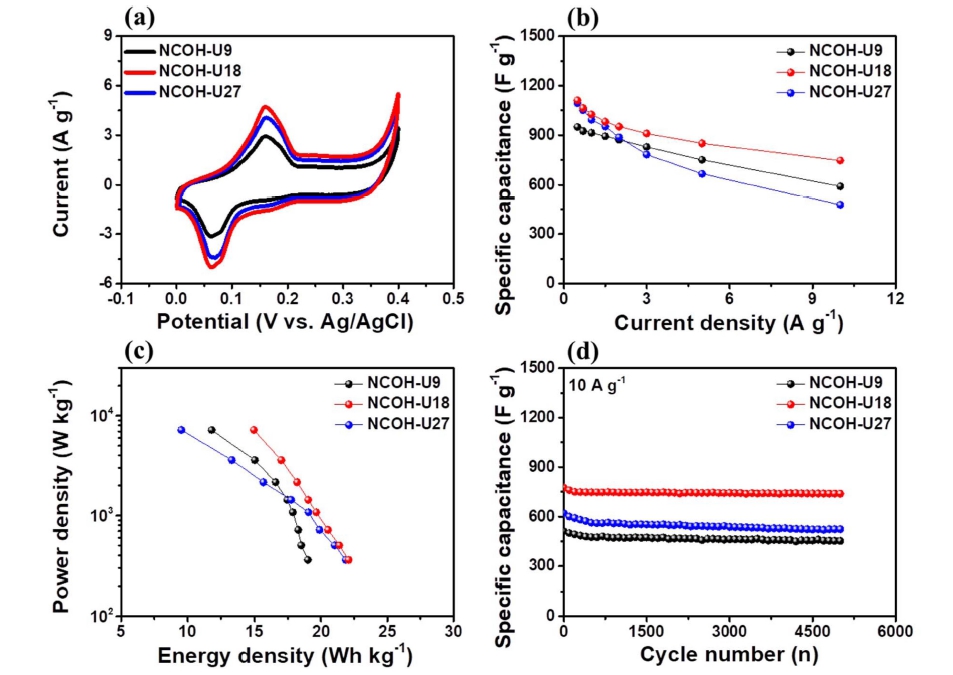
Fig. 6
(a) Cyclic voltammetry test at scan rate of 1 mV/s, (b) specific capacitance measured at current densities of 0.5-10.0 A/g, (c) ragone plots, and (d) long-term cycling test at high current density of 10.0 A/g up to 5,000 cycles.
NCOH-U9와 비교하여 NCOH-U18 및 NCOH-U27의 그래프 면적이 증가한 것을 확인할 수 있으며, 이는 NCOH-U18 및 NCOH-U27이 높은 전하 저장 용량을 갖는 것을 의미한다. 또한, NCOH-U9 및 NCOH-U18의 산화 및 환원 반응은 ~ 0.145 V 및 ~ 0.074 V에서 나타난 반면, NCOH-U27의 경우 NiCo(OH)2 와 함께 형성된 α- NiOH2 입자로부터 산화/환원 peak가 이동되어 ~ 0.152 V 및 ~ 0.082V에서 나타나는 것을 확인하였다.10,17)
또한, 제조한 샘플들의 저속 및 급속 충∙ 방전 특성을 확인하기 위하여 0.5, 0.7, 1.0, 1.5, 2.0, 3.0, 5.0 및 10.0 A/g의 전류밀도에서 충∙방전 평가를 수행하였다[Fig. 6(b)]. 모든 샘플의 정전용량은 다음 식을 이용하여 계 산하였다[식 (6)].18)
본 식에서 I(A)는 충∙방전 전류, m(g)은 활물질 무게, dV는 측정 전압 범위 및 dt는 방전 시간을 의미한다. 낮 은 전류밀도(0.5 A/g)에서 NCOH-U9, NCOH-U18 및 NCOH-U27의 정전용량은 각각 950.1, 1110.9 및 1093.3 F/g으로 나타났다. NCOH-U9 전극은 가장 낮은 정전용 량을 보이는데, 이것은 판상 형태의 NiCo(OH)2 입자의 낮은 비표면적으로 인해 수산화 이온을 저장할 수 있는 활성화 반응 면적의 한계가 있기 때문이다.5,18) 반면에 NCOH-U18 및 NCOH-U27 전극은 바늘 형상으로 성장 한 NiCo(OH)2 입자로부터 높은 비표면적을 가지기 때 문에 우수한 정전용량을 나타내었다. 또한, 높은 전류 밀도(10.0A/g)에서 NCOH-U9, NCOH-U18 및 NCOHU27의 정전용량은 각각 591.4, 746.7 및 476.2 F/g으로 나타났다. 특히 NCOH-U18 전극은 높은 전류밀도에서도 각각 67.2 %의 정전용량 유지율을 보이는 반면 NCOHU27 전극은 가장 낮은 정전용량 유지율(43.6 %)을 나 타내었다. 이는 Faradaic 반응에 필요한 이온 및 전자의 이동과 관련되는데, NCOH-U18 전극은 바늘 형상의 NiCo(OH)2가 Ni foam 표면에 바로 성장되어 있어 이온 및 전자의 이동에 유리하기 때문이다. 하지만, NCOHU27의 경우 Ni foam 표면에 NiCo(OH)2 입자가 응집된 상태로 존재하기 때문에 전기화학 반응 중 전자의 이동 에 제한을 받아 낮은 정전용량을 나타낸다.
Fig. 6(c)는 모든 샘플의 정전용량을 이용하여 에너지 밀도 및 출력 밀도를 계산한 그래프이다. 에너지 밀도 및 출력 밀도는 다음 식을 이용하여 계산하였다[식 (7)- (8)].5,18)
본 식에서 Csp는 샘플의 정전용량, V는 측정 전압 및 dt는 방전 시간을 의미한다. 모든 샘플에서 출력 밀도가 증가함에 따라 에너지 밀도는 감소하는 경향을 나타낸 다. 360-7200W/kg의 출력 밀도에서 NCOH-U9, NCOHU18 및 NCOH-U27의 에너지 밀도는 각각 19.0-11.8 Wh/kg, 22.1-14.9 Wh/kg, 21.9-9.5 Wh/kg로 확인되었다. 특히, NCOH-U18 전극은 Ni foam 표면에 균일하게 담 지된 바늘형상의 NiCo(OH)2 입자로 인해 높은 출력에 서도 다른 전극들과 비교하여 우수한 에너지 밀도를 나 타낸다.
Fig. 6(d)는 제조한 샘플의 사이클 안정성을 확인하기 위하여 10.0 A/g의 전류밀도에서 5,000회 동안 충∙방전 평가를 진행한 결과이다. 5,000회 충∙방전한 이후 NCOHU9, NCOH-U18 및 NCOH-U27 전극의 정전용량은 각 각 452.5, 739.4 및 523.7 F/g으로 나타났다. 특히, 높은 전류밀도에서 5,000회 충∙방전 평가를 수행했음에도 불 구하고 NCOH-U18은 높은 정전용량을 나타냈는데, 이는 Ni foam 표면에 높은 비표면적을 가진 바늘 형상의 NiCo(OH)2 입자로 안정적인 Faradaic 반응이 일어나기 때문에다. 결과적으로, NiCo(OH)2 입자가 담지된 Ni foam의 전기화학적 특성 향상은 다음과 같은 두 가지의 효과에 기인한다. 첫번째로, 샘플의 우수한 정전용량은 바 늘 형상으로 성장한 NiCo(OH)2 입자로부터 전기화학적 활 성 면적 증가에 기인한다. 두번째로, 증가된 전기화학적 안정성은 Ni foam 표면에 균일하게 형성된 NiCo(OH)2 입자로 전기화학 반응이 안정적으로 유지되기 때문으로 판단된다.
4. 결 론
본 연구에서는 고성능 슈퍼커패시터의 전극 제조를 위 해 수열합성법을 이용하여 Ni foam 표면에 NiCo(OH)2 입자를 성공적으로 담지하였다. 특히, urea의 첨가량 조 절을 통해 수열합성 반응 동안 용액 내의 pH를 제어하 여 Ni foam 표면에 NiCo(OH)2 입자를 판 형상(NCOHU9), 바늘 형상(NCOH-U18), 바늘 형상이 응집된 이차 입자(NCOH-U27)로 합성하였다. 이러한 과정을 통해 Ni foam 표면에 바늘 형상의 NiCo(OH)2 입자를 균일하게 담지하였다. 결과적으로, Ni foam 표면에 균일한 바늘 형 상의 NiCo(OH)2 입자를 갖는 NCOH-U18 전극은 0.5 A/g의 낮은 전류밀도에서 1110.9 F/g의 높은 정전용량을 나타났으며, 10.0 A/g의 고속 전류밀도에서 746.7 F/g의 우수한 정전용량을 나타냈다. 특히, 10.0 A/g의 고속 전 류밀도에서 5,000회 동안 충∙방전 평가를 수행한 이후에 도 95.6 %의 가장 높은 정전용량 유지율을 나타냈다. 이 는 바늘 형상으로 성장한 NiCo(OH)2 입자가 전기화학 적 활성 면적을 증가시켜 높은 정전용량을 나타내고, Ni foam 표면에 균일하게 담지됨으로써 안정적인 전기화학 반응을 통해 높은 용량 유지율을 나타낸 것으로 판단된 다. 따라서, 최적화된 NiCo(OH)2 입자의 형상 제어 기 술을 통해 합성된 바늘 형상의 NiCo(OH)2 입자가 담지 된 Ni foam 전극은 고용량 및 고안정성 슈퍼커패시터 전극으로 사용이 가능할 것으로 기대된다.