1. 서 론
2. 실험방법
2.1. 합성방법
2.2. 분석방법
3. 결과 및 고찰
3.1. 용액 플라즈마 공정(solution plasma process, SPP)
3.2. 콜로이드 MnO2 합성
3.3. MnO2 나노 입자 합성
4. 결 론
1. 서 론
망간산화물은 광물 자원이 풍부하고 가격이 저렴한 환경 친화적인 재료로서 다양한 분야에 사용되고 있을 뿐만 아니라 다양한 결정학적 구조와 형태를 가지며 전기화학적 특성이 우수하여 이차전지 및 슈퍼커패시터용 전극 재료, 촉매, 흡착제와 같은 환경 재료 분야의 연구도 활발히 진행되고 있다.1-3) 망간은 주로 +2, +3, +4가의 산화물 상태로 존재하고 있으며 그 중 +4가인 이산화망간(MnO2)이 여러 분야에 가장 널리 사용되고 있다. MnO2는 MnO6 팔면체의 Link 방식에 따라 1차원 chain-like tunnel-type (α-, β-, and γ-MnO2), 2차원 layered-type (δ-MnO2, birnessite) 및 3차원의 spinel-type (λ-type) 구조 가지며 이러한 결정학적 형태에 따라 커패시턴스, 촉매 활성, 이온 흡착 특성 및 전기화학적 특성이 달라지는 것으로 알려져 있다.4) 이 중 birnessite MnO2는 수화된 K+, Li+ 및 Na+와 같은 양이온이 삽입된 독특한 층상구조로 ~7 Å의 층간 거리를 가지며(β-MnO2: ~1.89 Å, γ-MnO2: ~1.89 및 ~2.3 Å), 이러한 충분한 층간 거리는 이온의 확산, 이동 및 산화환원 반응에 효과적인 것으로도 알려져 있다.5,6) 합성 방법에는 수열합성법(hydrothermal), 졸-겔법(sol-gel), 환원법 및 화학적 침전법 등이 있으며, 일반적으로 고온의 열원을 필요로 하거나 강산, 강염기, 환원제 등을 사용하여 장시간 반응을 통해 합성한다.6,7) 최근에는 환경 문제가 중요시되면서 Multi-step 공정, 고온 반응 및 독성의 화학 약품의 사용을 최소화한 녹색합성(green synthesis)을 기반으로 한 합성법 및 재료에 대한 연구가 집중되고 있다.
용액 플라즈마 공정(solution plasma process, SPP)은 용액 중 플라즈마 방전에 의해 발생하는 고에너지 전자, 라디칼 및 이온을 이용하여 용액과의 상호작용에 의해 새로운 물질을 합성하는 방법으로 기존의 기상 플라즈마와 달리 저온 비평형 플라즈마로써 상온에서 고속 용액 반응을 실현할 수 있다는 특징이 있다.8-12) 또한 이 합성법은 상기의 방법과 비교하여 짧은 프로세스 시간(수 분~수 십분 범위), 상온 ‧ 상압의 실험 조건, 간단한 실험 장치 및 화학적 첨가제를 사용하지 않는다는 이점이 있으며, 선행연구에 따르면 용액 플라즈마를 이용한 나노 입자의 합성, 수 처리, 유기화합물 분해 뿐만 아니라 차세대 에너지원으로 각광받고 있는 이차전지 및 연료전지의 전극재료 합성 등 현대기술 분야에 있어서도 다양한 응용 연구가 활발히 진행되고 있다.13-15) 본 연구에서는 이러한 용액 플라즈마법을 이용하여 층상구조를 갖는 콜로이드 형태의 망간 산화물 및 다공성 나노 입자 형태의 망간산화물 합성 및 그 반응 메커니즘에 대한 연구를 진행하였다. 첫 번째로 계면활성제, 환원제 또는 산화제와 같은 화학 시약을 첨가하지 않은 순수 과망간산칼륨 수용액 중에서 플라즈마를 발생시켜 나노 시트 형태의 안정한 콜로이드 MnO2를 합성하였으며 용액 중 전기 방전에 의해 생성된 전자 및 라디칼에 의한 환원 반응 메커니즘에 초점을 둔 연구를 진행하였다. 두 번째로 저 비용, 친환경 환원제로 사용 가능한 포도당(glucose)과 용액 플라즈마 기술을 접목하여 나노 구조의 다공성 망간산화물 입자의 녹색 합성을 시도했으며, 흡착제, 전극 재료 및 산화환원 촉매로써 응용 가능성을 확인하였다.
2. 실험방법
2.1. 합성방법
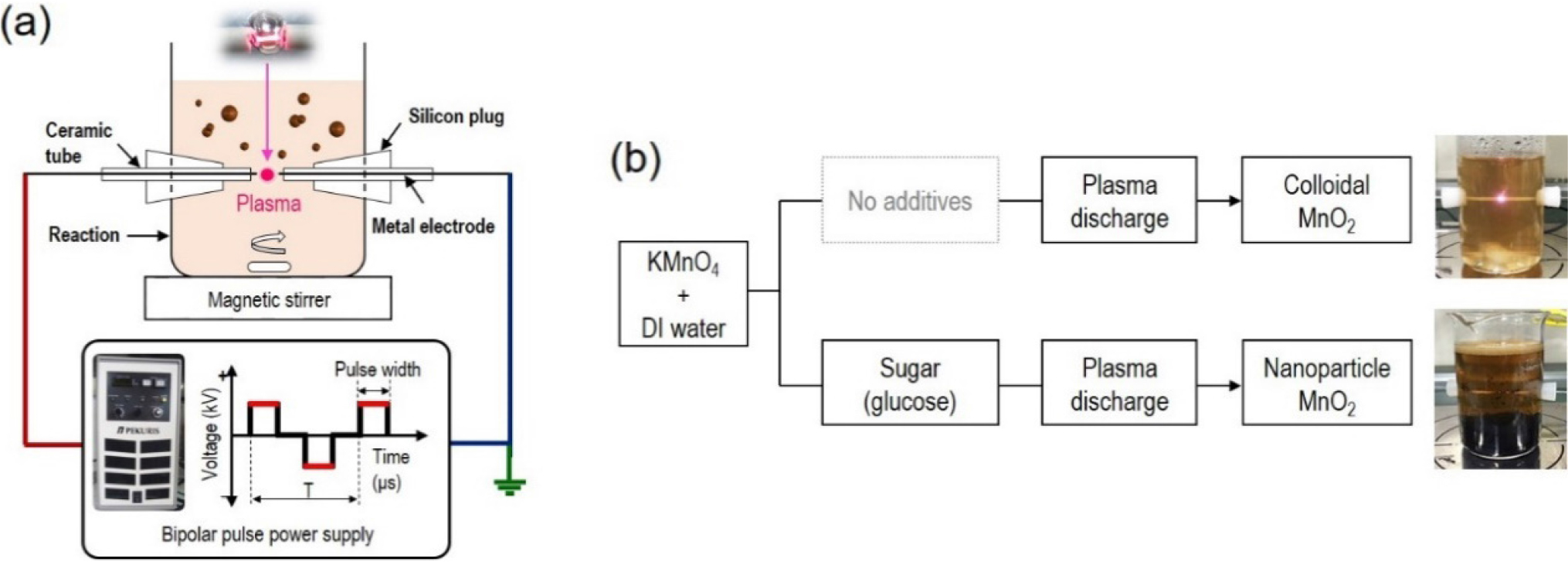
용액 플라즈마 장치는 Fig. 1과 같이 100 ml 유리 비커에 텅스텐 금속 전극(순도 99.95 %, Nilaco, Japan)을 1.5 mm 간격으로 마주보도록 구성하였으며, Bipolar pulse power supply (PEKURIS, Japan)를 통해 전압을 인가하였다. 망간산화물을 합성하기 위해 100 ml의 증류수에 과망간산칼륨(KMnO4, ≥99.5 %, Sigma Aldrich, Japan)을 용해시켜 전구체를 준비하였으며, 환원제의 유무에 따른 망간산화물 형상 제어 및 공정 단축 효과를 비교하기 위해 알데히드기(aldehyde group)를 가진 환원당인 포도당(glucose)을 소량 첨가하였다. 각각 준비된 용액에 인가 전압 1.5 kV, 펄스 폭 1.5 us, 주파수 20 Hz로 방전을 실시하여 MnO2를 합성하였다.
2.2. 분석방법
합성한 재료의 구조는 XRD (X-ray powder diffraction, Rigaku, Japan) 및 FT-IR (fourier transform infrared, Nicolet 8700), 몰포로지는 주사전자현미경(scanning electron microscope, SEM, S-4800, HITACHI)과 투과전자현미경(transmission electron microscopy, TEM, JEOL)을 이용하여 분석하였으며, 비표면적 및 기공분포분석기(BELSORP-mini II, BEL Japan, Inc.)를 통해 포어 구조 분석을 진행하였다. UV-vis (ultraviolet-visible spectrophotometer, Shimadzu UV-3600) 분광 분광법을 통해 방전 시간에 따른 Mn의 산화수(oxidation state) 변화 및 환원 반응을 확인하였으며, 수용액 중에서 전기 방전에 의해 발생하는 활성종에 대해 살펴보기 위해 optical emission spectroscopy (OES) 분석을 진행하였다.
3. 결과 및 고찰
3.1. 용액 플라즈마 공정(solution plasma process, SPP)
Fig. 1(a)는 SPP 장치 구성을 나타낸다. 금속 전극을 마주보도록 설치한 반응 용기에 전구체 용액을 넣어준 후 전압, 주파수 및 펄스 폭을 제어하여 플라즈마를 발생시키며 용액과 플라즈마 계면 사이의 반응 활용하여 물성 제어 및 재료를 합성한다. 본 연구에서는 SPP를 통해 두 가지 형태의 MnO2 합성 연구를 진행하였다. Fig. 1(b)는 과망간산칼륨 수용액 내 플라즈마를 발생시켜 안정적으로 분산된 형태의 콜로이드 MnO2를 합성하는 과정과 알데히드기를 갖고 있어 환원제 역할을 할 수 있는 포도당을 소량 첨가하여 분말 형태의 MnO2 나노 입자를 합성하는 과정을 나타낸 모식도이며 오른쪽 사진은 방전 후 각 시료 형상을 보여준다.
3.2. 콜로이드 MnO2 합성
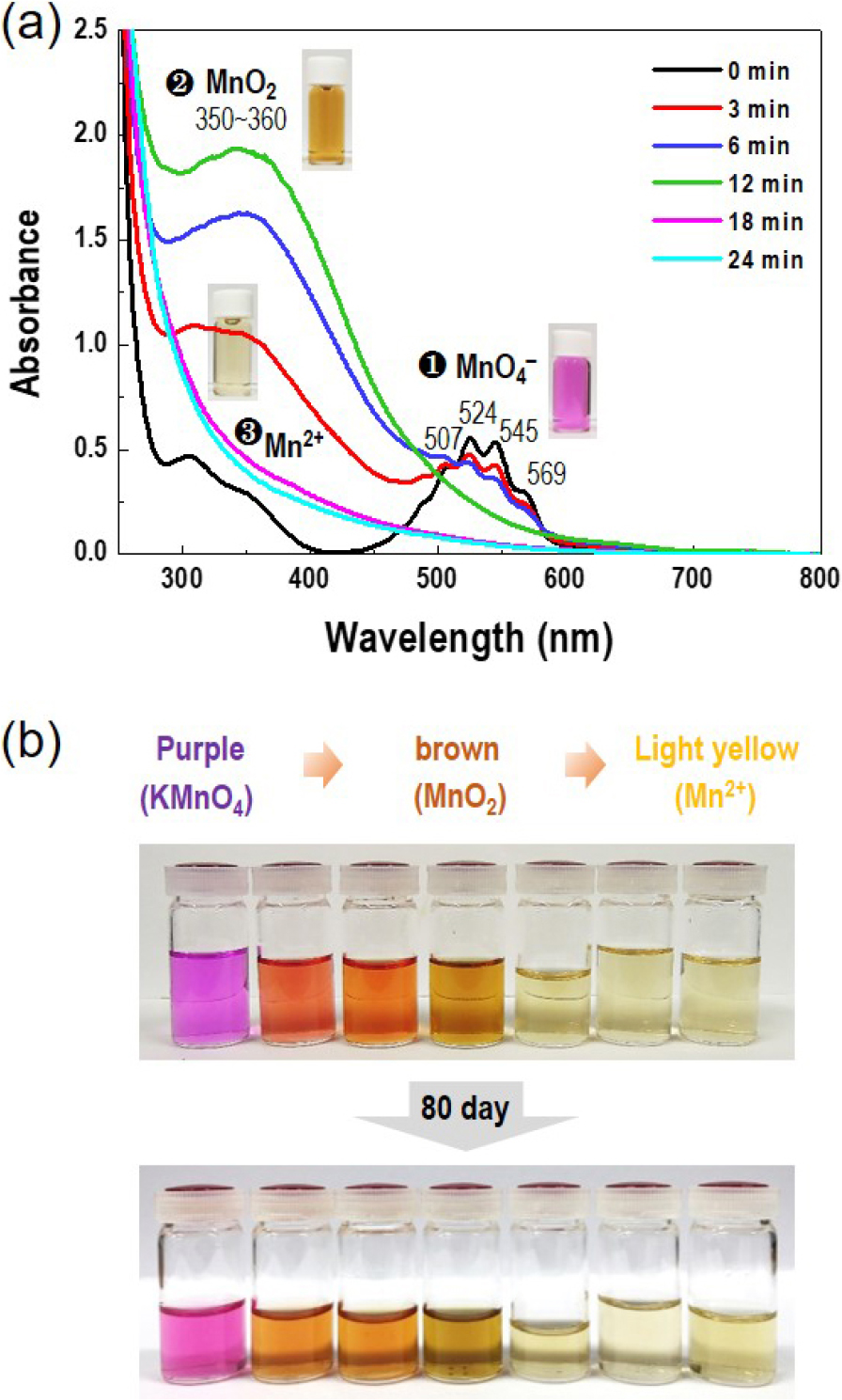
첫 번째는 계면활성제, 분산안정제 및 환원제와 같은 첨가제가 포함되지 않은 과망간산칼륨 수용액에서 SPP에 의한 콜로이드 MnO2 합성에 관한 연구이다. Fig. 2(a)는 플라즈마 방전 시간에 따른 UV-vis 스펙트럼을 나타낸다. 이는 빛의 파장에 따라 물질의 흡광도를 측정하여 Mn의 산화수를 추정할 수 있다. 검정색 선(0 min)은 전구체인 과망간산칼륨 용액의 흡수 스펙트럼으로 507, 524, 545 및 569 nm는 MnO4- (Mn7+) 특성 peak을 나타내며, 방전 시간이 증가함에 따라 MnO4- 특성 peak의 흡광도는 점차 줄어들고 300~400 nm 영역의 새로운 peak의 흡광도가 점차 증가하는 것을 볼 수 있다. 그에 따라 용액의 색깔도 보라색에서 점차 갈색으로 변하며, 12 min 후에는 500 nm 영역의 MnO4- 특성 peak이 전혀 관찰되지 않고 350~360 nm 영역의 하나의 peak만 관찰되는 것을 알 수 있다. 해당 peak는 MnO2 (Mn4+) 특성 peak인 것으로 알려져 있으며 이를 통해 초기 MnO4-가 MnO2로 환원되었음을 알 수 있다.16,17) 또한 12 min 이상 방전을 지속한 경우 MnO2 특성 peak이 사라지며 용액의 색깔도 점차 옅어지는 현상이 확인되었다. 따라서 방전 12 min 시점에 MnO2가 합성된 것으로 사료된다. 추가적으로 콜로이드 형태의 MnO2의 분산 안정성을 확인하기 위해 SPP 이후 1일 시점과 80일 저장 후의 상태를 비교해보았으며 Fig. 2(b)에서 볼 수 있듯이 침전물 없이 안정적으로 분산된 형태를 유지하는 것을 확인할 수 있었다. 이와 같은 결과를 통해 KMnO4 수용액 내에서 플라즈마 방전에 의해 계면활성제 및 분산 안정제 등과 같은 첨가제 없이 안정한 콜로이드 형태의 MnO2 합성이 가능한 것을 확인할 수 있었으며, SPP에 의한 MnO2 합성 메커니즘을 살펴보기 위해 OES 분석을 진행하였다.
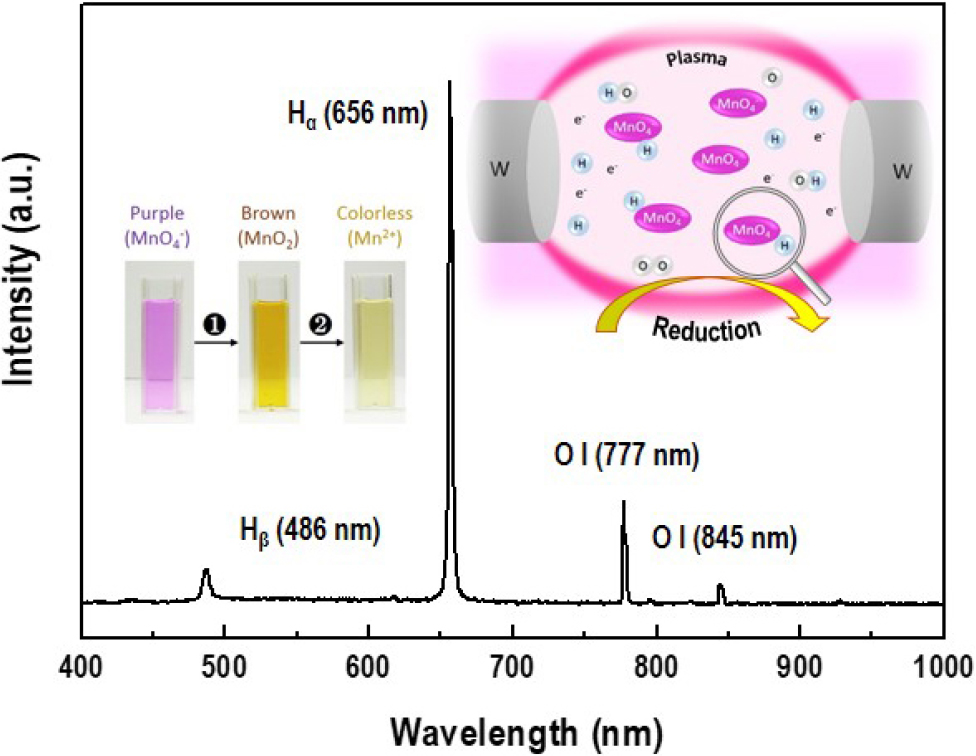
Fig. 3은 KMnO4 용액 내 방전 시 발생하는 플라즈마에서 방출되는 빛을 분석한 OES 스펙트럼을 나타내며, 파장 486, 656 nm의 H 라디칼 및 777, 845 nm 부근의 O 라디칼 peak이 두드러지게 확인되었다. 이는 수용액 중에서 플라즈마를 발생시키면 물 분자의 분해 반응이 진행되며 이때 발생한 다량의 수소, 산소 이온 및 라디칼 그리고 전자 등이 화학적 반응에 참여하는 것으로 알려져 있다.18) 이를 바탕으로 SPP에 의한 MnO2 합성 반응 메커니즘에 대해 살펴보면 다음과 같다. 먼저 KMnO4 수용액 내에서 발생시킨 플라즈마에 의해 분해된 물 분자로부터 수소 라디칼(H·), 이온(H+) 및 전자(e-)가 발생하며 해리되어 있는 MnO4-와 반응하여 MnO2로 환원 반응이 일어난다. 이는 Fig. 2에서 0 min에서 12 min 사이의 반응을 의미하며, 이후 방전을 지속하게 되면 +4가인 MnO2가 수소 라디칼 및 이온과 반응하여 +2가인 Mn2+로 환원 반응이 추가적으로 일어나는 것으로 사료된다. 주요 반응식은 아래 식 (1) 및 식 (2)와 같다.
합성한 콜로이드 MnO2의 형상 관찰을 위해 TEM 분석을 실시하였으며, Fig. 4와 같이 수백 나노 크기의 얇은 sheet 형태로 자가 응집(self-aggregation)된 flower-like 형상인 것으로 확인되었다. 분산된 상태에서는 mono-layer 형태로 안정적으로 분산되어 있는 것으로 사료되며 TEM 샘플링 특성 상 건조 과정에서 응집된 것으로 생각된다. 본 연구를 통해 SPP를 이용한 콜로이드 형태의 MnO2 합성 방법과 그 반응 메커니즘을 살펴보았으며, 전구체의 농도 및 방전 조건에 따라 최적의 방전 시간이 달라질 수 있으며 이를 활용한 형상 및 물성 제어가 가능할 것으로 사료된다.
3.3. MnO2 나노 입자 합성
두 번째는 SPP를 이용한 분말 형태의 MnO2 나노 입자의 녹색 합성 연구에 관한 내용이다. 일반적인 MnO2 합성법으로는 수열합성법, 화학적 침전법 및 공침법 등이 있으며 산화제, 환원제 또는 고온의 열원 또는 장시간 반응이 필요하다. 본 연구에서는 저 비용, 친환경 환원제로 사용 가능한 포도당(glucose)과 용액 플라즈마 기술을 접목하여 상온 ‧ 상압 하에서 나노 구조의 망간산화물의 녹색 합성을 시도하였다.
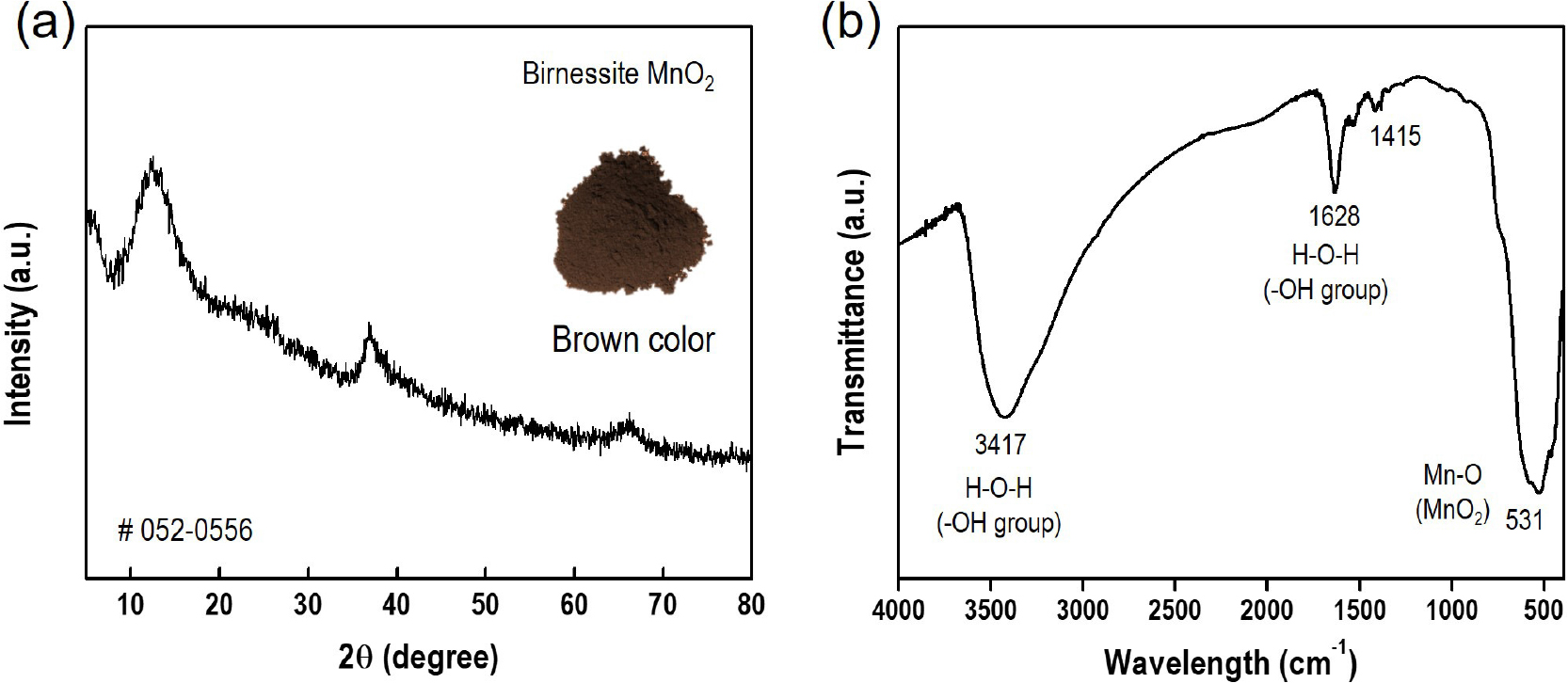
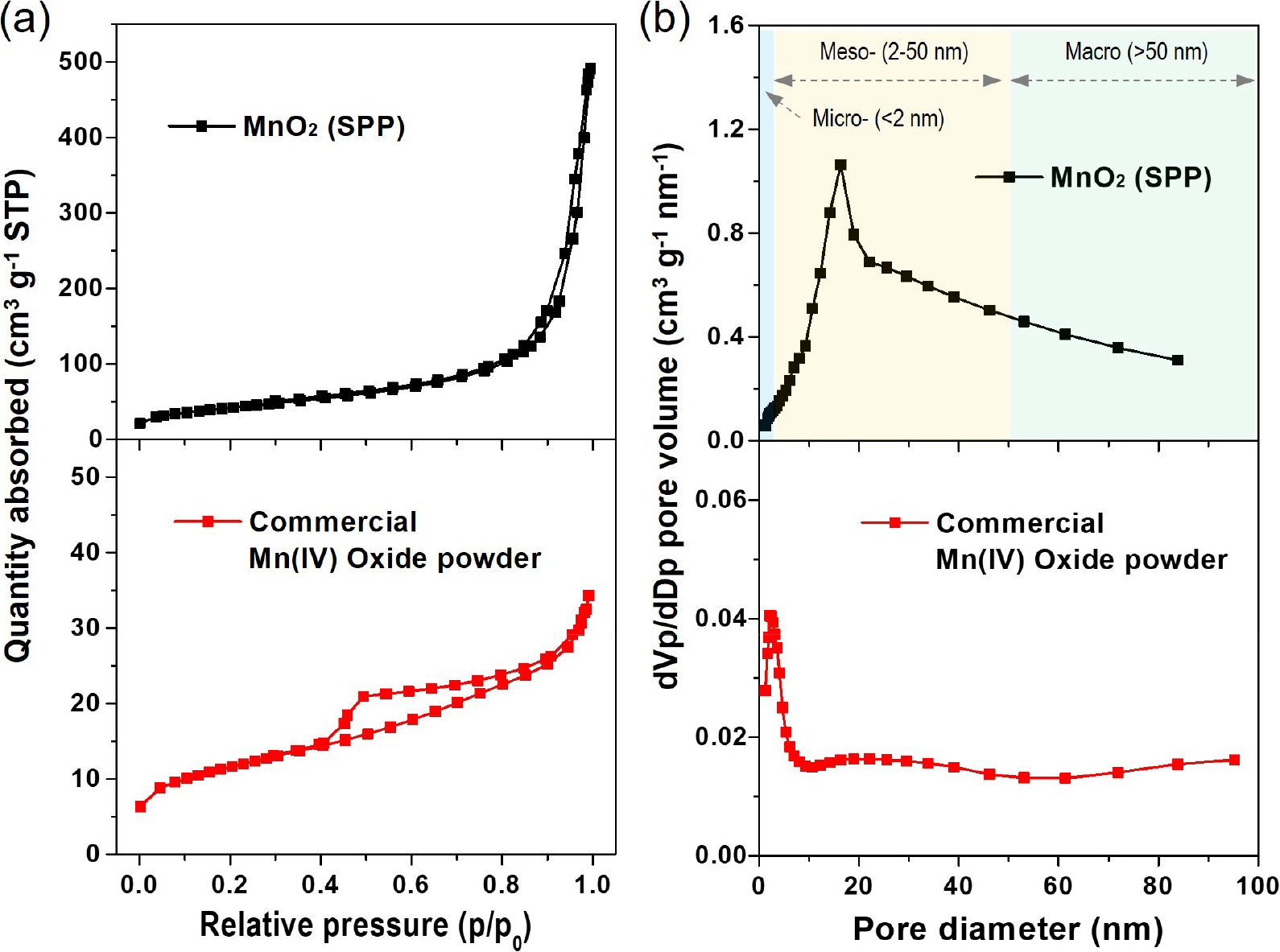
포도당(glucose, C6H12O6)은 알데히드(R-CHO)기를 갖는 단당류 중 하나로 환원제로 작용 가능한 환원당(reducing agent)에 해당한다. 본 연구에서는 플라즈마 방전 시 발생하는 다량의 활성종과 함께 환원제로 소량의 포도당을 첨가하여 공정 시간 단축 및 나노 입자 합성을 시도하였다. 100 ml 증류수에 80 mM의 KMnO4와 1 mM의 포도당을 첨가한 용액을 SPP 반응 용기에 넣어 플라즈마 방전을 실시하였다. 첨가제 없이 방전했을 때와 달리 방전 후 8 min 이내에 보라색을 띄던 KMnO4 수용액이 갈색의 침전물과 투명한 용액으로 분리되면서 반응이 종료되었다. 포도당은 알데히드기를 갖는 환원제이므로 반응 초기에 관여하여 작은 입자 형성에 기여하기 때문에 콜로이드 형태의 분산 안정성을 위한 충분한 반발력을 형성하지 못하기 때문에 입자들의 응집이 빠르게 발생하면서 침전물 형태로 얻어지는 것으로 사료된다. 이렇게 얻어진 침전물은 감압 여과 및 오븐 건조 후 갈색의 분말 형태로 회수하여 XRD, FT-IR 분석 및 형상 분석을 진행하였다. Fig. 5(a) XRD 결과, 2θ = 12°, 36° 및 66°에서 broad한 회절 피크가 관찰되었으며, 층상 구조의 birnessite type의 MnO2 (JCPDS No. 052-0556)인 것으로 확인되었다. Fig. 5(b) FT-IR 결과를 나타내며, 흡수광 파장 3,433 cm-1와 1,628 cm-1는 흡착된 물 분자에서 기인한 -OH기의 stretching vibration 및 O-H기의 bending vibration, 531 cm-1는 metal-O bond인 Mn-O stretching mode를 가리킨다.19) 이 결과를 통해 층상 구조의 MnO2가 성공적으로 합성되었음을 확인하였다. 또한 합성 재료의 비표면적 및 기공 크기 분석을 진행하였으며, 구조적 특성을 비교하기 위해 상용 MnO2 비표면적 분석을 추가적으로 진행하였다. Fig. 6(a)는 질소 흡착/탈착 등온선을 나타내며, SPP로 합성한 MnO2는 일반적으로 다공성 물질에서 확인되는 IV형의 흡착등온선 형태를 보였다. IUPAC 분류에 따르면 다공성 물질은 기공 크기에 따라 2 nm 이하는 micro-pore, 2~50 nm는 meso-pore, 50 nm 이상은 macro-pore로 구분한다.20) 본 연구에서 합성한 MnO2는 BET 식으로 계산된 비표면적 114 m2/g, BJH법으로 계산된 기공 부피 0.68 m3/g, 평균 기공 크기 23.9 nm로 확인되었으며, 특히 기공 분포를 살펴보면 micro- (13.2 %), meso- (84.7 %) 및 macro- (2.1 %) pore를 갖는 계층적 구조를 띄고 있는 다공성 물질인 것을 알 수 있다[Fig. 6(b)]. 추가적으로 측정한 상용 MnO2는 표면적 36.6 m2/g, 기공 부피 0.053 m3/g 및 평균 기공 크기 5.8 nm로 확인되었으며, 이를 통해 본 연구에서 합성한 MnO2의 경우 표면적 약 3배, 기공 부피 약 12배로 다공성 구조가 발달한 것을 알 수 있다. 이러한 계층적 다공성 구조는 전기화학적 분야에서 흡착 특성과 속도 향상에 있어 효과적인 구조로 알려져 있으며 흡착제 및 슈퍼커패시터 등 높은 반응 표면적이 요구되는 분야에 적용되는 것으로 알려져 있다.21) 이러한 구조적 특성은 SEM 및 TEM을 통한 형상 분석을 통해서도 확인할 수 있었다. Fig. 7(a)는 SEM 이미지로 약 20~30 nm 크기의 비교적 균일한 형태의 입자가 사슬 구조와 같이 서로 연결되어 있는 형상을 나타내며, Fig. 6(b, c) TEM 이미지에서도 동일하게 수십 나노 단위의 입자들이 서로 연결되어 있는 형태를 보였다. 또한 노란색과 파란색 화살표로 표시한 부분은 각각 mesopore (2~50 nm)와 macropore (>50 nm)를 나타내며, BET 기공 분석 결과와 일치하는 것을 알 수 있다. 이는 플라즈마 방전 시 발생하는 다량의 전자 및 활성종과 환원제인 포도당이 MnO4-에서 MnO2로의 환원 반응을 가속화하기 때문에 충분한 반발력을 형성할 수 있을 정도의 입자 성장을 억제하여 수분 이내에 수십 나노 크기의 입자 형태로 침전되어 얻어지는 것으로 사료된다. 이처럼 형성된 나노 입자는 플라즈마 영역을 벗어나 주변의 수용액 영역으로 분산됨과 동시에 냉각이 빠르게 이루어지기 때문에 무질서한 방향성을 갖는 입자들이 안정적으로 분산되어 있지 못하고 서로 부딪히면서 응집되어 다양한 크기의 기공 구조를 형성하는 것으로 추정된다. 추가적으로 Fig. 6(c)의 TEM 고배율 관찰 시 면간 거리 ~7Å로 관찰되었으며, 이는 K+와 물 분자가 삽입된 층상구조인 K-birnessite MnO2의 층간 거리를 의미하므로 XRD 결과와 일치하는 것을 알 수 있다. 또한 selected area diffraction (SAED) 패턴 결과를 통해 합성 MnO2는 비정질의 형태를 갖는 것을 확인하였다.
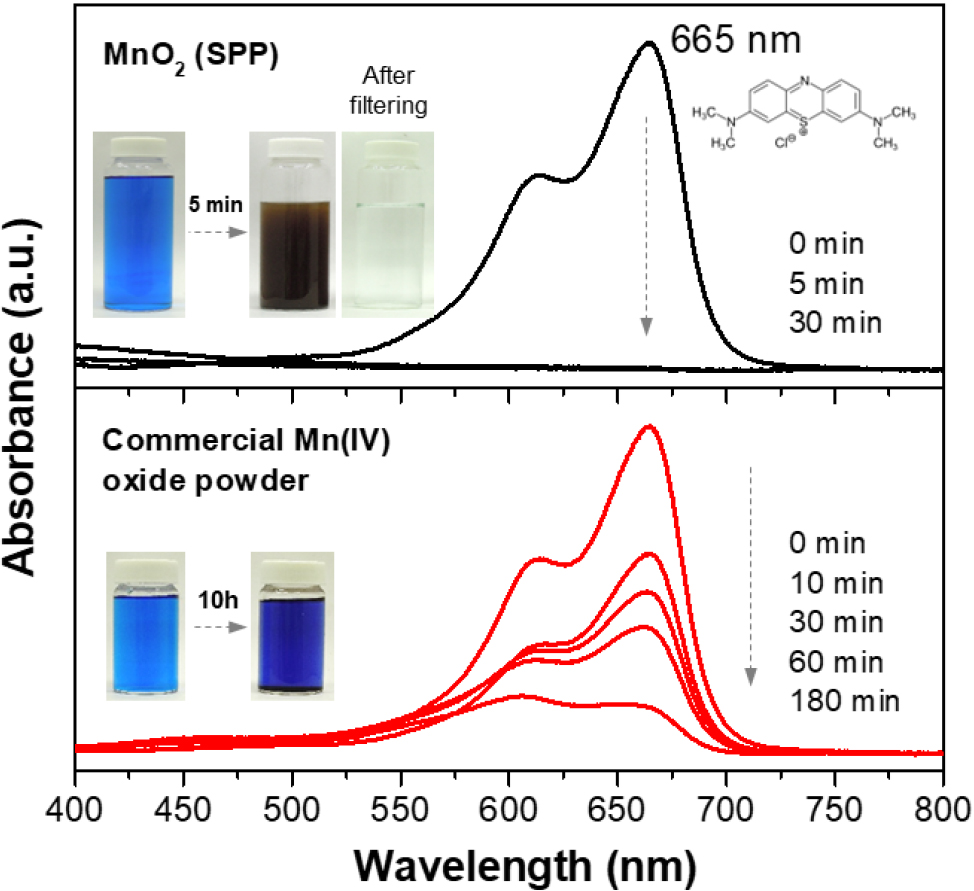
추가적으로 SPP로 합성한 MnO2의 수처리용 흡착제로서의 응용 가능성을 확인하기 위해 유기 염료인 메틸렌블루 제거 실험을 진행하였으며, 비교군으로 상용 MnO2를 사용하였다. 10 mg/L 농도의 메틸렌블루 수용액 100 ml를 준비하고 60 mg의 MnO2 분말을 투입하여 UV-vis 분광광도계를 통해 시간에 따른 흡광도를 측정하였다. Fig. 8에서 볼 수 있는 최대 흡수 파장 665 nm는 메틸렌블루의 특성 피크를 의미하며, 해당 피크의 흡광도에 따라 흡착 제거 여부를 판단하였다. SPP로 합성한 MnO2의 경우 5분 이내에 메틸렌블루의 특성 피크가 사라진 것을 확인하였으며, 필터를 통한 고형분 제거 후 투명한 용액이 얻어진 것으로 보아 완전히 제거된 것으로 판단할 수 있다. 이와 달리 상용 MnO2의 경우 흡착 3시간 후에도 여전히 665 nm의 메틸렌블루 특성 피크가 지속 관찰되었으며, 10시간 후에도 용액은 여전히 파란색을 띄고 있는 것으로 확인되었다. 이는 SPP로 합성한 MnO2 분말 시료의 경우 플라즈마 방전 시 빠른 환원 반응과 주변의 상온 용액에 의한 냉각 효과로 인해 높은 표면적 및 기공 구조가 발달한 MnO2가 얻어지기 때문에 흡착제로서의 우수한 성능을 보이는 것으로 사료된다.
본 연구에서는 SPP를 이용한 분말 형태의 MnO2 나노 입자의 친환경 합성 방법을 제시하였다. 이는 종래의 방법과 비교 시 친환경적이며 상온 상압 하에서 짧은 반응 시간 내 합성할 수 있다는 장점을 가진 합성법이라 할 수 있다. 이렇게 합성한 다공성 나노 구조의 MnO2는 유기 염료 제거를 위한 수처리 흡착제로서의 응용 가능성을 확인하였으며, 또한 앞선 연구에 따르면 SPP를 사용하여 합성한 MnO2/나노 탄소 복합체가 연료전지 및 금속 공기전지용 산화환원반응 촉매로서 특성을 보이는 것으로 보고되어 있다.22) 따라서 리튬이온전지, 슈퍼캐퍼시터 및 이기능성촉매를 활용하는 에너지 응용 분야 및 수처리 흡착제와 같은 친환경 응용 분야에 다양하게 적용될 수 있을 것으로 기대된다.
4. 결 론
본 연구에서는 SPP를 이용한 망간산화물의 친환경 합성 연구를 진행하였다. 첫 번째로 첨가제 없이 순수 과망간산칼륨 수용액 내 플라즈마를 발생시켜 물 분자의 분해에 따라 생성된 수소 이온, 전자, 라디칼 등의 활성종에 의한 환원반응을 통해 Sheet 형태의 콜로이드 MnO2를 합성하였다. 콜로이드 형태의 MnO2 합성에 있어 방전 시간이 중요한 인자인 것으로 확인되었으며, 전구체의 농도 및 방전 조건(전압, 주파수, 펄스폭)에 따른 형상 및 물성제어가 가능할 것으로 사료된다. 두 번째로 분말 형태의 MnO2 합성을 위해 소량의 포도당을 첨가하여 용액 중 플라즈마 방전을 통해 20~30 nm의 균일한 입자 크기를 갖는 MnO2를 합성하였다. 이와 같이 용액 중 발생시킨 플라즈마를 이용하여 나노 구조의 MnO2 합성 연구를 통해 친환경적이고 효과적인 합성 방법으로써 적용 및 확대 가능성을 살펴보았으며, SPP의 반응 메커니즘을 바탕으로 MnO2뿐만 아니라 다양한 기능성 나노 재료 합성을 위한 새로운 합성법으로 활용될 수 있을 것으로 기대된다.