1. 서 론
최근에 두드러지고 있는 탄소 기반 화석 연료의 연소 에 의한 기후 변화와 환경 오염 문제로 인해 재생 가 능한 청정 에너지원들에 대한 관심이 높아지기 시작하 였다. 그것들 가운데 수소는 에너지를 산출하는 과정에 서 부산물로 물만 배출하기 때문에 미래의 신재생 에너 지로서 각광을 받고 있다.1) 수소는 가볍고 에너지 밀도 가 높아서 적은 양으로도 많은 에너지를 배출할 수 있 다. 그리고 태양광 에너지를 전기 에너지로 저장하려면 배터리 용량만큼만 저장할 수 있지만, 수소나 탄화수소 화합물과 같은 화학 에너지로 저장하면 원하는 만큼 저 장할 수 있다는 장점이 있다. 그런데, 수소는 청정 에 너지원으로서의 이런 장점들에도 불구하고 생산하는 방 법에 있어서 심각한 문제가 있었다. 지금까지 대체로 수 소의 생산은 화석 연료의 개질(reforming)로부터 이루어 졌고, 그래서 수소 생산 과정 동안 기후 변화의 주범인 이산화탄소도 발생하기 때문이다. 이러한 현재의 수소 생 산 방법을 대체하기 위해 태양광 에너지와 물로부터 수 소를 생산하는 광전기화학적 물 분해(photoelectrochemical water splitting) 기술이 대두되었으며, 이 기술의 발전은 어쩌면 물이 수소가 되고 에너지원으로서 사용된 수소 는 다시 물이 되는 무한한 에너지 순환(물-수소-에너지 -물)을 현실화시킬 것이다.2)
인공 광합성 방법과 더불어 광전기화학적 물 분해 방 법은 태양광 에너지를 화학 에너지로 전환하는 방법으 로서 태양광 에너지를 이용하여 물(H2O)을 수소(H2)와 산 소(O2)로 분해하여 수소 에너지로 전환한다. 여기서 태 양광 에너지를 화학 에너지로 전환하는 시스템을 광전 기화학 전지(cell)라고 하는데, 이 시스템은 태양광을 흡 수한 후에 그 에너지로 전기화학 반응을 일으켜 수소 생 성물을 얻는다.3) 광전기화학 전지는 빛을 흡수하는 광전 극(photoelectrode)과 상대 반응이 일어나는 상대 전극 (counter electrode), 전해질(또는 물)로 구성된다. 광전기 화학 전지에서 광전기화학 반응이 일어나는 원리를 간 략히 서술하면, 반도체 물질로 이루어진 광전극은 빛(광 자)이 입사되면 전자(e−)와 양공(h+)을 생성하고 그 전자 와 양공이 각각의 전극으로 분리되어 반응하는데, 양극 에서는 산소가 발생하고 음극에서는 수소가 발생한다. 1972년에 Fujishima와 Honda는 n-형 반도체인 TiO2를 광양극(photoanode)으로, 백금을 상대 전극(음극)으로 사 용하여 광전기화학적 물 분해 반응을 최초로 발견하였다.4)
어느 반도체 물질이 광전기화학적 물 분해 전지의 전 극으로 활용되기 위해서는 기본적으로 물의 산화-환원 전 위(1.23 V)가 반도체 물질의 띠간격(bandgap) 사이에 포 함되어야 하는데, 전기화학적으로 전도대의 하단이 물의 환원(H+/H2) 전위(0 V vs. NHE)보다 부(負)가 되고 가 전자대의 상단이 물의 산화(H2O/O2) 전위(+1.23 V vs. NHE)보다 정(正)일 필요가 있다.5) 사실상 물의 산화-환 원 반응을 일으키기 위해서는 전기화학적으로 어느 정 도의 과전압(± 0.5 V)이 필요하고, 그래서 태양광 물 분 해 광전극용 반도체는 적어도 2 eV 정도의 밴드갭을 갖 고 있을 필요가 있다. 게다가 태양광을 효과적으로 활 용하기 위해서는 태양광의 대부분을 차지하는 가시광선 을 흡수하여 작동할 필요가 있기 때문에 광전극용 반도 체의 밴드갭이 3 eV 이하가 되어야 한다.
제1 구리 산화물(Cu2O)은 광전기화학적 물 분해를 통 한 수소 생산용 광음극(photocathode) 소재로서 적절한 특성들을 갖는 산화물 반도체로 알려져 있다, Cu2O는 지 구에 풍부한 비독성의 p-형 반도체로서 2.0 eV 정도의 직 접 밴드갭과 더불어 H2 생산에 대해 충분한 과전위를 나타내는 적절한 부의 전도대 위치를 갖고 있다. 게다 가 이론적으로 Cu2O는 −14.7 mA/cm2의 최대 광전류와 18.7 %에 해당하는 태양광 수소 변환 효율을 나타낼 수 있다고 보고되었다.6) 그런데 Cu2O를 물 환원용 광음 극으로서의 용도를 제한하는 주요 인자는 수용액에서 의 높은 광부식성으로 인한 불안정성이다. 또한 전해도 금법으로 제작된 단순한 Cu2O 박막은 이론적 최대값보 다 훨씬 작은 −0.25 mA/cm2 정도의 광전류를 나타내 고, 그래서 잠재적인 광활성이 충분히 구현되지 못하고 있는 것으로 알려져 있다.7) 최근에 Cu2O의 광활성과 부 식 안정성을 향상시키는 한 가지 방법으로 1.3-1.7 eV의 밴드갭을 갖는 제2 구리 산화물(CuO)을 활용하여 산화 물 반도체 이종접합 구조체를 제작하는 연구들이 시도 되었다.7-9) 여기서 이종접합 구조의 형성에서 비롯된 밴 드 구조의 구배에서 기인하는 전자 수송 및 광흡수 과 정의 개선이 산화물 반도체 이종접합 광전극에 있어서 전기화학적 물 분해 성능의 향상을 가져올 것으로 기대 된다.8-10)
본 논문에서는 수열합성법을 이용하여 합성된 CuO 나 노막대 집합체와 전해도금법을 이용하여 형성된 Cu2O 박 막으로 이루어진 Cu2O/CuO 산화물 반도체 이종접합 구 조체를 제작하였다. 제작된 Cu2O 박막/CuO 나노막대 이 종접합의 구조적 특성을 확인한 다음에 태양광 물 분해 용 광음극으로서의 광전기화학적 특성을 체계적으로 조 사하였다. 여기서 전기화학적 방법으로 제작된 산화물 반 도체 Cu2O/CuO 이종접합 구조체가 낮은 비용, 높은 성 능의 수소 생산용 광전기화학적 전극으로서의 가능성이 유망하다는 점이 제시될 것이다.
2. 실험 방법
먼저 산화인튬주석(ITO)이 코팅된 유리 기판 위에 스 파터링 방법을 사용하여 대략 20 nm 두께의 Cu층을 증 착시킨 다음에 400 °C에서 1시간 동안 열처리 공정을 시 행함으로써 CuO 나노막대 성장용 CuO 씨앗층을 형성 했다.11) 준비된 CuO 씨앗층 위에 수열합성법을 사용하 여 CuO 나노막대 집합체를 성장시켰는데, 여기서 사용 된 수열합성용 용액은 25 mM의 질산 제2구리 3수화물 [Cu(NO3)2·3H2O]과 40 mM의 헥사메틸렌테트라민(C6H12N4) 를 계량한 다음에 자기 교반자를 사용하여 균일하게 혼 합하여 준비하였다. 그 다음에 CuO 씨앗층이 형성된 기 판을 준비된 용액에 담근 후 85 °C에서 3시간 동안 수 열합성법으로 CuO 나노막대 집합체를 성장시켰다. CuO 나노막대 집합체가 코팅된 기판은 세척 후 건조한 공기 분위기에서 열처리 공정을 400 °C에서 1시간 동안 진행 하였다.
산화물 반도체 이종접합을 형성하기 위해 사전에 합성 된 CuO 나노막대 집합체 위에 Cu2O 박막을 3전극형 전 해도금법을 사용하여 성장시켰다.12) 도금 용액은 0.05 M 의 황산구리 5수화물(CuSO4·5H2O)과 0.1 M의 젖산(lactic acid)을 혼합한 용액에 수산화나트륨(NaOH)을 스포이드 를 사용하여 떨어뜨림으로써 pH 수치를 10, 11 그리고 12로 맞추어 세 가지로 준비하였다. CuO 나노막대 집 합체가 코팅된 기판을 고정시켜 60 °C의 도금 용액 안 에 넣은 다음에 전원을 연결하여 0.5 mA/cm2의 전류가 흐르는 조건에서 30분 동안 도금 공정을 시행하였다. 여 기서 기준 전극은 표준 칼로멜(Hg/HgCl2) 전극을 사용 하였고, 상대 전극은 백금을 사용하였다. 마지막으로 얻 어진 Cu2O/CuO 산화물 반도체 이종접합에 대한 열처리 공정을 건조한 공기 분위기에서 400 °C에서 1시간 동안 진행하였다.
제작된 Cu2O/CuO 산화물 반도체 이종접합의 결정 상을 알아보기 위해 X선 회절 분석기(XRD)와 라만 (Raman) 분광기를 사용하였으며, 미세구조 분석을 위해 냉전계형 장방출 주사전자현미경(SEM)를 이용하였다. 이 종접합 구조체의 물 분해 특성을 조사하기 위해서는 물 에 닿는 전극의 면적이 일정해야 하기 때문에 에폭시 경 화제를 사용하여 0.5 × 1.0 cm2의 면적 외의 부분을 차단 한 다음에 용제를 사용하여 전극 연결부의 Cu2O와 CuO 를 제거함으로써 ITO를 노출시켰다. 그렇게 얻어진 형 상의 Cu2O/CuO 광전극에 대해 3전극 배치를 사용하여 광전기화학적 물 분해 특성을 측정하였다. 여기서 0.1 M 의 NaSO4를 전해질로 사용하였고, 기준 전극과 상대 전 극은 각각 칼로멜 전극과 백금을 사용하였다. 각 전극 에 전원을 연결한 다음에 전압을 −0.6 V에서 0.1 V까지 변화시키면서 가시광선을 조사했을 때와 어두울 때의 전 류 밀도 차이를 측정함으로써 광 변환 효율을 계산하였 다. 전류 밀도 차이가 가장 크게 나타나는 전압 하에서 일정 시간 동안 반복적으로 빛을 조사하고 차단함으로 써 광전기화학적 성능을 평가하였다. 또한, 비교를 위 해, ITO가 코팅된 유리 기판 위에 단일한 Cu2O 박막 광전극을 제작하여 광전기화학적 성능을 조사하였다.
3. 결과 및 고찰
ITO가 코팅된 유리 기판 위에 수열합성법을 이용하여 합성된 CuO 나노막대 집합체에 대해 관측된 전형적인 SEM 영상들을 Fig. 1에 나타내었다. 이 그림으로부터 수 열합성된 CuO 나노막대들이 약 30 nm의 직경과 약 500 nm의 길이를 갖고서 수직으로 촘촘히 성장한 것을 확 인할 수 있다. 한편, 합성된 CuO 나노막대 집합체에 대 한 X-선 회절 실험 결과, 단사정계 테노라이트(monoclinic tenorite) CuO 결정상에 해당하는 (-111), (111), (022), (220) 등의 회절선들이 관측되었는데(Fig. 3 참조), 이것 으로부터 CuO 나노막대들이 다결정질로 성장하였음을 알 수 있다.

Fig. 1
Typical SEM images showing (a) top-view and (b) crosssectional view of the CuO nanorod array synthesized on an ITOcoated glass substrate.
일반적으로 전해도금법으로 형성되는 Cu2O 박막은 다 음과 같은 반응식으로 표현되는 전기화학적 반응을 거 쳐 Cu2O가 기판 위에 석출됨으로써 얻어지게 된다.
위 반응은 알칼리성 구리 전해도금 용액에서 온도와 pH값에 의존하여 일어나고, 그래서 전해도금된 Cu2O 박 막의 미세구조는 전해도금 용액의 온도와 pH값에 따라 조절될 수 있다.13,14) Fig. 2는 전해도금 용액의 온도를 60 °C로 고정시킨 뒤 pH값을 10, 11, 12로 바꾸면서 ITO가 코팅된 유리 기판 위에 30분 동안 도금된 박막 층의 전형적인 SEM 영상들을 보여준다. 얻어진 박막 층 은 깎인(faceted) 면의 결정립들로 이루어져 있는데, 이 것은 성장이 확산제어적(diffusion-limited)이라기보다는 운 동학적으로 이루어진다는 것을 가리킨다.13) 전해도금된 물 질은 Cu2O인 것으로 확인되었는데, X선 회절 스펙트럼 에는 입방정계(cubic) Cu2O 결정상에서 비롯되는 회절 선들만 관측되었다(Fig. 3 참조). Fig. 2를 살펴보면, 전 해도금 용액의 pH값이 증가함에 따라 얻어진 Cu2O 박 막의 결정립 크기가 증가한다는 것을 알 수 있다. 여기 서, pH 10인 경우에는 결정립의 깎인 면이 둥그러지고, pH 12인 경우에는 결정립 크기가 2 μm 이상으로 커지 며 기판을 촘촘하게 덮지 못한다는 것을 확인할 수 있 다. 따라서 이런 결과는 pH 11의 구리 전해도금 용액 으로부터 최적의 Cu2O 박막 층이 형성된다는 것을 가 리킨다.

Fig. 2
Typical SEM images of electrodeposited Cu2O thin films on ITO-coated glass substrates from lactate-stabilized copper sulfate solutions of (a) pH 10, (b) pH 11 and (c) pH 12 at 60 °C.
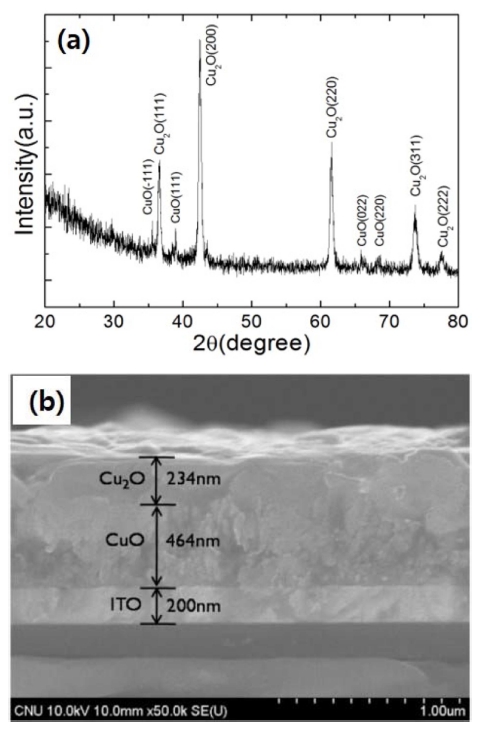
Fig. 3
(a) X-ray diffraction pattern and (b) cross-sectional SEM image of the Cu2O thin film/CuO nanorod heterostructure on an ITO-coated glass substrate.
ITO가 코팅된 유리 기판 위에 CuO 나노막대 집합체 를 수열합성법으로 성장시킨 다음에 pH 11의 도금 용 액을 사용하여 전해도금법으로 Cu2O 박막을 형성함으로 써 제작된 Cu2O/CuO 산화물 반도체 이종접합 구조체에 대해 관측된 전형적인 XRD 패턴을 Fig. 3(a)에 나타내 었다. 이 그림에서 표시된 것처럼, 관측된 회절선들은 입 방정계 Cu2O 결정상이나 단사정계 CuO 결정상에서 비 롯된 것으로 분석되었다. 여타의 2차상은 전혀 검출되지 않았으며, Cu2O 및 CuO는 다결정질로 형성되었음을 알 수 있다. Fig. 3(b)는 제작된 Cu2O 박막/CuO 나노막대 집합체 이종접합의 단면 SEM 영상을 보여주는데, 확연 히 구별되는 ITO 층의 표면 위에 각각 ~450 nm의 CuO 층과 ~250 nm의 Cu2O 층이 형성된 것을 확인할 수 있 다. 그리고 CuO 나노막대 층과 Cu2O 박막 층 사이의 명확히 구별이 잘 안 되는 모호한 계면이 관찰되는데, 이것은 Cu2O 박막 속에 CuO 나노막대들이 묻어 들어 가 있다는 것을 가리킨다.
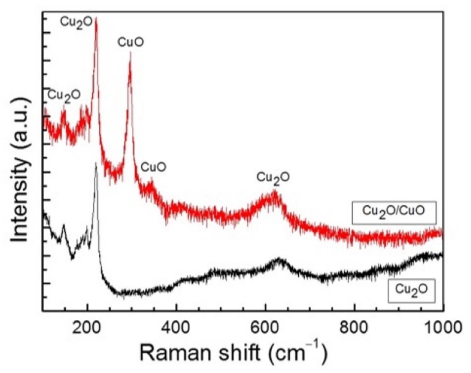
제작된 Cu2O 박막/CuO 나노막대 집합체 이종접합의 결정상 형성을 확인하기 위해 ITO가 코팅된 유리 기판 위에 전해도금된 단일한 Cu2O 박막과 더불어 라만 산 란 분석을 통해서 후속적으로 연구되었다. Fig. 4는 Cu2O 박막(아래 스펙트럼)과 Cu2O/CuO 이종접합(위 스펙트 럼)에 대해서 상온에서 얻어진 라만 산란 분광선들을 보 여준다. 이 그림에서 150, 220, 625 cm−1에 해당하는 또 렷한 분광선들은 Cu2O 결정상의 특성 포논 주파수들을 가리키는 한편으로, 300, 350 cm−1에 해당하는 또렷한 분 광선들은 CuO 결정상의 특성 포논 주파수들을 가리킨 다. Cu2O 결정상에서 비롯된 라만 산란 분광선들의 경 우에, 220 cm−1에 위치한 강도가 가장 센 분광선은 2차 포논 방식(2Γ12−)에 귀속되고, 625 cm−1에서 관측된 분광 선은 두 포논 방식(Γ12− + Γ15+)에서 기인하며, 150 cm−1에 서 나타난 분광선은 1차 포논 방식[Γ15-(1)]에서 기인하는 것으로 해명될 수 있다.15,16) 다른 한편으로, CuO 결정 상에서 비롯된 라만 산란 분광선들의 경우에, 300 cm−1 에서 관측된 강도가 가장 센 분광선은 1차 포논 방식 (Ag)에서 기인되고, 350 cm−1에서 나타난 분광선은 1차 포논 방식(Bg)에 귀속되는 것으로 판명된다.17) 여기서, Cu2O 박막에 대한 라만 산란 실험 결과를 살펴보면, CuO 결정상의 특성 분광선들이 관측되지 않는다는 것 을 볼 수 있다. 이것은 전해도금된 Cu2O 박막이 CuO 결정상이 혼합되지 않은 Cu2O 단일상으로 이루어져 있 음을 가리키고, 그래서 Cu2O/CuO 이종접합이 제대로 형 성되었음을 확인할 수 있다.
Fig. 5는 광전기화학적 물 분해 성능을 비교하기 위해 수소가 생성되는 Cu2O 박막 광음극과 Cu2O/CuO 이종 접합 광음극에 대해 바이어스(−0.5 V vs. Hg/HgCl2)를 가한 상태에서 측정된 전류 밀도-시간(J-T) 특성 곡선들 을 보여준다. 여기서 가시광선은 매 20초마다 켰다(on) 껐다(off)를 반복하였다. Fig. 5를 살펴보면, Cu2O 박막 광음극과 Cu2O/CuO 이종접합 광음극 둘 다 상당히 작 은 암흑 전류(dark current)를 나타낸다. 그리고 빛을 조 사하면, Cu2O/CuO 이종접합 광음극이 Cu2O 박막 광음 극보다 3배나 더 큰 광전류(photocurrent)를 생성한다는 것을 확인할 수 있는데, 이것은 Cu2O/CuO 이종접합 광 음극이 Cu2O 박막 광음극보다 훨씬 더 우수한 광전기 화학적 물 분해 성능을 갖추고 있다는 것을 가리킨다. Cu2O/CuO 이종접합 광전극에 있어서의 광전기화학적 물 분해 성능의 향상은 이종접합 구조를 형성함으로써 구 현되는 적절한 구배의 밴드 구조에 의거한 빛 흡수 능 력의 증가와 빛 흡수에 의해 생성된 전자-양공의 재조 합 과정의 억제에서 비롯되는 것으로 이해될 수 있다.8) 여기서, 최초 20초간 조사되었을 때의 평균 광전류 밀 도와 120초가 지난 후 20초간 조사되었을 때의 평균 광 전류 밀도를 비교함으로써 광음극의 광전기화학적 안정 성을 평가했을 때, Cu2O 박막 광음극과 Cu2O/CuO 이 종접합 광음극에 대해서 각각 80 %와 77 %라는 값을 얻 었다. 이 결과는 이종접합 구조의 형성이 광전기화학적 안정성을 향상하는 데에는 그다지 기여하지 않는다는 것 을 가리킨다.
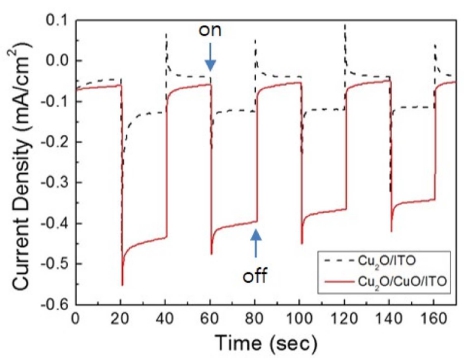
Fig. 5
Current density-time (J-T) curves measured at −0.5 V vs. Hg/HgCl2 on Cu2O and Cu2O/CuO photocathodes with visible light chopped (on/off) for each 20 sec.
Fig. 6(a)는 Cu2O/CuO 이종접합 광음극에 대해 암흑 상태와 가시광선을 조사한 상태에서 측정된 전류 밀도 -전압(J-V) 특성 곡선들을 보여준다. 여기서, 제작된 이 종접합 광음극의 전압이 −0.5 V (vs. Hg/HgCl2)에 이를 때까지 암흑 상태에서 무시할 만한 음극 전류를 나타낸 다는 것을 관측할 수 있다. Cu2O/CuO 이종접합 광음극 이 가시광선에 노출되었을 때, 음극 전압의 크기가 증 가함에 따라 음극 광전류 생성이 확연히 증가한다는 것, 즉 광전기화학적 물 분해의 활성이 증진된다는 것을 분 명히 알 수 있다. 예를 들면, −0.6 V (vs. Hg/HgCl2)의 전압에서 측정된 전류 밀도 차이는 약 1.05 mA/cm2인 것 으로 측정된다.
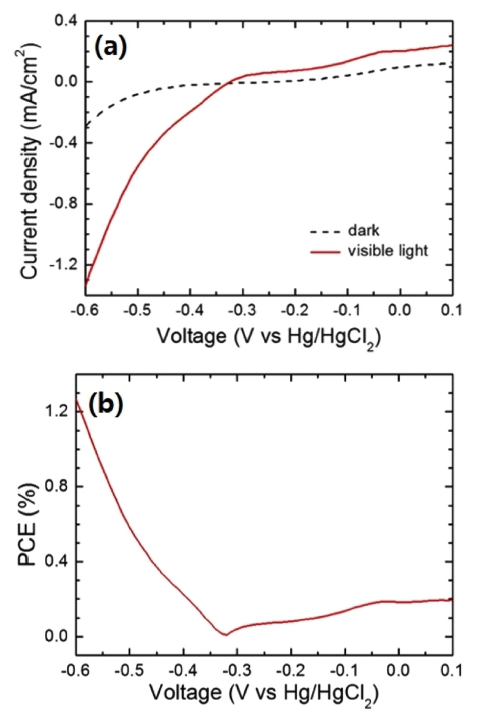
Fig. 6
(a) Current density-voltage (J-V) curves of the Cu2O/CuO heterojunction photocathode at dark and visible light illumination. (b) Variation of the photocurrent conversion efficiency (PCE) with the bias voltage vs Hg/HgCl2.
일반적으로 광전기화학적 태양광 물 분해용 광전극의 수소 생산 효율성을 나타내는 광전류 변환 효율(PCE, photocurrent conversion efficiency)은 측정된 J-V 특성 데이터를 이용하여 다음과 같은 식을 통해 추산될 수 있다.18)
여기서, Jp는 가시광선에 노출되었을 때의 전류 밀도 [mA/cm2], Vapp는 인가 전압에서 전류가 0일 때의 전압 을 뺀 값을 의미하고, 1.23[V]는 물 분해 전위를 나타 내며, Pi는 입력 가시광선의 세기 밀도[mW/cm2]를 가리 킨다. 이런 식으로 추산된 Cu2O/CuO 이종접합 광음극 의 광전류 변환 효율의 음극 전압의 크기에 따른 변화 를 Fig. 6(b)에 나타내었다. 여기서, 0.1에서 −0.32 V 사 이의 인가 전압 조건에서는 광전기화학적 태양광 물 분 해를 통한 수소 생산이 사실상 이루어지지 않는 반면 에, 광전류 변화 효율이 −0.32 V부터 증가하기 시작하여 −0.6 V까지 꾸준히 상승한다는 것을 알 수 있다. 예컨 대, −0.6 V (vs. Hg/HgCl2)의 전압에 대해 추산된 PCE 값은 1.27 %에 이르는 것으로 확인된다. CuO2의 경우에 광전류 변환 효율의 이론적 최대값이 대략 18 %에 이 른다는 추정 결과를 감안하면,6) Cu2O 기반 광전기화학 적 물 분해 소자에 대한 후속 연구가 더 필요하다.
4. 결 론
수열합성법을 이용하여 합성된 CuO 나노막대 집합체 와 전해도금법을 이용하여 형성된 Cu2O 박막으로 이루 어진 Cu2O/CuO 산화물 반도체 이종접합 기반 광음극의 광전기화학적 물 분해 특성을 체계적으로 조사하였다. X- 선 회절 및 SEM 분석뿐 아니라 라만 산란 실험을 통 해서 산화구리 기반 산화물 반도체 물 분해용 광전극이 이종접합 구조를 형성하였음을 확인하였다. 측정된 광전 기화학적 전류 밀도-전압(J-V) 특성 곡선들로부터 Cu2O/ CuO 이종접합 광음극이 무시할 만한 암흑 전류와 높 은 광전류 밀도, 예를 들면, −0.6 V (vs. Hg/HgCl2)에 서 −1.05 mA/cm2의 전류 밀도를 나타낸다는 것을 알 수 있었는데, 이것은 Cu2O/CuO 이종접합 광음극이 태양광 물 분해 전극으로서 효과적으로 작동한다는 사실을 가 리킨다. 제작된 Cu2O/CuO 이종접합 광음극의 광전류 변 환 효율은 −0.6 V (vs. Hg/HgCl2)에서 1.27 %에 이르는 것으로 추산되었다. 게다가 Cu2O/CuO 이종접합 광음극 및 단순한 Cu2O 박막 광음극에 대해서 측정된 광전기 화학적 전류 밀도-시간(J-T) 특성 곡선들로부터 Cu2O/ CuO 이종접합의 광전기화학적 성능이 단순한 Cu2O 박 막보다 상당히 향상된다는 것을 알 수 있었다. 여기서 관측된 광전기화학적 성능의 향상 현상은 이종접합 구 조를 형성함으로써 구현되는 적절한 구배의 밴드갭 구 조에 의거한 빛 흡수 능력 증가 및 전자-양공의 재조합 과정 억제의 상승작용적 효과에 귀속될 수 있다. 결론 적으로 이 연구는 전기화학적으로 제작된 Cu2O/CuO 산 화물 반도체 이종접합 광음극이 태양광 물 분해를 통한 수소 생산용 소자로 활용 가능하다는 점을 시사한다.