1. 서 론
금(gold, Au)은 전기전도도와 내식성이 우수하여 전기, 반도체 등 여러 분야에서 사용되고 있으며, 특히 장신 구용으로써 널리 사용되어온 귀금속이다.1)
이와 같이 금을 장신구로 사용하기 위해서는 내구성이 요구되는데 금의 경우 비교적 무른 성질을 가지고 있어 강도를 높일 필요가 있다. 이에 기존에는 순금 대신 14K, 18K 등으로 주로 구리와 은을 합금하여 사용하며, 합금 되는 은과 구리의 비율을 조절하여 옐로우, 화이트골드 등으로 제품화가 되고 있다.2,3)
최근에는 소비자의 다양한 니즈가 요구되어 기존의 옐 로우, 화이트골드 이외에 레드골드 및 그린, 퍼플골드 등 의 칼라골드가 개발되었으며, 이중 레드골드의 경우 옐 로우, 화이트골드 다음으로 수요가 급격하게 늘어나고 있 는 상황이다.
레드골드는 금합금 내 구리성분이 다량 포함된 합금으 로 Au-Ag-Cu 삼원 상태도 내에서 Cu 방향으로 치우친 함량을 보이는 레드에서 핑크 색상에 해당하는 합금재 이다.4)
그러나 레드골드 합금의 경우 AuCux의 규칙상이 존재 하는데, 이러한 Au, Cu 원자의 규칙적 배열로 인해 결 정구조가 변화하여 매우 취성이 높은 특성을 띠게 되어 제품화를 위한 가공 시 합금재가 파괴되어 불량률이 높 아지는 문제점을 가지고 있다.5)
따라서 이러한 문제를 해결하기 위해 레드골드 고유의 색상을 해치지 않고 Au, Cu에 모두 잘 고용되며 규칙 상을 방지할 수 있는 제 3 원소의 합금이 필요하다. 이 러한 조건을 충족시키는 원소로는 보론(B) 또는 백금족 원소인 이리듐(Ir) 등이 있으며, D. Ott 등6)은 Au-Ag-Cu 합금재에 Ir 등을 합금하여 결정립 크기를 조절함으로써 이러한 문제를 해결할 수 있는 가능성을 제시하였다. 최 근에는 레드골드용 구리 모합금에 루테늄(Ru) 등을 투 입한 합금 재료를 사용하고 있다.
그러나 Au, Cu의 융점은 1200 °C 이하이며, B, Ru, Ir과 같은 고융점 원소의 융점은 약 2500 °C로 이들을 합 금하기 위해서는 초고온을 유지할 수 있는 열처리공정 인 아크멜팅 또는 스컬멜팅 방법을 사용해야 한다.7) 아 크멜팅은 흑연 등으로 제조된 전극 또는 용해하고자하 는 금속 자체 전극과 금속 사이에 아크방전을 일으켜 발 생하는 열을 이용하여 금속을 녹이는 방법으로 이때 용 융된 금속의 증발을 막기 위해 비활성 기체 분위기 또 는 진공분위기에서 열처리를 진행하는 방법이다.8) 스컬 멜팅법은 1960년대 고안된 열처리 방법으로 용해시키고 자하는 물질을 자체 도가니로서 사용하며 고주파유도 가 열을 통해 이론상 원하는 온도로 승온이 가능하며 주로 지르코니아 단결정 합성에 사용되는 방법이다.9) 그러나 아크멜팅과 스컬멜팅법의 공정비용은 진공 또는 대기분 위기에서 열처리하는 비용보다 고가이기 때문에 제품의 단가가 높아지는 문제점이 있다.
반면에 이러한 고융점 금속 원소들의 산화물인 B2O3, RuO2, IrO2의 용융온도는 각각 450, 1200, 1100 °C로 구 리, 금과 같이 1200 °C의 열처리를 통해 용융시키면 모 두 용해되어 액상 산화물로 존재한다. 이때 액상 산화 물은 순금속과 비중차에 의해서 상부에서 위치하고 하 부에는 금속으로 위치하여 액상에 의한 계면부의 빠른 상호확산에 의해 산화물로부터 유리된 고융점 원소가 구 리 내로 확산하여 합금화 시키는 것이 가능할 수 있다.
상기 B 및 백금족 원소인 Ru, Ir 등을 구리 내에 확 산, 투입하기 위해 금속의 환원에 대해 산소분압을 고 려하여 표시한 엘링감 다이어그램에 근거하여 열역학적 인 평형상태에서는 1200 °C 10–34 atm PO2 라는 초고진공 이 필요하지만 실제적으로 비평형상태에서는 비교적 큰 산소분압에서 가능한지에 대해 규명되지 않았다.10)
따라서 본 연구에서는 레드골드를 제작을 위한 구리 투 입 시 Au-Cu 규칙상 방지를 위한 미량의 초고융점 원 소를 합금 투입하기 위해 5.0 × 10–3Torr 이하의 진공분 위기 내에서 산화물을 이용한 비교적 저온의 열처리를 통한 합금을 진행하고 이에 대한 물성을 확인하고자 하 였다.
2. 실험 방법
B, Ru, Ir의 세 가지 고융점 원소를 비교적 저융점인 구리에 합금하기 위해 각각 B2O3(SigmaAldrich, Boric anhydride, 99.98 %), RuO2(SigmaAldrich, Ruthenium(IV) oxide, 99.9 %), IrO2(SigmaAldrich, Iridium(IV) oxide, 99.9 %) 산화물과 고순도 구리(Kojundo chemical Lab Co., LTD., pure copper, 99.99 %)를 사용하였다. 합금비 99.9 : 0.1의 구리 :고융점 원소 제조를 위해 산화물 내 oxide를 제외한 실제 고융점 원소의 함유량을 계산 하 여 최종적으로 각각 19.99 g의 구리 내 B2O3-0.0646 g, RuO2-0.0264 g, IrO2-0.0233 g을 칭량하여 합금을 진행하 고자 하였다.
진공열처리는 준비된 판상형의 합금용 구리를 도가니 내에 위치시킨 후 칭량한 B, Ru, Ir 금속산화물 파우더 를 각각 구리 상부에 균일하게 도포한 뒤 진공로(YL-TF- 40/13모델)를 이용하여 5.0 × 10–3Torr 이하의 진공도 하 에서 승온 속도 5 °C/min로 1200 °C-30분 열처리 후 공 랭하여 진행하였다.
각 시료의 미세구조를 분석하기 위해 결정립계를 선택 적으로 에칭 후 광학현미경을 이용하였다. 에칭시료는 35 wt%의 HNO3 용액에 폴리싱 된 구리시료를 15 초간 침 적시켜 준비하였다. 이후 광학현미경(GIA Instruments사 815000모델)을 이용하여 시편의 상부로부터 광원이 조사 되는 두상광 조명하에서 에칭 된 결정립계 확인을 통해 결정립의 크기분석을 진행하였다. 광학현미경 이미지는 광 학현미경 접안렌즈부에 부착된 디지털카메라(Nikon사 Coolpix4500모델)를 이용하여 확보하였다.
합금된 구리시료에 대해 비커스경도를 확인하기 위해 미세경도기(vickers hardness test, Mitutoyo사, MVK-H1 모델)를 이용해 비커스 경도를 측정하였다. 0.5 kgf의 하 중을 15 초간 시료에 인가하여 측정하였으며 오차율을 줄이기 위해 시료 당 3회 측정 후 평균값을 계산하여 경도값을 정하였다.
합금된 구리시료 내 초고융점 원소의 함량을 정량적으 로 확인하기 위해 D-SIMS(dynamic SIMS, Cameca사, IMS4FE7모델)를 이용하여 분석을 진행하였다. 측정을 위 해 각 시료를 5 × 5 × 1 mm의 판상형으로 준비한 후 O2+ ion gun을 이용하여 Impact energy-8 keV, current-30 nA, raster size 200 μm, MRP 약 1500 조건으로 진행하였다.
합금된 구리합금 시료에 대해 초고융점 합금의 정량 적인 투입량을 확인하고자 wavelength-dispersive X-ray spectroscopy(WD-XRF, Shimadzu사, XRF-1700) 분석을 진행하였다. Rh 타겟을 사용하여 40 kV의 전압, 90 mA 전류의 분석조건으로 각 합금재에 대해서 분석을 진행 하였다.
3. 결과 및 고찰
Fig. 1은 (a)의 순수한 구리와 (b)~(d)의 고융점 원소 의 산화물과 함께 열처리한 구리 시료의 단면을 70 wt% 의 질산과 DI water를 1:1로 혼합한 용액을 이용하여 15 초간 에칭 한 후 확인한 광학현미경 이미지이다.

Fig. 1.
Microscope images of (a) Cu only, (b) Cu+B2O3, (c) Cu+RuO2 and (d) Cu+IrO2 alloys after heat treatment 1200 °C - 30 min. at vacuum atmosphere and etching for 15 seconds.
Fig. 1(a)는 진공열처리한 순수한 구리시료의 단면을 15 초간 에칭한 후 확인한 광학현미경 이미지이다. 결정립의 크기는 2.97 mm로 나타내었으며, 이는 진공 열처리 후 공 랭 처리 시 느린 냉각속도로 인해 입계가 성장하여 나 타난 결과로 판단되었다. 또한 명확하게 결정립계가 확 인되어 목적한 바와 같이 에칭이 된 것을 확인할 수 있 었다.
Fig. 1(b)는 진공열처리한 B2O3 산화물이 첨가된 구리 합금 시료의 단면을 15 초간 에칭 한 후 확인한 광학 현미경 이미지이다. 시료 전반부에 걸쳐 평균 약 1.24 mm크기의 결정립을 확인할 수 있으며, 시료전반부에 걸 쳐 세포상을 확인할 수 있었다. 세포상은 단일성분의 금 속에서의 열처리로는 생성되지 않으며, 2원계 이상의 합 금 시에만 응고과정에서 나타나는 상이다.11) 따라서 B2O3 산화물이 첨가된 구리합금의 경우 순수한 구리에 비해 결정립의 크기가 줄어들고 세포상이 확인되어 간접적으 로 B이 용해 중에 환원되어 구리와 합금 된 것을 확인 할 수 있었다.
Fig. 1(c)는 진공열처리한 RuO2산화물이 첨가된 구리 합금 시료의 단면을 Fig. 1(a)와 동일하게 에칭한 후 확 인한 광학현미경 이미지로 시료 중앙부와 우측부에 평균 1.77 mm의 결정립계를 확인할 수 있었으며, Fig. 1(b)와 마찬가지로 진회색의 세포상을 확인할 수 있었다. 따라 서 RuO2 첨가에 따른 결정립 미세화와 세포상을 통해 RuO2로부터 환원된 Ru이 구리와 합금된 것을 간접적으 로 확인할 수 있었다.
Fig. 1(d)는 진공열처리한 IrO2 산화물이 첨가된 구리 합금 시료의 단면을 Fig. 1(a)와 동일하게 에칭을 진행 한 광학현미경 이미지이다. 평균 약 2.23 mm의 결정립 계를 확인할 수 있었으며 Fig. 1(a)에 비해 결정립 미세 화가 진행된 것을 확인할 수 있었다. 이러한 Ir의 경우 대표적인 고융점 원소로 통상 다른 금속 모재에 미량원 소로 첨가하여 결정립 미세화를 시킨다고 이미 잘 알려 진 바 있다.6) 또한 시료 전반에 걸쳐 세포상이 성장한 수지상이 생성된 것을 확인할 수 있었으며, 이를 통해 IrO2로부터 환원된 Ir이 구리와 합금된 것을 확인할 수 있었다.
따라서 광학현미경 분석을 통해 진공열처리 후 공랭에 의한 느린 냉각속도로 인해 결정립의 크기가 비교적 커 정량적인 입도변화를 확인할 수는 없었으나 기존 구리 에 비해 결정립의 크기가 감소하고 세포상과 수지상이 생성되어 고융점 원소와 구리의 합금이 목적한 바와 같 이 가능함을 확인할 수 있었다.
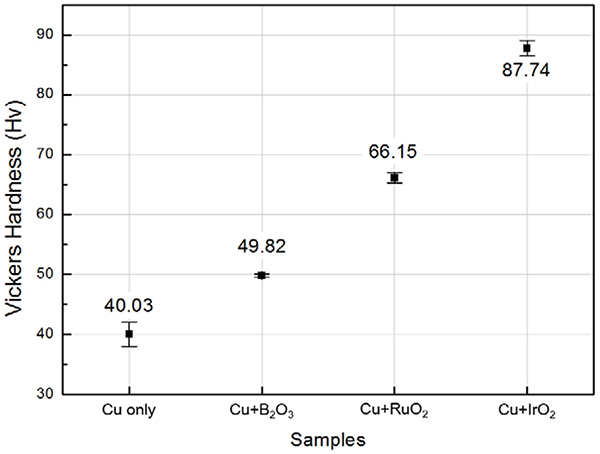
Fig. 2는 순수한 구리와 고융점 원소의 산화물을 구리 와 합금한 시료의 비커스경도 결과를 나타낸 그래프이 다. 순수한 구리 시료의 경우 비커스 경도가 40.03으로 가장 낮았으며 B, Ru, Ir이 합금된 시료의 경우 각각 49.82, 66.15, 87.74 로 순수한 구리시료에 비해 최대 2.2배 증가하였다. 순구리에 비해 고융점 원소가 합금된 구리시료의 경우 앞선 광학현미경 결과에서 나타난 바 와 같이 결정립의 크기가 감소함에 따라 경도가 증가하 는 것을 알 수 있었다. 이는 Oh 등12,13)이 합금의 기계적 특성향상의 경우 결정립의 미세화를 통해 가능하다고 보 고한 바와 잘 일치하였다. 한편, 고융점 원소가 합금된 3가지의 구리 시료만을 비교할 경우 결정립이 커짐에도 불구하고 경도가 증가하는 것을 확인하였다. 이는 B, Ru, Ir의 원자반지름이 각각 90, 134, 136 pm로 금속의 여 러 강화기구 중 원자반지름의 차이에 의해 발생되는 고 용체 강화에 의한 결과로 판단되었다.14,15)
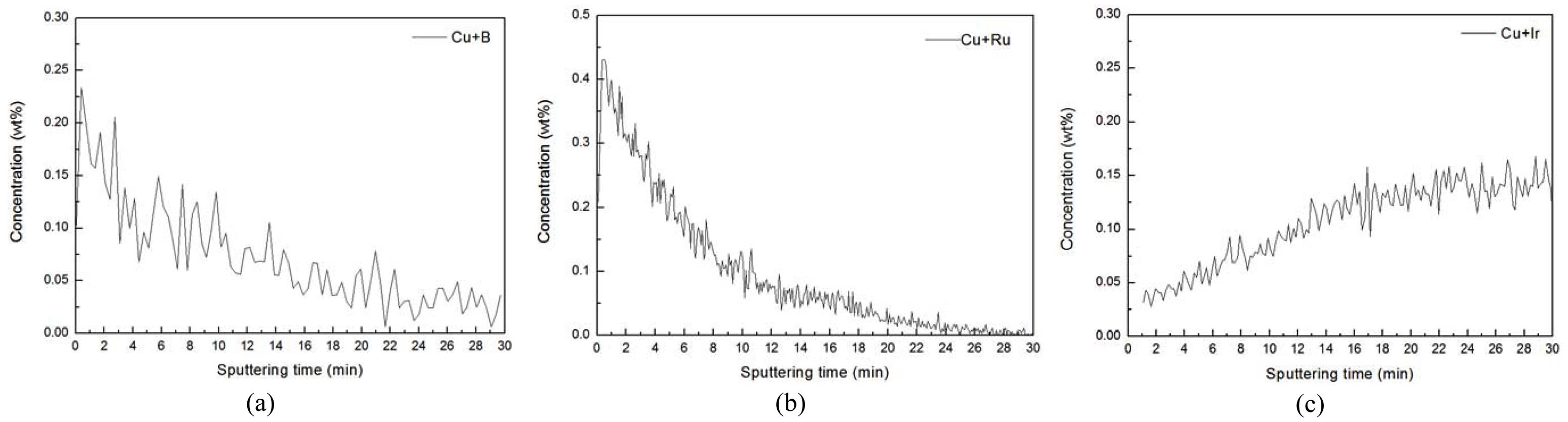
Fig. 3은 Cu-B, Cu-Ru, Cu-Ir 합금재의 D-SIMS 결과 를 나타낸 그래프로 표면으로부터 스퍼터링을 30분간 진 행하여 각각 B, Ru, Ir의 농도 값을 wt%로 환산하여 나 타내었다.
Fig. 3(a)는 Cu-B 합금재의 D-SIMS 결과를 나타낸 그 래프이다. 이때 0~4분까지의 함량은 D-SIMS에서 발생 할 수 있는 산소에 의한 표면효과라고 가정하여 측정한 결과, 4~30분 동안의 B의 평균함량은 0.059 wt%로 나 타났다. 또한 이를 스퍼터링 시간에 따른 거리환산을 분 당 1 μm라고 가정한 후 식(1)의 확산계수 공식을 이용 하여 계산한 결과 B의 확산계수는 3.64 × 10–11cm2/sec로 확인되었다.
Fig. 3(b)는 Cu-Ru 합금재의 D-SIMS 결과를 나타낸 그래프로 Fig. 3(b)와 마찬가지로 0~4분까지는 표면효과 에 의한 오차범위를 제외하고 4~30분 동안의 Ru의 평균 함유량은 0.030 wt%로 확인되었으며, 확산계수는 5.82 × 10–13cm2/sec로 확인되었다. 이는 목표했던 함량인 0.1 wt%에 못 미치는 수치이나 장비의 특성 상 오차범위를 고려해 보았을 때 충분히 합금된 것으로 판단되었다.
이러한 B, Ru의 확산계수 결과를 볼 때 B가 Ru에 비 해 더 높은 확산계수를 가지고 있는 것을 확인할 수 있 으며, 이를 통해 B의 경우 확산 속도가 Ru에 비해 빨 라 같은 시간동안 합금 시 Cu 내부까지 더 많이 고용 되는 것으로 판단되었다.
Fig. 3(c)는 Cu-Ir 합금재의 D-SIMS 결과를 나타낸 그 래프로 Fig. 3(a)와 동일하게 Ir의 평균 함유량을 계산해 본 결과 0.114 wt%를 나타내었다. 이러한 결과는 목표 했던 함량인 0.1 wt%보다 높게 나타내었는데 이는 기기 특성상의 오차범위로 판단되었다. 한편 Fig. 3(a)와 3(b) 와는 달리 스퍼터링 시간이 증가함에 따라 Ir의 함량이 감소하지 않고 그대로이거나 증가하는 것을 확인할 수 있었다. 이는 Ir이 식각 깊이 이상으로 고용되었거나 CuO 형태로의 역확산에 의한 산화물 함유량의 감소로 인해 나타난 결과로 판단되었다.
따라서 D-SIMS 분석을 통해 구리 내에 각 금속산화 물로부터 고융점 원소가 확산되어 합금될 수 있음을 정 량적으로 확인하였다.
Table 1은 Cu, Cu-B, Cu-Ru, Cu-Ir 합금재의 WDXRF 결과를 나타낸 표이다.
Table 1.
WD-XRF Results. [wt%]
| elements | Cu | B | Ru | Ir | Si | Fe |
|---|---|---|---|---|---|---|
| samples | ||||||
| Cu only | 99.212 | - | - | - | 0.751 | 0.036 |
| Cu-B | 98.953 | - | - | - | 1.007 | 0.040 |
| Cu-Ru | 98.805 | - | 0.086 | - | 1.060 | 0.048 |
| Cu-Ir | 98.523 | - | - | 0.062 | 1.387 | 0.027 |
순수한 구리의 경우, 본 실험에서 사용된 99.99 wt%의 시료를 사용하여 측정을 진행하였으나 결과로서 Cu의 함 량은 99.212 wt%와 이외에 소량의 불순물로 Si, Fe가 각 각 0.751, 0.037 wt%가 함유되어있는 것을 확인할 수 있 었다. 이는 WD-XRF의 분석 시 나타나는 오차 범위로 판단되었다.
Cu-B 합금재의 경우, 구리는 98.953 wt%로 나타났으 며 이외의 불순물로 Si, Fe가 각각 1.007, 0.040 wt%로 나타났다. B을 합금하였음에도 불구하고 B의 함량이 측 정되지 않았는데, 이는 WD-XRF 장비 특성상 Na 이 하의 경원소의 경우 인텐시티의 확인이 불가능하여 B의 검출이 안된 것으로 판단되었다.16) 한편, Cu의 함량은 98.953 wt%로 순구리에 비해 낮은 것을 확인할 수 있었 다. 본 실험에 사용된 WD-XRF 기기의 경우, 분석 시 검출되는 원소들의 총합을 100 wt%로 설정하고 각 원소 의 비율을 나타내기 때문에 이러한 결과에 B가 표현되 지 않았으나 상대적으로 구리의 비율은 낮아지고 Si와 Fe 불순물의 비율은 높게 표현된 것으로 판단되었다. 따라 서 이전의 순구리 분석결과를 고려해 보았을 때 간접적 으로 B가 합금된 것으로 판단 할 수 있었다.
Cu-Ru 합금재의 경우, 다른 합금재와는 달리 Zr 필터 를 장착하여 측정하였다. 이러한 이유는 기존 WD-XRF 장비의 경우 x-선을 생성하기 위해 Rh 양극을 사용하는 데, Rh 양극의 경우 Ru 피크와 중첩되기 때문에 이를 피하기 위해 Zr 필터를 이용하여 Ru의 함량을 측정하 였다. 이때 Ru의 함량은 0.086 wt%로, 본 논문에서 제 시한 0.1 wt%보다는 비교적 낮게 측정된 것을 확인하였 다. 그러나 이러한 결과는 기기 분석 오차율을 고려해 볼 때 Ru의 투입이 성공적으로 진행되었음을 직접적으 로 의미하였다.
Cu-Ir 합금재의 경우, Ir의 함량이 0.062 wt%로 나타났 으며, 이는 목적한 0.1 wt% 보다는 비교적 낮은 수치이 나 WD-XRF의 분석 오차율을 고려하면 성공적으로 Ir 의 투입이 진행되었음을 확신할 수 있었다.
따라서 WD-XRF를 통해 구리 내에 각 금속산화물로 부터 고융점 원소가 확산되어 합금될 수 있음을 직간접 적으로 확인하였다.
4. 결 론
고융점을 가진 B, Ru, Ir과 같은 원소를 비교적 융점 이 낮은 구리에 합금하기 위해 이들의 금속 산화물을 이 용하여 진공분위기 하에서 1200 °C-30분 열처리를 통해 합금을 진행하였다. 미세구조 분석 결과 금속산화물을 이 용한 고융점 원소가 합금 된 구리 시료의 경우 기존구 리에 비해 결정립의 미세화가 진행되었으며 시료 전반에 걸친 세포상과 수지상의 생성을 확인할 수 있었다. 비 커스경도 분석 결과 기존 구리 시료에 비해 최대 2.2배 증가하여 합금의 유무를 간접적으로 확인할 수 있었다. DSIMS분석결과 구리 내에 각 고융점 원소의 피크를 확 인하였으며 WD-XRF를 통해 이들의 정량적인 함량을 측 정하여 금속산화물을 이용한 고융점 원소의 구리 내 합 금 가능성을 정량적으로 확인할 수 있었다.