1. 서 론
이산화티타늄(TiO2)은 광촉매로 널리 사용되는 금속산 화물 중에서 가장 적합한 광촉매이며 높은 광반응성, 화 학적 안정성, 무독성, 친환경성, 낮은 비용의 장점을 가 진다. 자외선을 받으면 전자(electron)와 정공(hole)을 생 성하여 강한 산화력을 지니게 되고, 수중과 공기 중에 존재하는 각종 환경오염물질을 무해한 이산화탄소와 물 등으로 분해시킨다.1-3)
그러나, TiO2는 wide bandgap semiconductor (3.2 eV for anatase)로서 자외선(UV-light, λ ≤ 390 nm)의 흡수에 의해 광촉매 반응이 일어나지만 가시광선에서는 일어나 기 어렵다. 이러한 TiO2의 한계를 극복하기 위해서 전자 -정공 분리를 향상 시키면서, 가시광선 영역까지 빛의 흡 수범위를 확장시킬 수 있는 합성방법에 대한 연구가 진 행되고 있다. TiO2에 금속 또는 비금속 이온을 결합,4) TiO2 표면에 안료 감광,5) TiO2 표면에 귀금속 증착6) 등 이 대표적인 연구이다. 특히, TiO2 표면에 귀금속 증착 에 관한 연구가 가장 활발히 진행되고 있다. 귀금속이 증착된 TiO2는 접합면에서 높은 schottky barriers를 가 지고 있기 때문에 전자-정공 분리가 촉진되며, 가시광선 영역까지 빛의 흡수범위가 확장된다.7)
귀금속 중에서 Ag는 가격이 싸고 구하기 쉽기 때문 에 산업적으로 적용하기에 적합하다.8) 따라서, Ag-doped TiO2는 현재 귀금속 증착에 관한 연구에서 많은 관심을 받고 있다.
본 연구에서는 TiO2 nanoparticle 합성법의 대표적인 방법인 졸-겔공정(sol-gel process)을 이용하여 TiO2 nanoparticle을 합성하고, 실험공정이 매우 간단하면서 상온에 서 효율적으로 Ag를 도핑 시킬 수 있는 광증착법(photodeposition) 으로 Ag를 도핑시켜 Ag-doped TiO2를 제조하 였다. 제조된 Ag-doped TiO2를 X-ray diffractometry (XRD), scanning electron microscopy(SEM), energy dispersive spectroscopy(EDS), transmission electron microscopy( TEM)를 이용하여 물리적 특성을 고찰하였다. 또한, 자외선과 가시광원에서 TiO2와 광분해 특성을 gas chromatography( GC)를 이용하여 비교 고찰하였다.
2. 실험 방법
2.1. 졸-겔공정을 이용한 TiO2 합성
TiO2는 졸-겔공정을 이용하여 합성하였다. 출발원료는 TiO2 의 전구체인 TTIP(Titanium Isopropoxide, Ti[OCH(CH3)2]4, Aldrich)와 가수분해 촉매제인 H2O, 용매인 C2H5OH (DUKSAN, 99.99 %)를 사용하였다.
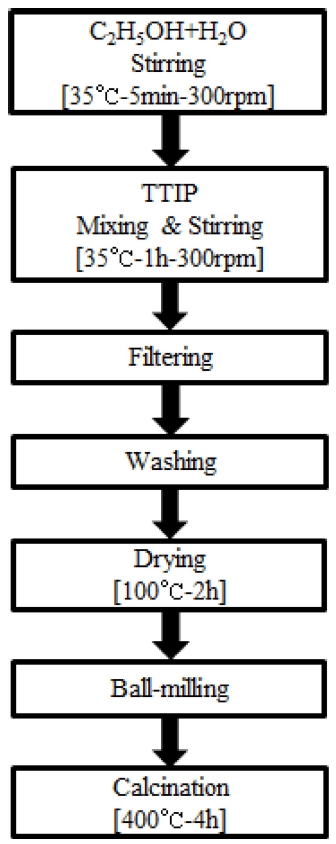
먼저 C2H5OH 10 mL와 H2O 15 mL를 혼합한 용매에 TTIP 5 mL를 첨가하고 35 °C에서 1시간 동안 300 rpm 으로 교반하여 Ti-sol 용액을 제조하였다. 이후에는 Tisol 용액을 여과 및 세척을 하고, 100 °C에서 2시간 건 조시켜서 TiO2 분말을 얻어 ball-milling하였다. TiO2 결 정화가 일어나도록, 최종적으로 400 °C에서 4시간 열처 리하였다. Fig. 1에 졸-겔공정에 의한 TiO2 나노분말 합 성에 대한 공정순서도를 나타내었다.
2.2. 광증착법으로 Ag를 도핑시킨 Ag-doped TiO2
TiO2 광촉매 분말에 Ag 촉매금속의 도핑은 광증착법 을 이용하였으며, Ag 도핑의 전구체는 AgNO3(DUKSAN, 99.8 %), pH를 조절하는데 필요한 NH4OH(DUKSAN, 25~30 %), 용매인 H2O를 출발원료로 사용하였다.
먼저 TiO2 1 g과 H2O 500 mL를 35 °C에서 5분 동안 300 rpm으로 교반하면서 혼합하였고, 5분 동안 상온에 서 sonication을 하였다. 그리고 AgNO3를 AgNO3:TiO2 = 1:10과 같은 조성비(molar ratio)로 첨가하여 35 °C에서 30분 동안 300 rpm으로 교반하면서 혼합하였다. pH가 6보다 낮은 경우 혼합한 용액에 존재하는 TiO2 입자표 면은 OH2+상태이고, pH가 6보다 높은 경우 혼합한 용 액에 존재하는 TiO2 입자표면은 O–상태이다; 후자의 경 우 TiO2 입자표면은 음전하를 띄기 때문에 Ag+이온을 도 핑하는데 적합한 조건이다.9) 그리고 pH가 7, 10인 경우 Ag가 TiO2에 도핑된 상태는 다음과 같다10):
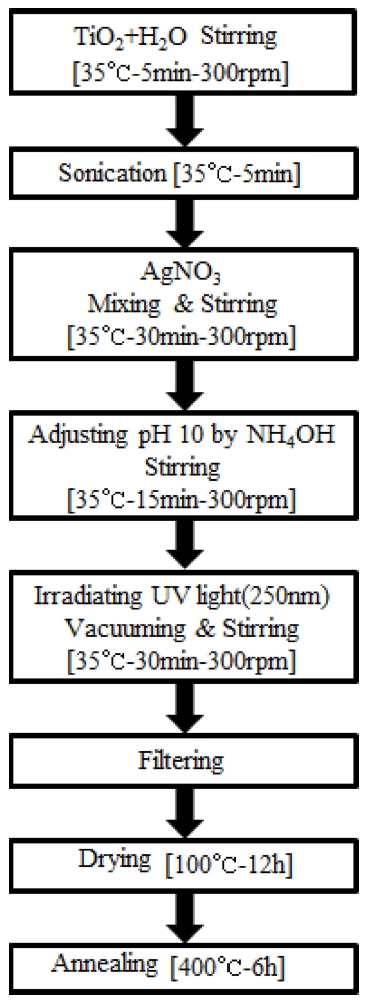
그래서 혼합한 용액에 NH4OH를 첨가하여 pH 10으로 조정하고, 15분 동안 교반하였다. 이후에는 Ag의 산화 를 방지하기 위해서 진공 상태에서 교반을 하고, 동시 에 자외선(λ = 250 nm)을 조사하여 Ag를 TiO2에 도핑하 였다. 이렇게 제조된 용액을 여과공정을 통하여 수용액과 분말을 분리시키고, 100 °C에서 12시간 건조시켜 잔류 H2O를 제거하였다. 그리고 최종적으로 Ag-doped TiO2에 잔유 할 수 있는 유기불순물을 제거하기 위하여 400 °C 에서 6시간 동안 annealing하였다. Fig. 2에 Ag-doped TiO2의 도핑공정인 광증착법의 공정순서도를 나타내었다.
시편의 결정구조는 X-ray diffractometry(New D8- Advance, Bruker-AXS)로 분석하였고, 미세구조와 성분분 석은 scanning electron microscopy(Field Emission S- 4700, Hitachi) 및 energy dispersive spectroscopy(EDS, Oxford)와 transmission electron microscopy(TECNAI F20 G2, FEI)로 관찰하였다. 광분해 반응은 gas chromatography (7890A, Agilent)를 사용하여 VOCs 유해 가스의 주요 성 분 중 하나인 벤젠가스(C6H6)에 대한 광분해 반응을 측 정하였다.
3. 결과 및 고찰
3.1. 결정구조 및 미세구조 분석
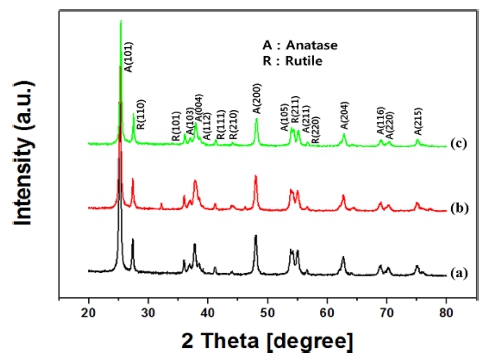
Fig. 3은 졸-겔공정으로 합성한 TiO2 및 광증착법으로 Ag를 도핑시킨 Ag-doped TiO2의 XRD 패턴이다. 세 시 편에 대한 XRD 패턴이 거의 동일하고, 도핑된 Ag의 양 이 매우 작기 때문에 Ag에 대한 회절피크가 나타나지 않았다. TiO2와 Ag-doped TiO2는 anatase 상과 rutile 상 이 혼재되어 있다(JCPDS 21-1272 / JCPDS 76-1940). Table 1은 결정립의 크기 및 상의 분포를 나타내었다. 결 정립의 크기는 아래 식(3)의 Scherrer’s equation을 이용 하여 계산하였다.11)
Table 1.
Crystalline phase and crystallite size of the synthesized TiO2, Ag-doped TiO2 and Ag-doped TiO2 annealed at 400 °C.
D는 평균결정립크기(nm), λ는 X선의 파장, k는 평형 상수이며 일반적으로 0.89라는 값을 가진다. β는 반가폭 (full width at half maximum), θ는 회절각도이다. 결정 상의 분포는 아래 식(4)를 이용하여 계산하였다.12)
IA는 anatase (101) 회절피크의 intensity, IR은 rutile (110) 회절피크의 intensity이다. 결정립의 크기는 21~30 nm, 상의 분포는 anatase 상이 75~78 %이고 rutile 상이 22~25%로 세 시편 모두 비슷한 크기와 분포를 보였다. 이는 TiO2 결정화를 위하여 모두 열처리를 400 °C로 실 시해서 동일한 크기의 열에너지가 가해졌기 때문이다.
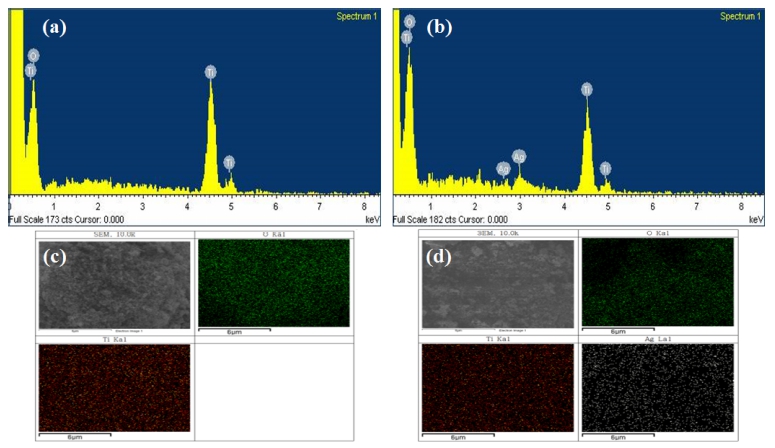
Fig. 4는 TiO2 및 Ag-doped TiO2를 SEM으로 관찰한 사진이다. 세 시편의 입자형상이 구형에 가까운 것을 확 인 할 수 있었다. 그리고 도핑된 Ag의 결정립 크기는 모재인 TiO2에 비해서 매우 작기 때문에 SEM으로 관 찰 할 수 없었다. Fig. 5는 TiO2의 Ag 도핑 유무에 따 른 EDS spectrum 및 mapping 이미지로서 Ti, O, Ag 원소의 피크 및 분포상태를 나타낸다. 이를 통해서 TiO2 에 도핑된 Ag를 확인 할 수 있었고, 균일하게 분포된 Ag 의 분포상태도 알 수 있었다. Fig. 6는 Ag-doped TiO2를 TEM으로 관찰한 사진으로서, Ag의 분포 상태를 명확히 보여준다. 광증착법은 TiO2와 같은 복합체의 발색단이 빛 을 흡수하면 광 여기가 일어나고, 이때 생성된 전자(e–) 와 정공(h+)에 의해서 금속을 상온에서 효율적으로 증착 시키는 방법이다.13-17) 따라서 광증착법에 의해서 TiO2에 Ag가 비교적 도핑이 잘 되었다고 사료된다.
3.2. 벤젠가스(C6H6)에 대한 광분해 반응 분석
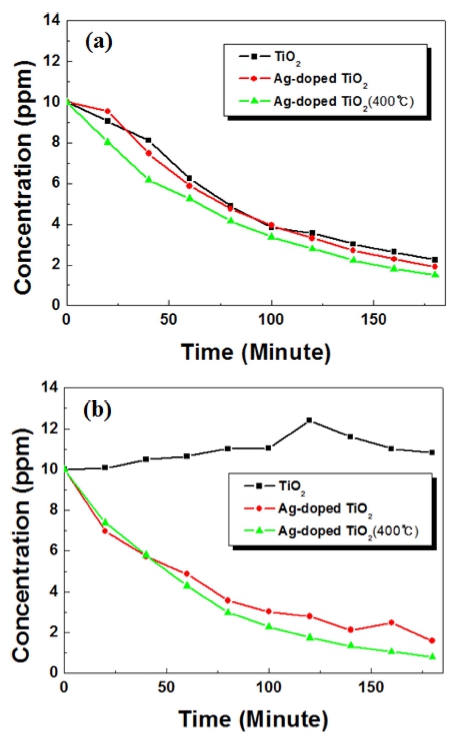
Fig. 7(a)는 자외선(λ = 365 nm)하에서 Fig. 7(b)는 가시 광선(λ ≥ 410 nm)하에서 시간 변화에 따른 TiO2 및 Agdoped TiO2의 벤젠가스에 대한 광분해 반응을 측정한 그 래프이다. 가시광선 하에서 측정하는 경우에는 200-W 백 열전구에 자외선 차단 렌즈(UV-filter Lens, Kenko)를 부 착하여 자외선을 제거하였다. Fig. 7에서 그래프가 일정하 지 않은 이유는 실험적 오류로 인한 것으로 생각된다. 하지만 광분해도의 경향성에는 영향을 미치지 않았다. Fig. 7의 그래프 결과를 살펴보면 자외선과 가시광선 하 에서 Ag-doped TiO2는 TiO2보다 광분해 속도가 빨랐다. 이는 TiO2 표면에 Ag와 같은 나노금속이 도핑되면 나노 금속은 낮은 페르미준위에 의해 분리된 전자의 임시 저 장소 역할을 하게 되고 전자(e–)-정공(h+)쌍(electron-hole pair, EHP)의 분리효율을 향상시켜 주기 때문이다.18-19) 그 리고 TiO2는 band gap이 3.2 eV(λ = 388 nm)이기 때문에 가시광선 하에서는 광분해가 일어나지 않고, Ag가 도핑 된 Ag-doped TiO2 시편은 광분해가 일어났다. 이는 Ag 가 도핑되면서 TiO2의 흡수 스펙트럼이 가시광선 영역 대로 확장되기 때문이다.20) TiO2를 제외하고 Ag-doped TiO2를 살펴보면 annealing하지 않은 시료보다 400 °C에 서 annealing한 시료의 광분해 속도가 빨라졌다. 이는 annealing하지 않은 시료는 광분해 속도를 저하시키는 흡 착수, 수산기, 불순물 등의 잔유물이 남아 있고, annealing 한 시료는 잔유물이 제거되었기 때문이다.21)
4. 결 론
본 연구에서는 졸-겔공정을 이용하여 TiO2를 합성하고, 합성한 TiO2를 사용하여 광증착법으로 Ag를 도핑시켰 다. 또한, Ag 도핑과 annealing에 따른 결정구조 및 미 세구조 변화를 관찰하고 벤젠가스에 대한 광분해 반응 특성을 고찰하였다.
EDS와 TEM을 통해서 TiO2에 도핑된 Ag의 분포 상 태를 확인 할 수 있었다. 그리고 TiO2와 Ag-doped TiO2 의 벤젠가스에 대한 광분해 특성을 측정한 결과, 자외 선 및 가시광선 하에서 TiO2보다 Ag-doped TiO2가 광 분해 속도가 빠르게 나타났다. 그 원인은 TiO2 표면에 Ag와 같은 나노금속이 도핑되면 나노금속은 낮은 페르 미준위에 의해 분리된 전자의 임시 저장소 역할을 하게 되고 전자(e–)-정공(h+)쌍의 분리효율을 향상시켜 주기 때 문이다. 또한 TiO2는 가시광선 하에서는 광분해가 일어 나지 않고, Ag가 도핑이 되면 광분해가 일어났으며, 이 는 Ag가 도핑되면서 TiO2의 흡수 스펙트럼이 가시광선 영역대로 확장되었기 때문에 가시광선 하에서도 광분해 가 일어날 수 있었다. 400 °C로 annealing한 경우는 유 기물, 수산기, 불순물 등의 잔유물이 제거되어 광분해 속 도가 가장 빠르게 나타났다.