1. 서 론
최근에 백색 발광 다이오드는 백열 전등과 할로겐 램 프에 비하여 친환경적이며 높은 효율과 긴 수명을 나타 내기 때문에 차세대 디스플레이 광원, 의료 영상과 조 명 장치로 그 응용성을 확장하고 있다.1,2) 다양한 색상 의 고휘도 디스플레이를 제작하기 위해서는 화학 및 열 적으로 안정한 적색, 황색, 녹색, 청색 발광 형광체의 개 발은 필수적이다. 기술적으로 사마륨(samarium)과 유로퓸 (europium)을 활성제 이온으로 사용하여 주황색, 적색과 같은 가시광선 영역에서 장파장의 빛을 방출하는 형광 체의 제작은 비교적 용이하지만, 황색과 녹색의 빛을 방 출하며 화학적으로 안정한 형광체의 개발은 상대적으로 많지 않은 실정이다.
알루민산염(aluminate)를 기반으로 하는 형광체 물질은 플라즈마, 전계발광, 디스플레이와 같은 다양한 산업 영 역에 사용되고 있으며, 알루민산염은 희토류 이온을 치 환 고용하기에 화학 및 열적으로 안정한 발광 모체 물 질로 알려져 있다.3) 특히, CaAl2O4(calcium aluminates) 는 시멘트의 주성분이며, 최근에 정보 저장 소자, 야광 페인트, 내화 물질과 발광 모체 결정으로 그 응용성을 찾고 있다.4) 희토류 이온이 도핑된 CaAl2O4는 높은 양 자 효율, 예외적으로 긴 인광 시간과 우수한 안정성 때 문에 광범위하게 연구되고 있으며, CaAl2O4의 결정 구 조는 소결 온도와 제조 방법에 따라 두 종류의 결정 구 조, 즉 육방정계(hexagonal system)와 단사정계(monoclinic system)을 갖는 것으로 보고되고 있다.5-7) Aitasalo 등8) 은 졸겔 방법(sol-gel method)을 사용하여 850 °C에서 소 결한 Eu2+가 도핑된 CaAl2O4 형광체는 불안정한 육방 정 계 구조를 나타내었고, 950 °C에서 소결한 경우에 육방 정계에서 단사정계로 상(phase) 전이가 발생함을 관측하 였다. ZhaO와 Chen9)은 연소법(combustion method)을 사용하여 Eu3+와 Nd3+ 이온이 동시 도핑된 CaAl2O4 형 광체를 합성하였으며, 초기 연소 온도 400 °C에서 제조 한 형광체 분말의 경우에는 CaAl2O4의 주 회절 피크와 함께 세기가 약한 CaAl4O7의 회절 피크가 나타났으나 연 소 온도가 증가함에 따라 CaAl2O4의 단사정계 회절 피 크만 관측하였음을 보고하였다. Ryu와 Bartwal10)는 고상 반응법을 사용하여 900 °C에서 6 h 동안 소결 공정과 1300 °C에서 2 h 동안 환원 작업을 수행하여 CaAl2O4: Eu2+, Ti3+ 형광체를 제조하였으며, 그 분말의 결정 구조 는 단사정계임을 제시하였다.
본 연구에서는 모체 결정 CaAl2O4에 두 종류의 활성 제 이온 Tb3+와 Dy3+를 각각 몰 비로 도핑하여 녹색과 황색을 발광하는 고효율의 형광체를 제작하고자 한다. 특 히, 최대 발광과 흡광 세기를 갖는 Tb3+와 Dy3+ 이온의 농도를 결정하고, 두 이온의 농도를 체계적으로 변화시 켜 합성한 형광체의 결정 구조, 흡광과 발광 스펙트럼 의 파장과 세기, 결정 입자의 형상을 조사하였다.
2. 실험 방법
CaAl2O4:RE3+(RE = Tb, Dy) 형광체 분말은 고상반응법 을 사용하여 초기 물질 CaCO3(순도: 99.9 %), Al2O3 (99.9 %)와 희토류 이온(RE3+)인 Tb4O7(99.9 %)와 Dy2O3 (99.9 %)를 화학양론적으로 준비하였으며, RE3+ 이온의 농 도(x)를 각각 0, 0.01, 0.05, 0.10, 0.15, 0.20 mol로 변화 시켰다. 화학 반응식은 식 (1)-(2)과 같다:
상기의 초기 물질을 정밀 저울로 측량하여 에탄올을 매 개체로 사용하여 ZrO2 볼과 함께 플라스틱 병에 넣고 10 시간 동안 볼밀(ball-mill) 작업을 수행하였다. 혼합 분쇄 된 용액을 몰 비로 각 비커에 담아서 50 °C에서 20 시 간 동안 건조시켰다. 건조한 시료를 막자사발에 넣고 미 세한 크기로 갈아서 80 μm의 체(sieve)로 걸러낸 후에, 알루미나 도가니에 담아서 전기로에 장착하여 2 °C/min 의 속도로 승온시켜 350 °C에서 3 시간 하소 공정을 실 시하였고, 계속 4 °C/min의 속도로 증가시켜 1100 °C에 서 5 시간 동안 소결하여 제조하였다.
형광체 분말의 결정 구조는 Cu-Kα 복사선(파장: 1.5406 Å)을 사용하는 X-선 회절 장치(Ultima IV, Rigaku)를 사 용하여 회절각 10-80° 영역에서 4°/min의 스캔 속도로 측 정하였다. 표면의 미세 형상 구조는 주사전자현미경(FESEM, S-4300, Hitachi)으로 조사하였으며, 발광과 흡광 스펙트럼은 제논 램프를 광원으로 갖는 형광광도계(FS- 2, Scinco)를 사용하여 상온에서 측정하였다.
3. 결과 및 고찰
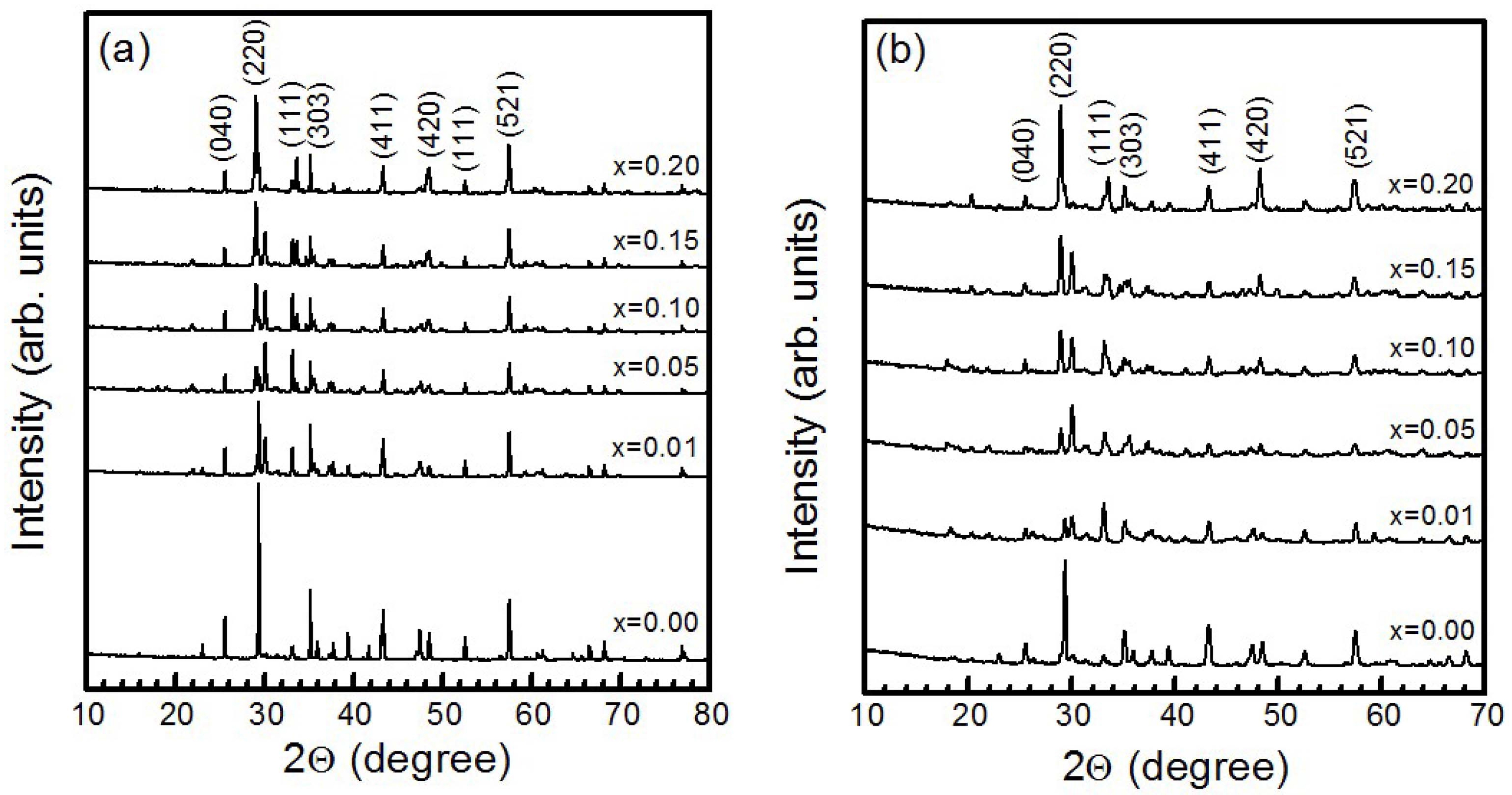
Fig. 1(a)와 (b)는 각각 Tb3+와 Dy3+ 이온의 몰 비(x) 를 x = 0, 0.01, 0.05, 0.10, 0.15, 0.20 mol씩 변화시키 면서 합성한 CaAl2O4:RE3+(RE = Tb, Dy) 형광체 분말 시료의 XRD 데이타를 나타낸 것이다. Tb3+와 Dy3+ 이 온이 각각 도핑된 형광체 시료는 2θ = 29.41o에서 최대 회절 세기를 갖는 주 피크와 상대적으로 약한 세기를 갖 는 25.58°, 35.15°, 43.34°, 47.50°, 57.50°에 중심을 둔 회절 피크들이 관측되었다. 전자는 (220)면에서 발생한 회 절 피크이며, 후자는 (040), (303), (411), (420), (521)면 에서 발생한 피크들이다. Tb3+와 Dy3+ 이온의 몰 비에 관계없이, 합성한 형광체 분말은 JCPDS #70-0134에 제 시된 회절 상과 일치하는 단사정계(monoclinic system) 의 결정 구조임을 확인할 수 있었다. 두 종류의 활성제 이온의 회절 피크는 관측되지 않았다. Tb3+와 Dy3+ 이 온의 몰 비가 0.01 mol에서 0.20 mol로 증가함에 따라 주 회절 피크 (220)의 세기는 증가하였고, 반치폭(full width at half maximum)의 크기는 감소하는 추세를 나 타내었다. (220)면에서 얻은 회절 피크의 반치폭과 회절 각, X-선의 파장을 잘 알려진 Scherrer의 식11)에 대입하 여 계산한 결과, 결정자(crystallites)의 평균 크기는 Tb3+와 Dy3+ 이온의 몰 비가 0.20 mol일 때 각각 50 nm와 30 nm 이었다.
Fig. 2는 Tb3+ 이온의 몰 비를 (a) x = 0, (b) 0.01, (c) 0.05, (d) 0.10, (e) 0.15, (f) 0.20 mol로 합성한 CaAl2O4: Tb3+ 형광체 분말과 Dy3+ 이온의 몰 비를 (g) x = 0.01, (h) 0.05, (i) 0.10, (j) 0.15, (k) 0.20 mol로 제조한 CaAl2O4: Dy3+ 형광체 분말의 미세 표면 형상을 SEM으로 촬영 한 것을 나타낸 것이다. Fig. 2(a)-(f)에서 보듯이, Tb3+ 이온이 치환 고용된 형광체 분말은 평균 크기 1.5 μm인 구형의 결정자들이 서로 뭉쳐져서 조약돌 모양의 불규 칙한 형태를 보였다. Fig. 2(g)에서 보듯이, Dy3+ 이온이 0.01 mol 도핑된 CaAl2O4 형광체의 경우에 결정 입자의 평균 크기는 1.6 μm이었고, 전반적으로 결정 입자들은 체 인 모양으로 결합되어 있는 비대칭적인 형태를 나타내 었다.

Fig. 2.
SEM surface images of CaAl2O4 phosphors doped with different contents of (a-f) Tb3+ and (g-k) Dy3+ ions.
Fig. 3(a)와 (b)는 활성제 이온 Tb3+와 Dy3+의 몰 비를 각각 변화시키면서 합성한 CaAl2O4:Tb3+와 CaAl2O4:Dy3+ 형광체 분말에서 측정한 흡광 스펙트럼과 세기를 나타 낸 것이다. Fig. 3(a)에서 보듯이, 방출 파장 552 nm로 제어한 Tb3+ 이온의 몰 비가 0.01 mol인 Ca0.9825Al2O4: 0.01Tb3+ 형광체의 흡광 파장은 245, 271, 283 nm에서 발생하였으나, 통상적으로 Tb3+ 이온의 4f→4f 전이에 의하여 350-500 nm 파장 영역에서 발생하는 흡광 신호 는 검출되지 않았다. 상기의 흡광 신호들은 Tb3+ 이온 의 4f8 →4f75d1 (f-d) 전이에 의해 발생한 신호이다.12) Tb3+ 이온의 함량이 0.01 mol일 때 f-d 흡광 신호는 283 nm에 피크를 갖는 비대칭적인 형태를 나타내었고, Tb3+ 이온의 함량이 0.05-0.15 mol 영역에서 흡광 신호는 271 nm에 정점을 갖고 단파장 쪽에 작은 피크가 분리되어 나타나기 시작하였고, 0.20 mol에서는 완전히 세 피크로 분리되었다. 이러한 현상은 Tb3+ 이온의 함량이 증가함 에 따라 모체 격자에서 결정장(crystal field)의 세기가 변 하여 흡광 피크의 위치가 이동하면서 분리된 것으로 설 명할 수 있다.13) Fig. 3(b)는 Dy3+ 이온의 몰 비를 0.01- 0.20 mol로 변화시키면서 합성한 CaAl2O4:Dy3+ 형광체 분 말을 발광 파장 581 nm로 제어하여 측정한 흡광 스펙 트럼을 나타낸 것이다. Dy3+ 이온의 몰 비가 0.05 mol 일 때 두 종류의 흡광 스펙트럼이 발생하였다. 첫째는 220- 320 nm에 걸쳐 넓게 분포하며 298 nm에 피크를 갖는 Dy3+-O2– 이온들 사이의 에너지 전달에 의하여 발생하는 CTB(charge transfer band: 전하전달밴드) 흡광 신호이며, 둘째는 320-500 nm 영역에 위치하며 흡광 세기가 상대 적으로 약한 327, 354, 366, 392, 430, 457 nm에 피크 를 갖는 여섯개의 흡광 신호이다. 여기서 여섯개의 흡광 파장은 Dy3+ 이온이 6H15/2→ 6P3/2, 6H15/2→ 6P7/2, 6H15/2→ 6P5/2, 6H15/2→ 4M21/2, 6H15/2→ 4G11/2, 6H15/2→ 6I15/2 전이 에 의해 발생한 흡광 신호들이다.14) CTB 신호의 흡광 세기는 Dy3+ 이온의 몰 비가 0.05 mol일 때 최대값을 나 타내었다. Dy3+ 이온의 몰 비가 증가함에 따라 CTB 신 호의 흡광 세기는 감소하였으나 Dy3+ 이온의 4f→4f 전 이에 의한 354 nm의 흡광 신호의 세기는 0.10 mol에서 최대이었고, 0.15 mol에서는 감소하는 추세를 보였다. 이 결과는 고상반응법으로 합성한 CaMoO4:Dy3+ 형광체에서 Dy3+ 이온의 몰 비가 0.01 mol에서 0.20 mol로 증가함에 따라 CTB 흡광 신호의 세기가 감소하는 결과와 일치하 였다.15) Dy3+ 이온의 몰 비가 0.10-0.20 mol 영역에서 세 기가 최대인 354 nm의 흡광 파장은 GaN를 기반으로 하 는 LED 칩의 자외선 출력 파장과 일치함으로써 그 응 용성은 광범위하다.
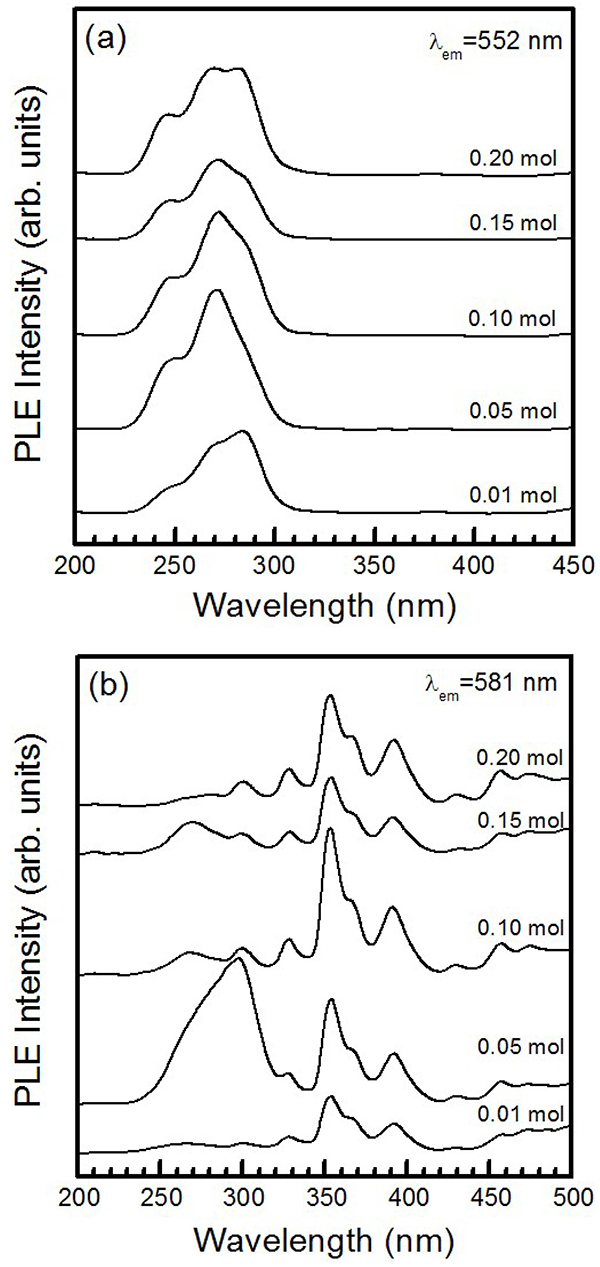
Fig. 3.
Excitation spectra of CaAl2O4 phosphors doped with different contents of (a) Tb3+ and (b) Dy3+.
Fig. 4(a)와 (b)는 각각 활성제 이온 Tb3+와 Dy3+의 함 량비로 제조한 CaAl2O4:Tb3+와 CaAl2O4:Dy3+ 형광체 분 말에서 측정한 발광 스펙트럼을 나타낸 것이다. Fig. 4(a) 에서 보듯이, 파장 271 nm로 여기시킨 CaAl2O4:Tb3+ 형 광체 분말의 경우에, Tb3+ 이온의 몰 비에 관계없이 다 섯 종류의 발광 스펙트럼이 관측되었다. 발광 세기가 가 장 강한 552 nm의 녹색 주 발광 피크를 포함하여 590 nm와 630 nm에 약한 세기를 갖는 주황색과 적색 발광 스펙트럼과 주 피크에 비하여 상대적으로 약한 448 nm 와 491 nm에 피크를 갖는 청색 발광 스펙트럼이 나타 났다. 이 발광 스펙트럼들은 Tb3+ 이온에 의한 전형적인 발광 신호들인데, 단파장부터 차례대로 Tb3+ 이온의 5D3 → 7F3, 5D4→ 7F6, 5D4→ 7F5, 5D4→ 7F4, 5D4→ 7F3 전이 에 의해 발생한 발광 스펙트럼이다.16) 여기서 발광 세기 가 가장 강한 스펙트럼은 552 nm에서 발생한 녹색 발광 신호이며, 이것은 Tb3+ 이온의 5D4→ 7F5 자기 쌍극자 전 이(magnetic dipole transition) 신호로 알려져 있다.17) Tb3+ 이온의 몰 비가 0.01 mol에서 0.05 mol로 증가함에 따라 다섯 종류의 모든 발광 신호의 세기는 증가하여 0.05 mol에서 최대 발광 세기를 나타내었으나, Tb3+ 이 온의 몰 비가 더욱 증가함에 따라 전반적으로 발광 스 펙트럼의 세기는 감소하는 경향을 나타내었다. 이 결과 로부터 CaAl2O4 모체 결정에 주입되는 Tb3+ 이온의 최 적의 몰 비는 0.05 mol이며, 몰 비가 더욱 증가하면 Tb3+ 이온이 서로 뭉쳐져서 발광 신호의 세기가 급격하게 감 소하는 농도 소광(concentration quenching) 현상이 일어 남을 알 수 있었다.18)
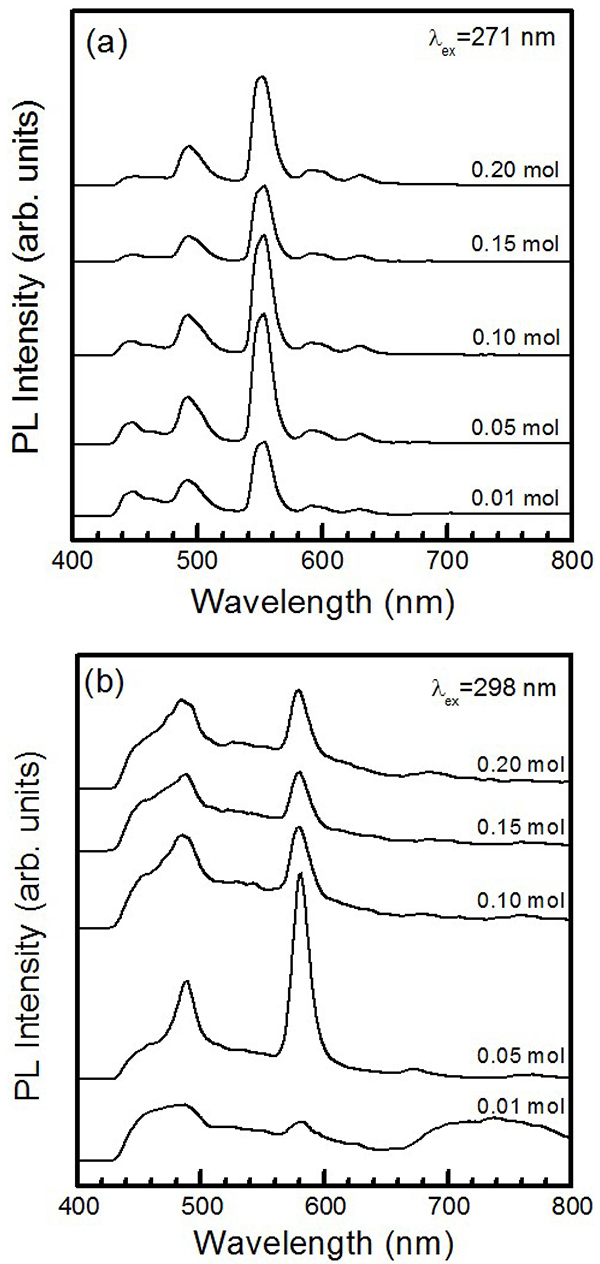
Fig. 4.
Photoluminescence spectra of CaAl2O4 phosphors doped with different contents of (a) Tb3+ and (b) Dy3+.
Fig. 4(b)는 파장 298 nm로 여기시킨 Dy3+ 이온의 몰 비 변화에 따른 CaAl2O4:Dy3+ 형광체 분말의 발광 스펙 트럼을 나타낸 것이다. Dy3+ 이온이 도핑되지 않는 모체 결정 CaAl2O4의 자체 발광은 관측되지 않았으며, Dy3+ 이온의 몰 비가 0.05 mol인 경우에 형광체 분말의 발광 스펙트럼은 세 종류로 구성되었다. 발광 세기가 제일 강 한 581 nm에 피크를 갖는 황색 발광 스펙트럼과 상대 적으로 발광 세기가 주 피크의 반 정도로 작은 488 nm 에 피크를 갖는 청색 발광 신호와 상기의 두 피크에 비 하여 발광 세기가 매우 약한 672 nm에 피크를 갖는 적 색 발광 스펙트럼이 관측되었다. 주된 발광이 황색인 결 과는 연소법을 사용하여 합성한 Dy3+ 이온이 도핑된 LiMgBO3 형광체 분말에서 측정된 발광 결과와 일치한 다.19) 상기의 발광 스펙트럼들은 Dy3+ 이온의 전형적인 4f→4f 전이 신호들이다. 청색 발광 스펙트럼은 Dy3+ 이 온의 4F9/2→ 6H15/2 자기 쌍극자 전이 신호이고, 황색 발 광 스펙트럼은 4F9/2→ 6H13/2 전기 쌍극자 전이(electric dipole transition) 신호이며, 적색 발광 스펙트럼은 4F9/2 → 6H11/2 전이 신호이다.20) 이 형광체는 자외선을 기반으 로 하는 백색 LED에 사용하기에 적합한 형광체임을 알 수 있다. 일반적으로 전기 쌍극자 전이의 발광 세기는 모체 결정에서 자리 대칭성(site symmetry)에 상당히 민 감하나, 자기 쌍극자 전이는 반전성이 허용(parity-allowed) 되기 대문에 자리 대칭성에 크게 영향을 받지 않는다.21) 만일 Dy3+ 이온이 결정 격자에서 반전 대칭(inversion symmetry) 자리를 차지한다면 자기 쌍극자 전이가 주된 전이가 되고, 반대로 Dy3+ 이온이 결정 격자에서 비대 칭 자리에 위치하면 전기 쌍극자 전이가 주된 전이가 되 는 것으로 알려져 있다.22) Fig. 4(b)에서 581 nm에 피크 를 갖는 황색 발광 스펙트럼의 세기가 488 nm의 청색 발광 스펙트럼의 세기보다 훨씬 강하기 때문에 활성제 이온 Dy3+는 모체 격자에서 반전 대칭 자리에 위치하지 않음을 알 수 있다. 세 발광 스펙트럼의 세기는 Dy3+ 이 온의 몰 비가 0.05 mol일 때 최대이었으며, Dy3+ 이온 의 몰 비가 증가함에 따라 세 종류의 발광 스펙트럼의 세기는 전반적으로 감소하는 추세를 나타내었다. 발광 신 호의 세기가 0.05 mol에서 감소하기 시작한 것은 Dy3+ 이온의 몰 비가 더욱 증가함에 따라 이온들 사이의 거 리가 가까워져서 서로 뭉침으로써 발광 세기가 감소하 는 것으로 해석할 수 있다.
4. 결 론
두 종류의 활성제 이온 Tb3+와 Dy3+의 몰 비를 각각 변화시키면서 CaAl2O4 형광체 분말을 제조하였으며, Tb3+ 와 Dy3+의 몰 비가 형광체 분말의 특성에 미치는 영향 을 체계적으로 조사하였다. 모든 형광체 분말의 결정 구 조는 활성제 이온의 몰 비와 종류에 관계없이 주 피크 (220)을 갖는 단사정계이었으며, 결정 입자는 서로 뭉치 면서 비대칭적인 형태를 보였다. Tb3+가 도핑된 CaAl2O4 형광체 분말의 주 흡광 스펙트럼은 271 nm에 피크를 갖 는 넓은 흡광 스펙트럼이었으며, 주 발광 신호는 552 nm 의 녹색 발광 스펙트럼이었다. Dy3+ 이온이 0.05 mol 도 핑된 CaAl2O4 형광체의 경우에 주 흡광 스펙트럼은 298 nm에 피크를 갖는 CTB 신호이었으며, 주 발광 스펙트 럼은 581 nm의 황색 발광 스펙트럼이었다. 본 연구 결 과로부터 Tb3+와 Dy3+의 몰 비가 각각 0.05 mol일 때 최적의 녹색과 황색 발광 형광체를 제조할 수 있음을 제 시한다.