1. 서 론
Hydroxyapatite(HA)는 그 조성이 뼈나 치아의 무기질 성분과 비슷하고 생체활성이 우수해서 생체조직과 생물학 적으로 반응하여 직접 결합, 합체할 수 있기 때문에 생 체경조직 대용으로 매우 적합하다. 그러나 소결체의 강도 가 낮은 단점으로 큰 하중이 걸리는 정형외과나 치과영 역에서의 다양한 활용이 제한되고 있다. HA의 기계적 성 질을 향상시키기 위해 Al2O3,1-7) ZrO2,8-10) 또는 mullite11) 와 같은 강한 재료를 보강성분으로 첨가하는 방법이 주 로 연구되어 왔다.
생체활성과 강한 성질을 겸비한 재료를 만드는 또 다 른 방법은 HA를 강한 재료에 생체활성 부여 성분으로 첨가하는 것인데, Al2O3,12) ZrO2,13,14) ZrO2 80 wt%/Al2O3 20 wt%,15) Al2O3 80 wt%/ZrO2 20 wt%,16) mullite17) 기 지 등에 적용되었다. HA의 분해 억제와 치밀화(상대밀 도 99 % 이상)를 위해 hot isostatic pressing(HIP),12,13) spark plasma sintering(SPS),14) hot pressing(HP)15) 등 의 가압소결법(1,150-1,400 °C)이 주로 사용되었다. 상압소 결(1,400 °C, 1,320 °C)을 한 경우에는 치밀화가 80 % 정 도로 매우 낮았거나,16) HA가 TCP로 완전히 분해되면서 88 %의 낮은 치밀화를 얻었다.17)
순수한 HA의 결정구조는 약 1,400 °C까지 분해 없이 유지될 수 있다. 그러나 Al2O3, ZrO2, 또는 TiO2와 복합 화되면 900-950 °C에서 분해가 시작된다.18) HA-40 vol% Al2O3 복합재료의 경우, CaF2의 첨가를 통해 HA의 OH 자리를 F 이온으로 완전 치환고용 시켜 fluorapatite(FA) 화 하면 분해 개시온도가 1,200 °C까지 높아질 수 있다. 이는 HA가 600 °C 이상의 온도에서 탈수가 되면서 생 성되는 OH 자리의 공공(vacancy)이 없게 되어 결정구조 가 안정화되기 때문이다.18) 한편, HA-20 vol% Al2O3 복 합재료에 5 vol% MgF2(완전 치환고용의 양)를 첨가를 하 면 1,400 °C에서도 apatite 결정구조가 유지된다. 그런데 같은 양의 CaF2를 첨가할 경우엔 일부 TCP로의 분해가 일어난다.6) 이는 apatite의 열적 안정성에 있어서 MgF2 가 CaF2 보다 더 효과적임을 보여준다. 열적 안정성 이 외에 FA는 HA와 비슷하거나 더 우수한 생체적합성을 가 지고 있으며,19) F− 이온으로 인해 충치를 막고 뼈 재생 을 증진시킬 수 있는 이점이 있다.2,20)
HA-Al2O3계 복합재료의 이전 연구들을 보면, Al2O3가 첨가된 경우가 대부분이며1-7) HA가 첨가된 경우는 드물 다. Fartash와 Hermansson12)은 Al2O3에 HA 15, 25, 30, 또는 70 vol%를 첨가한 조성에 대해 HIP(1,275 °C, 200 MPa, 2 h)을 사용하여 99 % 이상의 밀도를 얻었다. 순 수한 Al2O3 기지는 아니지만, Singh과 Reddy16)는 Al2O3 80 wt%/ZrO2 20 wt% 기지에 HA를 10, 20, 30, 또는 40 parts 첨가한 조성에 추가로 CaF2와 MgF2를 각각 3 parts씩 동시 첨가 후 상압소결(1,400 °C, 3 h)을 하여 80 % 정도의 낮은 밀도를 얻었다. 소결체 상분석 결과 의 제시 없이 2차상으로 HA나 FA가 아닌 Ca4P2O9 또 는 Ca3(PO4)2·CaO가 생성되었다고 보고하였는데, CaF2와 MgF2를 첨가했음에도 HA의 분해가 일어난 것으로 여 겨진다.
본 연구에서는 기존 연구와 달리 Al2O3에 HA가 30 wt% 첨가된 복합재료의 제조를 상압소결을 통해 시도하 였다. 30 wt% 조성을 선택한 이유는 HA/ZA(ZrO2 80 wt%, Al2O3 20 wt%) 복합재료에서 세포 증식률 측정을 통해 생체 활성을 부여하기 위해 충분한 HA 양으로 확 인되었기 때문이다.15) Apatite 결정구조의 열적 안정화를 위해 HA를 FA로 만들 수 있는 양의 MgF2를 첨가한 시 편과 첨가하지 않은 시편에 대해 소결밀도, 결정상, 미 세구조 및 강도를 조사하고 비교하였다.
2. 실험 방법
30 wt% HA/Al2O3 복합재료(이하 HAC라고 명명)를 제 조하기 위해, HA 분말(HA-10, Sunkoo, South Korea)과 Al2O3 분말(AKP-53, Sumitomo Chemical, Japan)을 사 용하였다. 이전 연구에 의하면17) HA 분말은 1,250 °C/1 h 소결 시 99 %의 치밀화가 가능하고, 1,350 °C/1 h 소결 후에도 HA 상을 유지한다. 또한 Al2O3 분말은 1,350 °C/ 2 h 소결 시 95 % 이상의 치밀화가 가능하다. 두 분말들 을 칭량하여 isopropyl alcohol과 함께 12 h 볼밀링을 하 였다. 그리고 나서 가열교반을 통해 용매를 제거한 후 60 °C oven에서 건조하였다. 이를 Al2O3 유발를 이용하 여 분쇄한 후 bar 시편(8 × 5 × 35 mm3)을 200 MPa의 압 력으로 정수압 성형을 하였고, 1,300 °C/2 h과 1,350 °C/ 2 h 두 가지 조건으로 소결하였다. HA를 FA로 만들 수 있는 양(HA 무게에 대해 6.7 wt%)의 MgF2(99 %, Alfa Aesar, USA)가 첨가된 복합재료(이하 HAC-M이라고 명 명)의 경우에도 마찬가지 방법으로 준비하였다.
Archimedes 방법으로 소결시편들의 밀도를 측정하였고, X선 회절분석을 통해 결정상을 조사하였다. 3-P MOR test(span 20 mm)로 강도를 측정하였으며, 시편 4개로부 터 평균값을 구하였다. 시편의 파단면에 대해 SEM으로 미세구조 분석을 하였다.
3. 결과 및 고찰
3.1 HAC
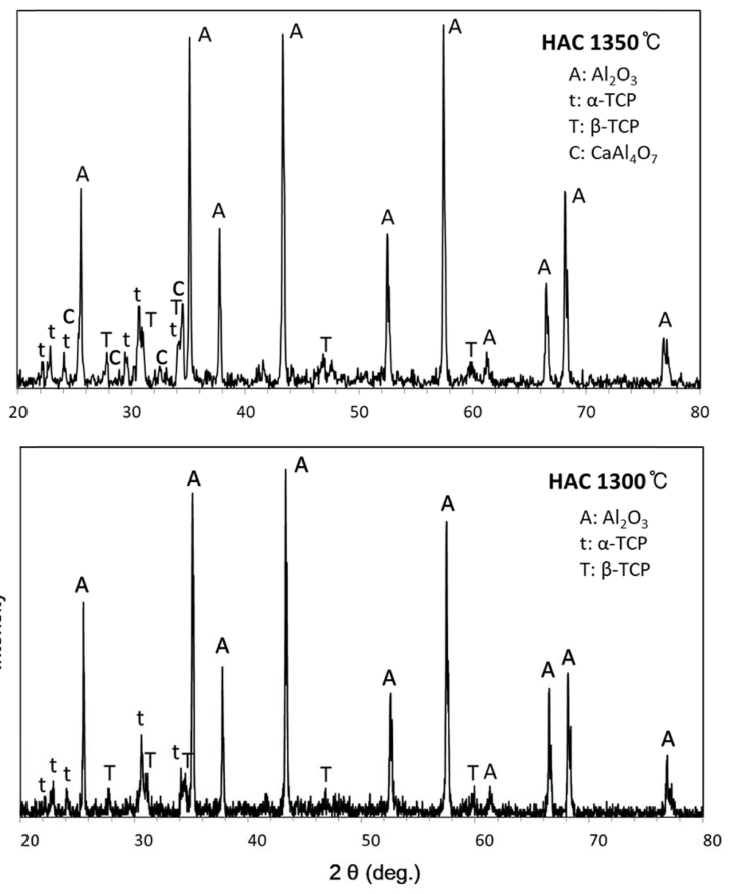
Fig. 1은 HAC의 XRD 분석결과이다. 두 소결온도(1,300 °C, 1,350 °C)에서 다 HA 상은 없었으며, α와 β TCP 상 이 Al2O3와 함께 존재하였다. 1,350 °C의 경우 CaAl4O7 상이 추가로 확인되었다. 이는 HA의 분해가 발생하였 고, 분해 생성물인 CaO가 1,350 °C에서는 Al2O3와 반응 까지 했음을 말해준다. 1,300 °C의 경우 CaO는 단일상 으로 존재한다고 생각되며, Al2O3와 TCP에 비해 그 양 이 많이 적기 때문에 XRD에서는 미확인된 것으로 판 단된다. XRD 결과로부터 다음과 같은 반응식을 추정할 수 있다. HAC의 조성(30 wt% HA)은 Al2O3와 HA의 mole 비로 환산하면 23:1이다.
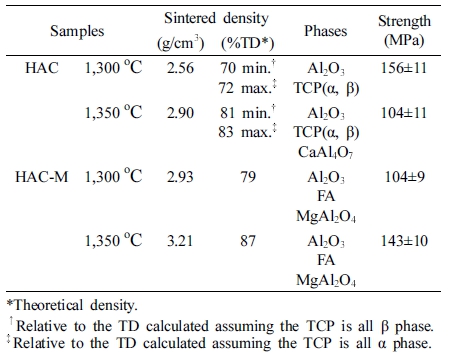
Table 1에 HAC의 소결밀도를 절대값과 이론밀도에 대 한 상대값으로 나타내었다. Minor 상들(β-TCP, α-TCP, CaAl4O7)의 개별적인 양을 알 수 없기 때문에, TCP가 전부 β상(이론밀도 3.07 g/cm3)이라고 가정한 이론밀도와 전부 α상(이론밀도 2.86 g/cm3)이라고 가정한 이론밀도를 각각 사용하여 HAC 상대밀도의 최소값과 최대값을 구 하였다. CaAl4O7의 경우 이론밀도가 2.88 g/cm3로서21) α- TCP의 이론밀도와 비슷하므로 α-TCP로 간주하였다. 1,300 °C 시편의 경우 소결밀도의 최소값과 최대값이 각각 70, 72 %로서 매우 낮았다. 반면에 1,350 °C 시편의 경우엔 81, 83 %로서 1,300 °C 시편 보다 10 % 가량 높았다.
Fig. 2와 3은 각각 1,300 °C와 1,350 °C에서 소결된 HAC의 SEM 분석결과를 보여준다. 1,300 °C와 1,350 °C 시편 둘 다 HA 분해 시 기상의 H2O 발생으로 인해 생 성된 것으로 보이는 5-6 μm 크기의 큰 기공들이 관찰되 었다[Fig. 2(a), 3(a)]. 1,350 °C 시편의 경우 이러한 기공 의 양이 더 많았는데(SEM 분석 시 시편 전체를 구획, 관찰하여 같은 양상임을 확인), 이는 더 높은 소결온도 에서 분해 반응 속도가 빨라져서 H2O 발생이 동시 다 발적으로 일어났기 때문인 것으로 보인다. HAC의 경우 소결 시 HA(밀도 3.16 g/cm3)가 더 낮은 밀도를 갖는 TCP(β 3.07, α 2.86 g/cm3)와 CaAl4O7(2.88 g/cm3)로 상 전이하면서 부피 팽창이 발생한다. 이것이 기상의 H2O 발생과 더불어 소결에 따른 수축을 방해하여 70-83 %의 낮은 치밀화가 얻어진 것으로 생각된다. 1,300, 1,350 °C 시편 둘 다 입자크기가 1 μm 보다 작았으며, 0.2-0.3 μm 크기의 입자들이 주를 이루고 있었다[Fig. 2(b), 3(b)]. 그 리고 입자들 사이에 1 μm > 크기의 작은 기공들이 고 르게 분포되어 있음을 알 수 있는데, 이 또한 치밀화가 낮음을 보여준다. Table 1에서 보듯이 강도(편차 ±11 MPa)는 156과 104 MPa로서 1,300 °C 시편이 더 높았는 데, 이는 소결밀도는 더 낮았지만 큰 기공의 양이 더 적 었기 때문인 것으로 파악된다.
3.2 HAC-M
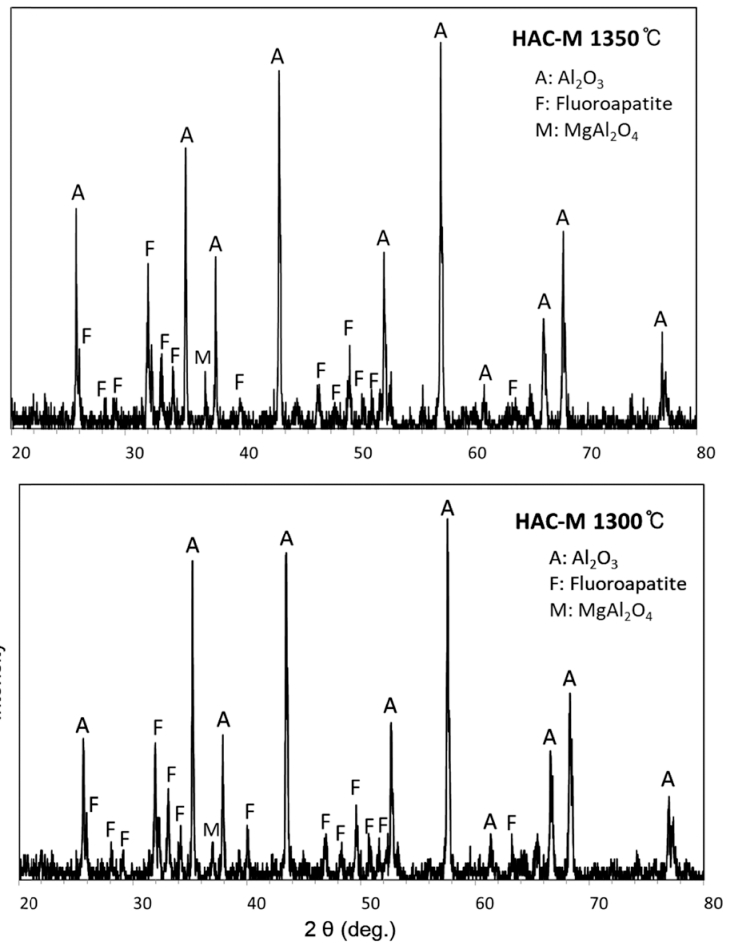
Fig. 4는 HAC-M의 XRD 분석결과이다. 두 소결온도 (1,300, 1,350 °C)에서 다 FA 상이 Al2O3와 함께 존재하 였고 TCP 상은 없었다. 이는 MgF2 첨가에 의해 HA의 OH가 F로 완전히 치환되어 1,350 °C까지 HA 결정구조 가 안정화 되었음을 보여준다. 두 온도에서 MgAl2O4 상 이 추가로 확인되었고, 이는 FA 생성 시 발생하는 MgO 가 Al2O3와 반응까지 했음을 말해준다. XRD 결과로부 터 다음과 같은 반응식이 추정된다.
소결밀도는 79, 87%로서, 그리고 강도는 104, 143 MPa 로서 두 경우 다 1,350 °C 시편이 더 높았다(Table 1).
Fig. 5와 6은 각각 1,300 °C와 1,350 °C에서 소결된 HAC-M의 SEM 분석결과를 보여준다. 두 경우 다 HAC (MgF2 무첨가)에서와 같은 큰 기공들은 없었다[Fig. 5(a), 6(a)]. 이는 FA 생성이 승온 중에 900 °C22)나 1,000 °C18) 의 낮은 온도에서부터 일어나고, OH− 자리에 F− 이온 의 치환에 따른 기상의 H2O 발생이 소결온도(치밀화가 본격화되는 시점)에 도달하기 이전에 완료되었기 때문인 것으로 생각된다. 또한 HAC와 달리 소결 중 HA(밀도 3.16 g/cm3)가 FA(밀도 3.19 g/cm3)로 상전이 시 부피 감 소가 일어나기 때문에 소결 수축을 방해하지도 않는다. 그 래서 HAC 보다 더 높은 치밀화가 얻어진 것으로 파악 된다. 입자크기는 1,300 °C 경우 0.3-1 μm, 1,350 °C 경 우 0.5-2 μm 정도였다[Figs. 5(b), 6(b)].

Fig. 5
SEM results of HAC-M sintered at 1,300 °C, observed at magnifications of (a) 1000 and (b) 5000 times.

Fig. 6
SEM results of HAC-M sintered at 1,350 °C, observed at magnifications of (a) 1000 and (b) 5000 times.
단일 TCP와 HA의 강도(본 연구에서와 같이 3-P 시 험 측정값)는 각각 15 MPa23)과 26 MPa5) 정도로 알려져 있는데 본 연구의 HAC(28 wt% TCP/Al2O3)와 HACM( 30 wt% FA/Al2O3)는 104-156 MPa로서 이 보다 훨씬 우수하다.