1. 서 론
최근 디스플레이 및 에너지 분야의 급속한 성장에 따 라 고성능 및 고효율을 지닌 소재들에 대한 관심이 높 아지고 있다. 특히 첨단 고부가가치 산업인 휴대용 전 자산업계에서 이러한 특성을 충족시키는 소재의 개발이 요구되고 있으며 전기/광학적 우수성을 지닌 유리가 후 보로 대두되고 있다. 유리는 소재 합성 차원에서 원소 의 비율을 다양하게 할 수 있는 장점이 있기 때문에, 에 너지 분야에서 폭넓은 응용성을 가진 물질로 관심이 증 대되고 있다.1,2) 이 중 리튬 전도성 산화물 유리는 차세 대 소형 시스템의 전원인 리튬 이차전지의 구성요소 중 하나인 전해질로 이용 가능한 물질이다. 또한 리튬 전 도성 산화물 유리는 등방성의 전도도와 화학적, 열적 안 정성 및 넓은 전압 범위에서 전기화학적 안정성을 지니 고 있어 많은 연구가 이루어지고 있다.3,4)
Li2O-SiO2계는 화학구조가 간단하고 유리로의 제조가 용 이하다. 또한, fast ionic conductor로 저온에서 전도도가 좋고, 강도 및 화학적 안정성이 우수하여 이차전지 구 성 재료로 많은 관심을 받고 있다.5-8) Li2O-SiO2계 유리 중 유리 형성에 이점을 가진 Li2O-2SiO2 (LSO)를 선택 하였다. LSO 유리의 결정화에 대한 연구는 온도, 압력 및 가스 분위기9-11)가 핵 생성12) 및 결정 성장에 미치는 효과13)를 고려하여 진행되고 있다. 이러한 LSO 유리 연 구를 바탕으로 산업계에 응용하기 위한 시도가 지속되 고 있다. 그러나 LSO 유리의 결정화 메커니즘에 대한 명확한 자료가 부족하며 균일한 결정의 획득을 위해서 는 고온 및 고압 처리가 필요하므로, 산업으로의 적용 이 쉽지 않다. 따라서 유리에서 결정의 핵 생성과 성장 및 상전이 연구를 통하여 마이크로 구조 및 물성을 이 해할 수 있다면, 핵 생성과 결정 성장 정도를 제어함으 로써 크기가 조절된 마이크로 복합 물질을 합성할 수 있 을 것으로 기대된다.
본 연구에서는 LSO 유리를 제조하고, 유리 입자의 크 기에 따른 결정화 효과 및 결정으로의 상전이 과정을 해 석하였다. 또한 등온 및 비등온법에 따른 열적 특성을 Johnson-Mehl-Avrami 모델과 개선된 Ozawa 모델을 적 용하여 분석하였다. 이러한 모델들의 적용은 실험 방법 의 차이로 인한 시간과 온도에 대한 부피비 변화를 고 려하였기 때문으로 열처리 방법에 따른 결정화 활성화 에너지 및 결정 성장방식을 비교 분석하여 LSO 유리의 결정화에 대한 상전이 메커니즘을 밝혔다.
2. 실험 방법
Li2O-2SiO2 (LSO) 유리는 용융-급냉법을 이용하여 제 조하였다. 시료의 제조를 위하여 먼저 Li2CO3(Sigma- Aldrich chemistry, 99%)와 SiO2(Sigma-Aldrich chemistry, 99.9 %) 시약을 1:2 몰비로 혼합하여 지르코니아 막자사 발에 투입하고 2시간 동안 충분히 교반하였다. 잘 교반 된 혼합물은 백금도가니에 넣어 전기로에서 용융시켰다. 이때, 전기로는 승온 속도 20 °C/min으로 가열하였으며, 1150 °C에서 1시간 동안 용융하였다. 용융된 시료의 용 액을 황동판으로 급냉하여 두께가 0.05~1 mm인 무색 투 명한 판 형태의 Li2O-2SiO2 유리를 제조하였다.
제조된 LSO 유리의 결정화 과정에서 나타나는 열 특 성을 조사하기 위해 시차주사열량계(DSC, differential scanning calorimetry, Netzsch STA409, Germany) 실험 을 하였다. 유리 시료는 ball mill(Fritsch, P-6(ZrO2 bowl), Germany)로 분쇄하여 분말 상태로 만들었다. 분말 상태 의 유리 시료를 시험용 체(testing sieve, #325, 200, 140, 120, 100, Orto Alresa)로 나누어 45 μm 이하, 75~106 μm, 125~150 μm의 3가지 입자크기로 분리하였고, 이를 비등온법과 등온법으로 측정하였다. 등온 및 비등온 측 정은 10 mg의 LSO 유리 분말을 백금용기에 넣고 Ar 분 위기에서 하였다. 비등온법 측정은 4, 6, 8, 10 °C/min의 승온율에 따라 측정하였으며, 온도는 상온에서부터 700 °C 까지로 하였다. 등온법 실험에 사용한 온도는 10 °C/min 의 비등온 측정결과로부터 선택되었고, 결정화가 이루어 지는 온도(Tc)보다 낮은 온도로 택하였다.
등온 측정은, 유리 입자의 크기가 45 μm이하인 경우 는 535 °C, 545 °C, 555 °C의 온도에서, 유리 입자의 크 기가 75~106 μm인 경우는 555 °C, 560 °C, 565 °C의 온 도에서, 유리 입자의 크기가 125~150 μm인 경우는 565 °C, 575 °C, 585 °C의 온도에서 각각 수행하였다. LSO 유리의 결정 구조를 관찰하기 위해 XRD(X-Ray Diffraction, Rigaku, Japan) 측정을 하였다. XRD 측정 시 40 kV의 가속 전압과 30 mA의 전류를 사용하였고, 측정 산 란각(2θ) 범위는 10~80o, scan speed는 1o/min로 하였다. 이때 X-선은 Cu-Kα 선을 사용하였고, 파장(λ)은 1.54056 Å이었다.
3. 실험 결과 및 고찰
미세구조(microstructure) 물질은 덩어리(bulk or coarse grain) 물질에 비해 열적, 전기적, 광학적 및 기계적 특 성이 민감하게 변화함으로 기술 및 학문 발전에 기여가 크다. 따라서 미세구조 물질을 이해하는 것은 매우 중 요하다. 본 연구에서는 입자의 크기에 따른 결정화 메 커니즘과 활성화 에너지를 확인하고 미세구조 물질에 대 한 열적 특성을 이해하고자 하였다. 4, 6, 8, 10 °C/min 의 다양한 승온율에서 측정한 DSC 곡선들 중 유리 분 말의 크기에 따른 10 °C/min에 대한 측정 결과를 Fig. 1 에 나타내었다. Fig. 1에서 분말 크기에 따른 LSO 유리 의 DSC 곡선은 발열봉우리가 모두 하나만 나타났다. 하 나의 발열봉우리는 결정화에 관여하는 결정상이 하나임 을 의미하며, 이는 Fig. 2의 XRD 무늬가 단일 결정상 을 나타내는 것으로 확인할 수 있다. 열역학적으로 준 안정상태의 유리상은 외부 에너지에 의해 안정 상태인 결정상으로 상전이가 일어나며, 유리가 지니고 있던 잠 열(latent heat)이 발열로 나타난다. 그러므로 DSC 곡선 에서의 발열은 각각의 온도에서 유리상이 결정상으로 결 정화가 이루어질 때 단위 온도당 진행된 결정 부피 비 (crystallized volume fraction)에 비례한다. 따라서 임의 온도까지 발열 봉우리를 적분한 면적은 결정화가 이루 어진 부피 비를 나타낸다. 유리 시료를 열 분석 할 경 우, 온도 증가에 따라 흡열반응이 나타나게 된다. 이는 주어진 외부 에너지 즉 열 에너지를 유리가 흡수하면서 유리의 점성이 급격히 감소하는 영역이 발생하기 때문 이며, 이 영역을 유리 전이 온도(Tg)라 한다. 또한, 열 분석 곡선에는 결정화가 이루어지는 온도(Tc)와 결정화에 따른 열 방출 크기가 가장 큰 결정화 봉우리 온도(Tp) 가 있으며, 과냉각 액체 구간에서 열적 안정성을 표현 하는 ΔT ≡ (Tc − Tg)가 있다. Fig. 1에서 보면, Tg는 모 두 같은 온도에서 나타나고, Tc는 분말의 크기가 커질수 록 증가하였다. 즉 ΔT가 입자크기의 증가에 따라 커지 고 있음을 알 수 있다. 이는 유리의 안정성이 입자크기 에 따라 변함을 의미한다. 즉, 입자크기가 작을수록 더 큰 표면적에 의해 큰 입자보다 많은 에너지를 흡수하여 결정화가 좀더 낮은 온도에서 이루어진다는 것을 의미 한다. 이러한 이유로 입자크기가 증가할수록 상대적으로 유리의 열적 안정성이 높아짐을 알 수 있다.
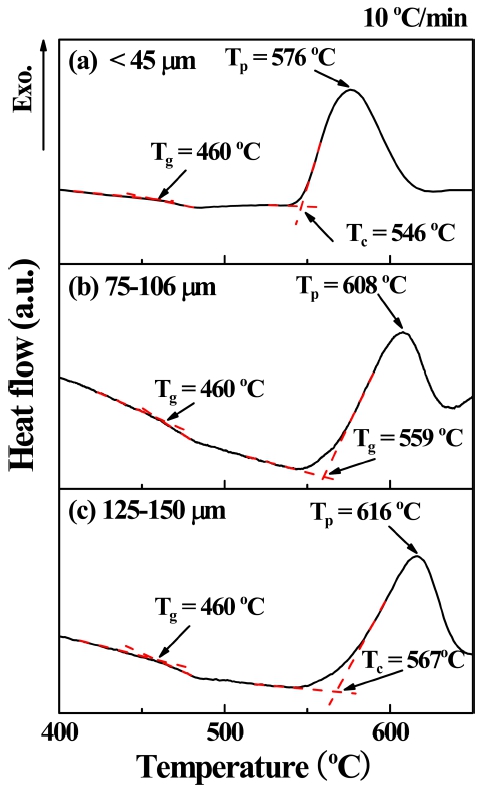
Fig. 1.
Thermal histogram of Li2O-2SiO2 glass in DSC for (a) under 45 μm, (b) 75~106 μm and (c) 125~150 μm glass particles. Tg, Tc, and Tp are the glass transition temperature, crystallization temperature and maximum crystallization temperature, respectively.
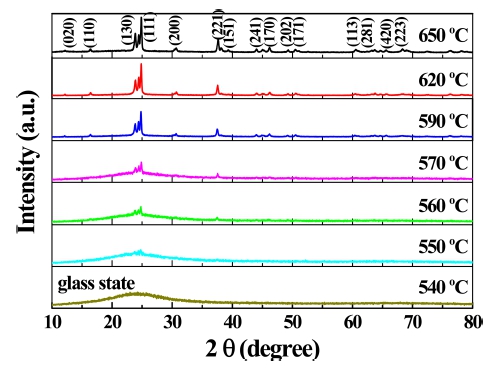
Fig. 2.
X-ray diffraction patterns at room temperature for Li2O-2SiO2 glass. The sample quenched after heat treatment of the glass at various temperatures with a heating rate of 10 °C/min using under 45 μm particles. The Miller indices of the Bragg peaks in the crystalline phase at 650 °C are indexed.
Fig. 2는 LSO 유리의 열처리 온도에 따른 XRD 곡선 으로 유리의 결정화에 따른 상전이 과정을 보인다. XRD 측정은 45 μm 이하의 입자크기를 가진 LSO 유리를 이 용하였고, 열처리 온도는 10 °C/min의 DSC 열 분석 결 과를 활용하였다. 결정화가 시작(Tc = 546 °C)되기 바로 전 의 온도인 540 °C에서 결정화가 모두 이루어진 온도인 650 °C까지 구분하여 열처리한 후 상온에서 측정하였다. Fig. 2에서 열처리 온도가 540 °C인 경우, 결정으로의 상 전이가 이루어지기 전인 유리 상태로서 브레그(Bragg) 반 사 면에 대응되는 회절 봉우리가 나타나지 않고, 단거 리 질서에 의한 완만한 곡선만 보임을 확인할 수 있다. 결정성에 의해 나타나는 브레그 산란 봉우리는 Tc(= 546 °C) 이상의 온도인 550 °C에서부터 출현하였으며, 열처리 온도가 증가할수록 브레그 산란에 의한 결정화 봉우리 는 더욱 뚜렷하게 나타났다. 이는 Fig. 1의 45 μm 이하 의 입자크기를 가진 LSO 유리의 DSC 곡선의 결과와도 일치하였다. XRD 무늬로부터 LSO 결정상이 사방정계 구 조의 Li2Si2O5 단일 결정상(a = 5.807 Å, b = 14.58 Å, c = 4.773 Å)임을 알 수 있었다. 결정면과 관련한 밀러 지 수(hkl)는 650 °C의 XRD 무늬 위에 표시하였다.
Fig. 3은 LSO 유리 시료를 입자크기에 따라 분류하여 상온부터 700 °C까지 측정한 비등온법 DSC 곡선으로, 결 정화와 관련한 발열 봉우리 부분만을 선택적으로 나타 낸 것이다. 승온율은 4, 6, 8, 10 °C/min로 하였다. Fig. 3에서 승온율이 증가함에 따라 봉우리의 크기가 점점 커 지고 고온으로 이동하는 것을 볼 수 있다. 이와 같은 현 상은 승온율의 변화에 따라 반응이 더 높은 온도에서 일 어나는 열적 뒤처짐(thermal delay) 때문이다. 열적 뒤처 짐은 승온율이 커짐에 따라 임의 온도를 지나가는 시간 이 짧아지고 그 온도에서 결정화에 기여하는 반응시간 또한 짧아져 더 높은 온도에서 반응이 급격히 일어나게 되는 현상이며, 봉우리의 크기 증가는 결정화에 의한 잠 열의 방출이 짧은 시간에 집중되어 나타나기 때문이다. Fig. 3의 발열 봉우리를 이용하여, 유리에서부터 결정으 로 상전이가 일어날 때의 결정화 부피 비를 계산하였다.
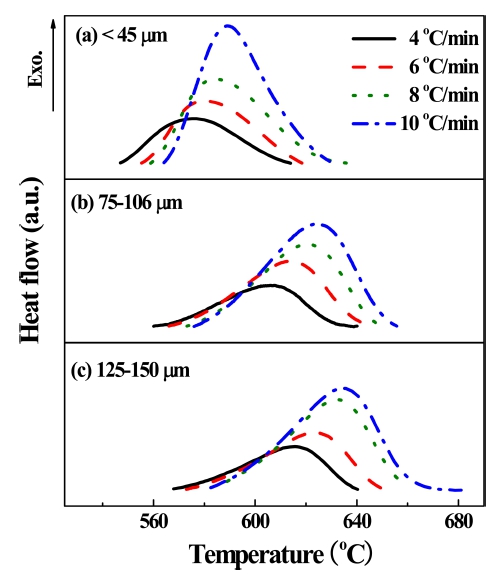
Fig. 3.
DSC curves for the Li2O-2SiO2 glass with heating rate of 4, 6, 8, and 10 °C/min for the glass particles sized (a) under 45 μm, (b) 75~106 μm and (c) 125~150 μm.
Fig. 4는 유리에서 결정으로 상전이가 일어날 때 결정 화된 부피 비를 온도의 함수로 나타낸 것이며 직선의 기 울기로부터 결정화에 대한 활성화 에너지(E)를 구하였 다. 일반적으로 결정화에 대한 활성화 에너지는 온도의 함수이다. 그러나 적당한 온도 구간에서는 활성화 에너 지가 온도에 민감하지 않을 수 있으며, 온도에 대한 부 피비가 Fig. 4에서와 같이 선형적으로 나타나면 기울기 로부터 단일 값의 활성화 에너지를 구할 수 있다. 본 연 구에서 결정화에 필요한 활성화 에너지는 다음과 같은 개선된 Ozawa 모델을 이용하여 계산하였다.14-18)
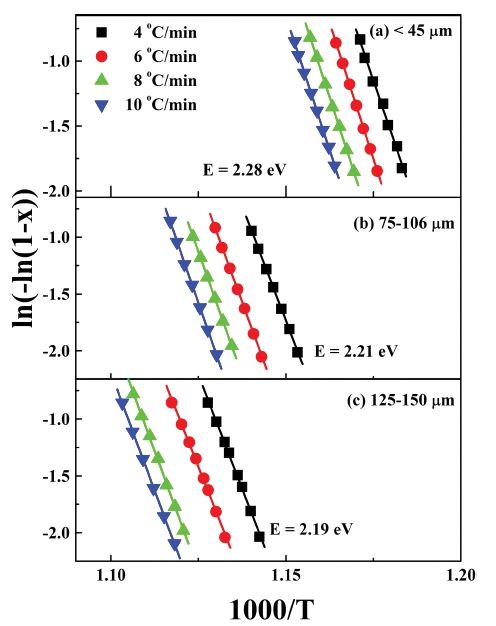
Fig. 4.
Modified Ozawa plot for the Li2O-2SiO2 glass to obtain the activation energies (a) E = 2.28 eV for under 45 μm glass particles, (b) E = 2.21 eV for 75~106 μm glass particles and (c) E = 2.19 eV for 125~150 μm glass particles.
여기서 x는 결정화와 관련한 발열 봉우리의 전체 면 적에 대한 임의 온도 T까지의 면적 비인 결정화 부피 비를 나타내고, n은 결정화 기구를 나타내는 Avrami 지 수19)이고, α는 승온율, R은 기체상수이며, m은 결정의 성장 차원을 나타낸다. 본 연구에서는 결정의 성장차원 m을 3으로 두었고, 이는 광학적 표면 영상으로부터 결 정 입자를 확인하고 결정하였다.10) 개선된 Ozawa 모델을 이용하여 활성화 에너지를 기울기의 평균 값으로부터 구 하였다. 결정화에 대한 활성화 에너지는 유리 입자크기 가 45 μm 이하에서는 2.28 eV, 75~106 μm는 2.21 eV, 125 ~150 μm는 2.19 eV이다. 활성화 에너지는 입자크기가 작 을수록 크게 나타남을 알 수 있다. 이 결과는 유리 내 부의 결정 핵 생성 및 성장으로 인한 입계 면의 표면 변형 효과 때문으로 설명할 수 있다.20,21) 즉, DSC로부 터 주어진 열 에너지는 유리 내부의 결정화에 일부 이 용되고 유리 입자 경계 면의 표면 변형으로 소모되었을 것으로 판단된다. 그러므로 작은 크기의 유리가 큰 크 기의 유리보다 상대적으로 더 많은 표면 입계 에너지를 가지며, 상대적으로 큰 크기의 유리에 비해서 결정화에 더 많은 에너지를 필요로 함을 알 수 있다.
Fig. 5는 LSO 유리의 결정화 부피 비와 승온율에 대 한 그림이다. 개선된 Ozawa 모델을 이용하여 기울기 값 으로부터 핵 생성 및 성장과 관련한 Avrami 지수 n 값 을 구하였다. 유리 입자크기에 따라 45 μm 이하에서는 n = 1.32, 75~106 μm는 n = 1.29, 125~150 μm는 n = 1.26 이다. 유리 입자의 크기에 무관하게 n은 약 1.3의 값으 로 유사하다. 이는 n = 1.3은 Avrami 지수 값에 의해 감 소하는 핵 생성을 가진 확산제어 방식의 결정성장을 나 타낸다. 초기에 핵 생성이 급격하게 이루어지며, 차츰 핵 생성이 감소하게 된다. 이는 등온 실험에 의한 결과(Fig. 6)로부터 확인되었다. 이에 따라 결정화 메커니즘이 초 기 핵 생성이 다량으로 급속하게 형성되고, 이후 핵 성 장보다 핵 생성에 더 민감한 확산제어 방식을 따름을 알 수 있다. 이로부터 LSO 유리가 입자의 크기에 따른 결 정화 과정에서, 활성화 에너지 값과 결정화 메커니즘의 지수를 결정하였다. 비등온법에 의한 Avrami 지수는 열 변화에 따른 영향 때문에 n 값의 변화가 등온법에 비해 더 클 것으로 추정된다. 따라서 등온법에 의한 실험과 비 교할 필요가 있다. Kissinger, Ozawa 등이 발표한 비등 온법14)은 Johnson, Mehl, Avrami가 발표한 등온법15,16,18) 에 비해 실험적 접근성이 좋으나, 온도변화에 따른 제 약조건이 있어 상대적으로 오차가 발생할 수 있는 단점 이 있다. 따라서 본 연구에서는 이러한 차이에 대한 규 명을 위하여 등온법의 실험도 실시하여 그 결과를 비교 하였다.
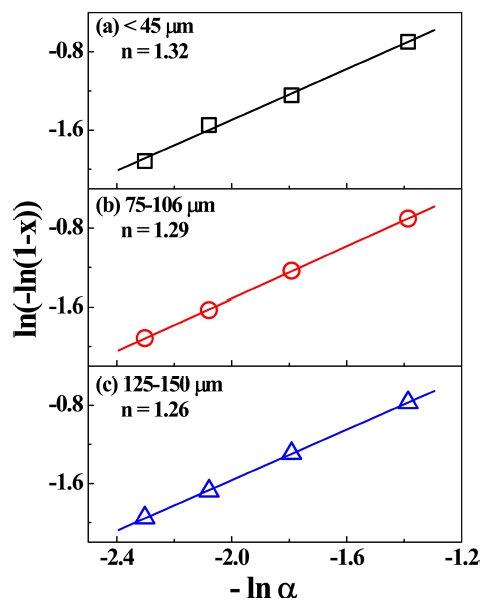
Fig. 5.
Modified Ozawa plot for the Li2O-2SiO2 glass to obtain the crystallization parameters n = 1.32, 1.29 and 1.26 for (a) under 45 μm, (b) 75~106 μm and (c) 125~150 μm glass particles, respectively. The symbols are measured data and the lines are for the eyes from the linear fit. Slopes are the parameters concerned crystallization mechanism.
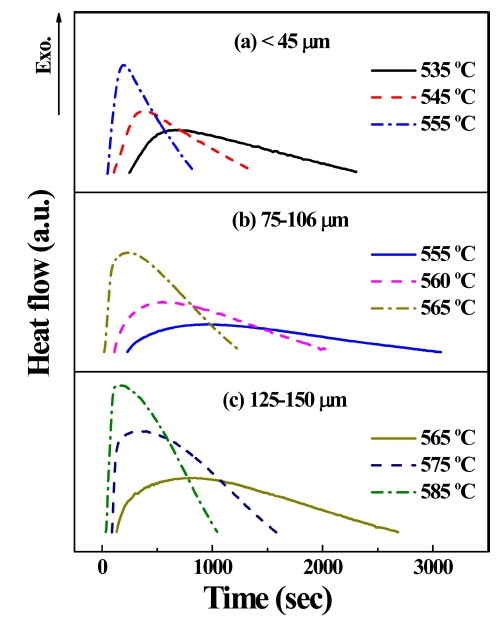
Fig. 6.
Isothermal DSC curves as a function of time, for the glass particles sized (a) under 45 μm at 535, 545 and 555 °C, (b) 75~106 μm at 555, 560 and 565 °C and (c) 125~150 μm at 565, 575 and 585 °C.
Fig. 6은 등온법을 이용한 LSO 유리의 시간에 따른 DSC 곡선이다. 등온법은 비등온법에 비해 정확한 결정 화 메커니즘을 알 수 있으나 실험시간이 길고, 등온과 정을 유지하기 쉽지 않은 단점이 있다. 본 연구에서는 등온법을 이용할 수 있는 최적의 조건을 찾아 측정할 수 있었고, 이를 비등온법으로 구한 결과와 비교할 수 있 었다. 등온법에서는 다음의 Johnson-Mehl-Avrami(JMA) 모델을 사용하여 Avrami 지수를 구하였다.
위 식에서 x(t)는 시간 t까지 결정상으로 전이된 체적 비이고, k는 결정화율 상수이다. n은 Avrami 지수이다. Fig. 6에서 (a) 유리 입자크기가 45 μm 이하인 경우로써 측정온도는 535 °C, 545 °C, 555 °C, (b)는 75~106 μm인 경우로 측정온도는 555 °C, 560 °C, 565 °C, (c)는 125~ 150 μm인 경우로 측정온도는 565 °C, 575 °C, 585 °C이 다. 등온 측정에는 동일한 질량(10 mg)의 Li2O-2SiO2 유 리 시료를 사용하여 비교 분석하였다.
Table 1은 등온 온도에 따른 결정화가 최대로 일어나 는 시간을 입자크기에 따라 분류하여 나타낸 것이다. Table 1에서 보면, 555 °C 등온 실험에서 입자크기 45 μm 이하와 75~106 μm의 결정화율이 최대일 때의 시간 이 각각 195초와 850초로 나타났다. 이로부터 입자크기 가 클수록 결정화로 진행되는 시간이 길게 나타남을 확 인할 수 있다. 이 같은 현상은 같은 온도에서 상대적으 로 작은 입자가 결정화와 관련된 열 에너지에 더 민감 하기 때문으로 판단되며, 입자크기 75~106 μm와 125~150 μm의 동일 온도 565 °C에서도 같은 경향이 나타남을 볼 수 있다. 작은 LSO 유리 입자는 상대적으로 큰 유리 입 자에 비해 DSC에서 주어진 열에 민감하기 때문에, 열 처리 시 열전도도의 분포가 표면에서부터 입자 내부까 지 유사하여 온도 구배(gradient)가 크지 않다. 작은 입 자에 비해 상대적으로 큰 입자는 온도 구배가 확연하게 나타나게 된다. 따라서 같은 온도에서 열처리 시 큰 입 자에 비해 작은 입자가 더 빨리 결정화되는 것으로 해 석할 수 있다.22,23)
Table 1.
The time required for a peak crystallization rate is for the glass particle with different sized for isothermal process.
| Isotherm temperature | |||||||
|---|---|---|---|---|---|---|---|
| Particle size ↓ | 535 °C | 545 °C | 555 °C | 560 °C | 565 °C | 575 °C | 585 °C |
| < 45 μm (sec) | 660 | 375 | 195 | ||||
| 75~106 μm (sec) | 850 | 520 | 227 | ||||
| 125~150 μm (sec) | 745 | 320 | 150 | ||||
JMA식을 이용하여 시간에 의존하는 결정화 부피 비 를 Fig. 7에 나타내었다. Fig. 7에서 기울기로부터 Avrami 지수(n)를 구하였다. 입자크기가 45 μm이하, 75~106 μm, 125~150 μm에 대한 n 값은 각각 1.7, 1.5, 1.4이다. n의 평균은 1.5로 LSO의 성장 메커니즘은 감소하는 핵 생 성률을 가진 확산 제어임을 확인할 수 있다. 비등온에 서의 n 값인 1.3과는 차이가 있으나 결정성장 메커니즘 은 동일하게 나타났으며, 이러한 값의 차이는 측정 방 식에 따른 오차의 범위로 볼 수 있다.
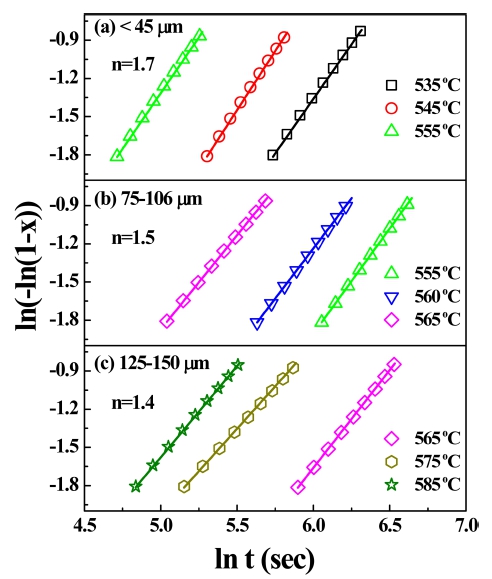
Fig. 7.
Transformed crystalline volume fraction at the given temperature is plotted as a function of time. For the glass particles sized (a) under 45 μm, (b) 75~106 μm and (c) 125~150 μm glass particles. The slopes are the parameters concerned crystallization mechanism.
Fig. 8은 다음의 Arrhenius 식(3)으로부터 구한 활성화 에너지이며, 결정 부피 비가 30 %에 도달하였을 때의 값 을 이용하여 계산한 결과이다.
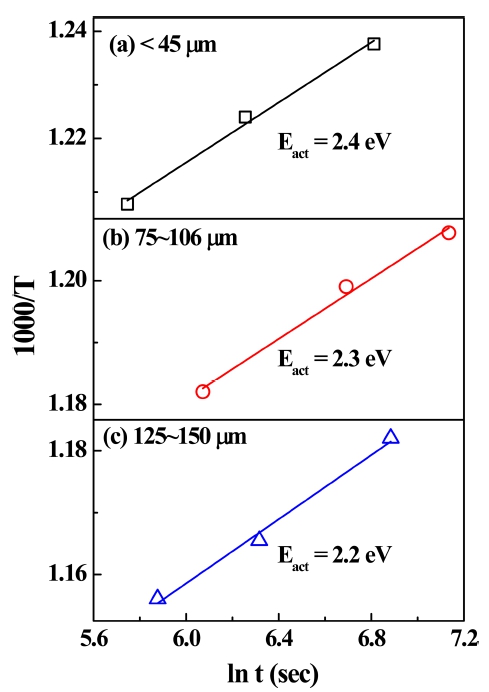
Fig. 8.
The time to require the transformed crystalline volume fraction to be 30 % is plotted for each experimental temperature. For the glass particles sized (a) under 45 μm, (b) 75~106 μm and (c) 125~150 μm glass particles. The slopes are the activation energies.
여기서 t는 주어진 온도 T에서 결정화 부피비가 30 % 가 될 때까지의 시간이며, to는 초기 지수인자이고, E는 활성화 에너지, k는 볼쯔만 상수이다. 활성화 에너지는 45 μm 이하에서 2.4 eV, 75~106 μm에서 2.3 eV, 125~150 μm에서 2.2 eV이고 이는 비등온법으로 얻은 활성화 에 너지 값과 유사함을 알 수 있다. 이 결과로부터 입자크 기가 작을수록 결정으로 상전이 될 때 더 많은 에너지 를 필요로 함을 재확인할 수 있다. 작은 크기의 유리 입 자가 큰 입자에 비해 빠른 시간 내에 결정화가 일어나 고, 열에너지를 흡수하는 것에 더 민감하며, 입계면의 변 형율 차이로 인하여 더 큰 활성화 에너지를 가짐을 확 인할 수 있다.
4. 결 론
Li2O-2SiO2 유리의 결정화 과정을 연구하였다. Li2O- 2SiO2 유리 시료를 급냉법으로 제조하고 유리 입자의 크 기에 따른 열 특성을 등온 및 비등온 실험으로 비교 분 석 하였다. 제조된 비정질 상과 상전이에 따른 결정상을 XRD 측정을 통하여 확인하였으며, Li2O-2SiO2 유리는 사방정계 구조를 가진 Li2Si2O5 단일 결정상으로 상전이 함을 알 수 있었다. 유리 입자크기에 따른 비등온과 등 온 실험 결과로부터 활성화 에너지와 Avrami 지수 값 을 구하였다. 결정화와 관련한 활성화 에너지는 유리 입 자크기가 작을수록 크게 나타났으며, 이는 큰 입자에 비 해 빠른 시간에 결정화가 일어나고, 열에너지를 흡수하 는 것에 더 민감하기 때문이다. Avrami 지수(n)는 모든 입자크기에서 약 1.5이며, 이것으로부터 Li2O-2SiO2 유 리의 결정화 메커니즘은 감소하는 핵 생성률을 가진 확 산 제어 성장임을 알 수 있었다. 따라서 Li2O-2SiO2 유 리의 결정화는 핵 성장보다는 핵 생성에 더욱 민감하다 는 것을 밝힐 수 있었다.




