1. 서 론
EDLC(electric double-layer capacitor)는 이차전지보다 빠른 충·방전 속도, 높은 출력 밀도, 긴 수명 사이클 을 가지고 있어 에너지 저장장치 시스템(ESS)이나 하이 브리드 자동차(HEV)의 보조동력으로 많이 쓰이고 있다. 하지만 이차전지에 비해 낮은 에너지 밀도를 가지고 있 어 이를 높이기 위한 연구가 진행되고 있다.1-4) EDLC의 에너지 밀도는 보통 단위 질량당 용량(F/g)으로 많이 표 현되는데, 만들어진 EDLC의 크기를 줄이기 위해서는 단 위 부피당 용량(F/cc)이 보다 의미가 있고, 이를 달성하 기 위해 전극의 밀도를 높이는 것이 중요하다.5-6)
일반적으로 EDLC의 전극재는 높은 비표면적을 가진 활성탄을 주로 사용한다. 활성탄을 만드는 방법은 물리 적 활성화와 화학적 활성화로 나뉘는데, 물리적 활성화 는 가격이 저렴하지만 용량이 낮다는 단점을 가지고 있 다. 반면, 화학적 활성화는 가격이 비싼 대신 용량이 높 은 장점이 있어 EDLC용 전극재로 많이 사용되고 있다. 활성탄을 만드는 화학적 활성화제로 KOH, NaOH, ZnCl2, H3PO4등의 약품들이 주로 사용되며, 특히 KOH는 가장 높은 비표면적을 얻을 수 있어 널리 사용되고 있다. 하 지만 KOH를 이용한 활성탄은 일반적으로 높은 비표면 적을 가지나, 전극의 밀도가 낮아 단위 부피당 용량(F/ cc)에 부정적인 영향을 끼친다.7-10) 또한, KOH, NaOH 및 H3PO4 같은 강염기나 강산의 화학적 활성화제는 장 치를 부식시켜 수명을 단축시키며 다루기 위험한 단점 이 있는 반면, K2CO3는 약염기 활성화제로 KOH와 같 은 강염기에 비해 위험하지 않고 저렴하며 장치의 부식 문제가 없어 이를 이용한 활성탄 제조가 주목을 받고 있 다.11-13) K2CO3를 이용한 활성탄은 상대적으로 낮은 비 표면적을 갖지만, 고밀도로 인해 상대적으로 높은 단위 부피당 용량(F/cc)을 가진 EDLC전극을 제조할 수 있다 고 보고되었다.14)
본 연구에서는 풍부하고 저렴하여 탄소재료의 전구체 로 많이 사용되고 있는 coal tar pitch(CTP)15-16)를 원료로 하여 높은 전극밀도를 갖는 EDLC를 제조하고자 K2CO3 에 의한 활성화를 진행하였다. K2CO3 처리된 CTP 활 성탄을 EDLC 전극재로 적용하여 전기화학적 특성을 조 사하였다. CTP와 K2CO3의 비율, 활성화 온도 및 활성 화 시간을 변화시켜 구조적 특성과 전기화학적 특성에 미치는 영향을 조사하였고, 유사한 조건에서 KOH 활성 화된 CTP 활성탄과 특성을 비교하였다.
2. 실험 방법
2.1. 활성탄 제조
연화점이 292 °C 인 CTP(OCI Co., Ltd)를 튜브형 전 기로 안의 공기 분위기에서 300 °C에서 2시간 동안 안 정화를 시킨 후, K2CO3분말과 1:1~1:6의 질량 비율로 혼 합하고, 튜브형 전기로 안의 질소 분위기에서 800~1000 °C의 온도범위로 1~7시간 동안 활성화시켰다. 승온속도는 5 °C/min으로 설정하고 활성화 과정이 끝난 후, K2CO3성 분이 완전히 제거될 수 있도록 증류수로 3차례 세척하 여 여과시키고 120 °C 오븐에서 건조시켰다.
2.2. 비표면적과 기공 특성
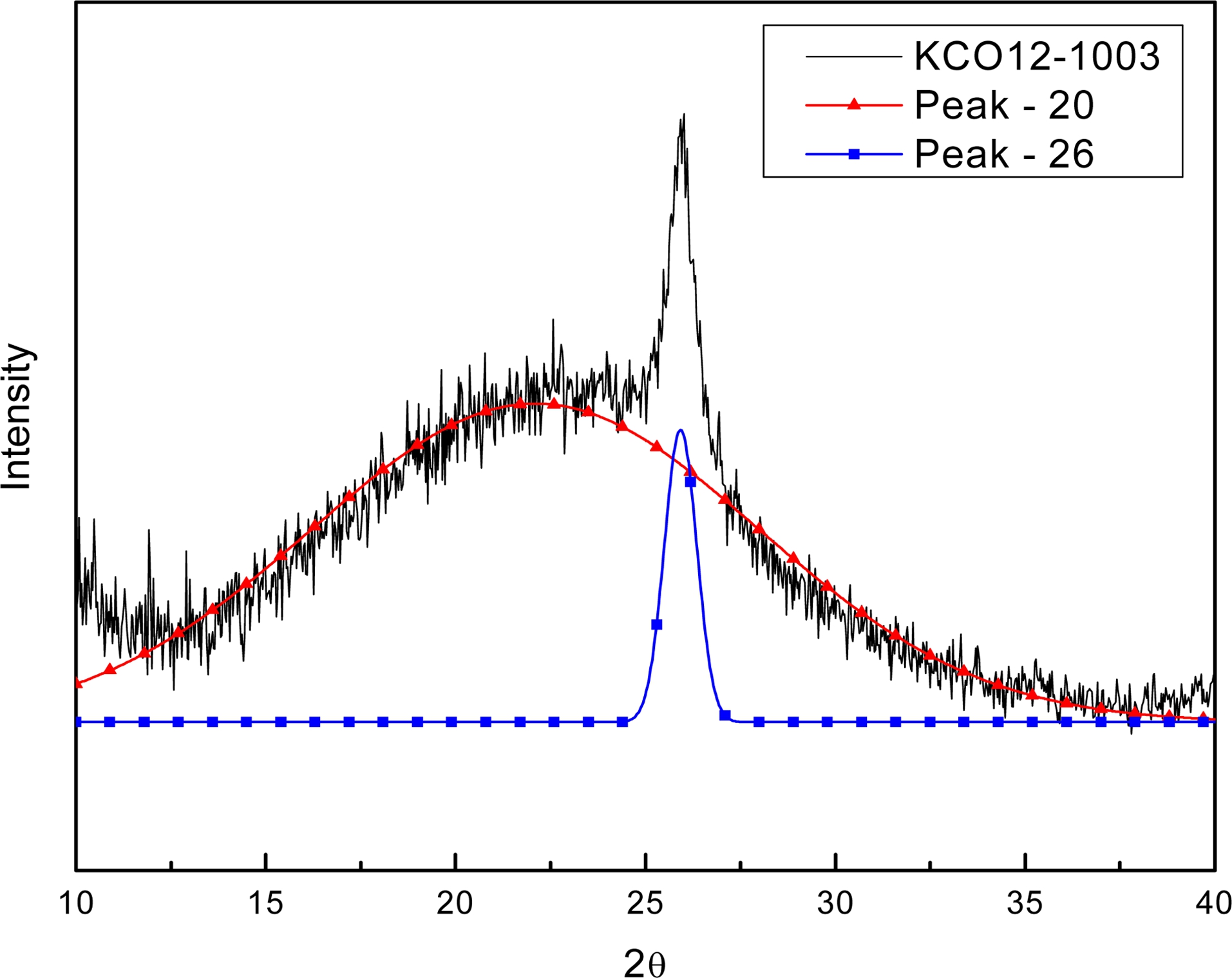
활성탄의 비표면적과 기공특성을 관찰하기 위해 300 °C 에서 12시간 동안 진공 상태에서 전처리 과정을 거친 후, 질소 흡·탈착 실험(Micrometrics, ASAP-2020)을 수 행하였고, Brunauer-Emmett-Teller(BET) 방법을 통해 물 질의 비표면적을 계산하였다. 기공크기분포를 보기 위해 질소의 흡·탈착 등온선과 Barret-Joyner-Hallender(BJH) 및 MP-plot을 이용했다. XRD(Shimadzu, XRD-7000)는 Cu-Kα 방사선(λ = 1.54056 Å), 40 kV, 30 mA의 조건으 로 분석했다. XRD상의 피크에서 Origin Pro 8.5 프로그 램을 이용하여 Fig. 1에 나타낸 것처럼 베이스라인을 제 거하고 평편하게 만든 후, 2θ = 20°와 26° 근처에서 두 개의 Gaussian 피크로 분리(deconvolution) 하여 분석하였 다.17) 종방향 결정크기, Lc는 2θ 값이 26°일 때의 (002) 피크를, 횡방향 결정크기, La는 43.5°에서의 (100) 피크 를 사용하여 다음의 Scherrer 식17,18)에 의해 계산하였다.
여기서 λ는 X-ray 파장이고, Ba와 Bc는 (100)과 (002) 피크의 50 % 높이에서의 폭을 나타내며, φa와 φc는 (100) 과 (002) 피크의 2θ 값을 나타낸다. 한편, 시료의 결정성 의 차이에 따른 표면 비저항값을 측정하기 위해 four-pointprobe( CMT-1000N, Chang Min Tech.)를 사용하였다.
2.3. 전극 제조 및 코인형 전지 조립
제조된 활성탄과 바인더로 PVDF(poly vinylidene fluoride, Sigma-Aldrich) 그리고 도전재로 카본블랙(Super-P)을 각 각 8:1:1 질량 비율로 혼합했다. 용매로는 NMP(1-methyl- 2-pyrrolidone, 99.5 %, Sam Chun Pure Chem. Co., Ltd) 를 사용했다. 혼합 된 슬러리를 에칭 된 알루미늄 호일 에 닥터블레이드 법으로 코팅하고, 70 °C 오븐에서 24시간 건조시켰다. 그리고 80 °C의 롤 프레스를 이용해 압착 시 킨 후, 70 °C의 진공오븐에서 24시간 동안 건조시켜 전 극으로 사용했다.
건조된 전극물질을 알맞은 크기로 펀칭한 후 무게와 두 께를 잰 후 질소 기체가 충전된 글러브 박스 안에서 전 해액이 들어있는 유리 바이알에 넣고 전해액이 전극물질 에 충분히 스며들 수 있도록 24시간 동안 담가두었다. 그 리고 코인 셀 케이스와 캡 사이에 분리막, 가스켓, 전 극물질, 스프링 및 디스크를 차례로 올려놓고 전해액을 충분히 가한 후 압착하여 조립했다. 분리막은 PP(poly propylene), 전해액은 1 M의 TEABF4염이 녹아있는 AN (acetonitrile) 용액을 사용하였다.
2.4. 전기화학적 특성 평가
전극재의 충·방전에 따른 전기화학적 반응특성을 CV (cyclic voltammetry, Potentiostat/Galvanostat Model 273 A)에 의해 순환전압전류법으로 측정하였다. 조립한 코인 형 전지의 한쪽에는 working 전극을, 다른 한쪽에는 reference 전극과 counter 전극을 연결하였다. 안정화를 위 해 scan rate를 100 mV/s로 하여 충·방전을 0~2.7 V범 위까지 10회 반복한 뒤에 측정을 시작했다. 충·방전 특 성실험은 안정화 된 코인형 전지를 10 mV/s의 scan rate 로 측정했다. 단위 질량당 용량(C, F/g)은 다음과 같은 식을 사용했고, 단위 부피당 용량(F/cc)은 다음의 식으로 구한 단위 질량당 용량에 전극의 밀도를 곱해주어 계산 하였다.
여기서 v는 scan rate(10 mV/s)를 의미하고, m은 전극 물질의 질량, ΔV는 측정 전압 범위(0~2.7 V)를 적용하였다.
3. 결과 및 고찰
3.1. CTP활성탄의 물리적 특성 및 정전용량
공기 분위기에서 300 °C의 온도로 2시간 동안 안정화 를 거친 CTP를 원료로 K2CO3의 혼합비를 1:1~1:6으로 바꿔가며 900 °C의 온도로 3시간 동안 활성화를 진행한 샘 플을 K2CO3의 혼합비에 따라 각각 KCO11-903, KCO12- 903, KCO14-903 및 KCO16-903라고 명명하였다. 또한, 혼합비를 1:2로, 활성화 온도를 900 °C로 고정하고 활성 화 시간을 1~7시간으로 바꾸어 본 샘플을 각각 KCO12- 901, KCO12-903, KCO12-905 및 KCO12-907로 명명 하였다. 마찬가지로, 혼합비를 1:2로, 활성화 시간을 3시 간으로 고정한 후, 800~1000 °C까지 활성화 온도를 바꾸 어 본 샘플을 각각 KCO12-803, KCO12-903, KCO12- 953 및 KCO12-1003으로 명명하였다. 이러한 활성탄들 의 물리적 특성과 정전용량을 Table 1에 나타내었다. 비 교를 위해 같은 조건의 CTP를 KOH와 1:4의 비율로 혼 합한 후, 900 °C의 온도로 3시간 동안 활성화 시킨 시 료(KOH14-903)를 포함시켰다.19,20)
Table 1.
Properties of CTP activated carbons with different activation conditions.
| Sample | aSSA (m2/g) | bVmicro (cm3/g) | cVmeso (cm3/g) | ddave (nm) | Density (g/cc) | Capacitance (F/g) | Capacitance (F/cc) | µF/cm2 |
|---|---|---|---|---|---|---|---|---|
| KCO11-903 | 648 | 0.27 | 0.03 | 1.69 | 1.02 | 12.6 | 12.9 | 1.94 |
| KCO12-903 | 1267 | 0.54 | 0.09 | 1.80 | 0.93 | 14.5 | 13.5 | 1.14 |
| KCO14-903 | 1040 | 0.43 | 0.07 | 1.79 | 1.12 | 8.9 | 10.0 | 0.86 |
| KCO16-903 | 998 | 0.41 | 0.06 | 1.76 | 1.15 | 7.9 | 9.1 | 0.79 |
| KCO12-901 | 1054 | 0.47 | 0.09 | 1.85 | 1.08 | 11.6 | 12.5 | 1.10 |
| KCO12-903 | 1267 | 0.54 | 0.09 | 1.80 | 0.93 | 14.5 | 13.5 | 1.14 |
| KCO12-905 | 1313 | 0.58 | 0.12 | 1.85 | 0.91 | 15.7 | 14.3 | 1.20 |
| KCO12-907 | 1485 | 0.67 | 0.16 | 1.92 | 0.90 | 18.1 | 16.3 | 1.22 |
| KCO12-803 | 66 | 0.03 | 0.16 | 2.10 | 1.51 | 6.2 | 7.1 | 9.39 |
| KCO12-903 | 1267 | 0.54 | 0.09 | 1.80 | 0.93 | 14.5 | 13.5 | 1.14 |
| KCO12-953 | 1431 | 0.64 | 0.16 | 1.93 | 0.93 | 17.4 | 16.2 | 1.22 |
| KCO12-1003 | 1489 | 0.65 | 0.21 | 2.01 | 0.80 | 21.8 | 17.4 | 1.46 |
| KOH14-903 | 3004 | 1.55 | 0.83 | 2.36 | 0.63 | 30.4 | 19.1 | 1.01 |
| MSP-20 | 2277 | 0.85 | 0.11 | 1.76 | 0.74 | 25.0 | 18.5 | 1.10 |
K2CO3의 혼합비를 변화시켰을 때, 1:2의 비율로 혼합 한 샘플이 1267 m2/g으로 가장 높은 비표면적과 기공부 피 및 14.5 F/g의 가장 높은 정전용량을 나타냈고, K2CO3 혼합비가 1:2를 초과하면 비표면적과 정전용량이 떨어지 는 현상을 확인할 수 있었다. 이러한 현상은 다른 연구 자들도 발견하였는데,21) K2CO3 혼합비가 1:2이하에서는 K2CO3 함량이 증가할수록 CTP와 약품 사이에 아래의 화 학반응을 일으킬 수 있는 접촉면적이 증가하고 반응 생 성물 및 휘발분이 방출되면서 형성된 기공 비표면적이 증가되는 반면, 혼합비가 1:2를 초과하면 과도하게 전구 체의 네트워크 구조를 무너뜨리고 수축하게 되어 비표 면적과 기공부피가 줄어드는 것이라고 설명하였다.
활성화 시간 및 온도에 따른 물리적 특성과 정전용량 도 Table 1에 나타내었다. 활성화 시간이 증가할수록 비 표면적 및 기공부피 등이 증가하였고, 정전용량도 증가 함을 확인할 수 있었다. 활성화 시간이 2시간 증가할 때 마다 100~200 m2/g 정도의 비표면적이 증가하였다. 활성 화 시간이 증가하면서 위의 화학반응에 의해 다량의 미 세기공을 형성하고, 일부 미세기공은 확장되어 중기공을 형성하면서 미세기공과 중기공 및 평균기공크기가 모두 증가하는 경향을 보였다. 밀도는 활성화 시간이 증가할 수록 약간 감소하였지만, 질량당 용량의 증가 폭이 커 서 부피당 용량도 계속 증가하였다.
활성화 온도 역시 증가할수록 비표면적과 정전용량이 증가하였고, 800 °C의 온도에서는 비표면적과 기공부피가 아주 낮아 800 °C 이하의 온도에서는 활성화 반응이 미 미하게 진행되었음을 확인하였다. 900 °C부터 활성화 반 응이 활발히 진행되고, 반응온도가 950 및 1000 °C로 증 가함에 따라 증가된 반응속도로 인해 미세기공에서 중 기공으로 기공의 확대 및 새로운 미세기공의 형성이 평 형을 이루어 가며 미세기공 부피가 거의 일정한 값을 유 지하는 것을 알 수 있었다. 밀도는 활성화 온도가 증가 할수록 감소하였지만, 질량당 용량의 증가 폭이 더 커 서 부피당 용량이 계속 증가하여 1000 °C일 때, 최고 값 인 17.4 F/cc(질량당 용량은 21.8 F/g)을 나타냈다. 이러 한 KCO12-1003의 부피당 용량은 비표면적이 2 배 이상 되는 KOH 활성탄(KOH14-903)에 91 %에 달했고, 비표면 적이 1.5 배 수준인 ELDL 전극용 상용활성탄(MSP-20) 과 거의 유사한 값을 나타내었다.
활성화 조건에 따른 기공의 특성을 심층적으로 분석하 기 위해 Fig. 2 및 3에 등온흡착곡선과 기공크기분포를 각각 나타내었다. 등온흡착곡선들을 살펴보면, KOH 활 성탄(KOH14-903)이 미세기공과 중기공이 고루 발달한 반 면 K2CO3 활성탄은 미세기공이 주로 발달하였고, 활성 화 시간과 온도가 증가함에 따라 중기공이 점차 증가하 는 것을 알 수 있었다. Fig. 3(a)에 보인 기공크기분포 에서도 KOH 활성화된 시료는 1 nm 근처에서 상당량의 미세기공과 2 nm 이상의 중기공이 고루 발달한 반면,19-20) K2CO3 활성화 시료는 약 0.6 nm 부근에서 미세기공이 주로 발달한 모습을 확인할 수 있었다.
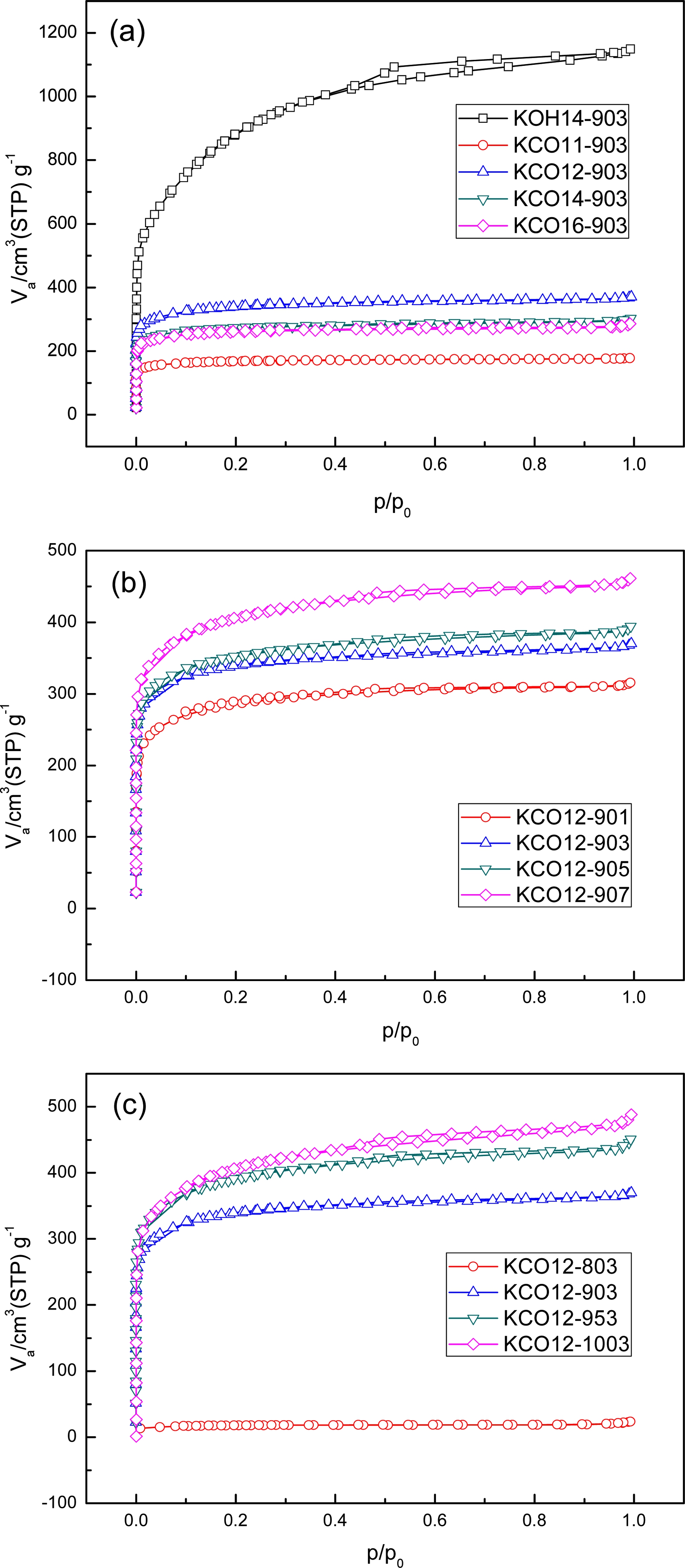
Fig. 2.
N2 adsorption-desorption isotherms of CTP activated carbons with different K2CO3 mixing ratios (a), activation times (b), and activation temperatures (c).
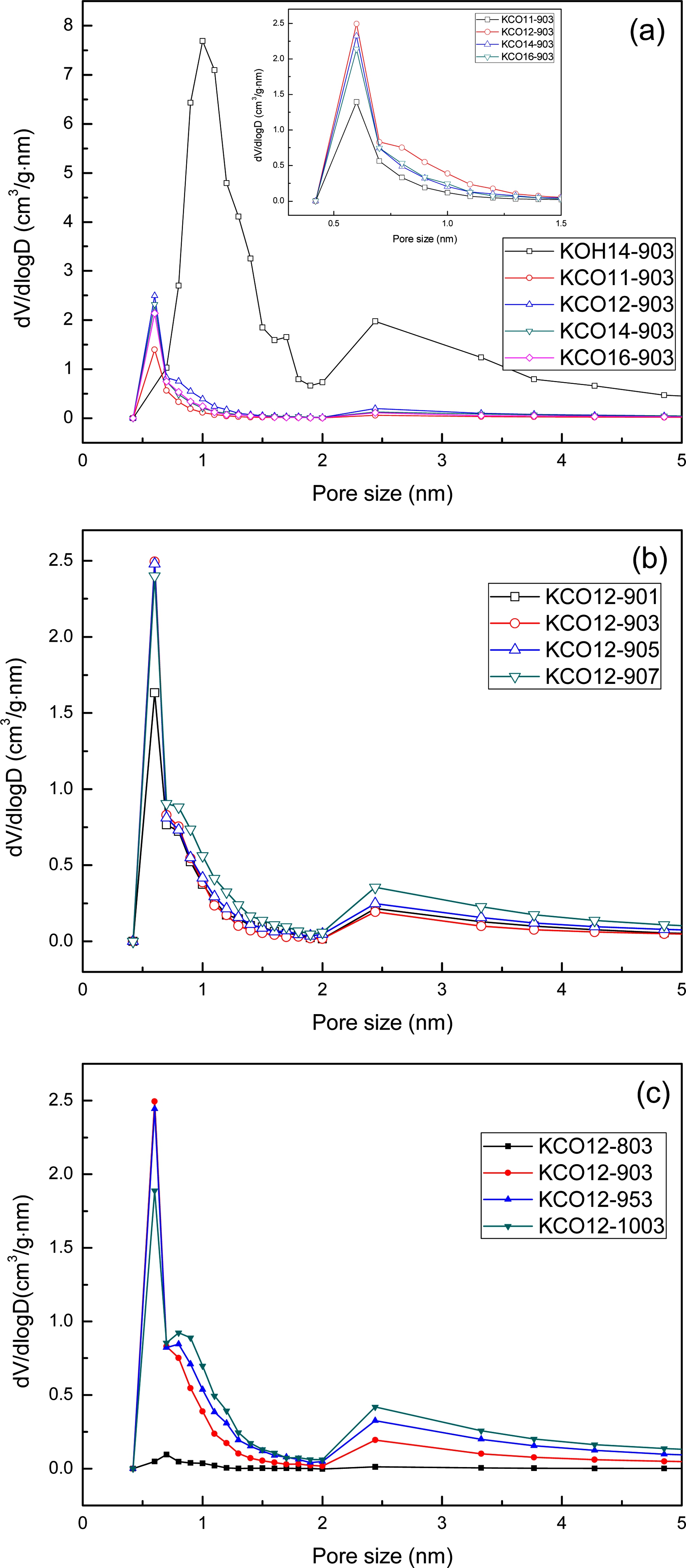
Fig. 3.
Pore size distribution of CTP activated carbons with different K2CO3 mixing ratios (a), activation times (b), and activation temperatures (c).
J. Hayashi 등22,23)은 폐 우레탄을 K2CO3를 이용해 활 성화를 했을 때, 0.6 nm 주변의 유사한 크기의 미세기 공이 잘 발달하고, 중기공은 약하게 형성함을 보고하였 다. KOH 활성화 과정에서는 KOH가 CTP 내부에 침투 하여 강력한 산화반응으로 인해 미세기공이 형성하고, 형 성된 미세기공의 중기공으로 확장이 왕성하게 발생하여 미 세기공 및 중기공의 부피가 K2CO3 활성화 보다 훨씬 크 며, 미세기공의 크기분포도 상대적으로 크게 얻어졌다. 한 편, K2CO3는 마일드한 활성화 과정에 의해 주로 미세 기공을 형성시키고, 중기공으로 확장은 미미하였던 것으 로 판단된다. 하지만 활성화 시간 및 온도가 증가함에 따라 2 nm 이상의 중기공의 생성이 증가된 것을 관찰할 수 있었고(Fig. 3(b, c)), 활성화 시간에 따른 변화가 활 성화 온도에 다른 변화보다 시료들간의 기공분포 차이 가 크지 않아, 활성화 온도가 활성화 시간보다 기공형 성에 미치는 영향이 상대적으로 큼을 알 수 있었다.
3.2. CTP활성탄의 결정성
여러 가지 조건에서 제조된 활성탄들의 X-선 회절 (XRD) 분석 결과 그래프를 Fig. 4에 나타냈다. KOH 활 성탄(KOH14-903)은 26° 부근에서 (002) 피크가 완전히 사라진 것과 대비하여 K2CO3 혼합비를 변화시킨 시료 들에서(Fig. 4(a)), (002) 피크가 존재함을 확인하였다. 원 료 CTP에 비하여 (002) 피크의 강도는 매우 약해진 것 은 활성화 과정에서 K2CO3과 반응으로 미세기공이 형 성됨에 의해 탄소 결정구조가 많이 파괴되었기 때문으 로 판단된다. K2CO3 혼합비 1:2의 경우(KCO12-903)가 가장 피크 강도가 낮아 활성화가 적절한 것을 확인하였 다. 나머지 1:1, 1:4 및 1:6의 비율로 섞은 시료들은 피 크 강도가 상대적으로 유지되고 있었다. 활성화 시간은 길어질수록 증가된 K2CO3 산화반응으로 인해 결정성이 사라지며, 피크 강도가 점점 약해지는 것을 확인하였다 (Fig. 4(b)). 활성화 온도는 높아질수록 둥글고 넓게 형 성된 피크 강도는 줄었고, 대신 950 °C 이상의 높은 온 도에서는 26° 부근에서 날카로운 피크가 생성하는 것을 관찰할 수 있었다(Fig. 4(c)). 높은 온도의 활성화 공정 에서 K2CO3의 마일드한 활성화과정에 의해 비정질 탄 소는 상당 부분 제거되지만, 상대적으로 결정질의 탄소 는 산화되지 않고 오히려 높은 열처리온도로 인하여 결 정성이 증가되어 26.5°에서 날카로운 피크가 형성되는 것 으로 추론할 수 있었다. 이러한 마일드한 활성화 과정 은 미세기공을 주로 형성시키며, 26.5°에서 형성된 날카 로운 피크에 의한 결정성의 증가는 950 °C 이상에서 활 성화된 전극의 전기전도성 증가에 기여할 것으로 예상 된다. Table 3에 four-point-probe 방법으로 나타낸 전극 물질의 비저항 값을 비교해보면, 예상한 바와 같이 활 성화 온도가 증가할수록 감소하였다.
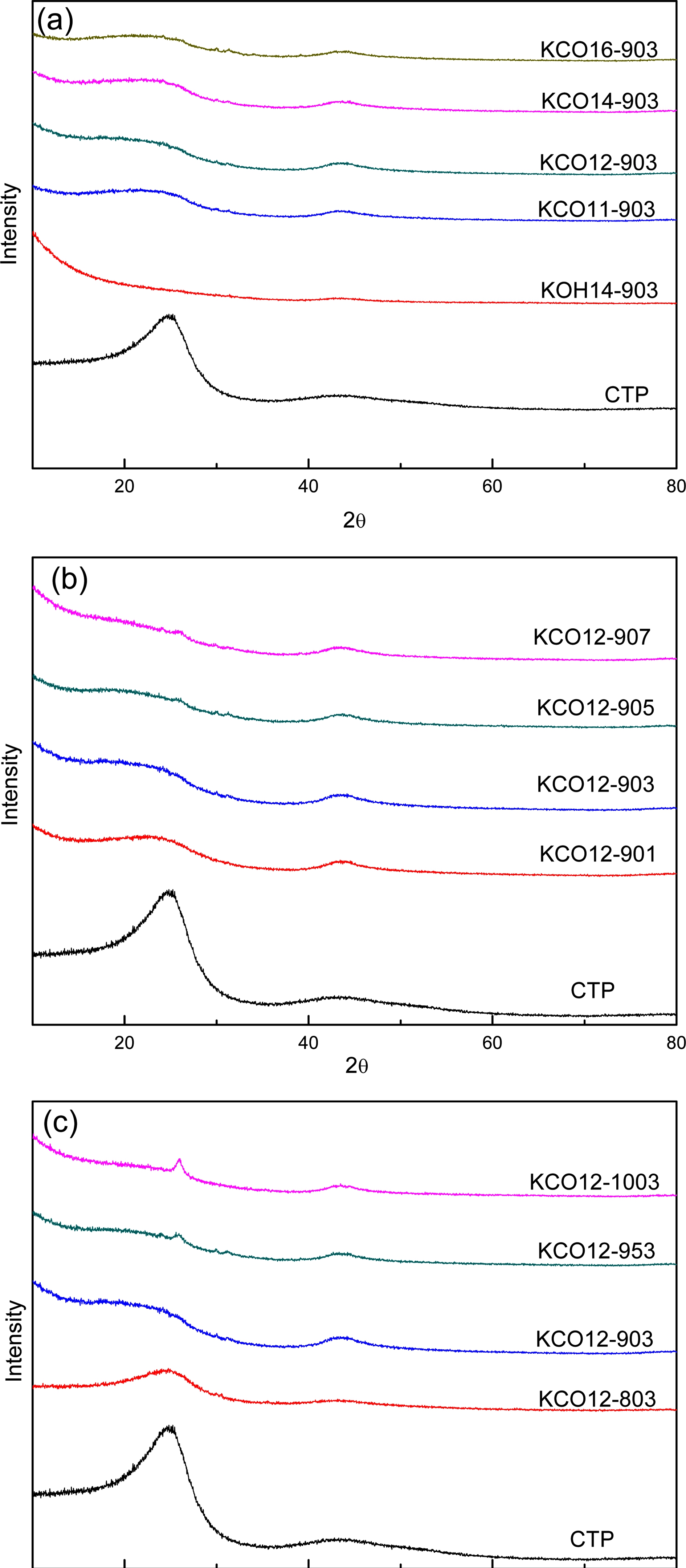
Fig. 4.
XRD patterns of CTP activated carbons with different K2CO3 mixing ratios (a), activation times (b), and activation temperatures (c).
Table 3.
Specific resistivity of CTP activated carbons with different activation temperatures.
| Sample | Specific resistance (Ω•cm) |
|---|---|
| KCO11-903 | 3.4 ± 0.2 |
| KCO12-953 | 2.8 ± 1.0 |
| KCO12-1003 | 2.6 ± 0.7 |
활성탄과 같은 난층구조(turbostratic structure) 탄소시 료에서 횡방향 및 종방향 결정의 크기, La와 Lc를 계산 하기 위해 둥글게 형성된 (002) 피크는 2θ = 20°(γ-band) 와 26°(Π-band) 근처에서 두 개의 Gaussian 피크로 deconvolution 하여 분석하였다. 이론적으로 γ-band와 Π- band 피크 아래의 면적은 aliphatic chain 및 aromatic ring에 포함된 탄소 원자수에 대응된다.17,18) Lc는 Π-band 피크를 적용하고, La는 (100) 피크를 Scherrer 식에 적 용하여 얻어진 결정의 크기를 Table 2에 나타내었다. 활 성화제의 비율이 늘어남에 따라 La는 거의 비슷하지만 소폭 증가하는 추세를 보였고, Lc는 감소하는 추세를 보 였다. 난층구조의 탄소시료에서 K2CO3 첨가량의 증가로 화학반응을 일으킬 수 있는 접촉면적이 증가할 때, 흑 연 결정의 활성점이 많은 엣지(edge)에서 선택적으로 산 화반응을 일으켜 구조가 붕괴되어 종방향 결정의 크기 (Lc)는 감소하였고, 활성점이 거의 없는 기저면(basal plane) 에서는 산화반응이 거의 일어나지 않아 횡방향 결정의 크기(La)는 변화가 적었던 것으로 판단된다.
Table 2.
La and Lc of CTP activated carbons by K2CO3.
La는 활성화 시간과 온도가 증가함에 따라 대체적으로 증가하는 경향을 보였으며, 활성화 온도를 변화시켰을 때 증가하는 폭이 더 컸다. 한편, Lc는 활성화 시간이 증 가함에 따라 대체적으로 감소하는 경향을 보였지만, 활 성화 온도가 950 °C 이상일 때는 2θ가 26.5°일 때 날카 로운 피크가 생성됨에 따라 큰 폭으로 상승하는 것을 확 인할 수 있었다. 활성화 시간과 온도가 증가함에 따라 La가 증가한 것은 활성점이 거의 없는 basal plane에서 는 산화반응이 거의 없는 상황에서 열처리 효과에 의해 횡방향 결정 크기가 증가한 것으로 판단된다. 이러한 열 처리 효과는 처리 온도가 처리 시간에 비해 민감한 것 을 추론할 수 있다. 한편, 활성화 시간과 온도가 증가 함에 따라, 활성점이 많은 엣지에서는 산화반응에 의한 기공의 형성이 활발해져 구조의 붕괴가 심해서 일반적 으로는 종방향 결정의 크기는 감소하는 경향을 보이지 만, 상대적으로 결정질의 탄소는 마일드한 산화반응으로 제거되지 않고 950 °C 이상 열처리온도에서 오히려 결 정성이 증가되어 갑자기 Lc가 증가한 것으로 추론할 수 있다. 따라서 K2CO3 처리된 CTP 활성탄은 KOH 처리 된 CTP 활성탄이 (002) 피크가 완전히 사라져 비정질 을 나타낸 것에 비하여 상대적으로 결정성이 높았고, 활 성화 조건에 따라 난층구조의 미세결정 크기를 제어할 수 있음을 확인하였다.
3.3. CTP활성탄 전극의 전기화학적 특성
여러 가지 K2CO3 활성화 조건에서 만들어진 CTP 활 성탄들로 조립된 코인형 전지를 10 mV/s의 scan rate로 측정한 CV 결과를 Fig. 5에 나타내었다. K2CO3의 혼합 비를 변화시켰을 때(Fig. 5(a)), K2CO3 함량이 적었던 KCO11-903과 KCO12-903은 각각 12.6 F/g 및 14.5 F/g 으로 비교적 높은 용량을 구현했지만, 오히려 활성화제 가 많았던 KCO14-903과 KCO16-903는 과도한 네트워 크 구조 붕괴로 인해 낮아진 비표면적과 기공부피 때문 에 더 낮은 용량이 얻어진 것으로 판단된다. 전체적으 로 CV 그래프 형태가 럭비공 형태로 얻어져 이상적인 직사각형 형태에서 다소 벗어난 것을 볼 수 있었다. 이 러한 현상은 K2CO3 처리된 CTP 활성탄이 중기공의 발 달이 저조하여 전극의 기공 내부에서 전해질 이온들의 이동 저항이 상대적으로 크기 때문으로 판단된다. 따라서 활성화 시간 및 활성화 온도를 증가시킴에 따라(Fig. 5(b, c)), 형성된 중기공 부피가 증가되면서 CV 그래프 형태 가 럭비공에서 직사각형 형태로 개선되는 것을 확인할 수 있었고, 중기공이 가장 많이 발달한 1000 °C에서 활 성화한 시료(KCO12-1003)에서 가장 이상적인 CV 형태 를 나타냈다. 활성화 시간이 1시간에서 7시간으로 증가 할 때, 정전용량이 11.6~18.1 F/g범위에서 활성화 시간이 길어질수록 그래프의 면적이 커지며 정전용량이 증가하 였고, 활성화 온도가 800 °C에서 1000 °C로 증가할 때, 정전용량이 6.2~21.8 F/g범위에서 활성화 온도가 높아질 수록 그래프 면적이 점점 증가하여 정전용량이 증가하 는 경향을 보였다.
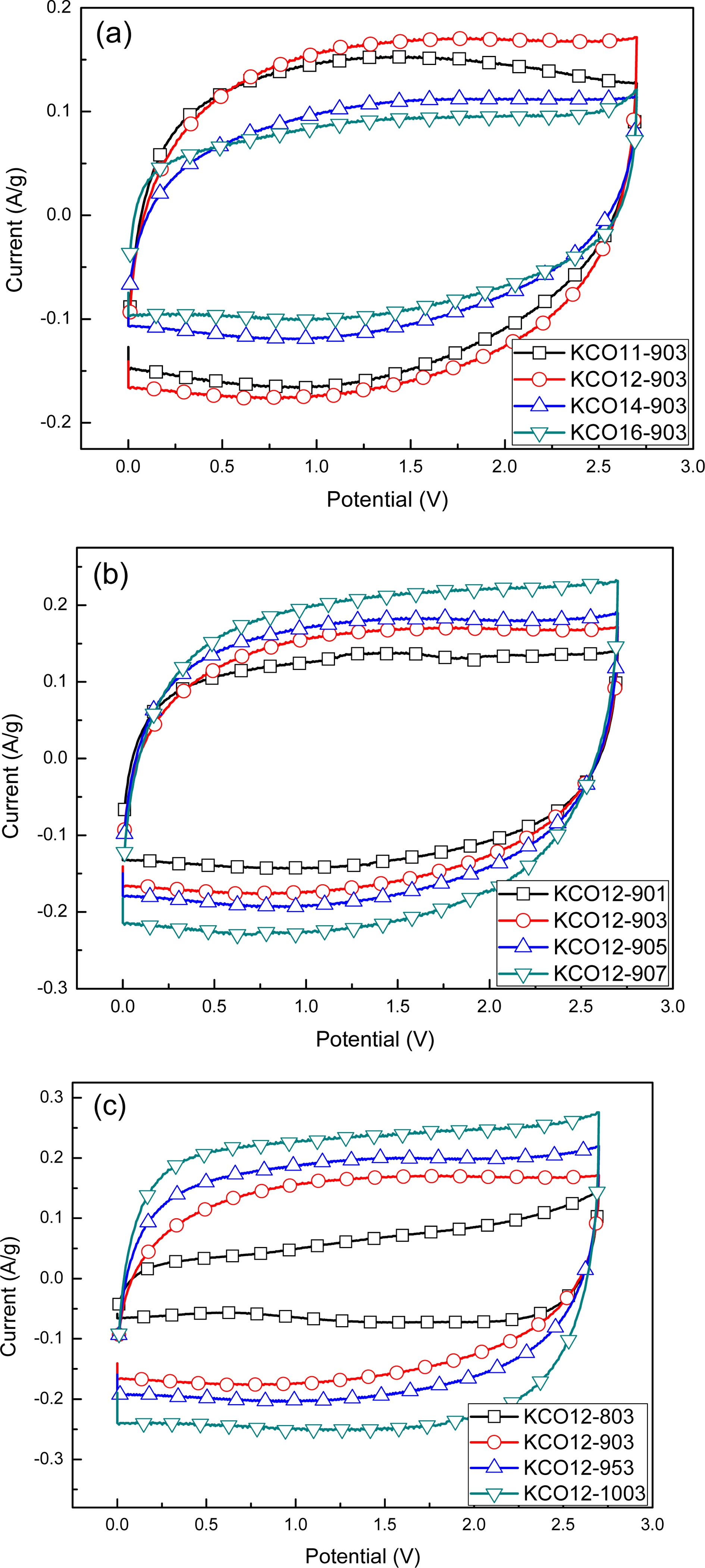
Fig. 5.
Cyclic voltammograms of CTP activated carbons with different K2CO3 mixing ratios (a), activation times (b), and activation temperatures (c).
한편, 800 °C에서 활성화한 시료(KCO12-803)가 매우 낮은 비표면적과 미미하게 형성된 기공부피로 인해 낮 은 정전용량을 나타내었다. 하지만 매우 낮고 미미한 세 공부피에 비해서는 정전용량이 비교적 높았고, CV 형태 는 직사각형에서 많이 벗어나는 특이한 형태를 나타내 었다. 이러한 전압이 증가할수록 전류 차가 커지면서 면 적이 증가하여 매우 낮은 비표면적임에도 비교적 높은 정전용량을 구현하는 현상은 전기화학적 활성화(electrochemical activation)가 발생할 때 관찰되는 것으로 보고 되었다.2,4,6,9,10,14,24-27) Table 1에서 KCO12-803 시료는 보 다 높은 활성화 온도의 시료들(KCO12-903, KCO12-953, KCO12-1003)에 비해 비표면적은 1/20 이하 이지만, 정 전 용량은 대략 1/3 수준으로 단위 비표면적당 용량(μF/ cm2)은 대략 7배 전후가 되어서 전기화학적 활성화가 발 생한 것을 추론할 수 있다. 전기화학적 활성화는 알카 리 처리된 소프트 카본계 비다공성 활물질이 EDLC 전 극 물질로 사용되었을 때, 시료에 따라 작동전압이 1~3 V 이상 도달하였을 때 발생하는 것으로 알려져 있다.6,25,26) 즉, EDLC 충전과정에서 전극 활물질이 높은 작동전압 에서 추가적으로 활성화되어 전해질 이온들의 저장 능 력이 증가되는 것이다. 높은 작동전압에서 전해질 이온 들이 미세기공에 틈새에 침투하여 미세한 흑연 결정의 graphene layer 층간에 전해질 이온들의 삽입/탈리(intercalation/ deinteracalation) 현상이 일어남에 의해 전기화학 적 활성화가 진행되며,4,27) 전압 인가 후 증가된 비표면 적, 기공크기 및 graphene layer 층간 거리는 전기화학 적 활성화 증거가 될 수 있다고 보고되었다.2,10,25,26)
4. 결 론
CTP를 원료로 K2CO3를 이용해 다양한 활성화 조건에 서 만든 활성탄으로 코인형 EDLC 전지를 제조하였다. 활성탄의 물리적 특성과 EDLC의 전기화학적 특성을 분 석하여 다음과 같은 결론을 얻었다. CTP/K2CO3의 비율 을 변화시켰을 때, 1:2의 비율에서 상대적으로 높은 비 표면적과 큰 정전용량을 나타내었고, XRD 분석에서도 1:2의 비율에서 (002) 피크가 완전히 사라져 활성화가 적 절히 진행 되었음을 확인할 수 있었다. 활성화 시간과 온도가 증가할수록 비표면적, 기공부피 및 그에 따른 정 전용량도 증가하였고, 이러한 증가는 활성화 시간보다 활 성화 온도에 민감하였다. KOH 활성화된 CTP는 1 nm 근처에서 상당량의 미세기공과 2 nm 이상의 중기공이 고 루 발달한 반면, K2CO3 활성화된 시료는 약 0.6 nm 부 근에서 미세기공이 주로 발달한 모습을 볼 수 있었다. 활성화 시간과 온도가 증가하면서 K2CO3의 산화반응에 의해 다량의 미세기공을 형성하고, 일부 미세기공은 확 장되어 중기공을 형성하면서 미세기공과 중기공 부피 및 평균기공크기가 모두 증가하는 경향을 나타냈다. 활성화 시간과 온도가 증가함에 따라 횡방향 결정 크기, La는 대체적으로 증가하는 경향을 보였지만, 종방향 결정 크 기, Lc는 활성화 시간이 증가함에 따라 대체적으로 감 소하는 경향을 보였고, 활성화 온도가 증가에도 감소하 는 경향을 보이다가 950 °C 이상일 때는 2θ가 26.5°일 때 날카로운 피크가 생성됨에 따라 큰 폭으로 상승하였다.
CTP/K2CO3 1:2비율로 1000 °C에서 3시간 활성화한 시 료(KCO12-1003)에서 비표면적과 기공부피 및 정전용량 (21.8 F/g, 17.4 F/cc)이 가장 높았고, 중기공이 가장 많이 발달함으로 인해 가장 이상적인 CV 형태를 보였다. KOH 활성탄 전극이 높은 단위 질량당 용량(F/g)으로 인 해 높은 단위 부피당 용량(F/cc)을 갖지만, K2CO3 활성 탄 전극은 상대적으로 낮은 단위 질량당 용량(F/g)에도 불구하고 높은 전극밀도로 인해 유사한 단위 부피당 용 량(F/cc)을 나타냈다. KCO12-1003시료는 상대적으로 높 은 밀도 및 결정성으로 인해 부피당 용량(F/cc)이 비표 면적이 2배 이상 되는 KOH 활성탄(KOH14-903)에 91 %에 달했고, 비표면적이 1.5배 수준인 ELDL 전극용 상 용활성탄(MSP-20)과 거의 유사한 값을 나타내었다. 한 편, 800 °C에서 활성화한 시료(KCO12-803)가 매우 낮은 비표면적과 미미하게 형성된 기공부피를 가짐에도 비교 적 높은 정전용량(비표면적당 용량은 7배 수준)을 구현 하여 전기화학적 활성화가 발생한 것으로 판단된다.