1. 서 론
희토류 이온이 활성제로 도핑된 형광체는 백색 발광 다 이오드(light emitting diode), 디스플레이 패널, 레이저 개발에 있어서 핵심적인 발광 요소로 응용되고 있다.1-3) 특히 희토류 Eu3+, Sm3+, Tb3+, Dy3+ 이온은 많은 가시 광 영역의 밴드갭 에너지를 갖고 있어서 램프와 발광 다 이오드용 형광체를 개발하는데 효율적인 활성제로 사용 되고 있다. 모체 CaNb2O6 결정은 화학적으로 안정하고 발 광 세기가 강하며 서로 다른 가시광 영역의 파장을 방 출하는 활성제 이온으로 에너지를 효율적으로 전달하기 때문에 Dy3+, Eu3+, Sm3+와 같은 다양한 활성제 이온이 치환 고용되기에 적합한 모체로 알려져 있다.4)
최근에 발광 효율을 향상시키고 다양한 색깔의 빛을 방 출시키기 위하여 두 종류의 발광 이온을 동시 도핑하여 형광체를 제조하는 연구에 많은 관심이 쏠리고 있다.5) 특 히, 백색 발광은 기본 삼색인 적색, 녹색, 청색 발광 세 기의 적절한 조합에 의하여 만들어지기 때문에 이에 적 합한 두 종류의 활성제 이온과 도핑 농도를 선택하는 것 은 중요하다. Natarajan 등6)은 고상반응법으로 Bi3+와 Sm3+ 이온이 동시 도핑된 YVO4 형광체를 합성하였으며, 여 기(excited) 파장에 따라 형광체의 방출 파장이 이동함을 보고하였다. 254, 365, 410 nm로 여기 하였을 때 형광 체는 각각 강한 주황색, 황색, 적색 발광을 나타내었다. Shen 등7)은 모체 Ba2MgSi2-xAlxO7 결정에 Eu2+와 Mn2+ 를 동시 도핑한 형광체를 제조하였으며, 350-450 nm의 파 장으로 여기 시켜 438, 501, 623 nm에 위치하는 삼색 발광 피크를 관측하였다. Al3+, Eu3+, Mn2+ 이온의 농도 가 각각 0.4, 0.1, 0.1 mol 일때 시료는 가장 강한 백색 광을 방출함을 제시하였으며, 모체 결정에 Al 이온을 도 핑함으로써 청색과 녹색 발광의 세기의 비를 변화시킬 수 있었다. Yang 등8)은 ZnS:Mn 형광체에 Ce 증감제 (sensitizer)를 동시 도핑함으로써 에너지 전달 원리에 의 하여 형광체의 발광 세기를 증가시켰으며, 900 °C에서 소 결시킨 형광체의 경우에 입방 정계와 육방 정계가 공존 함을 확인하였다. ZnS:Mn, Ce 형광체의 발광 피크는 도 핑 농도가 증가함에 따라 적색 이동하였고, 소결 온도가 증가함에 따라 청색 이동함을 보고하였다. Cao 등9)은 Sm3+와 Na+를 동시 도핑한 CaNb2O6 형광체를 제조하였 으며, 두 활성제 이온을 도핑함으로써 발광 특성이 향 상됨을 관측하였다.
본 연구에서는 높은 열 및 화학적 안정성을 갖는 CaNb2O6 모체 격자에 Dy3+ 이온을 도핑한 황색 형광체, Eu3+ 이온을 도핑한 적주황색 형광체, Dy3+와 Eu3+ 이온 을 동시 도핑한 백색광 형광체를 합성하였다. 특히 백 색광 형광체의 경우에는 Dy3+ 이온의 농도를 5 mol%로 고정하고 Eu3+ 이온의 농도를 순차적으로 변화시켜 방 출하는 발광 스펙트럼의 파장과 세기를 제어하였으며, CIE 1931 색 좌표를 측정하여 Eu3+ 이온의 농도 변화 에 따른 색 좌표의 이동 현상을 분석하였다. 결정 입자 의 크기와 발광 세기 사이의 상관 관계도 조사하였다.
2. 실험 방법
CaNb2O6:Dy3+, CaNb2O6:Eu3+, CaNb2O6:Dy3+, Eu3+ 형 광체 분말은 초기 물질 CaCO3(99.9 % 순도), Nb2O5 (99.9 %), Dy2O3(99.9 %), Eu2O3(99.9 %)를 화학양론적으 로 측정하여 합성하였다. 활성제 Dy3+와 Eu3+ 이온이 각 각 단일 도핑된 CaNb2O6 형광체의 경우에 Dy3+와 Eu3+ 이온의 몰 비는 각각 5 mol% 이었다. Dy3+와 Eu3+ 이온 을 동시 도핑한 경우에 Dy3+ 이온의 몰 비는 5 mol%로 고정하였고, Eu3+ 이온의 몰 비는 각각 1, 5, 10, 15 mol%로 변화시켰다. 정밀 저울을 사용하여 초기 물질을 측정하고 플라스틱 병에 ZrO2 볼과 적정 양의 에탄올을 넣고 10시간 동안 볼밀(ball-mill)과 80 °C에서 10시간 동 안 건조한 후에, 아게이트 막자 사발에서 건조시킨 시 료를 갈아서 80 μm의 체로 걸러내고 알루미나 도가니에 담아 전기로에 넣어 400 °C에서 3시간 동안 하소 공정 과 1100 °C에서 5시간 동안 소결하여 합성하였다.10)
형광체 분말의 결정 구조는 X-선 회절기(X-ray diffreactometer: XRD, Ultima IV, Rigaku)를 사용하여 측 정하였고, 흡광과 발광 특성은 상온에서 형광광도계(FS- 2, Scinco)를 사용하여 조사하였다. 표면의 미세 형상과 결 정 입자의 크기는 주사전자현미경(SEM, CX-200, Coxem) 으로 촬영하였다.
3. 결과 및 고찰
Fig. 1은 Dy3+와 Eu3+ 이온을 각각 5 mol% 단일 도핑 한 CaNb2O6 형광체와 Dy3+ 이온의 몰 비를 5 mol%로 고정하고, Eu3+ 이온의 몰 비를 1, 5, 10, 15 mol%로 변 화시켜 합성한 CaNb2O6:Dy3+, Eu3+ 형광체 분말을 XRD 를 사용하여 측정한 결과를 나타낸 것이다. Eu3+ 이온 의 몰 비에 관계없이 모든 형광체 분말의 주 회절 피 크는 29.22°에서 나타났다. 상기의 주 회절 피크 이외에 도 상대적으로 약한 회절 세기를 갖는 피크들이 11.88°, 23.64°, 50.60°, 60.58°에서 관측되었다. 주 회절 피크는 (131) 면에서 발생하였고, 약한 회절 피크의 세기는 (130), (262), (062), (020) 순으로 감소하였다. 이 결과를 통하 여 Dy3+와 Eu3+가 도핑된 CaNb2O6 형광체는 ICDD #00-039-1392와 일치하는 사방정계(orthorhombic system) 의 결정 구조임을 알 수 있었다. Eu3+ 이온의 몰 비가 1 mol% 일 때 주 회절 피크 (131) 면의 세기는 최대이 었으며, Scherrer의 식11)을 사용하여 계산한 결과 평균 결 정 입자의 크기는 50 nm이었다.
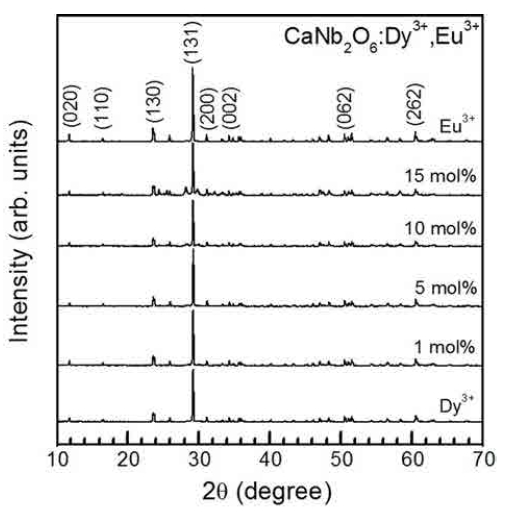
Fig. 1
XRD patterns of CaNb2O6 phosphors doped with Dy3+, Eu3+, and different concentrations of Eu3+ at a fixed Dy3+ of 5 mol%.
Fig. 2는 파장 267 nm와 263 nm로 각각 여기시켜 측 정한 CaNb2O6:Dy3+와 CaNb2O6:Eu3+ (삽입 그림) 형광체 의 발광(photoluminescence) 스펙트럼을 나타낸 것이다. Eu3+ 이온이 도핑되지 않은 CaNb2O6:5 mol% Dy3+ 형광 체 분말의 경우에 발광 세기가 약한 Dy3+ 이온의 4F9/2 → 6H15/2 전이에 의한 482 nm에 피크를 갖는 청색 발광 파장, 4F9/2→ 6H13/2 전이에 의한 575 nm의 황색 발광 파 장, 4F9/2→ 6H11/2 전이에 의한 664 nm의 적색 발광 파장 과 4F9/2→ 6H9/2 전이에 의한 753 nm의 적외선 발광 파장 이 관측되었다.12) 여기서 4F9/2→ 6H13/2 (575 nm) 전이는 ΔJ = 2의 선택 규칙(selection rule)을 만족하는 전기 쌍 극자 전이(electric dipole transition) 이고, 4F9/2→ 6H15/2 (482 nm) 전이는 ΔJ = 3을 충족하는 자기 쌍극자 전이 (magnetic dipole transition) 이다.13) 전자의 경우에, 모체 격자 내에 위치하는 활성제 Dy3+ 이온은 반전 대칭이 아 닌(non-inversion symmetry) 국소 자리(local site)에 위 치하고, 후자의 경우에 활성제 Dy3+ 이온은 반전 대칭 (inversion symmetry)을 갖는 자리에 위치하는 것으로 알 려져 있다.14) 본 연구의 경우에, 4F9/2→ 6H13/2 전기 쌍극 자 전이에 의한 575 nm에 피크를 갖는 황색 발광 스펙 트럼의 세기가 4F9/2→ 6H15/2 자기 쌍극자 전이에 의한 482 nm의 청색 발광 스펙트럼의 세기보다 약 1.8배 크 기 때문에, 모체 CaNb2O6 격자 내에 위치하는 활성제 Dy3+ 이온은 비반전 대칭 자리에 위치한다. Fig. 2의 삽 입 그림에서 보듯이, 활성제 Eu3+ 이온만 단일 도핑된 CaNb2O6 형광체의 경우에는 다섯 종류의 발광 스펙트 럼이 관측되었다. 5D0→ 7F2 전이에 의한 적주황색 발광 (612 nm)과 상대적으로 미약한 5D1→ 7F1 전이에 의한 녹 색 발광(536 nm), 5D0→ 7F1 전이에 의한 주황색 발광 (593 nm), 5D0→ 7F3와 5D0→ 7F4 전이에 의한 적색 발광 (650, 705 nm)이 발생하였다.15) 이중에서 5D0→ 7F2 (612 nm) 전기 쌍극자 전이에 의한 적주황색 발광 세기가 제 일 강하였으며, 이것은 5D0→ 7F1 (593 nm) 자기 쌍극자 전이에 의한 주황색 발광의 세기에 비해 4.4배 증가하였 기 때문에, 활성제 Eu3+ 이온은 모체 CaNb2O6 격자 내 에서 비반전 대칭 자리에 위치한다.
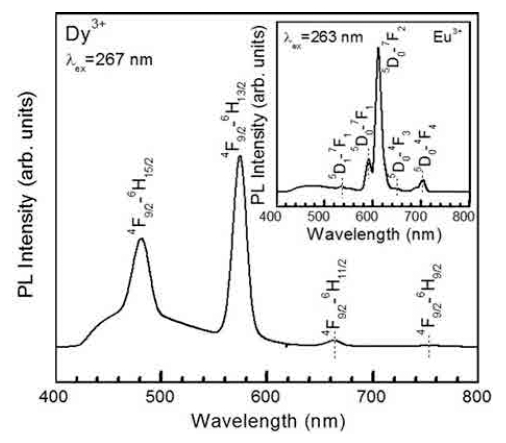
Fig. 2
Photoluminescence spectra of CaNb2O6 phosphors doped with Dy3+ and Eu3+ (inset), respectively.
Fig. 3은 파장 267 nm로 여기 시켰을 때 Dy3+ 이온의 몰 비를 5 mol%로 고정하고 Eu3+ 이온의 몰 비를 변화 시키면서 합성한 CaNb2O6:Dy3+, Eu3+ 형광체 분말의 발 광 스펙트럼을 나타낸 것이다. Eu3+ 이온의 몰 비가 1 mol% 일 때, Dy3+ 이온에 의한 482 nm의 청색 발광과 575 nm의 황색 발광 스펙트럼 뿐만 아니라 Eu3+ 이온에 의한 각각 612 nm와 705 nm에 피크를 갖는 적주황색과 적색 발광 스펙트럼이 나타나기 시작하였다. Eu3+ 이온의 몰 비를 5 mol%로 증가함에 따라 Dy3+ 이온에 의한 두 발광 피크의 세기는 현저히 감소하였으나, Eu3+ 이온에 의한 두 발광 피크의 세기는 증가하여 Eu3+ 이온의 몰 비가 10 mol% 일 때 최대를 나타내었고, Eu3+ 이온이 15 mol%로 증가함에 따라 Eu3+ 이온에 의한 발광 스펙 트럼의 세기는 감소하였고 Dy3+ 이온에 의한 발광 신호 들은 거의 사라졌다(Fig. 4 참조). 발광 스펙트럼의 세 기는 전반적으로 결정 입자의 크기에 비례하는 경향을 나타내었다. 이 현상은 활성제 Eu3+ 이온의 농도가 임 계값 이상으로 도핑되면 모체 CaNb2O6 격자 내에 위치 하는 Eu3+ 이온들 사이의 거리가 가까워져서 Eu3+ 이온 들이 서로 뭉침으로 인해 발광 세기가 감소하는 농도 소 광(concentration quenching) 현상으로 해석할 수 있다.
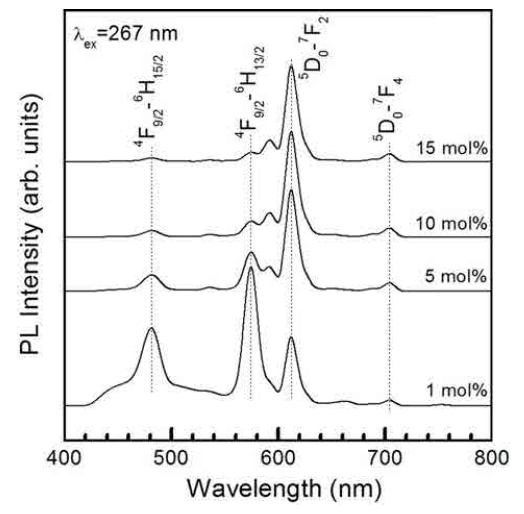
Fig. 3
Photoluminescence spectra of CaNb2O6:Dy3+, Eu3+ phosphors doped with different concentrations of Eu3+.
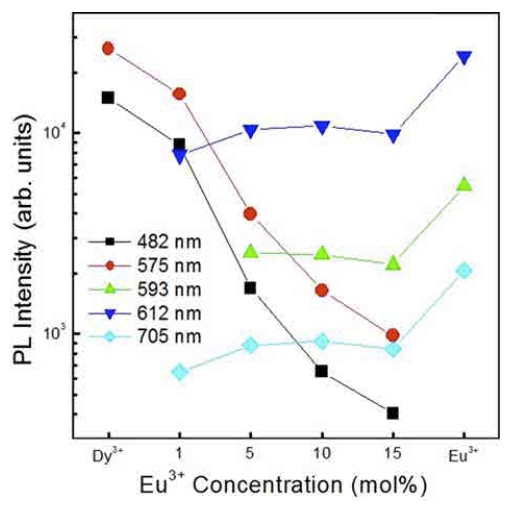
Fig. 4
The dependence of the emission intensities of peak wavelengths on the types and doping concentrations of activator ions.
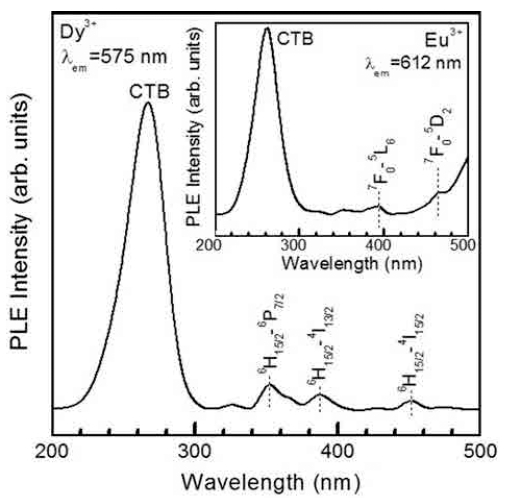
Fig. 5는 파장 575 nm와 612 nm로 각각 제어시켜 측 정한 CaNb2O6:5 mol% Dy3+와 CaNb2O6:5 mol% Eu3+ (삽입 그림) 형광체 분말의 흡광(photoluminescence excitation) 스펙트럼을 나타낸 것이다. CaNb2O6:5 mol% Dy3+ 형광체 분말은 267 nm를 정점으로 하여 210-310 nm 파 장 영역에 걸쳐서 넓게 분포하는 O2−-Dy3+ 이온들 사이 에 발생하는 전하 전달 밴드(charge transfer band: CTB) 와 320-500 nm 영역에서 관측되는 상대적으로 흡광 세 기가 미약한 Dy3+ 이온에 의한 흡광 신호로 구성되었다.16) 353 nm, 387 nm와 451 nm에 피크를 갖는 세 개의 흡광 파장은 Dy3+ 이온의 6H15/2→ 6P7/2, 6H15/2→ 4I13/2, 6H15/2→ 4I15/2 전이에 의하여 각각 발생한 흡광 파장들이다.17-18) 네 종류의 흡광 파장 중에서 CTB 흡광 스펙트럼의 세 기가 최대이었다. Fig. 5의 삽입 그림에서 보듯이, 파장 612 nm로 제어하였을 때 CaNb2O6:Eu3+ 형광체의 흡광 스펙트럼은 O2−-Eu3+ 이온들 사이에 발생한 263 nm에 피 크를 갖는 CTB 흡광 신호와 Eu3+ 이온의 7F0→ 5L6 (394 nm)와 7F0→ 5D2 (464 nm) 전이 신호로 구성되었다.
Fig. 6는 파장 575 nm로 제어 시켰을 때 Eu3+ 이온의 몰 비 변화에 따른 CaNb2O6:Dy3+, Eu3+ 형광체 분말의 흡광 스펙트럼을 나타낸 것이다. Eu3+ 이온의 몰 비에 관계없이 모든 형광체 분말은 최대 흡광 세기를 나타내는 267 nm에 피크를 갖는 CTB 흡광 스펙트럼과 Dy3+ 이온 의 6H15/2→ 6P7/2 (353 nm), 6H15/2→ 4I13/2 (387 nm), 6H15/2 → 4I15/2 (451 nm) 전이 신호를 보였다. Eu3+ 이온의 몰 비가 증가함에 따라 흡광 스펙트럼의 세기는 급격히 감 소하는 경향을 나타내었다.
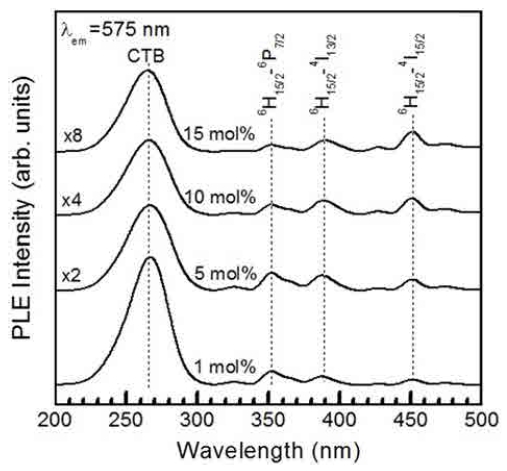
Fig. 6
Excitation spectra of CaNb2O6:Dy3+, Eu3+ phosphors doped with different concentrations of Eu3+ at a fixed Dy3+ of 5 mol%.
Fig. 7은 Dy3+와 Eu3+가 도핑된 CaNb2O6 형광체 분말 의 표면 형상을 SEM으로 촬영한 것을 나타낸 것이다. Fig. 7(a)에서 보듯이, CaNb2O6:5 mol% Dy3+ 형광체의 경우에 결정 입자의 평균 크기는 850 nm 이었고, 조약 돌 모양의 형태를 나타내었다. Dy3+와 Eu3+ 이온이 동 시 도핑된 형광체의 경우에 Eu3+ 이온의 몰 비가 증가 함에 따라 결정 입자의 모서리는 둥글게 변모되면서 불 규칙한 비대칭의 입자들이 서로 큰 덩어리를 형성하며 결정 입자의 크기는 증가하는 추세를 보였으나, Eu3+ 이 온의 몰 비가 15 mol% 일 때 감소하였다.

Fig. 7
SEM surface images of CaNb2O6 phosphors doped with (a) Dy3+, (f) Eu3+, and different Eu3+ concentrations of (b) 1, (c) 5, (d) 10 and (e) 15 mol%.
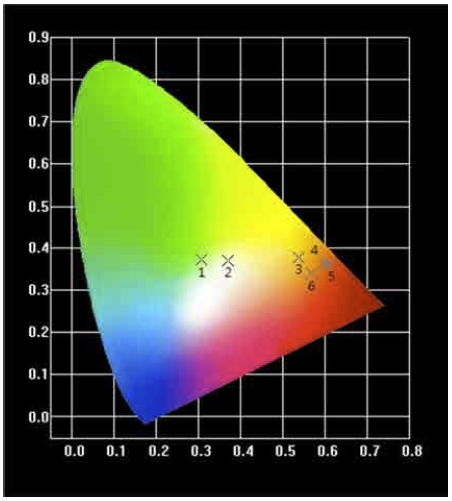
Fig. 8은 파장 267 nm로 여기 시켰을 때 형광체 분말 의 CIE(Commission Internationale de L’Eclairage) 1931 색 좌표(x, y)를 나타낸 것이다. 숫자 1과 6은 Dy3+와 Eu3+ 이온을 각각 단일 도핑한 경우이고, 숫자 2, 3, 4, 5는 Dy3+ 이온을 5 mol%로 고정한 상태에서 Eu3+ 이온 의 몰 비를 1, 5, 10, 15 %로 변화시켜 합성한 형광체 분말에 대한 CIE 색 좌표를 나타낸 것이다. Dy3+와 Eu3+ 이온을 각각 단일 도핑한 CaNb2O6 형광체의 경우에 색 좌표는 (0.308, 0.373)와 (0.568, 0.339)으로 각각 황색과 적색이었으나, Dy3+ 이온을 5 mol%로 고정하고 Eu3+ 이 온의 몰 비를 1 mol%에서 15 mol%로 증가시킴에 따라 색 좌표는 (0.369, 0.370)의 따뜻한 백색에서 (0.611, 0.360)의 적주황색으로 이동하였다.
4. 결 론
고상반응법을 사용하여 모체 CaNb2O6 격자에 활성제 Dy3+와 Eu3+ 이온의 몰 비를 변화시키면서 황색, 적주 황색, 백색광 형광체 분말을 제조하였으며, Dy3+와 Eu3+ 이온의 몰 비가 형광체 분말의 발광과 흡광 스펙트럼의 세기와 파장, 결정 구조, 미세 표면의 형상, CIE 색좌 표에 미치는 특성을 조사하였다. 모든 형광체 분말의 결 정 구조는 활성제 이온의 몰 비에 관계없이 주 피크 (131)을 갖는 사방정계이었으며, 결정 입자는 서로 뭉치 면서 비대칭적인 형태를 보였다. Dy3+가 도핑된 CaNb2O6 형광체 분말의 흡광 스펙트럼은 267 nm에 피크를 갖는 강한 CTB 흡광 스펙트럼과 Dy3+ 이온에 의한 4f-4f 전 이 신호로 구성되었고, 주 발광 스펙트럼은 482 nm와 575 nm에 피크를 갖는 청색과 황색 발광을 나타내었다. 상 기의 Dy3+가 도핑된 CaNb2O6 형광체에 Eu3+ 이온을 도 핑함에 따라 황색에서 적색으로 파장 이동 현상이 관측 되었다. 5 mol%의 Eu3+ 이온을 단일 도핑한 경우에 흡 광 스펙트럼은 263 nm에 피크를 갖는 CTB 신호와 Eu3+ 이온에 의한 흡광 피크가 관측되었으며, 주 발광 스펙 트럼은 612 nm의 적주황색 발광이었다. Dy3+가 도핑된 CaNb2O6 형광체에 Eu3+의 몰 비를 적절히 변화시킴으로 써 발광 파장을 제어할 수 있었다.