1. 서 론
유리분말(glass frit)은 각종 전기전자부품의 접합과 봉 착용도로 널리 이용되고 있으며 유리분말은 도포나 접 합 시 유기물, 용매, 분산제 등을 혼합하여 페이스트로 제조된다. 웨이퍼 레벨 패키지의 웨이퍼 전면에 칩을 본 딩, 태양전지 Si 웨이퍼와 Ag 전극의 접합 및 연료감응 형 태양전지의 레이저 실링1-3)등이 있다. 또한 진공복층 창호에서는 상/하판의 접합 시, 레이저 빔을 이용한 유 리 용접뿐만 아니라 유리분말을 이용한 접합도 있다.4,5)
진공복층 창호의 기판 유리는 일반 서냉 유리를 사용 했으나 최근 안전성을 고려하여 강도가 5배 높은 열강 화 소다라임 유리기판으로 바뀌는 추세이다. 하지만 열 강화 유리기판은 일정 온도 이상에서 강화 기능을 상실 하기 때문에 낮은 온도(< 400 °C)에서 열처리 공정에 적 용이 가능한 낮은 열물성의 유리조성이 필요하다. 유연 (Pb)계를 주성분으로 하는 유리가 대표적인 저온 소성용 유리로 사용되었으나, 최근 RoHS 와 같은 환경규제로 Pb 의 사용이 제한되기 때문에 무연(Pb-free)계 유리 조 성의 연구가 필요하다.6) 따라서 진공창호의 상/하판 유 리기판을 봉착할 수 있는 유리분말으로는 Pb 를 함유하 지 않으면서 낮은 열물성과 소다 라임 기판과 유사한 열 팽창계수(72~78 × 10−7/°C)를 갖는 유리 조성을 적용해야 한다.
저융점 무연계유리 봉착소재의 유력한 대체제로서 Bi 계 봉착재료들이 개발되고 있으나,7,8) 400 °C 이하 소성 조건에서는 유동성이 미흡하고 퍼짐성 면에서 극히 부 족하기 때문에 V2O5-P2O5 계 유리를 기본으로 많은 연 구가 진행되고 있다.9,10) V2O5 단독으로는 유리 형성 능 력이 부족하기 때문에 소량의 B2O3 나 P2O5 를 첨가하 면 저온의 융점을 갖는 안정한 유리를 얻을 수 있다. 그 리고 V2O5 가 함유된 유리는 가수변화로 인한 반도체 특성을 갖고 있기 때문에 전기전자 소자로 많이 사용된 다.11) 유리 내 에서는 V4+ 와 V5+ 상태로 동시에 존재하 는데, 존재하는 V4+ 와 V5+ 의 비율은 용융온도 또는 공 존하는 산화물의 양에 따라 달라지며 원자가 교환형 전 자전도가 일어난다.12)(1)
본 연구에서는 진공창호 봉착용 소다라임 기판과의 접 착력 향상을 위하여 다양한 산화물을 첨가하였다. Co3O4 는 결정화 억제, Sb2O3 는 내수성 향상, TiO2 는 기판과 의 접착강도 증가, B2O3 는 열적특성을 변화시키는 것 으로 보고되어 있기 때문에13-15) 이러한 다양한 산화물들 을 V2O5-P2O5-ZnO 계 유리조성에 첨가하였다. 각 산화 물 첨가에 따른 기계적 강도를 측정 후 접착강도가 우 수했던 B2O3 함량을 조절하여 조성을 변화하였다. B2O3 의 첨가에 따른 유리의 열 특성과 구조적 변화 및 소 다라임기판과 유리분말 사이의 계면반응을 확인하였다.
2. 연구 방법
본 연구는 문헌조사를 바탕으로 V2O5-P2O5-ZnO 계 3 성분계 유리조성을 선정하였다. 출발원료로 V2O5(Aldrich Chemical Co, USA, 99.6 %), P2O5(Aldrich Chemical Co, USA, 98.0 %), ZnO(Aldrich Chemical Co, USA, 99.9 %), H3BO4(Aldrich Chemical Co, USA, 99.97 %), Co3O4(Aldrich Chemical Co, USA, 99.5 %), TiO2(Aldrich Chemical Co, USA, 99.5 %), Sb2O3(Yakuri Pure Chemicals Co, Japan, 98.0 %)를 사용하였다. 각 조성의 조성 비에 맞게 배치한 분말을 칭량 후 충분히 혼합하였다. 전기로에 넣고 900 °C에서 20 분간 용융하여 리본롤러 에 급랭하여 컬릿을 제조하였다. 제조된 컬릿은 지르코니 아 볼과 함께 알루미나 자에 넣고 유성볼밀(Pulverisette- 7, Fritsch, Germany)로 분쇄 후 입도를 45 um 이하로 분 급하여 유리분말을 제조하였다. 유리 용융액을 미리 가 열한 탄소몰드에 부어 3시간동안 어닐링하여 벌크형태의 유리로 만들었다.
제조한 유리분말은 시차주사 열량계(Differential Scanning Calorimetery, DSC, Netzsch, STA 449, Germany)와 열 팽창계(Dillatometery, L75, Linseis, USA), 고온현미경 (Hot stage mocroscyopy, HSM, Misura, Italia)을 이용 하여 열 특성을 확인하였다. DSC는 10 °C/min 의 승온 속도로 상온에서 600 °C 범위에서 유리전이온도(Tg) 및 결정화 온도를 측정하였고, 고온현미경을 통해 10 °C/min 의 승온 속도로 상온에서 펠렛의 종횡비가 1:2가 되는 지점까지의 소결거동을 관찰하였다. 상온에서 300 °C 까 지 5 °C/min의 승온속도로 어닐링 한 벌크유리의 길이 변 화를 열팽창계로 측정하였으며, 30 °C에서 200 °C 구간 에서 온도 증가에 따른 벌크유리의 팽창 길이를 측정하 였다.
제조한 유리의 젖음성을 평가하기 위해 10 Φ의 몰드 에 유리분말을 넣어 펠렛 형태로 만든 후 유리기판 위 에 올려 놓고 400 °C에서 10분간 유지하였다. 소성 전 후의 펠렛 크기와 형태를 관찰하여 유동성과 젖음성, 실 투 여부를 관찰하였다. 접착강도 측정은 조성변화를 확 인하기 위하여 페이스트 형태로 제조하지 않고 유리분 말 만을 사용하였다. 유리분말을 5 Φ의 금속 몰드에 넣 은 뒤 일축 가압하여 펠렛형태로 성형하였다. 소다라임 유리기판에 펠렛을 올려놓고 디스펜서를 사용하여 400 °C 에서 30분간 1차 가소성을 한 후, 상판유리를 덮고 400 °C에서 30분간 2차 소성을 하여 봉착시료용 지그(jig)를 제작하였다. 만능시험기(MX-500N, Imada, Japan)로 측정 하였으며 6.0 mm/min의 속도로 5회 측정 후 평균값을 나타내었다.
제조한 분말의 유리 형성유무 및 소결 후 결정상을 확 인하기 위하여 X 선 회절분석기(X-ray Differactometer system, Rigaku, Japan)를 사용하여 40 kV, 150 mA 조 건에서 2°/min 의 속도로 10~90° 범위를 측정하였다. 상 용 소프트웨어 High Score Plus(Version 3.0e, PANalytical B.V., Netherlands)을 이용하여 RIR(Reference intensity ratio) 방법으로 B2O3 와 V2O5 의 결정상 질량 분율을 구 하였다. B2O3 의 함량변화에 따른 유리구조 분석을 위해 적외선 분광기(Fourier transform Infrared spectroscopy, Vertex 80V, Bruker, USA)를 이용하여 400~4000 cm−1 영역의 스펙트럼을 측정하였다. 이때, 주사 횟수는 20회 이며, 분해능은 2 cm−1 의 조건으로 측정하였다. 400 °C 에서 1시간 소결한 펠렛시편을 파쇄하여 KBr 과 1:100 의 비율로 균일하게 혼합하여 건조한 후 전용 몰드로 약 1 ton/cm2 정도의 압력을 가해 디스크형태로 성형하여 사 용하였다. 관찰하려는 소다라임 유리기판과 유리분말의 계 면을 주사전자현미경(FE-Scanning electron Microscope, S-4300SE, Hitach, Japan) 으로 관찰하였으며, EDAX 분 석을 통하여 계면 사이의 이온거동을 확인하였다.Fig. 1Fig. 2
3. 결과 및 고찰
3.1. 유리형성과 추가 산화물의 선정
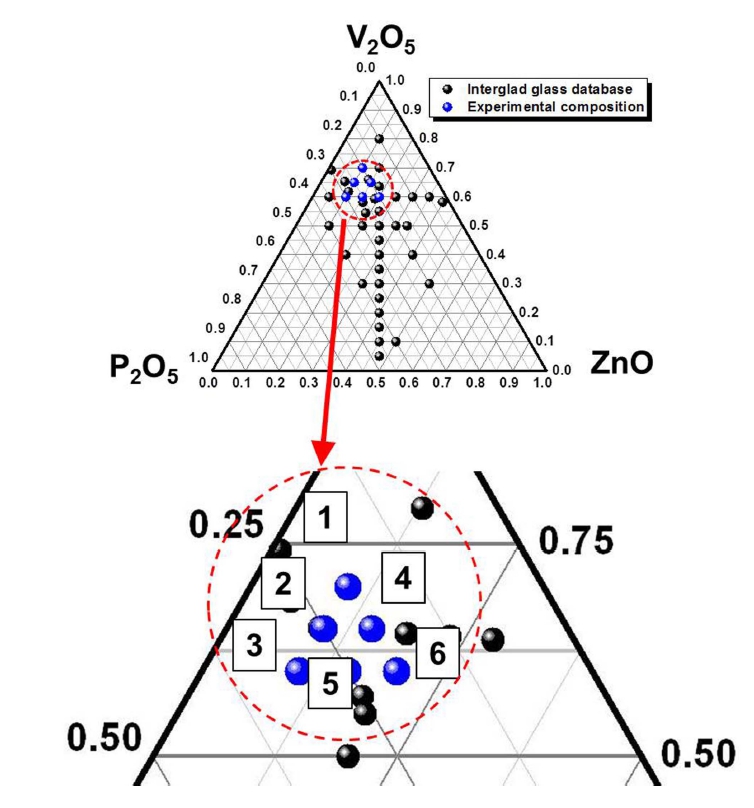
V2O5-P2O5-ZnO 계 유리형성 범위를 문헌조사16) (INTER GLAD Ver. 6.0, produced by New Glass Forum, Japan) 를 통해 6개의 유리조성을 선정하였다(Fig. 1). 각 성분 의 영향을 파악하기 위하여 3성분계 중 한 성분을 고 정하고 나머지 성분을 조절하는 방향으로 조성을 설계 하여 Table 1에 나타내었다. 유리전이온도는 242 °C에서 271 °C의 범위에서 나타났으며 V2O5/P2O5 몰비가 증가할 수록 유리전이온도는 감소하였다. 이것은 유리구조 형성 제인 P2O5 가 감소하고 수식제인 V2O5 가 증가함에 따 라 비가교산소가 감소하여 이러한 경향을 보이는 것으 로 추측된다.17,18)Fig. 3
Table 1
Composition and thermal properties of the glasses.
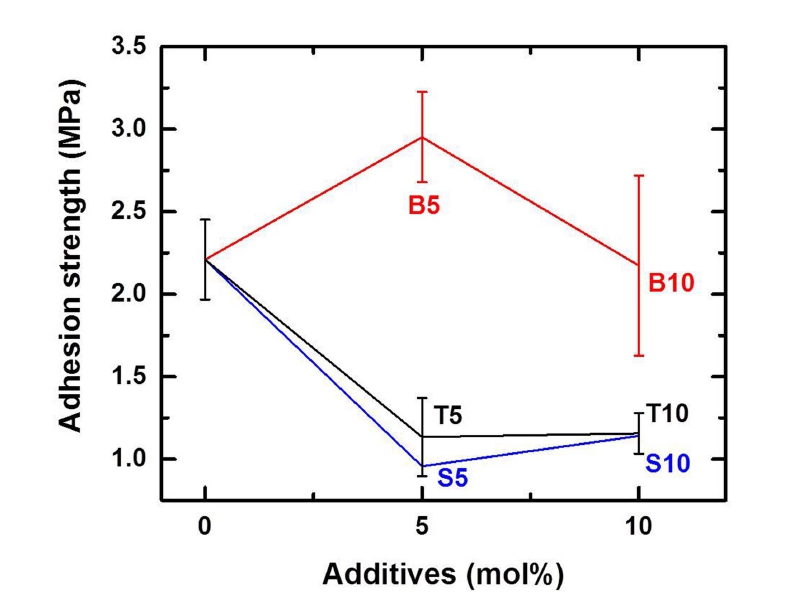
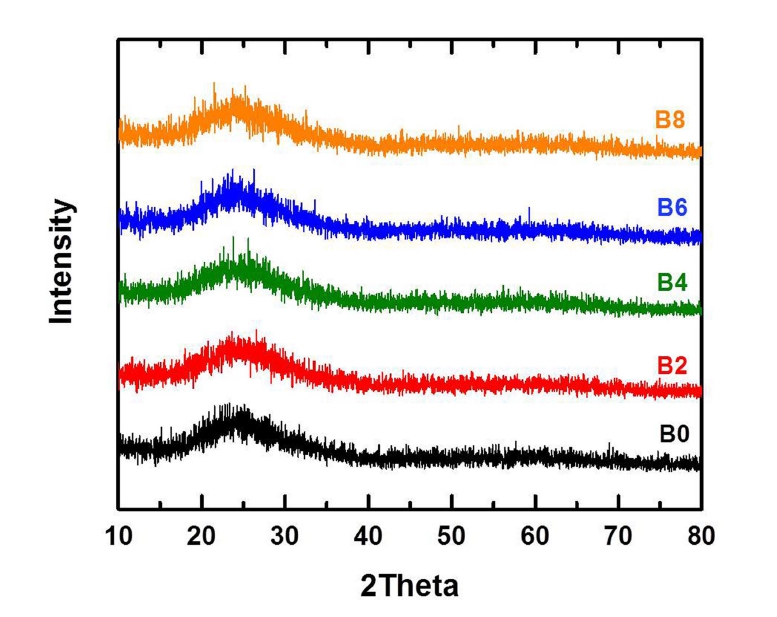
V2O5-P2O5-ZnO 계 유리의 flow button test를 통하여 기판과의 젖음성이 가장 뛰어나고 실투를 전혀 일으키 지 않으며 유리기판과의 접착성이 있는 PVZ_5 조성을 선정하고(Table 2), 선정한 조성과 유리기판과의 반응성 향상을 위하여 TiO2, Sb2O3, B2O3 산화물을 5 mol% 와 10 mol% 를 첨가하여 추가 조성을 설계 한 후 접착강 도 특성을 평가 하였다(Fig. 2). B2O3 를 첨가하였을 때 가장 높은 접착강도를 나타나며 5 mol%일 때 가장 높 은 값을 보였다. 이 특성을 파악하기 위해 3성분계는 고 정으로 하고 B2O3 첨가량만 변화시켜 유리조성을 설계 하였다(Table 3). XRD 결과를 보면 결정피크가 존재하 지 않는 완만한 전형적인 비정질상 패턴을 나타내어 유 리상이 잘 형성되었음을 확인하였다(Fig. 4).
Table 2
Diameter ratio, wetting and crystallization through flow button test.
| Samples | PVZ_1 | PVZ_2 | PVZ_3 | PVZ_4 | PVZ_5 | PVZ_6 |
|---|---|---|---|---|---|---|
| Diameter ratio(%) | –13.7 | –8.0 | –2.8 | –19.9 | 42.3 | –20.8 |
| Wetting | X | X | X | X | O | X |
| Crystallization | O | O | X | O | X | O |
| Adhesion | X | X | O | X | O | X |
Table 3
Compositions and thermal properties of glass frits fabricated.
3.2. B2O3 함량 증가에 따른 유리특성
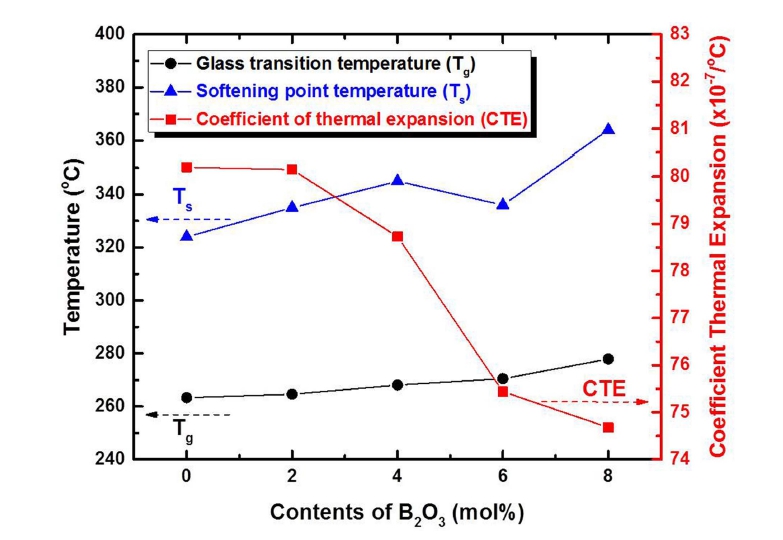
B2O3 함량의 증가에 따라 유리전이온도는 263.3 °C에 서 277.9 °C까지 증가하였다(Fig. 4). 유리전이온도와 연 화점은 B2O3 함량이 증가함에 따라 증가하였으며 열팽 창계수는 약 80 × 10−7/°C에서 약 74 × 10−7/°C 로 감소하 였다. 조성 모두 400 °C에서 소결이 가능하였으며 소다 라임 기판의 열팽창계수와 매칭할 수 있는 조성임을 확 인하였다.
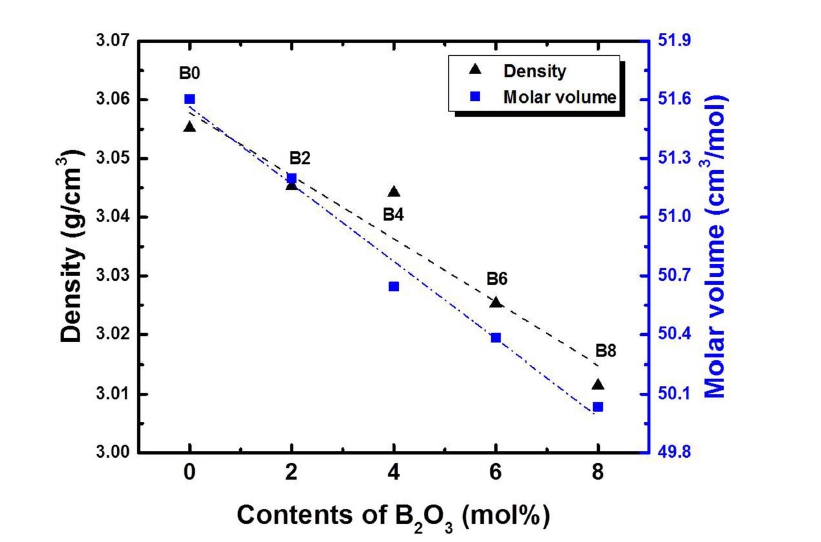
B2O3 첨가량 증가에 따른 밀도와 몰 체적의 변화를 Fig. 5에 나타내었다. 몰체적(Vm)은 Vm= M / ρ으로 계산 하였고, 여기서 M은 유리의 평균 몰 중량이다. 이는 B2O3(69.62 g/mol)의 분자량이 상대적으로 V2O5(181.88 g/ mol), P2O5(141.94 g/mol), ZnO(81.38 g/mol)의 분자량보 다 작기 때문에 V2O5-P2O5-ZnO 유리구조 내에 B2O3 첨 가량이 증가할수록 밀도가 감소하였다. 또한 B2O3 함량 이 증가할수록 가교산소의 증가에 따라 몰체적이 감소 하였다. 이 결과는 B2O3 가 망목형성 산화물로 유리 구 조 내에서 가교산소를 형성하여 유리 네트워크가 조밀 해지는 것으로 판단된다.19)
접착강도 측정 시 유리 내 구조변화 및 유리기판과의 반응성이 있을 것으로 판단하였고, 이를 확인하기 위하 여 접착강도 측정조건과 같은 방법으로 유리기판 위에 유리분말을 400 °C에서 1시간동안 소결하였다. 소결한 분 말은 BS 시리즈로 명명하여 X-선 회절분석 결과를 Fig. 6(a)에 나타내었다. 소결체내의 결정상은 V2O5(JCPDS No. 01-074-1595)와 VO2(JCPDS No. 01-071-0290)가 혼합된 형태로 존재함을 알 수 있었다.
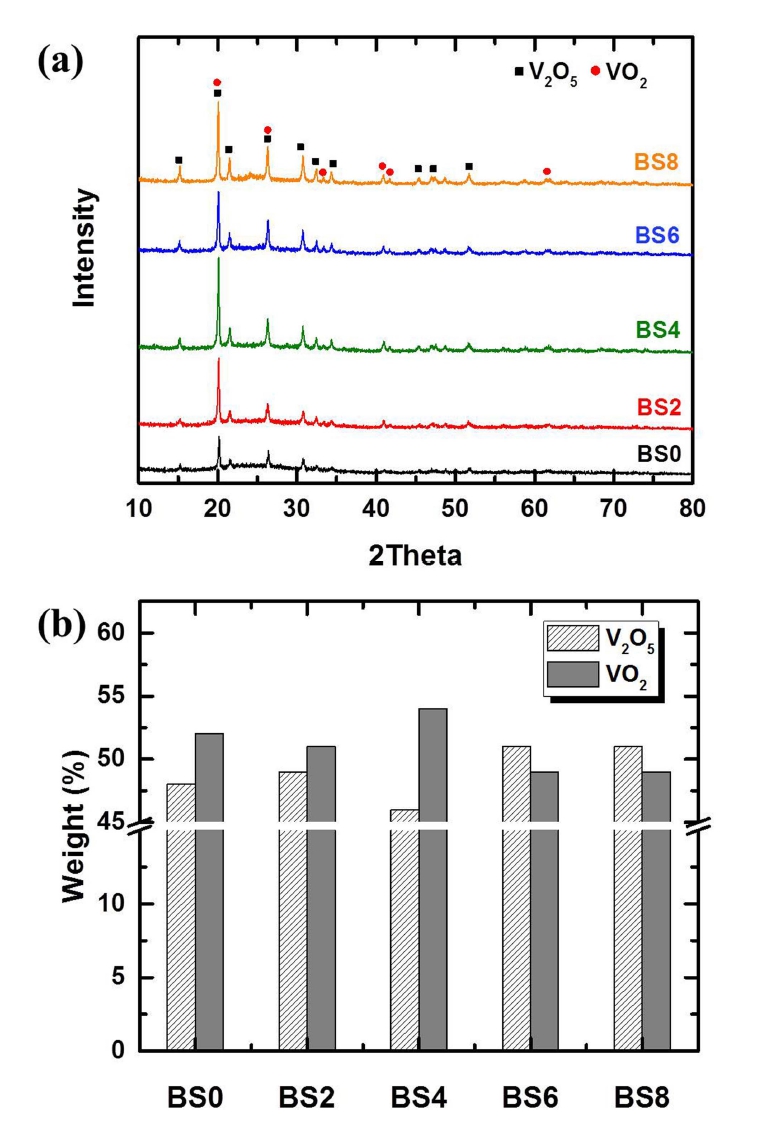
Fig. 6
(a) XRD spectra of different B2O3 content after sintering at 400 °C for 1h. (b) Weight fraction of glass frits using Rietveld-RIR quantitative analysis.
XRD 결정패턴을 바탕으로 결정상의 상대적인 양을 RIR 값으로 계산한 결과, 결정피크는 B2O3 를 첨가함에 따라 점차 증가하다가 4 mol%에서 VO2 상의 함량이 가 장 많이 존재하는 반면 V2O5 상은 가장 적게 존재하였 다. B2O3 를 더 첨가하였을 때(BS6과 BS8) VO2 상의 함량은 다시 감소하고 V2O5 상의 함량이 증가하였다(Fig. 6b). 이는 B2O3 함량증가에 따라 BO3 구조가 BO4 구조 로 변하면서 B2O3 의 함량이 어느 일정량을 넘어서게 되면 다시 BO3 구조로 전화되는 것으로 추정된다.20) 또 한 바나듐 산화물은 VO, VO2, V2O3, V2O5 로 다양하게 존재하는데 바나듐의 원자가가 식 (2)와 같이 V5+ 가 V4+ 로 감소는 V2O5 의 환원반응으로 VO2 로 형성된다.21) 이때 B2O3 함량이 증가(4 mol%) 함에 따라 식(3)과 같 이 구조적 변화한 것으로 생각된다.22)
결정화에 따른 바나듐 유리중의 V4+ 와 V5+ 의 비율 을 확인하였으며 이러한 유리소결체의 구조변화가 BO4 및 BO3 변화의 상관성은 FT-IR 결과에서인 Fig. 7(a)에 서도 확인할 수 있다. B2O3 첨가량이 증가함에 따라 400~1500 cm−1 영역에서 크게 5개의 흡수피크가 나타났 다. 655 cm−1 에서 새로운 피크가 발생하여 높은 파수로 이동하고 798 cm−1 에서의 이동은 각 각 VO4 다면체 구 조의 VO2 가교 산소의 비대칭 진동과 붕산염 망에서 BO- B 결합에 의한 것이라고 볼 수 있다.23,24) B2O3 함량 이 4 mol% 일 때 1000~1006 cm−1과 1207~1230 cm−1에 서 흡수피크가 높은 파수로 이동하였다가 B2O3 의 첨가 량이 더 증가하면(6 mol%와 8 mol%) 다시 1002 cm−1와 1226 cm−1 낮은 파수로의 이동하였다. 각각 BO3 단위 구 조의 B-O 신축진동과 VO5 다면체의 진동 영역으로 알 려져 있다.23,25) 이와 같은 변화는, V2O5 가 유리구조 내 에서 V4+ 와 V5+ 가 동시에 존재하고 있다가 B2O3 함량 이 증가하면서 VO4 다면체의 비율이 증가하는 구조적 변 화가 일어난 것으로 보인다.
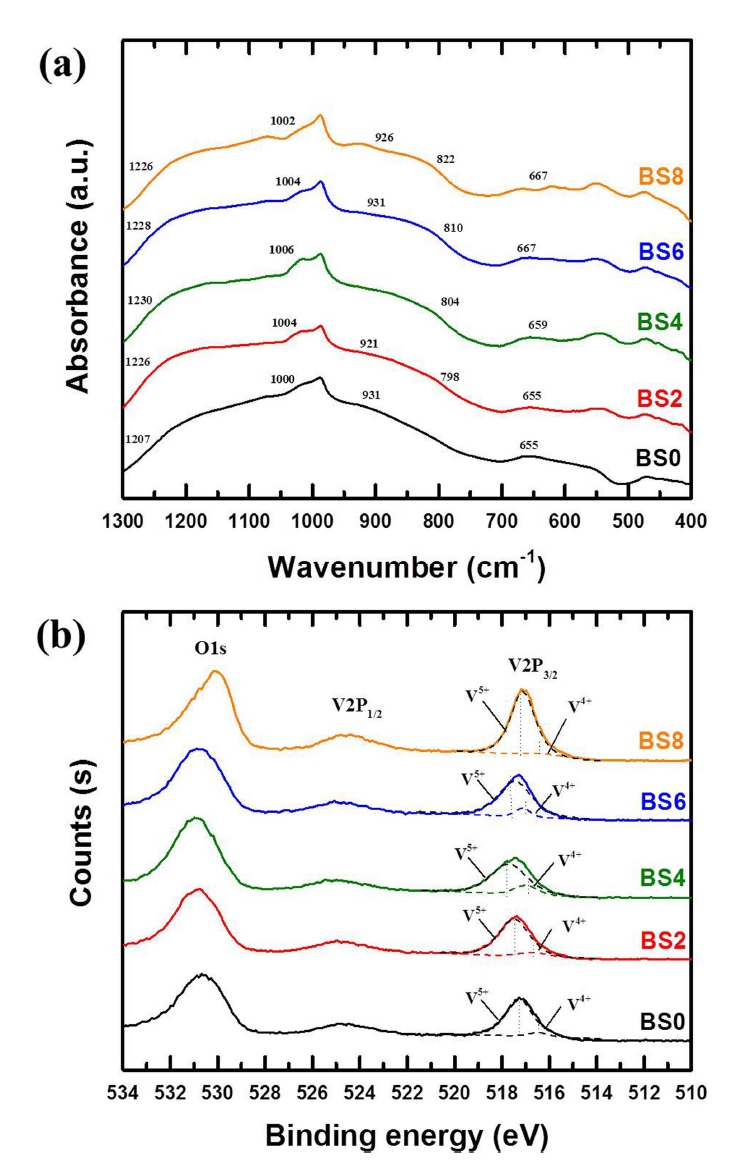
Fig. 7
(a) FT-IR spectra (b) Peak decomposition of the V2p XPS spectra of sinterd glass frit at 400 °C for 1h.
결정상 내에 B2O3 첨가에 따른 V5+ 와 V4+ 의 함량을 확인하기 위하여 XPS분석을 실시하였다(Fig. 7b). 각 조 성에서의 V2p3/2 peak를 Gaussian 피크 분리법을 이용하 여 V5+(517 eV 부근)와 V4+(516 eV 부근)으로 각각 분리 하였다.26) 이것을 바탕으로 V5+/Vtotal과 V4+/Vtotal 의 정량 적인 양을 Table 4에 나타내었다. B2O3 증가에 따라 4 mol%까지 V4+ 의 함량이 증가 하였다가 다시 감소하 는 경향을 나타내고 있다. 이는 B2O3 함량증가에 따라 V5+ 에서 V4+ 로 환원반응이 일어남을 의미하며 VO5 다 면체가 VO4 다면체의 비중이 증가한 것으로 예상된다.
Table 4
Fit parameters for the V2p3/2, variation of V5+ and V4+ with the B2O3 content.
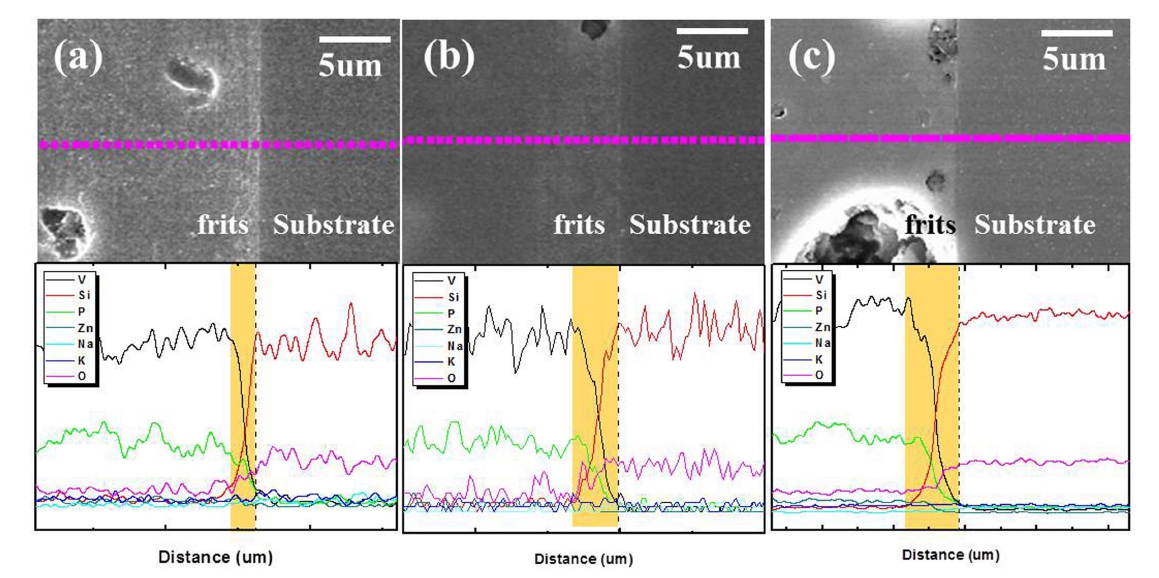
제조한 분말의 B2O3 함량이 증가함에 따른 소다라임 유리기판과의 계면반응을 충분히 진행하기 위해 400 °C 에서 3 시간 동안 소결하였으며, 그 단면을 주사전자 현 미경을 통해 관찰하였다. 눈에 보이는 뚜렷한 반응 층 과 결정상은 확인되지 않았으나, EDAX 분석을 통해 Si 이온의 확산거동을 확인할 수 있었다(Fig. 8). 기판에서 분말으로 Si 이온이 확산 되며, B2O3 함량이 증가할수 록 Si 이온의 확산거리도 증가하였다. 이는 앞서 나타났 던 소결체의 결정상과 구조적 변화와 관련된다.27) 즉, V4+ 와 V5+ 가 공존하던 V2O5 계 유리구조 내에서 소결 후 결정상의 V4+ 의 비율이 증가하면서 Si4+ 이온이 더 확 산하기에 유리한 구조가 되기 때문으로 판단된다.
4. 결 론
진공창호 봉착용 유리조성을 개발하기 위하여, Pb 을 함유하지 않은 무연계의 낮은 온도의 열물성을 갖는 V2O5-P2O5-ZnO-Co3O4-B2O3 유리조성을 설계하였다. 젖음 성과 결정화 여부를 확인하여 V2O5-P2O5-ZnO 삼원계 유 리조성을 선정하였다. 다양한 산화물을 첨가하여 접착강 도를 측정한 후, 결정화를 억제하는 Co3O4 와 접착강도 가 높았던 B2O3 를 첨가량을 변화하여 열 특성과 구조 적 변화, 계면 반응을 살펴보았다. B2O3 가 첨가되면서 V2O5 계 유리 내부의 V5+ 이온의 비가교산소가 가교산 소로 변화하였으며, 이에 따라 유리전이온도와 연화점은 증가하고, 열팽창계수는 감소하였다. V5+ 이온의 비율이 감소하고 V4+ 이온의 비율이 증가하면서, 기판에서 Si4+ 이온의 확산이 유리해지는 것으로 생각한다. 기판에서 프 릿으로 이온확산 거리 증가는 기판과 분말의 접착강도 의 향상에 영향을 주었다.