1. 서 론
최근에 백열등과 형광등을 대체하기 위하여 높은 연색 지수와 색 재현성이 우수한 백색 발광 다이오드(white light emitting diodes; WLEDs) 개발에 상당한 연구가 진행되고 있다.1-3) 일반적으로 WLED는 세 종류의 방법 으로 제작되고 있다. 청색 LED 칩 상부에 황색 형광체 를 도포하거나, 청색 LED 칩 상부에 적색과 녹색 형광 체를 동시에 도포하는 방법과 근자외선 LED 칩 표면에 적색, 녹색, 청색 형광체 분말을 도포하여 백색 발광을 구현하고 있다.4) 발광 파장 영역 중에서 적색과 녹색 발 광의 세기는 백색 발광의 연색 지수(color rendering index) 를 높이는 중요한 요소로 알려져 있어 이에 적합한 모 체 결정과 활성제 이온으로 구성되는 고효율의 녹색 형 광체 개발은 절실하다.5)
몰리브덴산염(molybdate), 알루민산염(aluminate), 붕산염 (borate), 규산염(silicate)을 포함하는 산화 화합물(oxide compounds)은 자외선 영역에서 강한 흡수력을 나타내고, 이 가운데서 몰리브덴산염은 회중석(scheelite) 형태의 결 정 구조를 보이며, 우수한 화학 및 열적 안정성을 나타 내기 때문에 발광 소재의 좋은 모체 결정으로 간주되고 있다.6,7) 특히, BaMoO4는 형광체, WLED, 레이저, 광섬 유, 촉매 등에 응용할 수 있는 몰리브덴산염 중에서 중 요한 물질이다. 최근에 희토류 이온이 도핑된 몰리브덴 산염 화합물은 높은 발광 효율과 화학적 안정성을 나타 내어 형광체의 유망한 후보로 부상하고 있으며, 이에 대 한 연구가 광범위하게 진행되고 있다. Du와 Yu8)는 고 상반응법을 사용하여 정방정계 결정 구조를 갖는 Eu3+ 이온이 도핑된 AMoO4 (A = Mg, Ca, Sr, Ba) 형광체를 합성하였으며, 이중에서 Eu3+ 이온이 도핑된 CaMoO4 형 광체가 가장 강한 적색 발광 세기를 나타내며, CIE 색 좌표가 (0.647, 0.352)임을 확인하였다. Wang 등9)은 수 열법(hydrothermal method)을 사용하여 3차원 호두 모양 의 형상을 갖는 CaMoO4:Eu3+ 형광체를 제작하였으며, 열 처리 온도가 증가함에 따라 결정 입자의 크기가 증가하 고, 파장 394 nm로 여기시켰을 때 615 nm에 피크를 갖 는 적색 발광을 관측하였다. Li 등10)은 고상반응법을 사 용하여 600-750 °C에서 3 h 동안 소결하여 Tb3+와 Na+ 이온이 도핑된 SrMoO4 녹색 형광체를 제조하였으며, 활 성제 이온 Tb3+와 전하 보상자(charge compensator) Na+ 이온이 결정 구조에 영향을 미치지 않으며, 파장 375 nm 와 488 nm로 여기시켰을 때 형광체의 최대 발광 세기 는 Tb3+ 이온의 5D4→ 7F5 전이에 의한 548 nm에서 발 생함을 보고하였다.
본 연구에서는 모체 결정 BaMoO4에 서로 다른 농도 를 갖는 활성제 이온 Tb3+을 도핑하여 고효율의 녹색광 을 발광하는 형광체를 제작하였다. 특히, WLED에 응용 하기 위한 최대의 녹색 발광세기를 갖는 최적의 Tb3+ 이 온의 농도를 결정하고, 활성제 이온의 농도 변화에 따른 결정 입자의 형상, 형광체의 발광과 여기 세기의 상호 관 계, 농도 소광을 일으키는 기본 원리를 체계적으로 조 사하였다.
2. 실험 방법
BaMoO4:Tb3+ 형광체는 고상반응법을 사용하여 합성하 였다. 초기 물질 BaCO3(순도: 99.995%), MoO3 (99.9%), Tb4O7 (99.9 %)를 화학양론적으로 준비하였으며, Tb3+ 이 온의 농도(x)를 각각 0, 1, 5, 10, 15, 20 mol%로 변화 시켰으며, 화학 반응은 식 (1)과 같다:
정밀 저울로 측량한 초기 물질을 농도별로 각각 분리 하여 에탄올, ZrO2 볼과 함께 플라스틱 병에 넣고 10 시간 볼밀(ball-mill) 작업을 수행한 후에, 비커에 담아서 60 °C에서 10 시간의 건조 과정을 거쳐서 건조한 시료 를 80 μm의 미세한 크기로 갈아서 6개의 알루미나 도 가니에 담아 400 °C에서 3 시간의 하소 공정과 1100 °C 에서 5 시간의 소결 공정을 통하여 합성하였다.
형광체의 결정 구조는 회절각 10~80° 영역에서 Cu-Kα 복사선을 사용하는 Rigaku Ultima IV X-선 회절 장치 를 사용하여 측정하였으며, 형광체 분말 표면의 미세 형 상은 Hitachi S-4300 주사전자현미경으로 촬영하였다. 형 광체의 광학 특성은 상온에서 Scinco FS-2 형광광도계 를 사용하여 조사하였다.
3. 결과 및 고찰
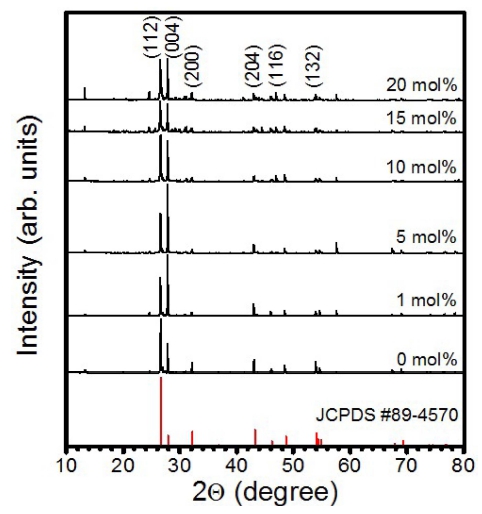
Fig. 1은 Tb3+ 이온의 몰 비를 0, 1, 5, 10, 15, 20 mol%씩 변화시키면서 합성한 BaMoO4:Tb3+ 형광체 분 말 시료의 XRD 데이터를 나타낸 것이다. Tb3+ 이온이 도핑된 형광체 시료는 2θ = 26.57°와 27.89°에서 강한 회 절 세기를 갖는 두 피크와 상대적으로 약한 32.12°, 43.01°, 48.48°, 53.89°에 중심을 둔 회절 피크들이 관측 되었다. 전자는 (112)와 (004)면에서 발생한 회절 피크 이며, 후자는 (200), (204), (116), (132)면에서 발생한 피크들이다. 합성한 형광체 분말은 JCPDS #89-4570에 제시된 회절 상과 일치하는 정방 정계(tetragonal system) 의 결정 구조임을 확인하였다. Tb3+ 이온의 몰 비가 증 가함에 따라 두 가지 주목할만한 현상이 관측되었다. 첫 째는 회절각 2θ = 13.27°에서 검출된 BaO+CO2 피크이 다. 이것은 반응물 BaCO3가 소결 과정 중에 CO2 가스 를 배출하고 BaO로 변환되는 과정에서 CO2 가스가 완 전히 배출되지 못하고 화학 흡착된(chemisorbed) 상태에 서 BaO+CO2를 남긴 것으로 추정된다. BaO 표면에 CO2 가 화학 흡착된 종(species)은 매우 안정한 흡착 에너지 Eads = −0.8 eV를 갖는다.11) 둘째는 Tb3+ 이온의 농도가 증 가함에 따라 결정 격자면 사이의 거리에 변화가 발생하 였다. 세라믹 산화물의 경우에 이온끼리 쿨롱 인력의 상 호 작용으로 용질의 농도에 따라 격자 크기가 선형적으 로 변하지 않는다.12) 이를 확인하기 위하여 회절각 2θ = 43.01°에서 발생한 (204)면에 의한 회절 피크를 확대하여 Fig. 2에 나타내었다. 이것은 배위수(coordination number) 8인 환경에서 유효 이온 반경(effective ionic radius) 이 1.42 Å인 Ba2+ 이온 3개를 유효 이온 반경이 1.04 Å 인 Tb3+ 이온 2개가 치환하면서 빈자리(vacancy) 1개를 만들어 내는 효과가 Tb3+ 이온의 농도가 증가하면서 나 타난 것으로 해석된다.13)
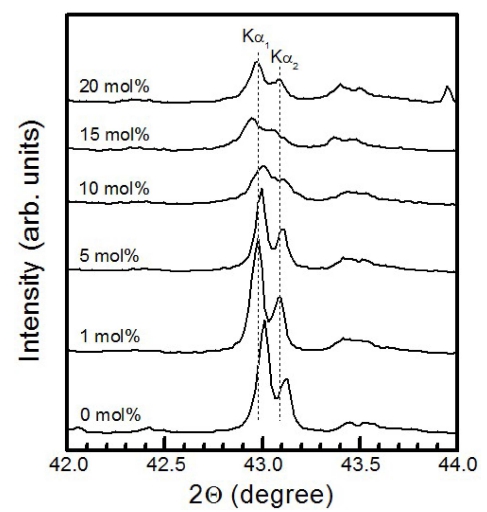
Fig. 2.
Enlarged version of XRD patterns of BaMoO4 phosphors doped with different concentrations of Tb3+. Main peaks correspond to Cu-Kα1 and shoulder sub-peaks with half intensity are Cu-Kα2.
Fig. 3은 Tb3+ 이온의 몰 비(x)를 (a) x = 0, (b) 1, (c) 5, (d) 10, (e) 15, (f) 20 mol%로 합성한 BaMoO4:Tb3+ 형광체 분말의 미세 표면 형상을 SEM으로 촬영한 것 이다. Fig. 3(a)~(f)에서 보듯이, 각 형광체 분말은 약 10~60 μm 크기의 입자들로 구성되며 입자 형상에 변화 가 있음을 볼 수 있다. Tb3+ 이온이 도핑되지 않은 형 광체의 경우에 입자 형상은 구형에 가깝지만, Tb3+ 이 온이 모체 결정에 치환 고용됨에 따라 입자의 모서리에 각이 생기면서 비정형의 입자 형상을 보였다. 특히, Tb3+ 이온이 1 mol% 도핑된 경우에 거대 결정 성장(secondary grain growth)의 형태가 관측되었다.

Fig. 3.
SEM surface images of BaMoO4 phosphors synthesized with Tb3+ ion concentrations of: (a) 0, (b) 1, (c) 5, (d) 10, (e) 15, and (f) 20 mol%.
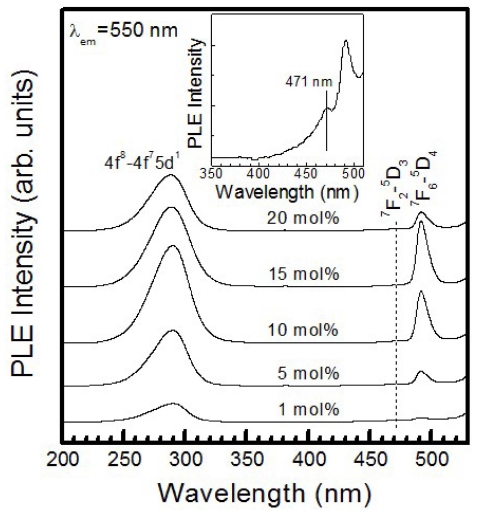
Fig. 4는 활성제 이온 Tb3+의 몰 비를 변화시키면서 제 조한 BaMoO4:Tb3+ 형광체 분말을 방출 파장 550 nm로 제어하여 상온에서 측정한 여기 스펙트럼을 나타낸 것 이다. Tb3+ 이온의 몰 비가 1 mol%인 BaMoO4 형광체 의 경우에 두 종류의 여기 스펙트럼이 관측되었다. 290 nm (34,483 cm−1)에 피크를 갖고 반치폭이 34 nm 정도 로 넓은 밴드폭을 갖는 강한 여기 스펙트럼과 주 여기 피크에 비하여 상대적으로 여기 세기가 매우 작은 471 와 492 nm에 정점을 갖는 여기 스펙트럼으로 구성되었 다. 전자는 Tb3+ 이온의 4f8 →4f75d1 (f-d) 전이에 의한 여기 신호이며, 여기서 주목할 점은 O2− →Tb3+ 이온들 사이의 에너지 전달에 의하여 발생하는 전하 전달 밴드 (charge transfer band; CTB)는 5d 에너지 준위보다 높 은 에너지(~60,000 cm−1)에 위치한다.14) 후자의 두 약한 여기 스펙트럼은 Tb3+ 이온의 7F2→ 5D3 (471 nm) 전이 와 7F6→ 5D4 (492 nm) 전이에 의하여 각각 발생한 신 호이다.15) Tb3+ 이온의 농도가 1 mol%에서 10 mol%로 증가함에 따라 f-d 전이에 의한 여기 스펙트럼의 세기는 계속 증가하여 10 mol%에서 최대값을 나타내었으나, Tb3+ 이온의 농도가 더욱 증가함에 따라 여기 세기는 감소하 였다. 한편, Tb3+ 이온의 7F6→ 5D4 (492 nm) 전이에 의 한 여기 신호의 세기는 Tb3+ 이온의 농도에 비례하여 계 속 증가하여 Tb3+ 이온의 농도가 15 mol%일 때 최대값 을 나타내었으나 20 mol%에서는 급격히 감소하는 추세를 나타내었다. 이 결과는 Tb3+ 이온이 도핑된 SrSnO3 형광 체에서 Tb3+ 이온의 몰 비가 증가함에 따라 f-d 전이에 의한 여기 신호의 세기가 감소하는 결과와 일치하였다.16)
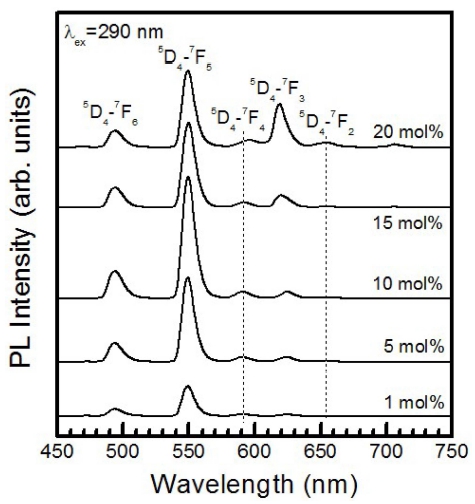
Fig. 5는 파장 290 nm로 여기시킨 Tb3+ 이온의 몰 비 변화에 따른 BaMoO4:Tb3+ 형광체 분말의 발광 스펙트 럼을 나타낸 것이다. Tb3+ 이온이 도핑되지 않는 모체 결정 BaMoO4의 자체 발광은 발생하지 않았으며, Tb3+ 이온의 몰 비에 관계없이 모든 형광체 분말에서 다섯 종 류의 발광 스펙트럼이 관측되었는데, 이 발광 신호들은 Tb3+ 이온의 전형적인 4f→4f 전이 신호임을 확인하였 다.17) 발광 세기가 제일 강한 550 nm에 피크를 갖는 녹 색 발광 스펙트럼, 상대적으로 발광 세기가 주 피크의 1/ 4 정도로 작은 493 nm에 피크를 갖는 청색 발광 신호, 주 피크에 비하여 발광 세기가 약 16배 작은 590 nm와 625 nm에 정점을 갖는 주황색과 적색 발광 스펙트럼, 제 일 세기가 약한 654 nm의 적색 발광 신호로 구성되었 다. 550 nm의 녹색 주 발광 스펙트럼은 Tb3+ 이온의 5D4 → 7F5 전이 신호, 493 nm의 청색 발광 스펙트럼은 5D4→ 7F6 전이, 590 nm의 주황색 발광 스펙트럼은 5D4→ 7F4 전이, 625 nm와 654 nm의 적색 발광 스펙트럼은 각각 5D4→ 7F3와 5D4→ 7F2 전이 신호이다.18) 상기의 형광체 는 근자외선(290 nm)을 여기 광원으로 사용하는 백색 LED 제작용 녹색 형광체로 응용할 수 있다. 여기서 주 목할 점은 Tb3+ 이온의 높은 에너지 준위인 5D3에서 방 출되는 파장 영역 320~400 nm의 발광 파장은 검출되지 않았다는 것이다. 에너지 준위 5D3와 5D4 사이의 에너 지 간격이 0.72 eV (~5800 cm−1) 정도로 크기 때문에 다 중 포논 이완(multiphonon relaxation)이 발생할 확률은 매우 적고, Tb3+ 이온의 농도가 증가함에 따라 에너지 준위 5D3에 위치하는 Tb3+ 이온과 바닥 준위에 위치하는 이온들 사이에 (5D3, 7F6)→(5D4, 7F0) 상호 이완(cross relaxation) 작용이 발생하여 5D3→ 7FJ 전이에 의한 320~ 400 nm 영역의 청색 발광은 억제되고, 그 대신에 5D4→ 7FJ 전이를 증가시키는 것으로 설명할 수 있다.19)
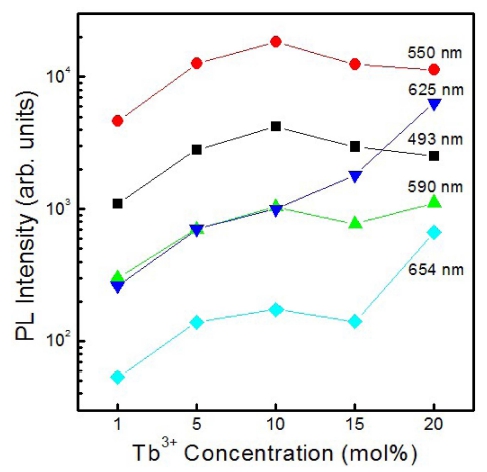
Fig. 6은 Tb3+ 이온의 몰 비 변화에 따른 BaMoO4: Tb3+ 형광체 분말의 발광 스펙트럼의 세기를 나타낸 것 이다. Tb3+ 이온의 몰 비가 1 mol%에서 10 mol%로 증 가함에 따라 다섯 종류의 발광 신호의 세기는 모두 점 차적으로 증가하여 10 mol%에서 발광 세기는 최대이었 고, Tb3+ 이온의 몰 비가 15 mol%와 20 mol%로 증가함 에 따라 5D4→ 7F3 (625 nm)와 5D4→ 7F2 (654 nm) 전 이에 의한 적색 발광 신호의 세기는 증가하였으나, 나 머지 세 종류의 발광 스펙트럼의 세기는 감소하는 경향 을 나타내었다. 전반적으로 발광 신호의 세기가 10~20 mol%에서 감소하는 현상은 발광 센터의 역할을 하는 활 성제 Tb3+ 이온의 몰 비가 임계 농도인 10 mol% 이상 으로 증가함에 따라 활성제 이온들 사이의 거리가 가까 워져서 이온들 사이에 교환 상호 작용(exchange interaction), 복사선 재흡수(radiation reabsorption), 다중극-다중 극 상호 작용(multipole-multipole interaction)이 발생하여 비복사선 에너지 전달(non-radiative energy transfer) 현 상에 의해 발광 세기가 감소하는 농도 소광(concentration quenching) 현상으로 해석할 수 있다.20) Tb3+ 이온의 몰 비가 증가함에 따라 나타나는 이러한 농도 소광 현상은 다른 모체 격자인 SrMoO4에서 관측된 결과와 유사하였 다.21) 그러므로 Tb3+ 이온이 도핑된 BaMoO4 형광체 분 말의 경우에 최적의 농도는 10 mol% 이었다. 상기의 세 가지 상호 작용 중에서 어떤 상호 작용이 우세한 역할 을 하는 지는 농도 소광 현상이 일어날 때 모체 결정 내에 위치하는 활성제 이온들 사이의 임계 거리(critical distance) Rc를 계산함으로써 규명할 수 있다. 일반적으 로, 임계 거리는 Blasse의 식 (2)를 사용하여 계산할 수 있다.22)
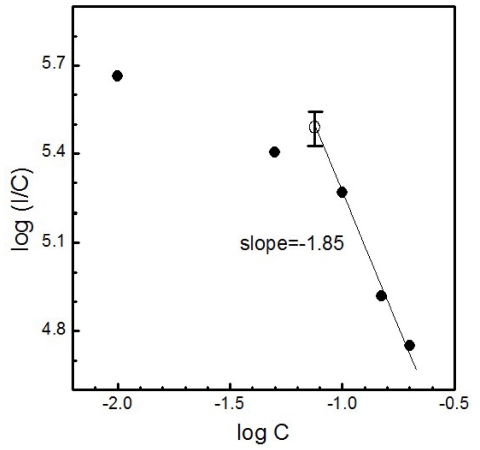
여기서 χc는 Tb3+ 이온의 임계 농도, V는 단위 셀의 체적, N은 단위 셀당 모체 양이온의 수이다. 본 연구의 경우에, BaMoO4 모체 결정의 체적과 단위 셀당 양이온 의 수는 V = 392.233 Å3, N = 4 이며, 농도 소광 현상이 발생하는 임계 농도 χc는 10 mol% 이므로, 상기의 값을 식(2)에 대입하면 임계 거리 RC의 값을 구할 수 있다: 즉, RC = 12.3 Å. 활성제 Tb3+-Tb3+ 이온 사이의 임계 거 리가 5 Å 보다 크기 때문에 이 경우에 농도 소광의 주 요 원인은 다중극-다중극 상호작용으로 판단된다.23) 일반 적으로, 다중극 상호 작용에는 세 종류, 즉 쌍극자-쌍극 자(dipole-dipole), 쌍극자-사중극자(dipole-quadrupole), 사 중극자-사중극자(quadrupole-quadrupole) 상호 작용이 있 으므로, Dexter가 제안한 활성제 이온의 농도와 발광 세 기 사이의 관계 식 (3)을 사용하여 어떤 상호 작용이 주 된 역할을 하는 지를 결정할 수 있다.24)
여기서 C는 활성제 이온의 농도, k와 β는 특정한 상 호 작용과 관련된 상수, s는 전기 다중극 상호 작용을 나타내는 인수로써, 숫자 6은 쌍극자-쌍극자, 8은 쌍극 자-사중극자, 10은 사중극자-사중극자 상호 작용을 나타 낸다.25) Fig. 7은 x축을 logC, y축을 log(I/C)로 취하여 데이터를 나타낸 것이다. 농도 소광 현상에 근접한 Tb3+ 이온의 농도가 1-20 mol%인 영역의 데이터를 가장 잘 맞 춘 직선의 기울기 값은 −1.85 ± 0.13 이므로 s의 값은 5.55 ± 0.39 이다. 이 값은 쌍극자-쌍극자 상호 작용의 이 론값 6에 근접하므로, 본 연구에서 Tb3+ 이온의 5D4→ 7F5 (550 nm) 전이에서 관측된 농도 소광의 주된 메카 니즘은 쌍극자-쌍극자 상호 작용에 기인함을 확인할 수 있다. 실험 결과를 종합하면, 본 연구에서 합성한 녹색 형광체의 경우에 Tb3+의 몰 비가 10 mol%일 때 최대 발 광 세기를 갖는 최적의 조건임을 알 수 있다.
4. 결 론
고상반응법을 사용하여 활성제 이온 Tb3+의 몰 비를 변 화시키면서 BaMoO4:Tb3+ 형광체 분말을 제조하였으며, Tb3+ 이온의 몰 비가 형광체 분말의 결정 구조, 미세 표 면의 형상, 여기와 발광, 농도 소광 현상에 미치는 영 향을 조사하였다. 형광체 분말의 결정 구조는 Tb3+ 이 온의 몰 비에 관계없이 정방정계이었으며, 결정 입자의 형상은 Tb3+ 이온의 몰 비에 따라 서로 다른 형태를 나 타내었다. Tb3+가 도핑된 BaMoO4 형광체 분말의 여기 스펙트럼은 290 nm에 피크를 갖는 반치폭이 넓은 여기 스펙트럼과 Tb3+ 이온의 4f-4f 전이 신호로 구성되었다. 파장 290 nm로 여기시켰을 때 형광체는 550 nm에 피크 를 갖는 강한 녹색 발광 신호를 방출하였다. Tb3+ 이온 의 농도가 증가함에 따라 녹색 발광의 세기는 점차 증 가하여 10 mol%에서 최대를 나타내었고, Tb3+ 이온의 농 도가 계속 증가하자 발광 세기는 점차적으로 감소하였 다. 이러한 농도 소광 현상은 쌍극자-쌍극자 상호 작용 에 의한 비복사선 에너지 전달로 발생함을 입증하였다. 본 연구의 결과로부터 최대 발광 세기를 갖는 녹색 형광체 제조를 위한 최적의 Tb3+ 이온의 농도는 10 mol%이며, 백색 발광 다이오드 제작을 위한 녹색 형광체로 응용 가 능함을 제시한다.