1. 서 론
시대의 변화에 따라 화석 연료의 고갈과 온실가스의 최 소화, 지속 가능한 에너지에 대한 요구가 증가하면서 여 러 방안들이 제시되어 왔다. 그 중에서도 리튬 이온 전 지(lithium ion battery)는 높은 에너지 밀도와 긴 수명을 가졌으며, 배기가스 배출이 없어 오늘날 스마트폰이나 노 트북, 전기차(EVs) 등에 전력을 공급하기 위한 중요한 에 너지 운반체로 여겨지고 있다.1-2)
그러나 리튬 이온 전지에 사용되는 유기계 액체전해질 이 대기 중의 산소나 열에 의해 발화나 폭발이 발생할 여지가 있고, 전해질의 기화에 의한 swelling 현상이 발 생해 안전성의 문제가 제기되고 있다.3) 이러한 발화 및 휘발의 문제는 리튬 이온 전지에 있어 가장 중요한 논 제 중 하나로 고려되고 있으며, 이를 위한 해결책으로 전고체 전지에 대한 연구가 주목받고 있다.
내부 유기계 액체전해질을 고체전해질로 대체한 전고체 전지는 액체전해질의 휘발성 및 가연성의 문제를 해소할 수 있으며, Li dendrite 성장을 억제하는 물리적 장벽 역 할을 하여 높은 안정성을 확보할 수 있다. 또한, 에너지 적 측면에서 전기화학적 창을 5 V (vs. Li/Li+)까지 증가 할 수 있으며, 액체전해질과 같이 Li metal anode와 반 응하지 않아 Li metal과 같은 대용량의 전극 소재를 사 용할 수 있어 고용량 확보가 가능하다.4) 그러나 계면 반 응과 낮은 이온전도도로 인해 상용화에 제한이 있으며 이를 개선하기 위한 연구가 진행되고 있다.
현재 전고체 전지 분야에서 가장 주목 받는 황화물계 물질은 10-2~ 10-3 S/cm 높은 이온 전도 특성을 지니고 있다. 그러나 주원료인 황화리튬(Li2S)의 가격이 높고, 밀 도가 커서 전고체 전지를 기반으로 하는 모빌리티의 중 량을 높이게 된다.5) 이 부분을 고려하여 상대적으로 가 벼우면서 저렴한 리튬계 수소화물에 주목하였다. 현재 리 튬계 수소화물 기반 고체 전해질은 여러 연구를 통해 10-3 S/cm 이상의 높은 이온전도도를 갖는 물질들도 발 견되고 있어 높은 연구 가치를 지니고 있다.6) 그러나 전 반적으로 상온에서 다른 고체 전해질 물질들에 비해 상 대적으로 낮은 이온전도도와 높은 계면 저항을 갖기 때 문에 이를 개선하기 위한 연구가 진행되고 있다.7,8)
본 연구에서는 리튬계 수소화물질 중 lithium hydride (LiH)에 대한 연구를 진행하였다. LiH는 Li+와 H-가 반 복적으로 구성된 입방(cubic) 구조를 갖는 물질로, 0.78 g/cm3의 낮은 밀도를 가지고 있어 경량형 배터리 연구 에 잠재력을 지닌 물질이라고 판단된다.9) 이번 연구에서 는 LiH의 EIS 분석을 통해 LiH의 이온 전도 특성을 분 석하고, 물질의 이온전도도를 향상시키기 위해 고분자 물 질과 결합한 복합 전해질을 형성하여 특성 변화 여부를 관찰하였다. 고분자 물질로는 우수한 전기화학적 및 열 적 안정성을 지니고 있는 PVDF를 선정하였다.10)
추가적으로 전해질 물질의 열 안정성을 분석하기 위해 열 전도 특성에 대한 연구도 진행하였다. 리튬 이온 전 지의 전기화학적 성능, 전하 수용도, 전력 및 에너지 성 능, 주기 수명 등이 작동 온도에 민감하기 때문에 전지 의 열적 관리(thermal management)는 수명 및 용량 저하 속도를 좌우하는 요인이 될 수 있어 열 안전성은 필수 적으로 분석해야 하는 요소이다.11) 특히, lithium hydride 계열 전해질이 다른 전해질 군에 비해 낮은 열 안전성 을 지닌다고 알려져 있어 더더욱 요구되는 공정이다.12)
2. 실험 방법
2.1. 액체 전해질 cell 제조
리튬계 수소화물질들의 이온전도도를 분석하기 위한 reference로 유기계 액체 전해질 기반의 리튬 전지를 제 조하였다. Cathode 전극을 제조하기 위해 활물질로 높 은 공칭 전압과 준수한 cycle 유지 특성, 충·방전 시의 구조적 안정성을 지닌 LiCoO2 (LCO)를 채택하였다.13) 전극을 제조하기 위해 polyvinylidene fluoride (PVDF, Aldrich)와 용매로 n-methyl-2-pyrrolidone (NMP, Aldrich) 을 1 :10 질량비로 비커에 넣고 플레이트 장비를 이용해 300 RPM으로 30 °C의 온도에서 1시간 혼합하였다. 이 후 LCO와 Carbon black (Timcal), PVDF를 막자사발을 이용해 각각 7:2:1의 질량비로 약 1시간동안 교반하였 다. 균일하게 도포하기 위해 혼합되는 전극의 농도는 NMP 용매로 조절하였다. 혼합된 cathode 혼합물을 Al foil에 film applicator를 통해 20 μm 두께로 균일하게 도 포한 후 진공 오븐을 통해 110 °C의 온도에서 3시간 건 조하였다. 건조된 전극을 직경 16 mm의 크기로 cutting 하고 전해질 1M LiPF6 in ethyl carbonate:diethyl carbonate (EC:DEC = 7:3 mass%)과 Poly Propylene (PP) 분리막, Li metal (Wellcos, 99.9 %)을 사용하여 cell을 제조하였다. cell 조립 과정은 Li metal의 산화를 방지 하기 위해 아르곤 분위기의 글로브박스에서 진행되었다 (H2O < 0.1 ppm).
2.2. 전해질 복합체 제조
LiH (aldrich, 95 %) 물질을 사용하여 리튬계 수소화물 의 특성을 분석하였다. PVDF와 NMP 용매를 1 :10 질 량비로 비커에 넣은 후 플레이트 장비를 이용해 두 물 질을 상온 300 RPM으로 1시간 동안 교반하였다. 그리 고 PVDF가 용해된 NMP 용매와 LiH를 일정한 질량비 로 hand-mixing하였다. 본 연구에서는 혼합 비율에 따른 이온 및 열 전도 특성의 변화를 비교 분석하기 위해 LiH와 PVDF의 비율을 9:1, 8:2, 7:3, 6:4의 질량비로 혼합하였다. 이 때, LiH가 습기에 반응할 가능성을 고 려해 아르곤 분위기의 글로브박스에서 PVDF 혼합물에 LiH 분말을 소량씩 혼합하여 용매와의 반응을 최소화하 면서 전해질 복합체를 합성하였다. 그리고 72시간 상온 건조를 통해 전해질 복합체를 제조하였다.
2.3. 고체 전해질 cell 제조
직경 14 mm stainless mold에 전해질 분말을 넣고 300 MPa의 압력으로 5분간 일축 가압하여 전해질 pellet 을 제조하였다. 이후 제조된 LiH 및 전해질 복합체의 양 면에 stainless metal을 접합하고 대칭 cell을 제조하였다.
2.4. 특성평가
복합 물질의 야금학적 특성을 분석하기 위해 X-ray diffraction (XRD) 및 Scanning Electron Microscope (SEM), Brunauer-Emmett-Teller (BET)분석을 진행하였 다. X-선 회절분석기(X-ray diffractometer [XRD], D8 Advance, Bruker, Billerica, MA, USA)를 사용해 결정 구조 및 상을 분석하였다. X선 target으로는 1.5405 Å 의 Cu Kα를 사용하고, scanning speed는 5 deg/min, scanning range는 2 0 ~80 ° 였다. 또한, 전해질 복합체의 조성비에 따른 시료의 표면 형상 변화를 관찰하기 위해 주사전자현미경(scanning electron microscopy [SEM], Quanta-400, FEI Company, Hillsboro, OR, USA)을 사 용해 표면 형상을 분석하고, 비표면적 측정 장비(brunaueremmett- teller surface analysis [BET], Micromeritics 3- Flex, Micromeritics, Norcross, GA, USA)를 통해 시료 의 표면 변화가 전도 특성에 미치는 영향을 확인하였다.
전해질 물질들의 이온전도도를 분석하기 위해서 전기 화학적 임피던스 측정 장비(Electrochemical Impedance Spectroscopy [EIS], nstat, IVIUM, Nederland)를 사용 해 1 MHz ~ 0 .1Hz의 주파수 범위와 진폭 10 mV의 조 건에서 EIS 측정을 진행하였다.
열 안전성 분석을 위해 LFA (laser flash analysis)방법으 로 물질의 열 확산 특성을 분석하였다. 열 전도도를 계산 하기 위해 열 확산도 측정장비(laser flash analysis [LFA], TC-9000H, ULVAC, Japan)를 통해 열 확산도 측정을 진 행하였고, 이를 위해 시료를 직경 10mm stainless mold에 넣어 2 0 0MPa로 압축 후 양면에 Li metal을 접합해 같은 압력으로 5분간 압축하여 두께가 1 mm 이내의 pellet을 제 조하였다. 분석 조건은 일반적으로 전지가 사용되는 온도 인 3 0 0~ 40 0K의 온도 범위에서 분석을 진행하였다.
3. 결과 및 고찰
Fig. 1은 LiH와 복합물의 XRD 분석 결과를 나타내고 있다. LiH의 경우 2θ의 peak 위치가 θ = 44°에서 강하 게 나타났으며, 이론적인 수치와 거의 동일한 것을 확 인하였다.14) LiH의 결정구조는 International Centre for Diffraction Data (ICDD)를 통해 이론과 같은 입방(cubic) 구조를 가지는 것을 확인할 수 있었다. 반면 PVDF와 합성한 전해질 복합체의 경우 θ = 28 ~ 37° 부근에서 다 수의 Li2CO3와 LiOH의 peaks를 관찰할 수 있었다. 형 성된 LiOH와 Li2CO3의 결정구조를 ICDD를 통해 분석 한 결과 각각의 물질들이 정방정(tetragonal)과 단사정 (monoclinic) 구조를 갖는 것을 확인하였다. 이러한 부산 물의 형성은 보통 LiH가 낮은 습도의 대기와 반응해 LiOH나 Li2O, Li2CO3 등을 형성한다. 이러한 변화는 앞 서 언급한 것과 같이 복합체 제조 과정에서 LiH가 NMP 용매에 민감하게 반응해 부산물이 형성된 것으로 판단 된다.15) 이러한 부반응에 의해 형성된 Li2CO3는 10-6 S/ cm의 낮은 이온전도도를 갖고, Li metal과의 계면 호환 성을 저하시킬 수 있어 복합체의 이온전도도 저하를 야 기할 수 있다.16,17)
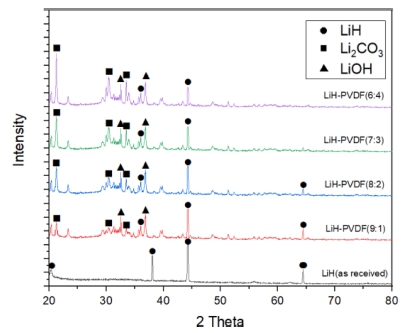
Fig. 1
XRD patterns of LiH and LiH-PVDF composite electrolytes [LiH(cubic) : ●, Li2CO3(monoclinic) : ■, LiOH(tetragonal) : ▲].
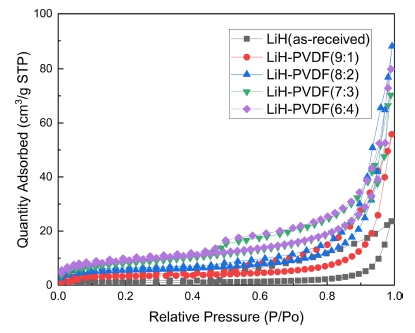
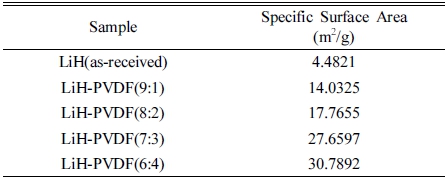
Fig. 2는 LiH와 복합체 형성에 따른 비표면적의 변화 를 나타내는 그래프이다. 고체 전해질 물질들의 질소에 대한 흡착 거동을 나타내며, 분석을 통한 비표면적 수 치를 Table 1에 정리하였다. 비표면적을 비교한 결과, PVDF의 질량비가 증가할수록 비표면적이 증가하는 거 동을 보였으며, 특히 7:3 (mass%) 비율로 혼합한 전해 질 복합체에서 급격한 비표면적의 증가를 확인할 수 있 었다. 이러한 변화는 복잡한 사슬 형태를 가진 PVDF의 구조가 NMP와 같은 용매에 용해 후 구조를 형성할 때 sponge-like와 같은 복잡한 다공성 구조를 갖게 되어 증 가한 것으로 보인다.18) 높은 비표면적을 가진 다공성 구 조를 형성하게 되면 내부 리튬 이온의 이온전도도를 감 소시키거나 기계적 결함을 유발할 수 있어 복합체의 형 성이 리튬 이온의 전도도가 감소할 수 있다.19)
복합체의 구조적 변화는 Fig. 3의 SEM 표면형상 이 미지를 통해 명확히 알 수 있었다. LiH의 경우 약 1~3 μm 정도의 미세결정들이 관찰된 것에 비해 전해질 복 합체는 1 μm 이하의 결정의 수가 증가한 것을 확인할 수 있었다. 또한, 부분적으로 군집체가 형성된 것을 관 측할 수 있었으며, 이러한 변화는 혼합비가 7:3, 6:4일 때 두드러지게 관찰되었다. 10,000배의 SEM 이미지[Fig. 3(f)-(j)]를 비교 분석한 결과 형성된 군집체는 미세기공 으로 이루어진 구조를 하고 있는 것을 알 수 있었다. 이 러한 구조적 변화는 BET 데이터와 연관 지어볼 때 합 성 과정에서 PVDF가 구조체 역할을 하면서 거대한 다 공성 구조를 형성해 비표면적이 증가하게 된 것으로 확 인된다. 다공성의 구조는 리튬 이온의 이동 경로를 단 축시킬 수 있어 이온전도도가 향상될 수 있다.

Fig. 3
SEM image of (a) LiH (× 5,000), (b) LiH-PVDF (9:1, × 5,000), (c) LiH-PVDF (8:2, × 5,000), (d) LiH-PVDF (7:3, × 5,000), (e) LiH-PVDF (6:4, × 5,000), (f) LiH (× 10,000) (g) LiHPVDF (9:1, × 10,000), (h) LiH-PVDF (8:2, × 10,000) (i) LiHPVDF (7:3, × 10,000), and (j) LiH-PVDF (6:4, × 10,000).
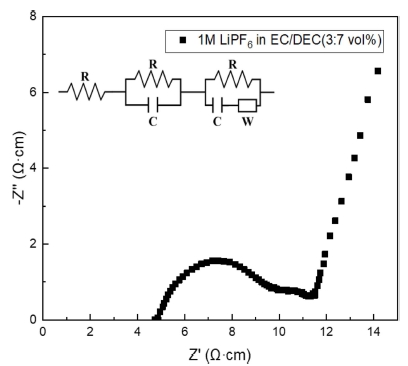
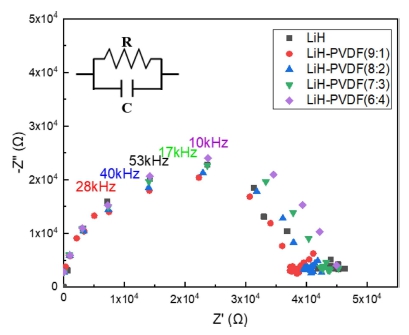
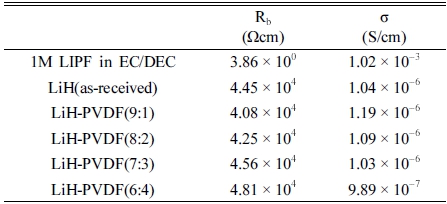
Fig. 4와 Fig. 5은 제조된 cell들의 Nyquist plots이다. Nyquist plots의 임피던스 성분은 주파수 대역에 따라 다 르게 나타나며, 분석된 전해질의 bulk resistance를 통해 각각의 이온전도도를 Eq. (1)을 통해 계산하였다.
여기서 σ는 전해질의 이온전도도를 나타내며, Rb는 전해 질의 저항, A는 전해질의 단면적, L은 전해질의 두께를 의미한다.20) 측정된 수치는 Table 2에 정리하였다.
측정된 1M LiPF4 in EC/DEC(3:7)의 경우 약 3.86 Ωcm의 낮은 저항이 측정되었으며, Eq. (1)을 통해 1 .0 2 × 10-3 S/cm의 높은 이온전도도를 갖는 것을 알 수 있 었다. 이에 비해 LiH는 4.0 8 × 104 Ωcm의 높은 저항이 확인되어 1.19 × 10-6 S/cm의 낮은 이온전도도가 계산되 었다. 9:1, 8:2 비율의 복합체의 경우 계산을 통해 이온 전도도가 개선된 것을 확인하였다. 이러한 거동은 비정 질 상태의 고분자 사슬 거동(polymer chain motion)과 이동성 Li+의 농도와 연관성이 있다. PVDF의 주사슬이 음이온 안정성에 대한 가속화 효과와 높은 유전상수 (ε = 8.4)를 가진 electron-withdrawing group에 해당하기 때문에 리튬 금속 염의 이온화를 촉진하고 리튬 이온의 농도 및 이동율(migration rate)을 향상시켜 물질의 이온 전도도를 증가시킬 수 있다고 보고되고 있다.21) 7:3, 6:4 비율의 복합체는 LiH의 감소로 Li+의 농도가 줄어 이온 전도도가 감소한 것으로 판단된다.
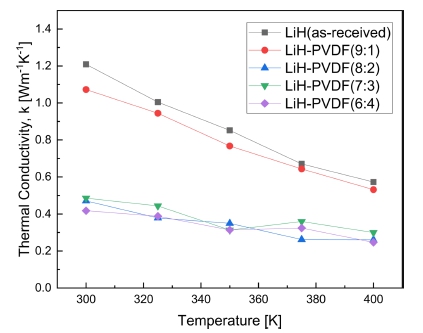
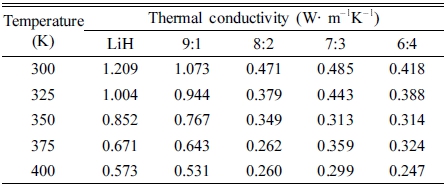
Fig. 6은 LiH와 전해질 복합체에 대한 열전도도 분석 결과를 나타내고 있다. 열전도도는 LFA 방법을 통해 열 확산도를 계산하고 Eq. (2)의 식으로 계산하였다.
여기서 k는 열전도도, α는 열 확산도, ρ는 밀도, CP는 비열을 의미한다.22) 각각의 데이터는 비교를 위해 Table 3에 표시하였다. 전체적으로 온도의 증가에 따라 감소하 는 경향을 볼 수 있었다. 고체의 경우 자유 전자와 격 자 진동(phonon)에 의해 열 전도가 이루어지는데, phonon 에 의한 전도가 지배적인 경우 온도의 증가에 따라 열 전도도가 점차 감소하는 경향을 지닌다.23) 보통 이러한 경향은 세라믹 등에서 주로 일어나는데, 이러한 사실은 LiH가 세라믹과 같은 열적 거동을 한다는 것을 알려준 다. LiH의 경우 상온에서 약 1.209 W∙m-1K-1의 열 전 도도를 갖는 것을 알 수 있었다. 이러한 수치는 lithium phosphorus oxynitride (LiPON)의 1.4 W∙m-1K-1보다 조 금 낮은 안정성을 보여준다. 그러나 PVDF의 상대적인 비율이 증가할 수록 열 전도도가 급격히 감소하였고, LiH와 PVDF의 조성이 8:2, 7:3, 6:4 일 때 sintered Li7La3Zr2O12 (LLZO)의 0.47 W∙m-1K-1와 유사한 열 전 도도를 갖는 것을 알 수 있다.24) 열 전도도는 물질내 원 자구조가 무질서하거나 불규칙할수록 phonon scattering이 증가하여 감소하는데, SEM 이미지상에서 전해질 복합체 합성에 따라 불규칙한 비정질 상으로 바뀐 것을 고려할 때 복잡한 고분자 구조형성에 의한 phonon scattering의 증가로 물질의 열 전도도가 저하된 것으로 보인다. 결과 적으로 물질의 열 전도도 변화를 고려할 때 LiH-PVDF (9:1) 복합체가 가장 열 안정성이 높다고 판단된다.
4. 결 론
저렴하고 밀도가 낮은 LiH의 고체 전해질로의 가능성 을 분석하기 위해 LiH 및 다른 비율의 LiH-PVDF 복합 체를 제조하여 이온전도도 및 열전도도 변화를 분석하 였다. 그 결과 다음과 같은 결과를 얻을 수 있었다.
1) 복합재료에 대한 XRD 분석 결과, LiH의 peak 변 화 및 결정구조를 확인할 수 있었다. 또한, Li2CO3 등 의 부산물의 peak 형성을 통해 LiH가 NMP용매와 높은 반응성을 보인다는 것을 알 수 있었다. 이러한 부반응 에 형성된 Li2CO3의 경우 이온전도도 감소와 계면 호환 성 저하 등의 원인이 될 수 있다.
2) SEM 및 BET 분석을 통해 LiH 내에서 1~3μm 크기의 비정질 상의 입자들을 관찰할 수 있었으며 약 4.4821 m2/g의 비표면적을 갖는 것을 확인할 수 있었다. 복 합체의 비율이 증가함에 따라 1 μm 이하 크기의 미세 결정 수가 증가하였고, 이와 동시에 비표면적이 급격히 증가하는 것을 확인하였다. 이러한 변화는 PVDF와 합 성을 통한 미세 다공성 구조를 갖게 된 것으로 판단된 다. 이러한 구조는 리튬 이온의 경로를 단축할 수 있지 만, 기계적 결함의 원인이 되어 오히려 이온전도도를 저 하시킬 수 있다.
3) EIS 분석으로 LiH가 4.0 8 × 104 Ωcm의 높은 저항 이 측정되었고, 결과적으로 1.19 × 10-6 S/cm의 낮은 이 온전도도가 계산되었다. LiH와 PVDF의 질량비가 9:1, 8:2인 경우 PVDF에 의해 리튬 농도가 증가하게 되어 이 온전도도가 상승하였고, 7:3, 6:4의 경우 LiH의 상대적 인 비율 저하로 이온전도도가 감소하였다.
4) 열 안정성 분석을 위한 LFA 분석을 통해 물질들 의 열 전도도를 분석할 수 있었다. LiH는 1.4 W∙m-1K-1 의 열 전도도를 갖는 LiPON보다 조금 낮은 1.209 W∙m-1 K-1의 값을 얻을 수 있었지만, 복합체 형성으로 급격히 감소해 LLZO와 같은 0.47 W∙m-1K-1 이하의 수치를 얻 었다. 열 전도도가 온도의 증가함에 따라 감소하는 이 유는 phonon에 의한 열의 전도가 지배적으로 나타나는 것으로 보이며, PVDF의 질량비에 따라 복잡하고 무질 서한 구조가 형성되어 phonon scattering이 증가해 열 전 도도가 감소한 것으로 보인다.
5) 결과적으로 LiH를 PVDF와 일정 질량비로 합성하 여 낮은 이온전도도를 개선할 수 있었고 준수한 열 안 전성을 확보하였지만, 여전히 낮은 이온전도도로 인해 상 용화에 한계가 있으며, 이를 위한 후속 연구가 이루어 져야 할 필요가 있다.