1. Introduction
전기를 동력으로 하는 수 전해 기술은 그린 수소 생 산을 통해 탄소 중립에 기여할 수 있을 것으로 기대된 다.1) 전기촉매는 수 전해에 요구되는 전기화학 반응의 과 전위를 낮추는 기능을 하며, 지구상의 풍부한 물질을 활 용해 고효율, 고안정성의 전기촉매를 대면적으로 합성 하는 것으로 수 전해 기술의 상용화를 실현할 수 있다.2) 하지만 환원 전극에서 일어나는 빠른 수소 발생 반응 (hydrogen evolution reaction, HER)에 균형을 맞출 수 있는 산화 전극 및 산소 발생 반응(oxygen evolution reaction, OER) 촉매 개발은 아직 도전적인 과제로 남아 있다. OER은 4번의 양성자를 동반한 전자 전달(protoncoupled electron transfer)로 구성되어 본질적으로 느린 반응 역학을 가지고 있으며,3) OH*와 OOH* 배위결합에 요구되는 흡착 에너지는 선형적인 관계 (linear scaling relationship)를 가지고 있어 촉매적 성능 향상이 제한되 는 문제가 있기 때문이다.4)
격자 산소 기작 (lattice oxygen mechanism, LOM)은 격자 산소의 활성화를 통해 O * -O* 결합이 가능하여 기 존의 흡착질 발생 기작(adsorbate evolution mechanism, AEM)이 가진 이론적 한계를 극복할 해결책으로 제안되 고 있다.5) LOM은 양성자를 동반하지 않는 전자 전달 (non-concerted proton electron transfer)을 포함하여 빠 른 반응 역학을 가지며, 높은 에너지를 요구하는 OOH* 배위결합을 생략할 수 있다.6) 그러나 활성화된 격자 산 소는 OER의 반응물로 참여하면서 촉매 구조 내부에 산 소 결함을 형성하기 때문에 촉매 성능 저하를 유발할 수 있어 안정한 산소 촉매 디자인에 대한 연구가 필요하다.7)
본 연구는 셀레늄 (Se)이 니켈철 (옥시)수산화물(NiFe (oxy)hydroxide, NiFe)의 격자 산소 활성화와 전기화학적 안정성을 효과적으로 향상시킬 수 있음을 검증하였다. 촉 매는 전기화학 증착법으로 합성되었으며, 증착용 용액의 조성을 조절하여 Se이 포함된 NiFe (NiFeSe)를 제작하 였다. Se의 도입으로 NiFe의 전이 금속은 환원된 원자 가 상태를 보였으며, 활성화된 격자 산소종인 과산화물 (O-/O22-)이 증가된 전자구조를 보였다. 상기 전하의 비 편재화에 의하여, NiFeSe는 향상된 OER 성능을 보였으 며, LOM이 안정화된 것을 확인하였다.
2. Experimental
2.1. 용액의 준비
Ni(NO3)2·6H2O, Fe(NO3)2·9H2O, CH4N2O, SeO2, 그 리고 C2H7NO는 Sigma Aldrich에서 구입되었다. 1 mM 의 Ni(NO3)2·6H2O와 Fe(NO3)2·9H2O, 그리고 3mM의 CH4N2O가 2mL의 C2H7NO를 포함하는 40 mL D. I water에 용해되었고 NiFe의 전기화학 증착에 사용되었 다. NiFeSe 제작을 위한 용액은 상기 용액의 준비와 같 지만, 3 mM의 CH4N2O 대신 2mM의 CH4N2O와 1mM 의 SeO2가 용해되었다.
2.2. 전기화학 증착
NiFe와 NiFeSe의 전기화학 증착은 1 cm2의 니켈 폼 (Ni foam)을 작업전극과 상대전극으로 하는 2 전극 시 스템에서 상기 용액들을 각각 전해질로 활용하여 수행 되었다. 작업전극에는 40 °C에서 2분 간 +50 mA cm-2 의 전류밀도를 가함으로써 전극 표면의 친수성을 향상 시켰다.8) 다음으로 작업전극에 10분 간 -50 mA cm-2의 전류밀도를 가하여 소재를 Ni foam 표면에 환원 증착 하였다. 전기화학 증착 후, 작업 전극으로 사용된 Ni foam은 D. I water로 충분히 세척하여 60 °C에서 건조 되었다.
2.3. 소재 분석
NiFe와 NiFeSe의 결정성은 X-ray diffractometer (XRD, New D8-Advance, Bruker-AXS)를 분석되었다. 소재 표면 과 원소 분포의 분석을 위하여 field emission scanning electron microscope (FE-SEM, JSM-7800F Prime, JEOL Ltd)와 장착된 electron dispersive X-ray spectroscope (EDS)가 활용되었다. 촉매 소재의 화학 결합 및 원자가 상태 분석을 위하여 X-ray photoelectron spectroscope (XPS, Versaprobe II, ULVAC-PHI)가 활용되었다.
2.4. 전기화학 평가
전기화학 측정은 상온의 1 M KOH 전해질에서 정전 위기(PGSTAT302N, Metrohm, Autolab)를 통해 수행되 었다. NiFe 또는 NiFeSe를 작업전극으로 하고, Pt sheet (1 cm2)를 상대전극, 그리고 Hg/HgO를 기준전극으로 하 는 3전극 시스템이 활용되었다. 모든 전위는 reversible hydrogen electrode (RHE)로 변환하여 사용되었다. 성능 평가에는 귀금속 촉매 IrO2 (Sigma Aldrich)를 활용하였 다. 전기화학 임피던스 분광법(electrochemical impedance spectroscopy, EIS)은 1.45 V versus RHE에서 10,000 Hz부터 0.1 Hz까지 측정되었다.
3. Results and discussion
Fig. 1(a)은 NiFe와 NiFeSe 전기화학 촉매 소재의 제 작과정을 나타낸 모식도이다. Ni와 Fe의 소스양과 전기 화학 증착 조건은 일정하게 유지하고, CH4N2O와 SeO2 의 소스양을 조절하여, NiFe와 NiFeSe 촉매가 제작되었 다. XRD 분석을 통해 전기화학 증착 방법으로 제작된 NiFe와 NiFeSe 촉매는 결정성의 픽이 뚜렷하게 관찰되 지 않았음을 확인하였다[Fig. 1(b)]. 또한 NiFeSe 촉매 입자는 수 ~ 수십 nm 크기로 형성 되었음을 FESEM 분 석을 통하여 확인하였다[Fig. 1(c)]. 일반적으로 전기화학 증착은 전위(또는 전류)가 높을수록, 또는 시간이 길어 질수록 선명한 결정질과 큰 입자 크기를 갖게 된다.9) 따 라서, 상기 분석을 통해 본 연구의 전기화학 증착 조건 은 비정질의 니켈철 (옥시)수산화물 나노 입자가 형성될 수 있는 충분히 낮은 크기의 전류와 짧은 시간임을 확 인하였다.10) EDS image는 Ni, Fe, O, Se 원소가 Ni foam 표면에 균일하게 분포하고 있음을 보여주고 있다.
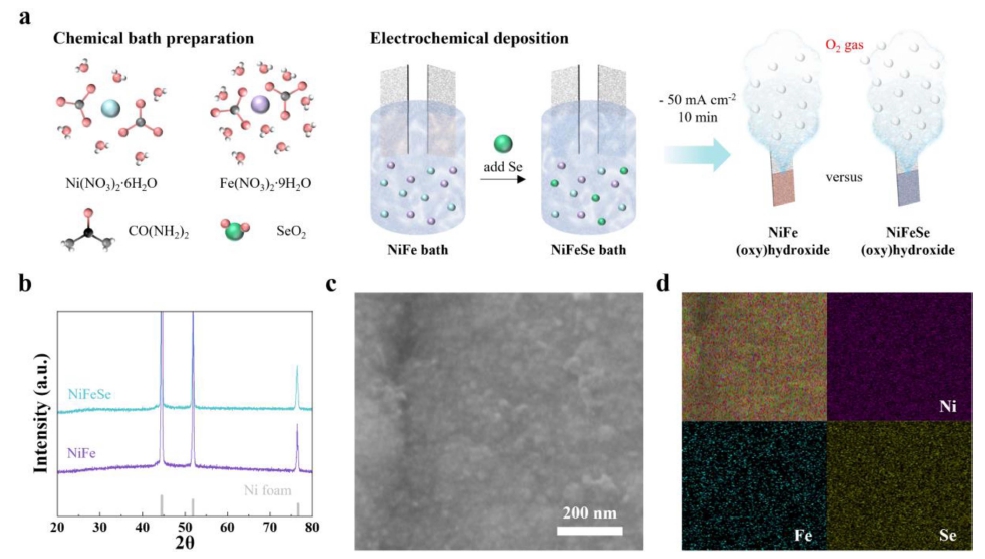
Fig. 1
(a) Schematics of catalysts preparations. (b) X-ray diffraction patterns of prepared samples. (c) Field emission scanning electron microscope and (d) energy dispersive X-ray spectroscope images of NiFeSe.
NiFe와 NiFeSe 촉매의 화학 결합과 원자가 상태 분 석을 위하여 XPS 분석이 수행되었다(Fig. 2). Ni의 2p3/ 2와 2p1/2 스펙트라는 각각 855.8과 873.3 eV의 결합 에 너지에서 확인되었으며, Se의 도입으로 약 0.8 eV의 결 합 에너지가 감소한 것이 확인되었다[Fig. 2(a)].11) 이와 유사하게, Fe의 2p3/2와 2p1/2 스펙트라는 각각 710.3과 723.4 eV의 결합 에너지에서 확인되었으며, Se의 도입으 로 각각 약 1.1와 1.2 eV의 결합 에너지가 감소하였다 [Fig. 2(b)].12) 상기 결합 에너지의 변화는 Se이 O의 위 치를 대체하면서 원자가 상태가 환원된 것을 나타낸 결 과이다.11,12) O 1s 영역에서, 금속-산소 결합(M-O), 산소- 수소 결합(O-H), 그리고 과산화종(O-/O22-)을 나타내는 결 합이 확인되었다[Fig. 2(c)].13) 각 결합 에너지는 Se의 도 입으로 약 0.5 eV의 결합 에너지 증가를 보였으며, 과산 화종의 양이 상당히 증가하였음이 확인되었다. 이는 Se 이 금속의 위치를 대신하면서 산소로의 전자 전달이 충 분히 되지 않은 것을 의미하는 결과이다. 이와 같은 결 과와 상응하게 NiFeSe의 Se 3d 영역에서는, 금속-Se 결 합을 나타내는 Se의 3d5/2와 3d3/2 스펙트라가 각각 55.3 과 56.6 eV의 결합 에너지에서 확인되었으며, Se-산소 결 합을 나타내는 SeOx 스펙트럼이 59.3 eV에서 확인되었 다[Fig. 2(d)].11,12)
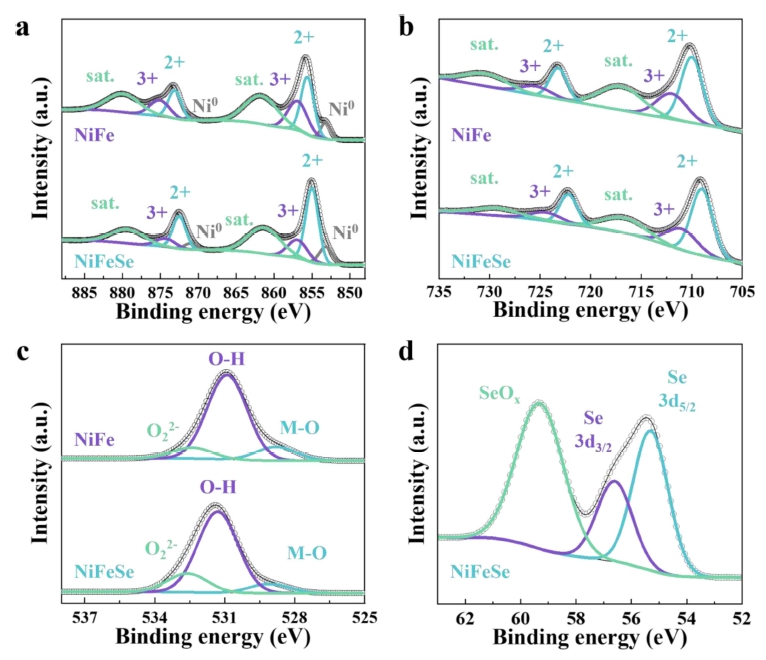
Fig. 2
X-ray photoelectron spectroscope spectra in (a) Ni 2p, (b) Fe 2p, (c) O 1s, and (d) Se 3d regions, respectively.
NiFe와 NiFeSe의 OER 평가는 상온에서 3전극 시스 템을 활용하여 염기성 전해질(1 M KOH) 분위기에서 수 행되었다[Fig. 3]. 성능은 5mVs-1의 주사 속도의 순환 전류법(cyclic voltammetry)으로 평가되었으며, 전위는 RHE 스케일로 변환되었다. NiFeSe는 전류 밀도 10, 그 리고 100mAcm-2를 얻는데 199와 223 mV의 과전위를 요구하였고, 이것은 NiFe (217, 272 mV)와 IrO2 (260, 337 mV) 대비 낮은 값이었다[Fig. 3(a)]. 또한, 전류 밀 도 10 mA cm-2에서 얻은 NiFeSe의 Tafel 기울기는 32.4 mV dec-1로 NiFe (40.1 mV dec-1)와 IrO2 (52.5 mV dec-1) 보다 작은 값이었다[Fig. 3(b)]. EIS로 분석된 전하 전달 저항(charge transfer resistance)은 NiFeSe, NiFe, IrO2가 각각 0.41, 1.07, 1.29 Ω으로 확인되었다[Fig. 3(c)]. 추가 로, NiFe와 NiFeSe는 전극 표면의 이중층에서의 전기용 량 측정을 통해 전기화학적 활성 표면적(electrochemical active surface area, ECSA)이 계산되었다. 이중층에서의 전기용량은 주사속도를 5mVs-1에서 50 mV s-1까지 변화 시키며 얻어진 전류의 변화로 계산되었다[Fig. 3(d,e)]. NiFeSe와 NiFe의 전기용량은 각각 3.33과 0.61mF cm-2 로 확인되었으며, ECSA 값은 각각 83.25와 15.25 cm2 로 계산되었다 [Fig. 3(f)].14) 상기 평가들로, NiFeSe는 Se의 도입으로 전기화학적 특성이 매우 향상되었음이 확 인되었다.
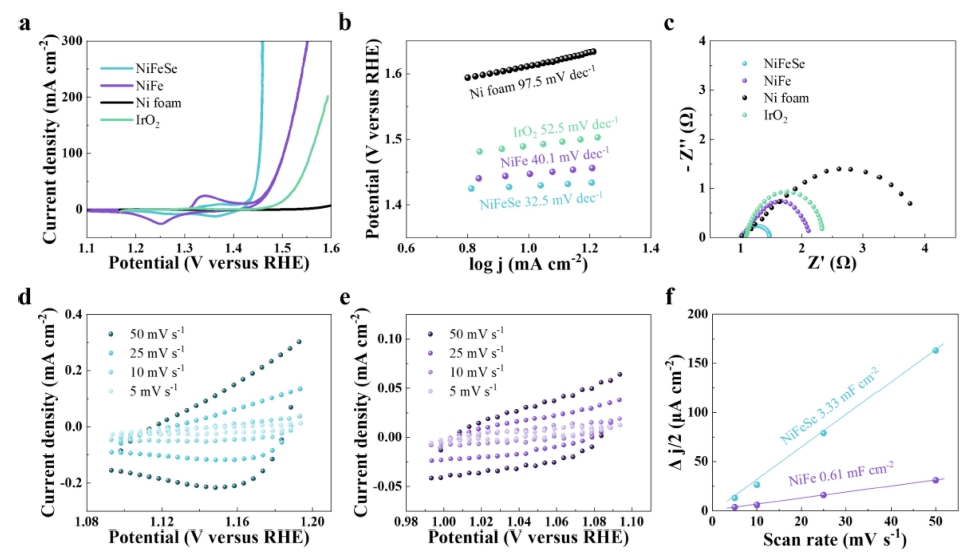
Fig. 3
Electrochemical measurements. (a) Polarization curves of prepared samples. (b) Tafel plots around the current density of 10 mA cm-2. (c) Electrochemical impedance spectroscopy (EIS) data of prepared samples. Cyclic voltammetry curves of (d) NiFeSe, and (e) NiFe in non-Faradaic region. (f) Summary of obtained currents with respect to scan rate. The gradient in the plot indicates double layered capacitance.
Se이 격자 산소 활성화에 미치는 영향을 분석하기 위 하여, pH에 따른 OER 활성도가 평가되었다. RHE는 pH 에 따른 전위의 변화가 보정된 scale로, 양성자를 동반 하는 전자 전달 경로를 따른다면 pH에 의존하지 않는 OER 성능을 보인다. 하지만 LOM은 양성자를 동반하지 않는 전자 전달을 포함하기 때문에 표면 전하의 불균형 으로 OH- 의 친화도가 증가하게 되어 RHE scale에서 pH 에 의존하는 OER 성능을 보이게 된다.5,6,13) NiFeSe는 RHE scale에서 pH가 증가함에 따라 성능이 급격하게 증 가하는 양상을 보였으며[Fig. 4(a)], pH 의존도는 1.55 decade pH-1로 NiFe (0.37 decade pH-1) 대비 4배 이 상 증가하였다[Fig. 4(b)]. 상기 결과는 Se 도입에 따른 전하의 비편재화로 NiFeSe의 격자 산소가 효과적으로 활 성화된 것을 보여주는 결과이다[Fig. 4(c)]. 또한, 전이 금 속은 환원된 원자가 상태에서 OER 배위결합 과정을 수 행할 수 있어 전기화학적인 안정성이 향상될 수 있다.15) NiFe와 NiFeSe는 전류 밀도 100 mA cm-2에서 장시간 안정성이 측정되었다. NiFe는 45시간 이후 성능이 크게 저하되었으나, NiFeSe는 100시간 동안 안정한 모습을 보 였으며, 100시간 후, 전류 밀도 100 mA cm-2를 얻는데 요구되는 과전위가 약 17 mV 만큼의 작은 증가폭을 보 였다.
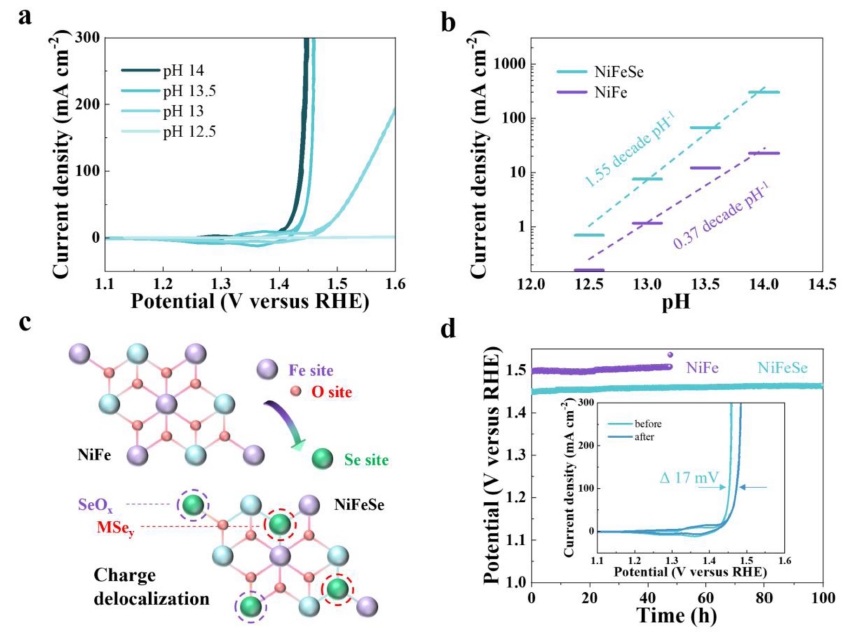
Fig. 4
(a) pH dependent activity of NiFeSe. (b) Summary of obtained currents at 1.45 V versus RHE with respect to pH. (c) Schematic of influence of Se introduced into NiFe. (d) Chronopotentiometry curves at the current density of 100 mA cm-2. Inset displays polarization curves of NiFeSe before and after stability test.
4. Conclusions
Se의 도입으로 니켈철 (옥시)수산화물의 격자 산소 활 성화와 전기화학적 안정성이 향상되는 효과를 조사하였 다. Se은 니켈철 (옥시)수산화물 구조에서 금속 또는 산 소의 위치를 대체하면서 SeOx와 금속-Se 결합을 형성하 였으며, 그 결과, 전이 금속은 환원된 원자가 상태를 나 타냈으며, 산소에 전자가 충분히 전달되지 않아 과산화 종(O-/O22-)이 증가하였음을 보였다. 전하의 비편재화로 NiFeSe는 향상된 전기화학적 특성을 보였으며, 격자 산 소의 활성도가 크게 증가하였음을 확인하였다. 또한, 전 이금속은 환원된 원자가 상태에서 배위결합 과정을 수 행할 수 있어 전기화학적 안정성이 향상 될 수 있다는 것을 증명하였다. 본 연구는 Se을 통한 전하의 비편재 화와 이에 따른 격자 산소의 활성화가 OER에 미치는 영 향을 분석하였으며, 이를 활용한 전기촉매 디자인 및 반 응 메커니즘 연구에 기여할 수 있을 것으로 기대된다.




