1. 서 론
2. 실험 방법
2.1. (TiO2-CeO2)/Sr4Al14O25:Eu2+,Dy3+ 혼성 복합소재 제조
2.2. 재료 특성 분석 및 광분해 반응 측정
3. 결과 및 고찰
3.1. 재료 특성
3.2. 광촉매 반응 특성
4. 결 론
1. 서 론
지속적인 환경오염으로 인해 다양한 환경 정화 기술이 개발되고 있는 가운데, 광촉매를 이용한 유해물질 저감 방법은 유망한 기술 중 하나로 꼽힌다. 광촉매는 조사된 광의 광자(photon)를 통해 valence band에 있는 전자(e-)가 conduction band로 전이된다. 이때 반응성이 매우 높은 정공(h+)도 함께 생성되고, 공기 중 수분과 반응하면서 형성된 하이드록시 라디칼(・OH) 이 강력한 산화제 역할을 하여 자일렌, 벤젠, 톨루엔과 같은 휘발성 유기화합물(VOCs)을 물과 탄소가스 등으로 분해한다.1) 본 실험에서 유해물질 광분해 성능 분석을 위해 사용한 톨루엔은 페인트나 접착제 등을 다루는 작업 환경에서 자주 발생하며, 장시간 노출될 경우 근력 저하, 환각, 뇌 손상 등이 발생하기 때문에 이를 제거할 필요가 있다.2,3) 광촉매의 유기오염물질 분해 효과는 이미 많은 연구 결과를 통해 검증되었으며, 많은 연구자들은 더 나아가 고성능, 고효율의 광촉매 소재를 개발하는 데에 노력하고 있다. 가장 널리 사용되고 있는 광촉매 소재는 이산화티타늄(TiO2)이며, 이는 광을 연속적으로 조사하여도 화학적 변형이 잘 일어나지 않고, 합성에 용이하며 인체에 미치는 해가 적은 친환경 소재이며, 또한, 값이 저렴하여 경제적으로도 유리한 소재로 알려져 있다. 그러나 순수 TiO2만을 사용하기에는 3.2 eV의 넓은 에너지 밴드갭(band gap) 때문에 활용 가능 범위가 태양광의 4 %에 불과한 자외선에 국한되고, e-/h+ 재결합 속도가 다소 높은 특징으로 광분해 효율이 제한적인 단점이 있다. 이러한 한계를 극복하기 위해 다른 반도체와의 이종 접합(heterojunction) 설계가 필수 전략으로 많은 관심을 불러일으키고 있다.
한편, 발광물질인 축광체(long-persistent phosphor)는 외부 광으로부터 광자를 흡수하여 내부 에너지로 저장된 후, 외부 광원이 꺼진 뒤에는 다시 저장된 에너지를 빛으로 긴 시간동안 방출하는 특성을 지닌다. 특히, Alkaline earth aluminate계 축광체는 장시간 발광하는 특성을 지닌 발광 물질로서, 보라색(violet) 파장으로부터 녹색(green)의 넓은 발광 스펙트럼 범위를 가지며, CaAl2O4:Eu,Nd (blue color), SrAl2O4:Eu,Dy (green color), Sr4Al14O25: Eu,Dy (blue green color), BaAl2O4:Eu,Dy (yellow green color) 등이 이에 속하는 대표적인 축광체 재료들이다.4)
본 연구에서는 좁은 에너지 밴드갭(2.4~2.7eV)과 우수한 내열성 및 전기 전도성을 지닌 산화세륨(CeO2)을 TiO2와 혼성화 시킨 (TiO2-CeO2) 나노 분말을 수열합성 방법을 이용하여 축광체 Sr4Al14O25:Eu2+,Dy3+ 고정체에 코팅 시켜서, (TiO2-CeO2)/Sr4Al14O25:Eu2+,Dy3+ 이종 접합 혼성 광촉매 소재를 제조하였다. TiO2를 CeO2 산화물과 혼성화 함으로서 서로 다른 에너지 밴드의 이종 접합(heterojunction)에 따른 가시광 파장대의 빛을 흡수하고, 또한 축광체 소재와 복합화 함으로서 축광체로부터 발광되는 빛이 광활성 반응을 촉진하는 효과를 얻을 수 있을 것으로 예상된다.5) 또한, TiO2 광촉매 물질은 나노 크기의 분말일 때 높은 광활성 기능을 나타내기 때문에, 광촉매를 실용적으로 활용하려면 광촉매 나노 분말을 견고하게 고정화시킬 수 있는 적절한 지지기판이 필요하다. 본 연구에서는 광촉매 나노분말을 높은 밀착력으로 고정시킬 수 있도록 축광체 고정체를 3 mm 크기 구형 비드(beads)로 제조하였다.
2. 실험 방법
2.1. (TiO2-CeO2)/Sr4Al14O25:Eu2+,Dy3+ 혼성 복합소재 제조
TiO2-sol은 전구체로써 9.7 mL의 TTIP [Titanium (IV) isopropoxide, 97 %, Sigma Aldrich]을 ethanol 38.8 mL, 증류수 50 mL과 혼합한 후, 30 °C에서 60 min 교반하여 제조하였다.6) 한편, CeO2를 첨가하기 위하여, 3 g 세륨 질산염(Ce(NO3)3・xH2O) 전구체를 ethanol (C2H5OH, 94.5 %) 12 mL, CTAB (cetyltrimethylammonium bromide) 2 g, 증류수 3 mL 와 혼합하고, pH를 조절하기 위해 질산(HNO3) 1 mL을 첨가한 후, 30 min 30 °C에서 교반하여 CeO2-sol을 합성하였다.
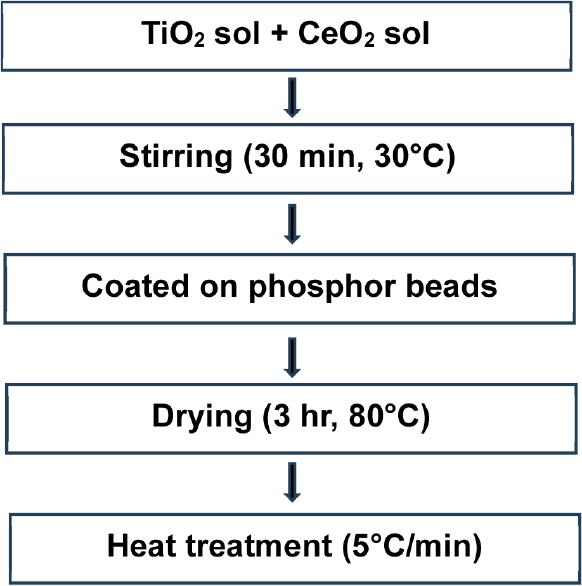
광촉매 물질의 고정체인 축광체 비드는 Sr4Al14O25:Eu2+,Dy3+ 축광체 분말 30 g을 제올라이트(zeolite) 12 g, 무기 결합제 sodium silicate 19 mL과 혼합하여 슬러리로 제조한 후, 3 mm 크기의 반구형 실리콘 몰드에 주입하여 사출하고, 최종적으로 건조 및 300 °C에서 열처리하여 제조하였다. (TiO2-CeO2) 혼성 나노 분말을 수열합성 방법을 이용하여 Sr4Al14O25:Eu2+,Dy3+ 축광체 비드형 고정체에 코팅 시키는 과정은 Fig. 1에 flow chart로 나타내었다. 앞서 제조된 TiO2-sol과 CeO2-sol 용액을 적정 조성비(0:10, 3:7, 5:5, 7:3, 10:0)로 칭량하여 초음파 교반으로 혼합한 후, 적정량의 축광체 비드(약 15 g)와 같이 오토클레이브(autoclave) 반응 용기에 넣은 후, 160 °C에서 수열반응이 일어나도록 하였다. 반응이 종료된 후 (TiO2-CeO2)가 코팅된 축광체 비드들을 용액과 분리하고 전기오븐에서 건조시킨 후, 최종적으로 300 °C~700 °C 온도에서 후열처리하여 비드형의 (TiO2-CeO2)/Sr4Al14O25:Eu2+,Dy3+ 혼성 복합소재 시편을 제조하였다.
2.2. 재료 특성 분석 및 광분해 반응 측정
제조된 시편의 물리적 결정학적 특성 분석은 FE-SEM (field-emission scanning electron microscopy, Hitachi S-4300), EDS (electron dispersive X-ray spectroscopy, Oxford, Extream), XRD (X-ray diffraction, Rigaku), TEM (transmission electron microscope, JEM-2021, JEOL Ltd.), BET (Brunauer-Emmett-Teller) analyzer (Micromeritics, USA), Confocal Raman Spectrometer (DXR-3xi, Thermo Fisher Waltham), XPS (X-ray photo electron spectroscopy, Thermofisher, Nexsa), UV/Vis-NIR (Cary-5000 Agilent Tech.)을 이용하여 측정 분석하였다. 광분해 성능은 자외선과 가시광선 조사 하에 톨루엔 가스의 분해 효율을 측정하여 분석하였다.7) 톨루엔 가스의 광분해율 측정은 패트리 접시에 10 g의 비드 시편을 담아 Tedlar 필름 백(1 L)에 넣고 30 ppm 농도의 톨루엔 가스를 주입하였다. 이후 가시광선 조사 하에 15 min마다 톨루엔 가스 1 mL를 주사기로 채취하여 가스 크로마토그래피(GC) 분석기로 분해율을 측정하였다. 광분해율 측정 전 톨루엔 가스의 흡착에 의한 농도 감소를 보정하기 위해서, 최초 측정이 시작되기 전에 광 조사 없이 20 min 동안 블랭크(blank) 실험을 진행하였다.8)
3. 결과 및 고찰
3.1. 재료 특성
Fig. 2는 (TiO2, CeO2)/Sr4Al14O25:Eu2+,Dy3+ 비드 표면을 관찰한 FE-SEM 사진이다. Fig. 2(a)는 축광체 비드 표면에 수십 나노 크기(~50 nm)의 CeO2 입자들이 응집체(agglomeration) 형상으로 지지체에 균일하게 코팅되었음을 보여준다. Fig. 2(b)는 TiO2/Sr4Al14O25:Eu2+,Dy3+ 비드 표면을 관찰한 FE-SEM 이미지로서, CeO2 분말의 경우와 유사하게 TiO2 나노 분말(≤ 10 nm)들이 응집체 형상으로 지지체에 균일하게 코팅되었음을 보여준다. 반면, (TiO2-CeO2)/Sr4Al14O25:Eu2+,Dy3+의 SEM 이미지[Fig. 2(c)]에서는 TiO2 나노 분말들이 응집체 형상으로 지지체에 코팅되었으며, 부분적으로 입자 크기가 작은 TiO2 나노 분말들이 큰 입자의 CeO2 분말을 감싸듯이 코팅된 응집체들을 보여주고 있다.9,10)
Fig. 3은 TiO2-CeO2/Phosphor composite (5:5 in TiO2-CeO2) 시편의 성분분석을 한 EDS spectrum이다. 성분분석 결과를 나타낸 Table 1에서와 같이, Ti와 Ce 원소의 atomic percent는 각각 54.1와 45.89의 비율을 보여 두 성분의 혼합 비율이 Ti-sol과 Ce-sol 각각의 전구체 혼합비와 유사하게 합성되었음을 확인하였다.
Table 1.
Comparison of experimental atomic composition for Ti, Ce in TiO2-CeO2/Phosphor composite (5:5 in TiO2-CeO2).
Fig. 4는 (TiO2, CeO2)/Sr4Al14O25:Eu2+,Dy3+ 혼성 복합소재의 미세구조를 관찰한 TEM 사진이다. TiO2/Phosphor 시편(a)의 경우, TiO2 나노 분말(≤ 10 nm)들이 응집체 형상으로 축광체에 균일하게 코팅되었음을 보여준다. 반면, CeO2/Phosphor 시편(b)의 경우, CeO2 입자들은 평균 입자 크기가 60 nm 이상으로서, 부분적으로 cluster 형태로 지지체에 코팅되었다. 한편, TiO2-CeO2/Phosphor composite (5:5 in TiO2-CeO2) 시편의 TEM 사진(c)에서는 입자 크기가 상대적으로 작은 TiO2 나노 분말(≤ 10 nm)들이 입자 크기가 큰 CeO2 입자(≥ 60 nm)들에 부분적으로 흡착되어 있음을 보여준다.
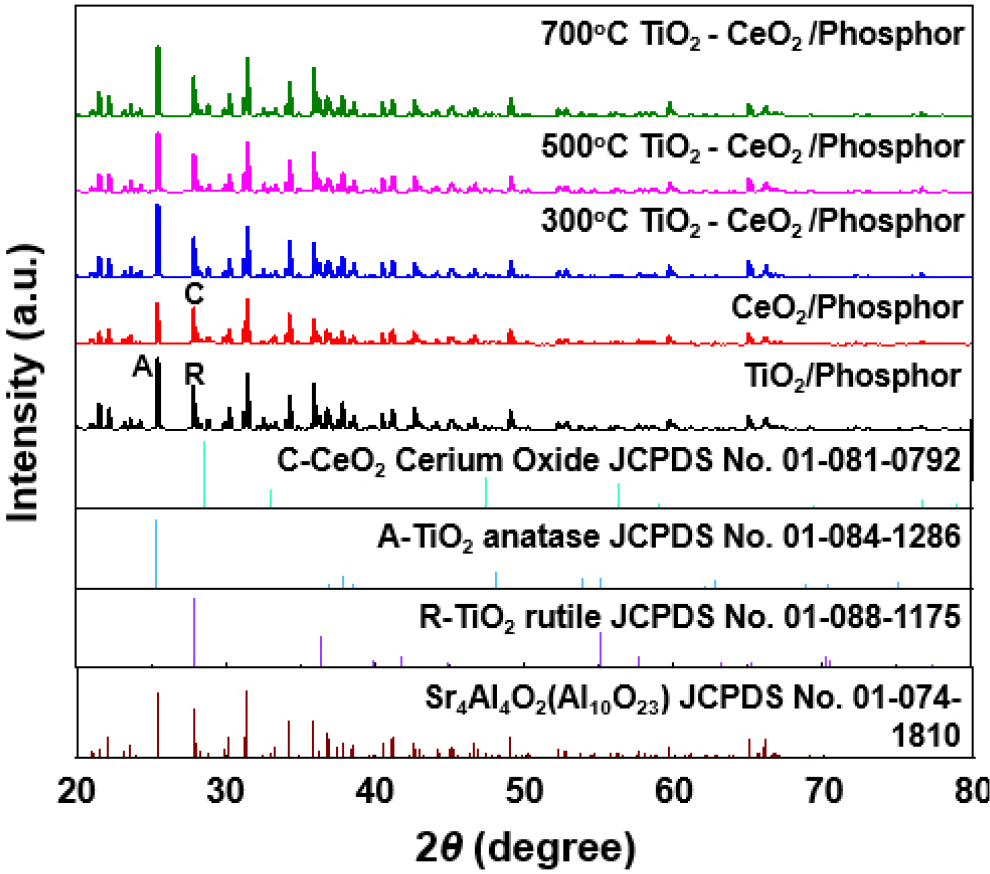
Fig. 5는 TiO2/Phosphor, CeO2/Phosphor, 그리고 300 °C, 500 °C, 700 °C에서 열처리한 TiO2-CeO2/Phosphor 복합체의 XRD 패턴을 비교한 것이다. 20~40° 사이에서는 축광체 기지인 Sr4Al14O2(Al10O23)의 회절선이 지배적으로 나타나며, 이는 JCPDS No. 01-074-1810과 일치한다. 순수 TiO2/ Phosphor 시료에서는 anatase TiO2 (JCPDS 01-084-1286)의 (101) 피크가 25.3°에서, rutile TiO2 (JCPDS 01-088-1175)의 (110) 피크가 27.4°에서 각각 확인되며, anatase-rutile 이중 상이 공존함을 보여준다. 한편 CeO2/Phosphor 시료에서는 fluorite CeO2 (JCPDS 01-081-0792)의 (111), (200), (220) 면이 28.6°, 33.1°, 47.5°에서 뚜렷하게 관찰되며, 이는 CeO2가 축광체 표면에 결정질로 코팅되었음을 의미한다.
TiO2-CeO2/Phosphor 복합체의 열처리 온도가 상승함에 따라 뚜렷한 상 변태와 결정 성장 경향이 나타난다. 300 °C에서 열처리된 시편에서는 anatase (101)와 CeO2 (111) 피크가 모두 비교적 넓고 낮은 강도로 존재해 결정화 정도가 제한적이다. 500 °C로 열처리된 시편의 경우, TiO2 anatase 및 rutile (110), CeO2 회절선도 피크가 점차 강화되며, 이는 TiO2・CeO2 양상의 결정 성장이 진행되었음을 시사한다. 700 °C에서 열처리될 경우, rutile (110), (101) 피크가 우세해져 anatase에서 rutile로 상전환이 진전되었고, CeO2 상의 피크 세기도 증가되었다.
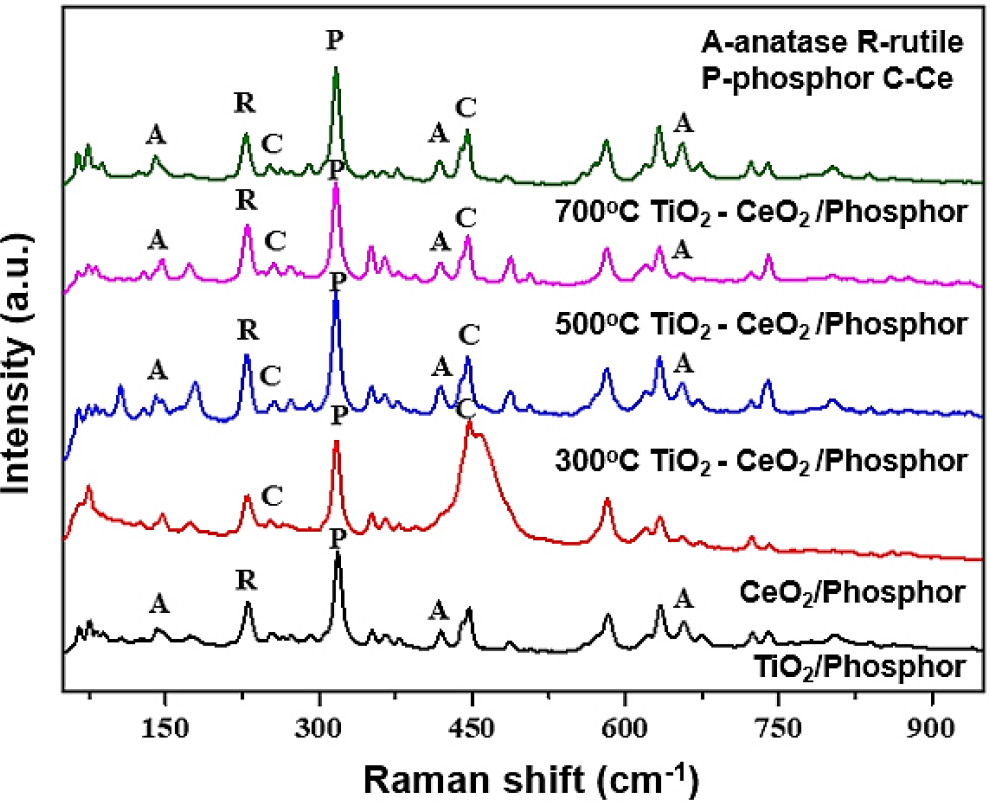
Fig. 6은 TiO2/Phosphor, CeO2/Phosphor, 그리고 서로 다른 열처리 조건(300 °C, 500 °C, 700 °C)에서 제조된 TiO2-CeO2/Phosphor 복합체의 라만 스펙트럼을 비교한 것이다. 순수 TiO2/Phosphor 시료에서는 anatase 특유의 Eg (144, 197, 399, 519, 639 cm-1) 밴드와 함께 rutile의 Eg (447, 612 cm-1) 피크가 뚜렷하게 관찰되어 anatase-rutile 이중 상이 공존함을 보여준다. CeO2/Phosphor 스펙트럼에서는 플루오라이트형 CeO2의 대표 Eg (≈ 465 cm-1)와 산소 공공에 기인하는 약한 불규칙 밴드(≈ 600 cm-1 부근)가 나타나며, 동시에 형광체 고유 피크(P, ≈ 300 cm-1)가 유지되어 CeO2가 기판 전면에 균일하게 코팅되었음을 확인할 수 있다. TiO2-CeO2 복합체의 경우 열처리 온도에 따라 상대 피크 세기가 뚜렷이 변한다. 300 °C 시료에서는 anatase Eg (144 cm-1)와 CeO2 Eg (465 cm-1)가 공존하되 피크 폭이 넓어 결정성이 낮고, rutile 피크가 거의 관찰되지 않는다. 500 °C로 승온하면 CeO2 Eg 피크가 뚜렷해지는 동시에 anatase → rutile 상전환이 진행되어 rutile (447, 612 cm-1)의 상대 강도가 증가한다. 700 °C 열처리 시에는 rutile 피크가 지배적으로 성장하고 anatase 밴드는 급격히 약화되며, CeO2 피크 또한 일부 소결・집적에 따른 결정성 증대로 인해 상대적 강도가 약화된다. 이러한 경향은 고온 열처리에서 TiO2 결정립 성장 및 상전환이 가속화되고, CeO2가 TiO2 입계로 확산, 도핑 되면서 격자 변형과 산소 공공 재구성이 발생함을 시사한다. 특히 500 °C 조건에서는 anatase・rutile・CeO2가 모두 분산 공존하여 이종접합 계면 밀도가 가장 높아질 것으로 예상되며, 이는 전하 분리 촉진과 광흡수 스펙트럼 확장에 유리해 광촉매 성능의 최적화 온도로 판단된다.
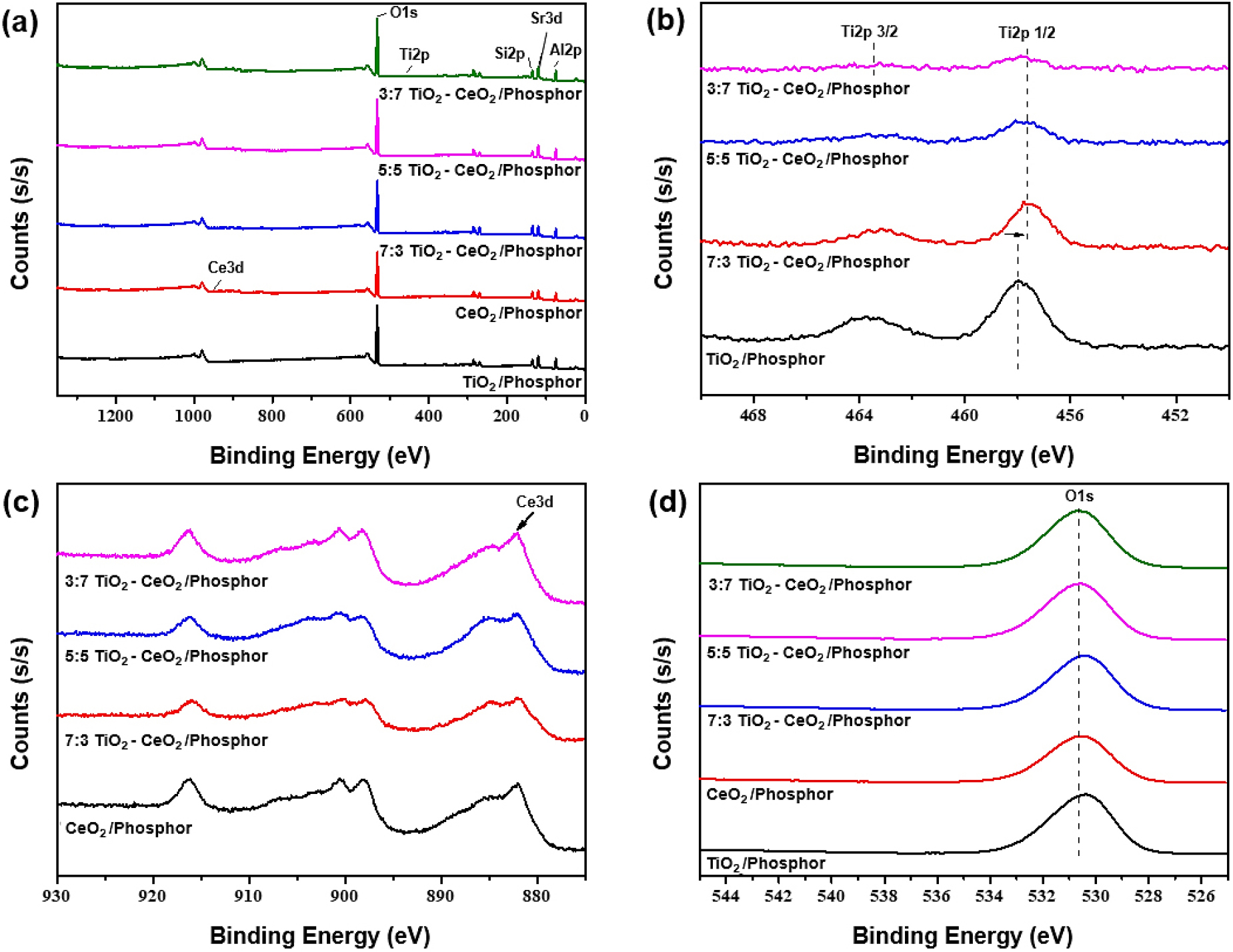
Fig. 7은 TiO2/Phosphor, CeO2/Phosphor, and TiO2-CeO2/ Phosphor 복합체에 대하여 측정된 XPS 결과를 나타낸 것이며, 순서대로 survey, Ti 2p, Ce 3d, O 1s의 스펙트럼이다. X선 광을 조사하여 역산한 결합에너지와 피크 위치를 통해 표면 원소 조성과 그 결합 상태 등을 추정할 수 있고, 이는 광촉매의 전자 구조 변화를 분석하기에 필수적이다. survey spectrum에서는 결합에너지의 범위가 넓어 육안으로 조성 비율에 따른 스펙트럼의 변화를 구분하기 어렵다. 그러나 Ti 2p 스펙트럼 부분을 보면 확연한 차이가 있다. Ti 2p 1/2 피크와 Ti 2p 3/2 피크가 있으며, Ti가 Ti4+로 산화 상태임을 나타내는 일반적인 위치이다. 그러나 CeO2의 농도를 달리하여 복합화를 거쳤을 때 결합에너지가 줄어드는 방향으로 shift가 일어났으므로 산소 결함과 Ti3+의 존재를 시사한다. CeO2와의 상호작용으로 Ti4+는 전자 교환이 일어나 Ti3+로 환원되었을 것이다. CeO2의 농도가 늘어날수록 Ti 2p의 스펙트럼이 완만해지는 것 역시 이 사실을 뒷받침한다. 같은 이유로 Ce 3d 피크는 4가지 시료 모두 비슷한 스펙트럼 형태를 띠지만, TiO2의 비율이 증가할수록 피크가 완만해짐으로 산소 결함과 Ce3+가 존재하며 탁월한 전하 운반체 전달을 기대할 수 있다. 결론적으로 TiO2와 CeO2 모두 산소 결함이 있으므로 Ti-O-Ce 결합이 형성될 가능성이 있고, 광촉매에 긍정적인 영향을 줄 수 있다.5) O 1s는 모두 단일 피크를 가지고 530.8 eV에 위치하여 산소 결함 주변 산소에서 나타나는 피크의 표준 값과 밀접하게 일치한다.
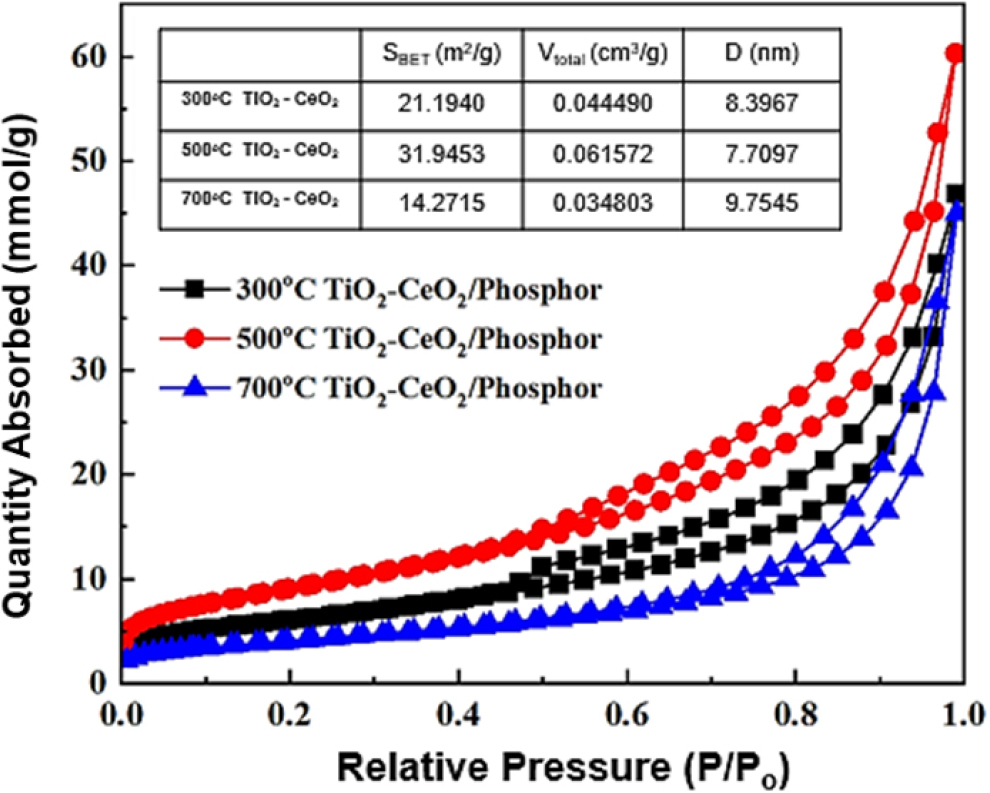
Fig. 8은 TiO2-CeO2/Phosphor 복합체에 대한 BET 분석 결과이다. BET 비표면적(S)과 기공 부피(V), 기공 크기(D)를 포함한 BET 비표면적(S)은 낮은 온도부터 순서대로 21.19 m2/g, 31.95 m2/g, 14.27 m2/g이며, 기공 부피(V)는 0.04449 cm3/g, 0.6157 cm3/g, 0.03480 cm3/g 으로 나타났다. 두 가지 요소 모두 500 °C에서 최댓값을 가지는데, 이는 기체의 흡착 가능 공간이 많아 활성 부위도 많음을 의미하므로 해당 온도에서 가장 우수한 광효율을 기대할 수 있다. 300 °C에서는 결정화가 완전히 되지 않았고, 700 °C에서는 고온 열처리로 인한 입자 성장으로 인해 비표면적이 감소하여 기공 구조가 붕괴되었을 것이다.11) 기공 크기(D)는 모두 광분해에서 가장 유리한 기공 크기인 메조 기공(2~50 nm)이다.12)
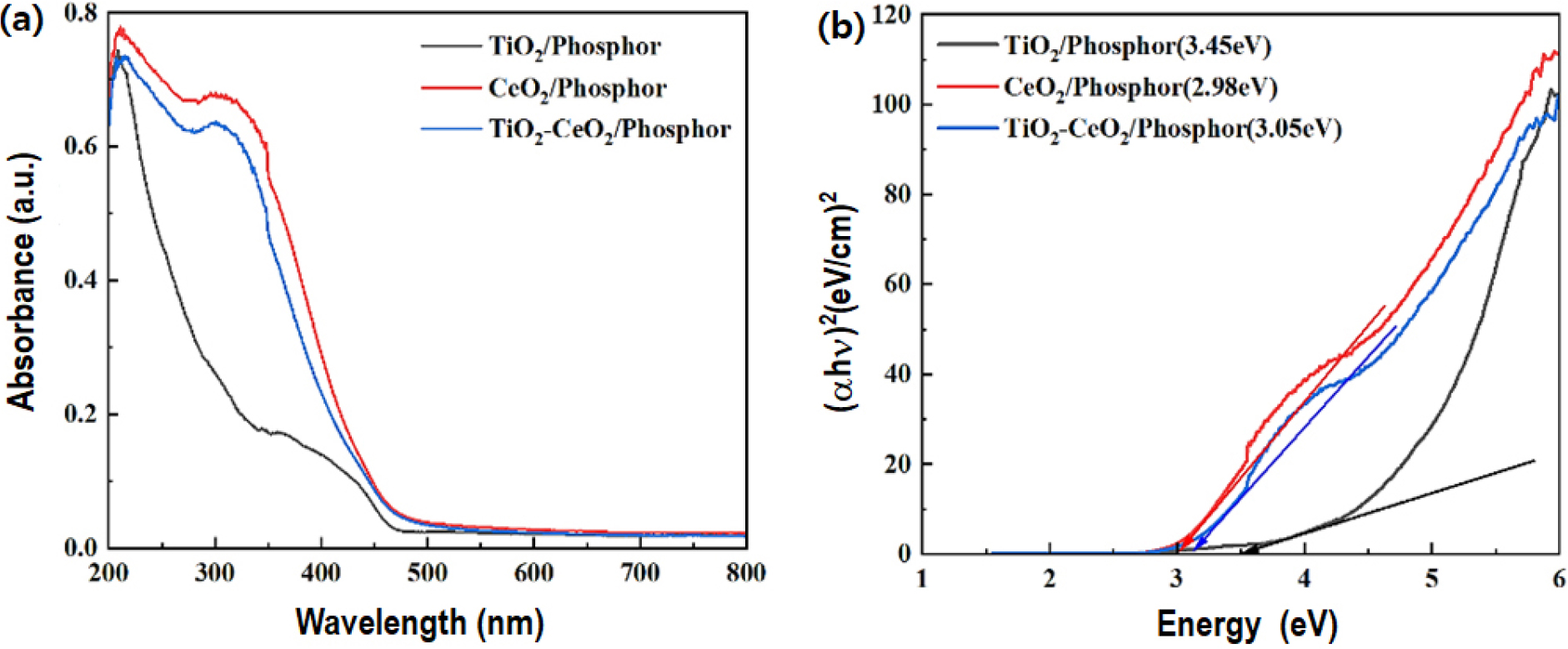
Fig. 9는 TiO2/Phosphor, CeO2/Phosphor, and TiO2-CeO2/ Phosphor 복합체에 대하여 광학 특성을 분석하기 위하여 diffuse reflectance spectra를 측정한 결과이다. Fig. 9(a)에 나타난 바와 같이, TiO2/Phosphor의 경우, 상대적으로 낮은 흡광도를 보이며, 전형적인 UV 흡수 특성이 나타난다. TiO2-CeO2/Phosphor는 300 nm-400 nm 영역의 흡광도가 증가하는 적색편이가 일어나는데, 이는 CeO2와의 복합화를 통해 흡광 성능이 향상되었음을 의미하며,13) 그 이유를 설명하고자 Fig. 9(b)와 같이 밴드갭을 추정하고 Tauc plot으로 도식화 하였다. TiO2/Phosphor, CeO2/Phosphor, and TiO2-CeO2/Phosphor composites는 순서대로 359 nm, 416 nm, 407 nm에서 absorption band edges를 보인다. TiO2/ Phosphor의 밴드갭은 3.45eV로 전형적인 순수 TiO2의 밴드갭이며 자외선 영역에서만 흡광 반응이 일어난다. CeO2/ Phosphor는 2.98 eV로 가장 낮은 밴드갭을 보이는데, 이는 가시광선 영역까지 흡수 가능 영역을 확장시키는 원인이 된다. 식 (1), (2)를 사용하면 UV-Vis를 통해 구한 TiO2와 CeO2의 밴드갭으로 전도대(CB)와 가전자대(VB)의 위치가 계산되므로 전자와 정공의 분리 가능성을 정량적으로 평가할 수 있다. 위 식에서 ECB는 전도대의 전위, EVB는 원자가대의 전위이며 Ee는 수소 기준 자유전자 에너지(4.5 eV), X는 반도체의 전기 음성도(TiO2: 5.81 eV, CeO2: 5.56 eV) 이며, Eg는 밴드갭을 의미한다.
계산을 통해 구한 TiO2의 ECB는 -0.415 eV, EVB는 3.035 eV이고, CeO2의 ECB는 -0.43 eV, EVB는 2.55 eV이다. 전자는 ECB가 높은 곳에서 낮은 곳으로 이동하므로 TiO2에서 CeO2로 이동할 것이며, 정공은 EVB의 값이 낮은 곳에서 높은 곳으로 이동하므로 CeO2에서 TiO2로 이동하게 된다. 이는 곧 전자와 정공이 공간적으로 분리되어 재결합이 억제됨을 의미하고,14) 전자와 정공의 수명 증가로 인한 광촉매 성능 향상으로 이어진다. 따라서 복합화를 거친 TiO2-CeO2/Phosphor는 순수 TiO2만을 합성했을 때보다 밴드갭이 감소하여 3.05eV로 결정되었다. 이러한 원인 중 하나는 계면 전하 이동 경로의 형성이다. 두 산화물의 접합으로 Ti4+-O-Ce4+ 또는 Ti4+-O-Ce3+ 결합이 계면에 생겨나는데, TiO2에서 발생한 전자가 계면 전하 이동 경로를 통해 CeO2로 이동함으로써 전자-정공의 재결합이 억제된다.15) 또한, 중간 에너지 준위 역할을 하는 4f 전자 궤도로 Ce4+와 Ce3+ 사이에 전환이 일어나 TiO2의 아래에서 중간 준위가 형성되어 전자와 정공의 재결합이 억제되는 효과가 있으므로 결과적으로 복합화로 인한 광촉매로써 성능이 증진된다.16)
3.2. 광촉매 반응 특성
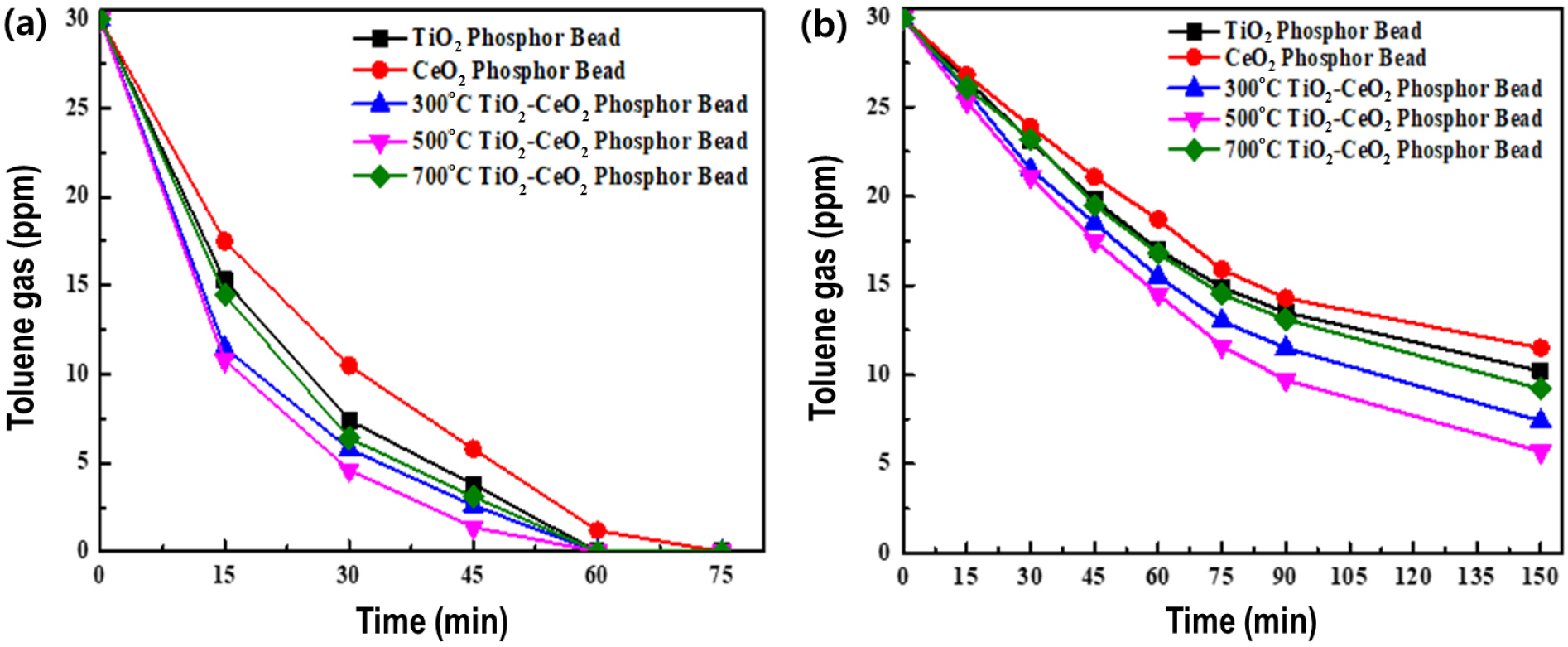
광촉매를 이용한 유해성 물질 제거 방법에 있어 광자 에너지는 필수적이다. 빛으로부터 얻은 광자 에너지는 전자-정공쌍을 생성하고, 전자와 정공의 재결합을 얼마나 지연하는가에 따라 광촉매의 성능이 결정된다. Fig. 10은 (a) 자외선과 (b) 가시광선을 각각 조사하였을 때 톨루엔 가스에 대한 광분해율을 측정한 결과이다. 광분해 실험은 매 시편에 대해서 2회 이상 실시하여 실험적 오류를 최소화하였다. 또한, TiO2-CeO2/축광체 비드의 경우, 시편의 열처리 온도에 따른 광분해율 변화를 보여주고 있다. 첫 번째 측정이 시작되기 전에 광 조사 없이 진행된 블랭크(blank) 실험 결과, 모든 시편은 톨루엔 농도 변화가 없었고, 이를 기준 삼아 톨루엔 분해 농도를 도시했다. 먼저, 자외선 조건에서 45 min 측정 기준으로 순수 TiO2, CeO2만을 따로 코팅한 축광체 비드의 경우 각각 88 %, 81 % 분해에 그쳤지만, TiO2-CeO2/축광체 비드의 경우 모두 90 % 이상 분해되었으며, 그중 500 °C에서 열처리한 시료의 분해도가 95 %로 가장 우수하다. 가시광선 조사 하에 150 min 동안 측정한 결과 역시 순수 TiO2, CeO2만을 따로 코팅한 축광체 시료의 경우 각각 64 %, 62 %씩 분해되었으나 TiO2-CeO2/축광체 중 가장 성능이 우수한 열처리 온도인 500 °C를 기준으로 약 20 % 상승하여 81 %의 분해가 진행됐다. 이를 통해 두 물질의 복합화가 전자, 정공의 분리와 재결합 억제가 효과적으로 일어나 광분해 성능이 향상된 것을 알 수 있다. 300 °C의 열처리 온도에서 광분해율이 떨어지는 이유는 온도가 충분히 높지 않아 아직 결정성이 낮으므로 전하의 이동이 원활하지 못해 전자, 정공의 재결합 가능성이 높기 때문이다. 반면, 700 °C의 높은 열처리 온도의 경우에는 광활성이 일어날 수 있는 비표면적이 줄어들고, 기공이 붕괴되기 때문에 낮은 분해율이 나타났다.17) 이에 대한 근거는 Fig. 9에서도 확인된다.
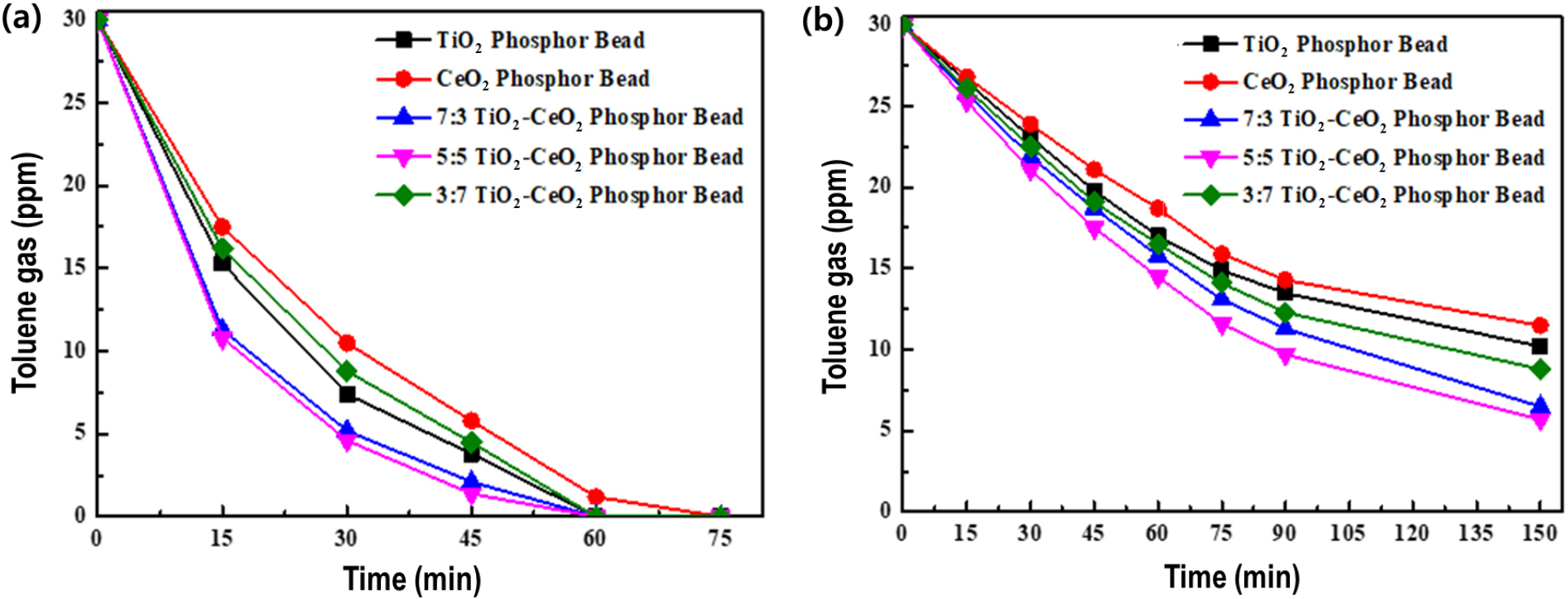
Fig. 11은 앞선 Fig. 10과 같이 TiO2/Phosphor, CeO2/ Phosphor, and TiO2-CeO2/Phosphor 세 가지 시편에 대해서 (a)자외선과 (b)가시광선을 각각 조사하였을 때 톨루엔 가스에 대한 광분해율을 측정한 결과이다. 추가로, TiO2-CeO2/축광체 비드의 경우, TiO2와 CeO2의 조성 비율에 따른 광분해율 변화를 나타내 주고 있다. 세 비율 중 TiO2와 CeO2를 5:5의 비율로 합성했을 때 45 min 기준 95 %로, 가장 좋은 성능을 보였고 3:7은 85 %로, 가장 부진한 성능을 보였다. 이는 전하 운반체의 다중 포획으로 인해 전자-정공의 재결합 가능성이 증가하고 표면까지 도달 가능한 유효 캐리어 수가 감소함과 동시에 응집 성질이 있는 CeO2의 과도한 첨가로 전체 표면적이 줄어들어 오히려 TiO2 표면으로의 확산이 저해되었음을 의미한다.13)
4. 결 론
본 연구에서는 수열반응 공정을 이용하여 TiO2-CeO2 이종접합 광촉매 화합물을 Sr4Al14O25:Eu2+,Dy3+ 축광체 비드에 균일하게 코팅하고, 서로 다른 열처리 온도(300~700 °C)와 TiO2/CeO2 몰비(3:7~7:3)가 톨루엔 가스의 광분해 효율에 미치는 영향을 체계적인 실험으로 측정 분석하였다. SEM, TEM, XRD, Raman Spectroscopy분석 결과, 500 °C에서 열처리한 TiO2/CeO2 (5:5 ratio) 시편은 TiO2 anatase 및 rutile, CeO2 3개 상이 균형 있게 공존하였으며, BET 분석에서도 해당 시료가 가장 큰 비표면적(≈ 32 m2 g-1)과 기공 부피(≈ 0.62 cm3 g-1)를 나타내어 광활성 사이트 밀도가 최적화될 수 있었다. UV-Vis DRS 및 Tauc plot분석으로부터 TiO2-CeO2/Phosphor 복합체의 밴드갭이 3.05 eV로 감소하였고, 밴드 정렬 계산에서 전자는 TiO2에서CeO2로, 정공은 CeO2에서 TiO2 방향으로 이동함에 따라 전자-정공 재결합 억제 효과를 제시하였다. 톨루엔 가스에 대한 광분해 성능 측정 평가로부터 TiO2-CeO2 (5:5 ratio, 500 °C 열처리)/Phosphor 복합체는 자외선광 조사 하에서 45 min 기준 95 %, 가시광선 하에서 150 min 기준 81 %의 광분해율을 나타냈다. 이러한 광분해 성능 향상은 CeO2의 산소 공공과 Ce3+/Ce4+ 적산-환원 준위에 의한 전자 저장・셔틀 효과, TiO2 anatase, rutile, CeO2 간 이종접합 계면의 공간 전하 분리, 축광체 잔광에 의한 지속적 광자 공급이 시너지로 작용한 결과이다. 본 연구결과로부터 개발된 TiO2-CeO2/Phosphor 혼성 광촉매 복합소재는 가시광에서 높은 광분해 효율을 나타내고, 또한 광이 부족한 그늘지거나 어두운 환경에서도 광활성이 지속되기 때문에 환경오염물질 저감이 필요한 실생활에 활용 가능성이 매우 높을 것으로 기대된다. 향후 연구에서는 축광체 지지체의 광 공급기능 극대화, 유해물질 및 환경 오염물질에 대한 광분해 효율 향상, 대기 및 수질 정화장치 적용 기술, 장기 안정성 향상 기술 등에 대한 체계적인 연구가 요구된다.