1. 서 론
화석 에너지 사용에 따른 환경문제가 전세계적인 문제 가 대두됨에 따라 화석에너지를 대체할 다양한 새로운 에너지원에 대한 연구가 진행되고 있다. 태양 에너지는 다른 에너지에 비해 비교적 쉽게 얻을 수 있으며, 발전 시 다른 환경 문제를 야기하지 않는다는 장점을 가지고 있다. 하지만, 태양광 발전을 위해 매우 넓은 부지가 필 요하며, 발전량이 날씨에 의한 영향을 많이 받기 때문 에 발전 효율에 대해 큰 문제를 가지고 있다. 그러나, 유연성 박막태양전지는 다양한 디자인으로 제작이 가능 하여, 건물 등에 설치할 수 있어 디자인과 설치 공간에 대한 이점이 많다. 스테인리스 스틸(stainless steel)판은 유연성 박막태양전지의 유연 기판으로써 매우 중요한 장 점을 가지고 있다. 스테인리스 스틸은 250 °C 이상의 박 막태양전지 제작 공정에서도 안정하며, 우수한 내식성으 로 인해 화학적으로 매우 안정적이다. 또한 기판을 통 해 수분, 산소 등이 박막태양전지 내부로 침투할 수 없 어 패키징 공정에 매우 적합하다.1-5) 하지만, 우수한 태 양광 효율을 얻기 위해서는 균일한 실리콘 무기 박막이 필요하며, 따라서 스테인리스 기판의 표면거칠기를 최소 화하는 것이 필요하다.
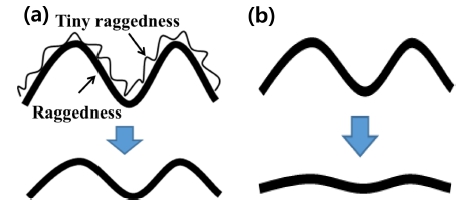
스테인리스 강은 니켈과 크롬으로 인해 표면에 자연 적으로 1 ~ 10 nm 산화 피막(oxide layer)인 부동태 막 (passive film)이 형성된다. 표면에 형성된 얇은 산화 막 은 비정질 상으로, 표면에 인접한 내부 산화물 층(inner oxide layer, barrier layer)과 금속이온이 산화물/수산화물 /수화물로 석출된 다층 구조를 가진다. 부동태 피막은 외 부 부식 인자와의 전자의 흐름을 막아 부식으로부터 모 재를 보호하고, 스크래치 등과 같은 물리적 결함이 생 기더라도 자연 치유되는 성질을 가지고 있다.6) 하지만 스 테인리스 표면 조직이 불균일하고 내부에 포함된 크롬 함량 편차가 존재할 경우, 균일한 두께의 피막이 형성 되지 않아 표면 거칠기가 커지며, 부식 응력(corrosion stress) 집중 현상으로 공식이 발생하며 이를 기반으로 부 식이 진행될 수 있다는 큰 문제점을 가지고 있어, 매끄 러운 표면 제작을 위한 후 공정이 필요하다.7,8)
전해연마는 표면 요철에 고 전류를 인가하고 에칭하는 기술로써, 표면 조도 감소와 함께 표면 결함(pin-hole, 금 속 이물 및 탄화물 등)을 제거하여 광택을 증대시키는 효과를 얻을 수 있다. 뿐만 아니라 균질한 산화 피막 형 성을 통해 모재 표면의 내식성을 크게 증가시킬 수 있 다.9,10) 전해연마는 전기-화학적 반응에 의한 금속 용출 을 기반으로 이뤄지며, 연마 조건(전해액 조성, 인가전 압, 시간 등) 조절을 통해 표면의 조도를 나노 단위로 미세하게 조절할 수 있다. 본 연구에서는 우수한 표면 특성을 가진 스테인리스 스틸 304 (STS304)을 얻고자 다양한 비율로 혼합된 전해 연마액을 이용하여 전해연 마를 진행하였다. 그리고 각 조성에서 금속이온 농도가 전해 연마 거동에 미치는 영향에 대해 고찰하였다.
2. 실험 방법
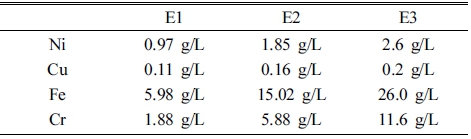
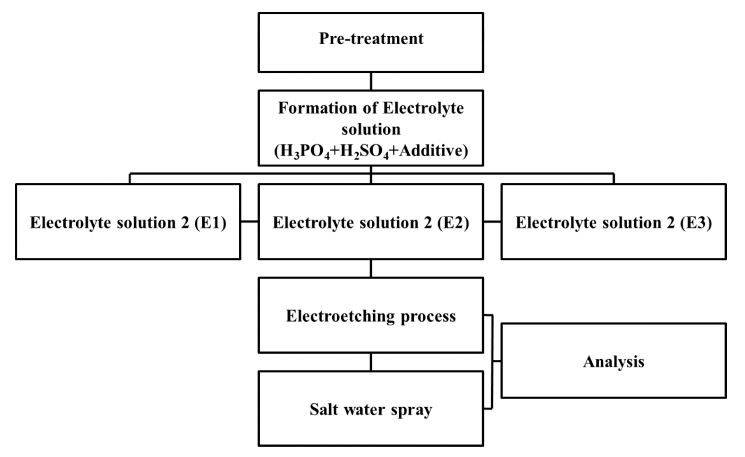
STS304 (POSCO, Stainless #304) 표면 불순물을 제 거하기 위해 아세톤 원액에 침지 후 10분간 초음파 처 리한 후 증류수로 세척하였다. 인산 85 % (Phosphoric acid solution, UN1805)과 황산 98 % (Sulfuric Acid, Sigma Aldrich) 그리고 첨가제(ASLES EPS-P, OKUNO) 를 7 : 2.95 : 0.05 부피 비율로 혼합하여 전해 연마액을 제조하였다. 제조한 전해 연마액에 모재 금속을 구성하 는 Ni, Cu, Fe, Cr을 금속 이온 용액을 일정 비율로 첨 가하여 E1, E2, E3을 제조하였으며, Table 1에 전해 연 마액 금속 이온의 첨가량을 나타내었다. 이때, 전해 연 마액을 구성하는 금속 이온의 종류 및 농도는 전해 연 마 과정에서 모재 내 포함된 금속 이온은 전해 연마액 으로 용출에 의한 부동태 피막 형성에 미치는 영향을 최 소화하기 위해 Ni, Cu 금속 이온을 첨가하였다. 그리고 전해 연마액 내 금속 이온 농도가 부동태 피막 형성에 미치는 영향을 확인하기 위해, 금속 이온 농도를 E1, E2, E3 순서대로 증량하였으며, Fe/Cr 비율은 감소하는 방향 으로 설계하였다. 구체적인 실험 진행 과정을 Fig. 1에 나타내었다. 전해 연마액 종류에 따른 분극 거동은 포 텐시오스탯(Potentiostat, VSP, Bio-Logic SAS) 사용하여 측정하였다. 전해 연마는 3전극법을 이용하여 실시하였 으며, 기준 전극은 포화 칼로멜 전극(saturated calomel electrode), 상대 전극(count electrode)은 백금 망(Pt mesh, 2.5 × 3.0 cm2)를 사용하였다. 전해액을 교반하지 않는 상 태에서 분극 거동을 측정하였으며, 작업전극(working electrode)과 상대전극(counter electrode)의 극간거리는 35 mm로 유지하였다. 전해 연마에 적합한 온도를 선정하기 위해, 실험 액 온도는 65, 75 °C로 설정하였으며 측정 전 압의 주사 속도(scan speed)는 1 mV/sec로 하여 평형전 위 대비 +1.0 V까지 주사하였다.
앞서 측정한 분극 곡선으로부터 선정한 온도로 유지되 고 있는 전해 연마 욕에 STS304시편을 넣었으며, 전도 도와 무관하게 양극과의 전자이동과 산 용액에서 부식 을 방지하기 위해 음극 재료로 양극과 동일한 STS304 를 이용하였다. 전해 연마는 5V의 전압을 300초 동안 인가하는 조건으로 진행하였으며, 이때 시편 전면에 전 해 연마가 이뤄질 수 있도록 기계적인 교반을 함께 진 행하였다. 그리고 앞서 제조한 세가지 전해 연마액을 이 용해 동일한 공정으로 전해 연마를 진행하였다. 전해 연 마액 종류에 따른 시편의 미세구조 변화는 광학현미경 (optical microscope, MSP-8000 pro, DIGIBIRD)을 이 용해 200배 확대하여 관찰하였다. 전해 연마액 종류에 따른 표면 조도(Rq, Rz, Ra)를 조도측정계(Surftest, Sj- 210, Mitutoyo)를 이용하여 측정하였다. 또한 광택 측정 기(Gloss Meter, AG-4563, BYK Gardner)를 이용하여 전해 연마한 시편 표면의 광택을 측정하였다. 신뢰성 있 는 조도, 광택 데이터를 얻기 위해 전해 연마액 당 2개 의 시편을 측정한 후, 평균값을 계산하였다. 전해 연마 액 종류에 따른 내식성은 제작한 시편을 35 °C로 유지 되는 NaCl 5 % 염수를 8시간 분무 후 16시간동안 건조 하는 과정을 10회(총 240시간) 반복하여, 염수 분무 후 광학현미경을 이용해 관찰한 시편 표면 상태로부터 평 가하였다.
3. 결과 및 고찰
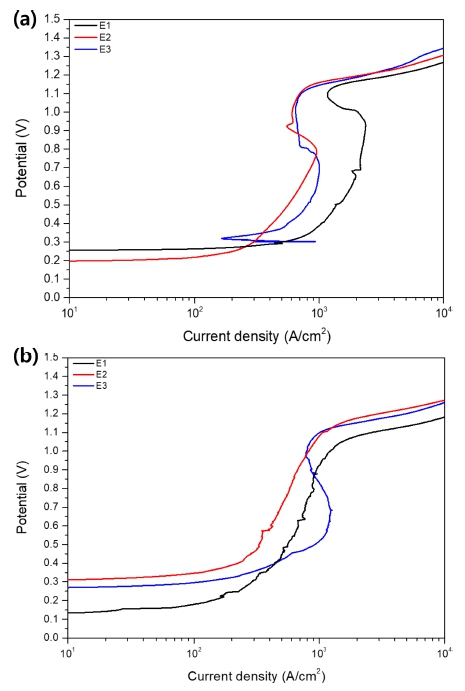
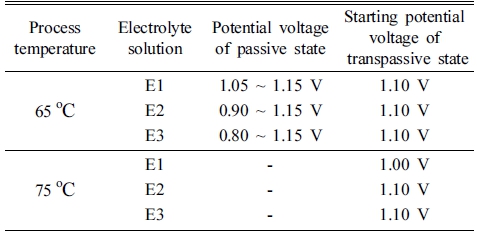
전해 연마에 적합한 온도를 판단하기 위해 E1, E2, E3 전해 연마 용액을 이용해 65, 75 °C에서 분극 곡선을 측 정하였으며, 그 결과를 Fig. 2에 나타내었다. Fig. 2로부 터 각 시편의 부동태 전위 및 과부동태 시작 전위를 추 출하여 Table 2에 나타내었다. 두 온도 조건에서 모두 전 해 연마가 되는 과부동태 영역(> 1.0 V)이 형성되어 있 음을 확인할 수 있었다. 하지만 65 °C에서 측정한 분극 곡선[Fig. 2(a)]에서는 전압(V)이 증가하지만 전류 밀도 (mA/cm2)가 유지되는 부동태 구간이 명확하게 나타난 것 에 비해 75 °C에서 측정한 분극 곡선[Fig. 2(b)]에서는 부 동태 구간이 거의 나타나지 않았다. 한편, 유연 박막태 양전지 기판으로 사용되기 위해서는 표면 광택뿐만 아 니라 내식성이 매우 중요하므로 부동태층이 형성되는 65 °C 조건에서 전해 연마를 진행하였다.
Table 2
Potential voltage of passive state and starting potential voltage of transpassive state for the various electropolishing conditions.
 |
E1, E2, E3으로 전해 연마한 시편의 사진을 Fig. 3에 나타내었다. 모든 시편의 표면은 금속 특유의 색을 띄 었으며, 약간의 광택이 나타나는 것을 확인할 수 있었 다. 전해 연마액 종류에 따른 시편 표면의 미세구조 차 이를 확인하기 위해, 전해 연마 처리 후 STS304 시편 의 표면을 200배 확대해 관찰하였으며 사진을 Fig. 4에 나타내었다. 전해 연마액의 금속 이온 농도가 증가함에 (E1: Ni 0.97, Cu 0.11, Fe 5.98, Cr 1.88 g/L, E2: Ni 1.85, Cu 0.16, Fe 15.02, Cr 5.88 g/L, E3: Ni 2.6, Cu 0.2, Fe 26.0, Cr 11.6 g/L) 따라 표면 굴곡이 더 작 아졌다. 모든 시편 표면에서는 결정립계가 관찰되었다. 이 는 STS 304에서 관찰되는 현상으로 높은 C 농도로 인 해 결정립계의 C r- C 화합물 형성으로 Cr이 결핍되어 입 계 부식 현상으로 인해 나타난다.11) 한편, 시편 표면에 서는 수 μm 크기의 미세 결함이 형성(빨간 화살표) 되 었으며, 연마액 내의 금속이온 양이 증가함에 따라(E1 → E3) 줄어드는 경향을 보였다. 이와 같은 현상은 전해액 중 물(H2O)의 전기 분해로 인해 제품 표면에 발생된 산 소(O2) 가스가 용액 표면으로 빠져나가지 못해 제품과 보 조 음극 간에 형성된 기공이 회로 단절 공간을 형성하 여, 전해 연마가 정상적인 일어나지 않아 나타난 것으 로 판단된다.12)

Fig. 4
Optical microscope images of electropolishing specimens by using (a) E1, (b) E2 and (c) E3 (× 200).
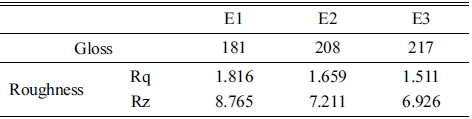
전해 연마액 종류에 따른 시편 표면의 조도 및 광택 도를 측정하였으며, 이를 Table 3에 나타내었다. Table 3 를 통해 E1, E2, E3으로 전해 연마한 시편의 Rq는 1.816, 1.659, 1.511이며, Rz는 8.765, 7.211, 6.926으로 미세구조 관찰 결과와 유사한 거동이 나타남을 확인할 수 있었다. 이와 같은 결과를 통해 전해액의 금속 이온 농도가 높아짐에 따라 전해 연마 시편의 조도가 낮아짐 을 알 수 있었다. 그리고 E1, E2, E3으로 전해 연마한 시편의 광택은 181, 208, 217 였으며, 굴곡도가 줄어듦 에 따라 표면의 광택이 증가하는 것을 알 수 있었다. 이 처럼 전해 연마액의 종류에 따라 표면의 물성이 달라지 는 것을 알 수 있다. 전해 연마에 의해 표면 조도가 낮 아지는 과정은 다음과 같이 설명할 수 있다. 일단 전해 연마액의 황산(H2SO4)은 팽윤 작용에 의해 시편 표면에 형성된 미세 요철이 제거하고 인산(H3PO4)은 나머지 요 철을 일률적으로 깍아 주는 역할을 한다. 첨가제는 모 서리 부분에서 형성되는 전류를 분산시켜 모든 면이 균 일하게 용해될 수 있게 하며(Fig. 5), 그 결과, 평탄한 피막층이 형성되어 우수한 표면 광택을 얻을 수 있다.13-16)
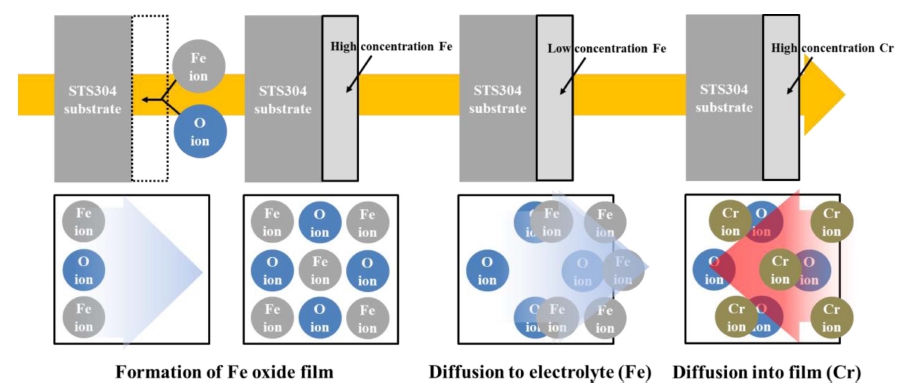
시편의 내식성을 확인하기 위해 E1, E2, E3로 제작 한 시편을 염수 분무 시험하였으며, 그 결과를 Fig. 6에 나타내었다. E1을 이용해 제작한 시편 표면에서는[Fig. 6(a)] 깨진 부동태 피막과 함께 표면 입계 부식이 확인 된다. 그리고 E2, E3을 이용해 시편표면에서는 염수 분 무에 따른 표면의 변화가 거의 없었음을 관찰할 수 있 었다. 이를 통해 E1은 STS304의 전해 연마에는 적합하 지 않음을 추정할 수 있다. E1으로 전해 연마한 시편에 서 나타난 현상은 표면 거칠기가 높은 부분의 부식 응 력 집중 현상에 의해 발생한 공식이 부식으로 발전되어 나타난 현상이다.9,10) 실험 결과를 통해 E3으로 전해 연 마한 시편에서 우수한 광택 및 방식 특성을 나타나는 것 을 확인할 수 있었으며, 이는 넓은 범위의 부동태 전위 (0.80 ~ 1.15 V)에 의한 것으로 판단된다[Fig. 2(a)]. 그리 고 E3의 분극 거동은 전해액 내 금속 이온의 양과 연 관 지어 설명할 수 있다(Fig. 7). 부동태 피막은 전해액 에서 가장 높은 비율을 차지하는 금속이온이 산화하여 양극의 금속 표면에 형성된다. 이렇게 형성된 금속 산 화층은 전해액에 비해 금속 이온 농도가 더 크며, 이로 인해 전해액-산화층 사이에서는 금속 이온 삼투압 농도 차이가 발생한다. 이로 인해 산화층 내 금속이온이 전 해액으로 용출되며, 전해액 계면 부근의 산화층에서 금 속 이온이 줄어들어 상대 산소 농도가 증가하게 된다. 이후 전해액 내에 잔존하는 다른 금속 이온이 산소와 반 응하여 안정한 부동태 피막을 형성시킨다. 앞서 말한 내 용을 본 연구에 대입하면, STS304 표면에 Fe 부동태 피 막이 형성되었다가 전해액으로 용출된 후 Cr와 반응하 여 안정적인 부동태 피막을 재형성시킨다. 따라서 전해 액 내 Fe 이온이 많을수록 보다 낮은 전위에서도 Fe 부 동태 피막을 형성시킬 수 있으며, 삼투력 차이로 인해 Fe 이온은 보다 빨리 용출된다. 그 결과 더 낮은 전위에 서 Cr 부동태 피막이 형성되기 시작하며, 우수한 평탄 도와 내식성을 가진 부동태 피막이 표면에 형성된다.13) 이러한 과정을 통해 형성된 부동태 피막은 매끄러운 표 면과 함께 높은 광택을 보이며, 기존 모재 보다 고농도 의 Cr, 저농도의 Fe를 가진다.17) 한편, Fe 부동태 피막 형성 및 Fe 이온의 용출로 인해 모재 내 Fe 감소되며, 이는 모재 내 상대적인 C농도를 높여 C r- C 형성으로 인 한 STS304 표면의 입계 부식을 촉진시킨다. 위와 같은 과정으로 인해 E1, E2로 전해 연마한 시편과는 다르게 E3로 전해 연마한 시편 표면에서[Fig. 4(c)] 입계가 명 확하게 형성된다. 부동태 피막이 형성되는 전위만을 고 려하여 전해액 내 Fe 이온을 과하게 첨가할 경우, 초기 형성된 Fe 부동태 피막에서 Fe 이온이 용출되지 않아 안 정적인 Cr 부동태 피막이 형성되지 않을 것이다. 반면, Cr 이온의 농도는 높을수록 Fe 이온이 용출된 부동태 피 막 내부로의 확산이 용이하므로 보다 빠르게 Cr 부동태 피막이 형성될 것으로 판단된다. 전해액 E3은 다른 전 해액에 비해 적은 Fe/Cr 비율을 (E1: 3.18, E2: 2.55, E3: 2.24) 보였다. 이는 다른 전해액에 비해 E3 전해액 에서 Cr 이온이 차지 하는 비율이 높다는 것을 의미하 며, 이는 안정적인 Cr 부동태 피막에 형성이 유리하다 는 것을 의미한다. 따라서 E3 전해액을 이용해 제조한 시편에서 가장 우수한 물성의 부동태 피막이 형성된 것 으로 추정된다.
4. 결 론
본 연구에서는 연마액 에 따른 부동태 피막형성 거동 에 대해 분석하였다. 분극 곡선 분석을 통해 전해 연마 에 적합한 온도(65 °C)를 선정하였으며, 각 전해액에 침 지시킨 STS304에 5V의 전압을 300초간 인가하여 전해 연마를 진행하였다.
1. 광학현미경을 이용해 각 시편의 표면을 관찰한 결 과, 전해액 종류에 따라 시편 표면의 미세구조는 다르 게 나타났으며, 연마액 내 철과 크롬 성분이 많을수록 표면이 점차 평탄해졌다. E3으로 전해 연마한 시편의 표 면에서는 은빛의 광택이 관찰되어 시편의 조도 또한 미 세구조 관찰 결과와 유사한 경향을 보였다. 연마액 내 철, 크롬 양이 증가함에 따라 더 감소하였으며, 이에 따 라 광택도는 증가하였다.
2. 염수 분무 후 E1에서 전해 연마한 시편의 표면 거 칠기가 높은 부분의 부식 응력 집중으로 인해 부식 현 상이 나타났으며, Cr의 양이 늘어남에 따라 부식현상이 사라졌다.
3. 전해 연마 과정을 통해 STS304 표면에 형성되는 부 동태 피막 형성 과정 및 조건은 아래와 같다.
-먼저, STS 304 표면에는 Fe 농도가 높은 부동태 피 막이 형성되며, Fe 이온 농도차에 기반된 삼투압에 인 해 부동태 피막의 철은 전해액으로 녹아 나오며, 형 성되는 빈자리를 Cr이 채워져 우수한 내식성의 부동 태 피막이 형성된다.
-전해액의 Fe 이온 농도가 과하게 높을 경우, 부동태 피막에서 Fe 용출과 함께 부동태 층으로의 Cr 이온 의 확산이 원활히 일어나지 않아 안정적인 Cr 부동 태 층이 형성되지 않는다.
-Fe 용출이 가능한 정도에서 전해액의 Fe 이온이 높 을수록, 그리고 전해액 내 혼합된 Cr 이온의 비율이 높을수록(Fe/Cr 비율이 낮을수록) 안정적인 Cr 부동 태 층 형성된다. 본 연구에서는 E3 전해액이 본 조 건에 가장 부합되는 조성으로 가장 우수한 특성의 부 동태 피막이 형성되었다.