1.서 론
오늘날 휴대용 전자기기의 사용이 증가하면서 에너지 저장 기술의 발전이 요구되고 있다.1) 이러한 요구를 충 족하고자 이차 전지가 개발되고 있으며, 특히 리튬이온 배터리는 중량이 작고, 부피당 에너지 밀도가 높은 장 점을 가지고 있다.2-5) 현재 리튬이온배터리는 대부분 유 기 용매인 액체 전해질을 사용하여 제작되게 된다. 그 러나 액체 전해질을 이용하여 제작하게 되면 충격 및 파 손에 의한 누액이 발생할 수 있으며, 누액으로 인한 발 화 및 폭발 위험성을 가지고 있다.6-9) 또한 액체 전해질 을 사용할 경우 형태 및 크기에 제한에 의해 점차 소 형화 되는 차세대 전자기기에 적용에 제한된다.
앞선 문제점들을 해결할 수 있는 방법 중 한가지로 모 든 구조가 고체로 되어있으며 박막 형태로 제작된 전고 체 박막 배터리(all-solid-state thin-film battery) 연구가 활발히 진행되고 있다.10) 전고체 박막 배터리는 액체전 해질의 누액에 따른 폭발 위험성에 대한 문제점을 해결 할 수 있을 뿐만 아니라 크기와 형태에 대한 제한을 받 지 않아 소형화 및 직접화가 가능하다는 장점을 가지고 있다. 그러나 고체전해질의 경우 액체전해질에 비해 낮 은 이온전도도 및 계면 저항 특성 때문에 낮은 전기화 학 특성을 나타내는 문제점들을 가지고 있다.11,12)
현재 산화물 고체전해질 중에서 Li7La3Zr2O12 (LLZO) 는 높은 이온전도도를 갖는 cubic phase를 갖기 위해서 고온 열처리 공정이 필요하며, 상온에서는 tetragonal phase로 바뀌면서 이온전도도가 떨어지기 때문에 Al, Ga 등의 원소를 도핑하여 상온에서도 cubic phase를 유지하 는 연구가 진행되고 있다. 그러나 박막 제조 시 5 00 °C 이상의 고온 열처리가 필요하며,13) 이는 전고체 박막 배 터리를 만들 때 계면 사이에 문제를 야기시킨다. 본 연 구에서는 sputtering 공정 중에 발생하는 리튬 손실을 보 상하기 위해 Li2O co-sputtering 방법을 사용하여 고온 열처리 공정이 요구되지 않는 비정질 LLZO를 제작하였 다.14) 이 때, Li2O의 power를 0, 20, 40, 60, 80 W로 변경하며 샘플을 제작하고 이온전도도를 측정했다. 또한, Pt 코팅된 Si 기판 위에 RF-sputtering으로 Li4Ti5O12 (LTO) 양극을 증착하고 위에 LLZO/Li2O 고체전해질을 적용한 전고체 박막 배터리를 제조하여 다양한 전기화 학 특성을 분석했다.
2. 실험방법
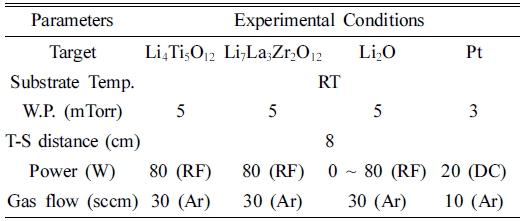
전고체 리튬이온배터리를 제작하기 위해 양극(LTO), 고 체전해질(LLZO) 그리고 음극(Lithium foil)을 사용했다. Silicon wafer 위에 DC sputtering 공정으로 Pt를 200 nm 증착한 후 RF sputtering 공정으로 LTO를 제작했으 며, 이때 Li4Ti5O12 target (LTO, TOSHIMA Manufacturing Co., Ltd, 3 In. Target, 99.99 %)을 사용하여 0.1 mm 두께로 증착했다. LTO 양극을 증착한 후 co-sputtering 공정으로 LLZO/Li2O를 제작했고, Li6.25La3Zr2Al0.25O12 target (LLZO, TOSHIMA Manufacturing Co., Ltd, 3 In. target, 99.99 %)과 Li2 O target (Li2O, TOSHIMA Manufacturing Co., Ltd, 3 In. Target, 99.99 %)을 사용 하여 0.5 mm 두께로 증착했다. 자세한 실험 조건은 표 1에 나타냈다. RF co-sputtering 방법으로 증착된 LLZO/ Li2O는 Li2O의 RF power를 20, 40, 60, 80 W로 변경 시키면서 증착하고 전기화학 특성을 평가하였다.
표면의 형상을 보기 위해 scanning electron microscopy (SEM; Hitachi, S4800)으로 확인했고, 박막의 표면거칠 기를 관찰하기 위해 atomic force microscopy (AFM; Nicon, Edipse Ti-U) 분석을 진행했다. RF co-sputtering 방법으로 제작한 박막의 결정 구조는 X-ray diffraction (XRD; Rigaku, Ultima iv) 분석으로 진행하였고, Cu Kα 방사선(Rigaku, D/MAX-2500)을 사용하는 기존의 X 선 회절로 분석했고 이때 측정 범위는 10 ~ 80° 사이에 서, 회절각은 2θ로 분석했다. 전기화학적 특성을 평가하 기 위해 글러브 박스(H2O < 1 ppm, O2 < 0.1 ppm)에서 2032 coin cell로 조립했다. 제작된 coin cell을 1 ~ 3V (vs Li/Li+) 범위에서 Cycle performance, C-rate 등 다양한 전기화학 분석을 진행하였다. 또한 이온전도도를 비교하기 위해 Pt/LLZO/Pt 계층 구조로 제작하여 electrochemical impedance spectroscopy (EIS; Ivium, Ivium-n-stat) 분 석을 진행하였다.
3. 결과 및 고찰
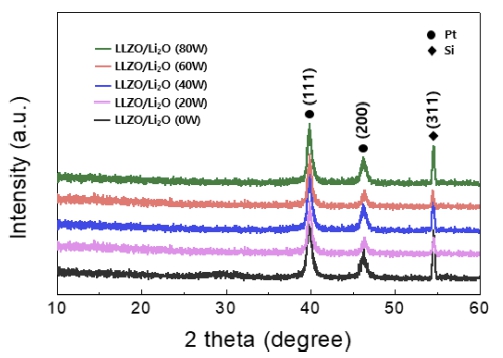
Fig. 1은 다양한 Li2O power 조건에 따른 LLZO 고체 전해질 박막들에 대한 XRD 분석 결과를 나타낸다. 모 든 샘플에서 (111), (200) 상이 확인되었으며, 각각의 피 크들은 기판에서 나타나는 Pt와 Si에 의해 나타나는 피 크들과 연관된다. 따라서, co-sputtering을 통해서 제작된 LLZO와 LLZO/Li2O 박막들은 기판 분석 결과와 동일 하게 나타나며, 결과적으로 모든 고체전해질 샘플은 비 정질 형태를 나타내며 Li2O co-sputtering에 의해서 고 체전해질 박막의 상 변화가 나타나지 않는 것을 알 수 있다.14-16)
다음으로, Fig. 2는 Li2O co-sputtering 유·무에 따른 표면 형상에 차이를 비교하기 위해 AFM 및 SEM 분 석 결과에 대해서 나타낸다. Fig. 2(a), (d)는 LLZO 및 LLZO/Li2O 샘플들에 대한 AFM 분석 결과이며 고체전 해질 박막의 표면 거칠기 root mean square (RMS) 값 차이는 각각 0.4, 0.5nm로 두 샘플 모두 부드러운 표 면 특성을 나타낸다. 이러한 결과는 Fig. 2(b), (e)의 SEM 표면 이미지에서도 동일하게 나타나는 것을 알 수 있다. 또한 SEM 단면 이미지를 통해 각각의 고체전해 질 두께가 약 500 nm로 제작되었음을 나타낸다[Fig. 2(c), (f)].
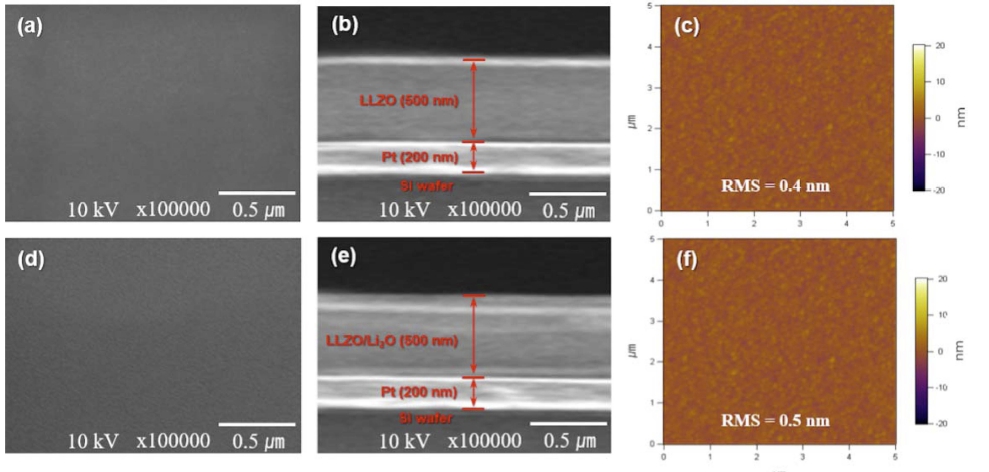
Fig. 2
SEM images of surface (a) LLZO, (d) LLZO/Li2O, and cross section (b) LLZO, (e) LLZO/Li2O. AFM images of (c) LLZO and (f) LLZO/Li2O.
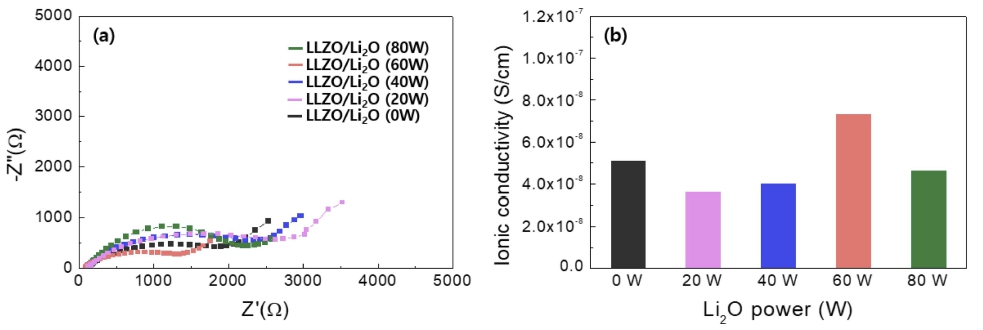
추가적으로, Li2O의 다양한 power에 따른 LLZO/Li2O 고체전해질 박막의 이온전도도 변화에 대해서 전기화학 임피던스 분광법을 통해 분석하였다. Fig. 3(a)는 각각의 조건에 따른 Nyquist plots을 보여주며, Pt/LLZO/Pt 형 태의 대칭구조 셀을 제작하여 AC 임피던스 분석기를 사 용하여 amplitude 5 mV, frequency 1,000 kHz ~ 1 Hz 범위에서 측정했다. 각 샘플에 대한 임피던스 값은 Li2O power를 0, 20, 40, 60, 80 W로 변경시켰을 때 각각 2000, 2800, 2500, 1400, 2200 Ω 값을 나타내며 Li2O 60 W 조건에서 가장 낮은 임피던스 값이 나타나는 것 을 알 수 있다. 또한, 측정된 임피던스 값을 이용하여 각 샘플에 대한 이온전도도를 계산하였으며 그 결과는 Fig. 3(b)에서 보여준다. 이온전도도는 식 (1)을 이용하 여 계산하였다.
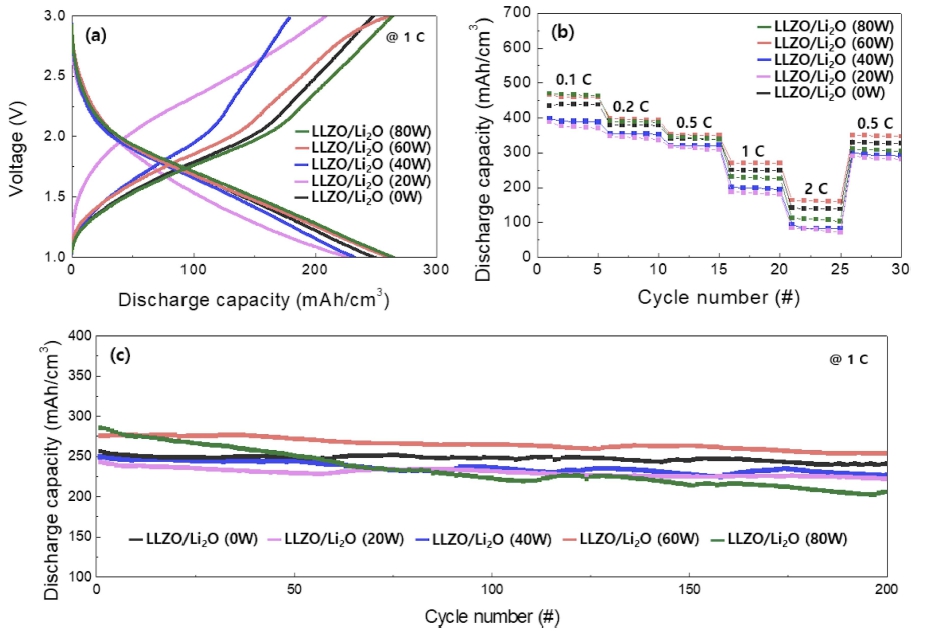
식 (1)에서 d는 박막의 두께 (cm), R은 박막의 저항 (ohm), A는 박막의 단면적(cm2)을 나타낸다.17,18) 이온전 도도 값은 LLZO/Li2O (0W)의 경우 5 .1 × 10-8 S/cm으 로 나타나며, Li2O power를 20, 40, 60, 80W로 변경했 을 때 각각 3.6× 10-8, 4.0 × 10-8, 7.3 × 10-8, 4.6 × 10-8 S/cm 값을 나타냈다. 다시 말해서, Li2O co-sputtering은 20 W 일 때 0 W 보다 낮은 이온전도도를 나타내지만 점차 Li2O 파워가 증가함에 따라서 점차 증가하는 결과 를 나타내며, 60 W 일 때 가장 높은 이온전도도를 나 타낸다. 그러나 80 W로 파워가 증가하게 되면 박막내 낮은 이온전도도를 나타내는 Li2O 함량이 증가함에 따 라서 임피던스 값이 증가하게 되고 이온전도도가 감소 되는 결과를 나타낸다.19,20) Fig. 4에서는 앞서 제작한 각 각의 고체전해질을 LTO 양극 위에 증착하여 전고체 박 막 배터리를 제작하고, 이에 따른 전기화학특성을 나타낸 다. Fig. 4(a)는 각 조건에 따른 charge-discharge curves 를 나타내며, Li2O power가 0, 20, 40, 60, 80W 일 때 각각의 방전 용량은 248, 227, 232, 260, 264 mAh/ cm3으로 나타난다. LLZO/Li2O (0 W) 기준으로 LLZO/ Li2O (20 W)와 LLZO/Li2O (40 W) 샘플들은 작은 방 전 용량이 구현되었으며, LLZO/Li2O (60 W), LLZO/ Li2O (80 W) 샘플들은 방전 용량이 향상되었고 특히 LLZO/Li2O (80 W)에서 가장 높은 방전 용량 특성이 구 현되었는데 이는 LLZO/Li2O co-sputtering 공정 중 LTO 전극 표면에 증착되는 Li2O가 리튬 보상 효과에 의한 일시적인 용량 상승 효과를 발생시킨다. 이러한 효과에 의해서 Li2O의 power가 증가할수록 점차 향상되는 것 을 알 수 있고 LLZO/Li2O (80 W)에서 높은 용량 특 성이 구현되는 것을 알 수 있다. Fig. 4(b)는 속도에 따 른 방전 용량 구현을 확인하기 위해 다양한 current density (0.1, 0.2, 0.5, 1, 2, 0.5 C)에서 율속 특성을 분석하였다. LLZO/Li2O (80 W) 샘플은 0.1 C에서 비 교적 높은 용량을 나타냈지만 current density가 증가할 수록 점차 방전 용량이 다른 조건에 비해 크게 감소하 는 결과를 보여준다. 또한, LLZO/Li2O (20 W), LLZO/ Li2O (40 W) 샘플들은 LLZO/Li2O (0 W) 샘플보다 모 든 current density 조건에서 낮은 방전 용량 특성을 보 여준다. 그러나 LLZO/Li2O (60 W) 샘플은 다른 샘플 들에 비해 current density 증가에 따라 용량 감소율이 작게 나타나며 결과적으로 Fig. 3에서 LLZO/Li2O (60 W) 샘플은 저항이 가장 작고 이온전도도는 가장 높은 것 을 확인했고 동일하게 율속 특성도 가장 높은 특성을 보 여주었다. Fig. 4(c)는 각각의 샘플들을 1 C (1 C = 598.5 mA)에서 200 cycle 동안 측정한 cycle performance 결 과를 나타낸다. LLZO/Li2O (0 W), LLZO/Li2O (20 W), LLZO/Li2O (40 W), LLZO/Li2O (60 W), LLZO/ Li2O (80 W) 샘플들에 대한 각각의 용량 유지율은 94, 91, 90, 90, 72 %로 대부분의 샘플들은 90 % 이상의 높 은 용량 유지율을 나타내는 반면에 LLZO/Li2O (80 W) 샘플은 가장 많은 리튬이 보상되면서 초기 용량이 가장 높게 나타나지만 Li2O의 비중이 증가함에 따라서 공기 중 노출에 대한 불안정성에 의하여 cycle 특성이 급격 히 저하되는 것으로 판단된다. 즉, Li2O co-sputtering은 리튬 보상 효과에 따른 전기화학적 특성 향상과 낮은 이 온전도성에 의한 리튬 이온의 이동 방해 효과가 상호 보 완적으로 작용하는 것을 알 수 있다. 따라서, LLZO/Li2O (20 W)는 낮은 이온전도성을 가지는 Li2O 첨가에 의해 LLZO/Li2O (0 W) 보다 낮은 전기화학 특성을 나타내 지만 Li2O의 파워 증가에 따라서 리튬 보상 효과에 의 해 전기화학 특성이 향상된다. 그러나 Li2 O의 파워가 80W 이상으로 증가하게 될 경우 낮은 이온전도성의 Li2O에 의해 전기화학 특성이 오히려 감소하는 것을 알 수 있다.
4. 결 론
LLZO를 Li2O와 co-sputtering을 통해서 고이온전도성 박막 고체전해질을 제작하였다. AFM으로 분석한 결과 RMS가 1 nm 이하의 부드러운 박막이 제조되었다. 박 막 고체전해질의 최적의 조건을 찾기 위해 Li2O의 파워 에 따라서 박막을 제작하였고, LLZO/Li2O (60W) 조건 은 7.3 × 10-8 S/cm로 가장 높은 이온전도도를 나타냈다. 최적화된 LLZO/Li2O (60 W) 고체전해질을 이용하여 LTO/LLZO/Li 구조로 전고체 박막 전지를 제작하였으 며, 전기화학 특성은 1 C에서 260 mAh/cm3의 높은 초 기 방전 용량과 200 cycle 후 90%의 용량 유지율 및 가장 높은 율속 특성을 나타냈다. 본 연구 결과를 통해 LLZO를 Li2O와 co-sputtering 방법으로 제작한 샘플이 전기화학 특성을 향상시키는 것을 확인했으며 이 고체 전해질을 사용하여 크기 및 형태에 제한을 받지 않는 고 성능 박막 배터리를 개발하는데 사용될 것으로 기대된다.