1. 서 론
최근에 고효율의 백색광 소자를 제조하기 위하여 기본 삼색인 적색, 녹색, 청색(RGB)을 발광하는 연색지수가 높 은 형광체 개발에 많은 연구가 진행되고 있다.1,2) 특히, 높은 발광 세기를 갖는 적색 계열의 형광체 분말의 제 조는 백색 발광 다이오드의 연색지수를 향상시키기 위 해서 필수적이며, 고체 광원과 디스플레이 같은 다양한 광 전자 소자 제작 영역으로 그 응용성을 확장시킬 수 있다.
희토류 원소를 기반으로 하는 적색 발광 계열의 형광 체를 제조하기 위한 중요한 요소는 열과 화학적으로 안 정한 모체 결정의 선택과 모체 결정에 주입되는 활성제 이온의 적절한 도핑 농도를 결정하는 것이다. 발광 센 터로 작용하는 활성제 이온의 주 발광 파장과 세기는 모 체 결정 내에 위치하는 활성제 이온 주위 환경에 따라 결정되는 것으로 보고되고 있다.3) 활성제 이온의 전기 쌍 극자 전이(electric dipole transition)에 의한 발광의 경우 에 발광 파장과 세기는 활성제 이온 주변의 환경에 매우 민감하고 활성제 이온은 비반전 대칭 자리(non-inversion symmetry)에 위치하지만, 자기 쌍극자 전이(magnetic dipole transition)에 의한 발광의 경우에 발광 파장과 세 기는 활성제 이온 주위의 결정장에 전혀 영향을 받지 않 으며 활성제 이온은 반전 대칭(inversion symmetry) 자 리를 차지한다.4)
최근 연구자들은 활성제 이온의 전이에 의한 발광 세 기를 증가시키고 모체 결정 내에 위치하는 활성제 이온 주변의 대칭성을 조사하기 위하여 다양한 제조 방법과 성장 조건을 선택하고 있다. 예를 들면, Li와 Liu5)는 졸 겔 방법을 사용하여 Ba2CaMoO6 몰리브덴산염 모체 결 정에 Eu3+ 이온을 도핑한 형광체를 제조하였으며, 380 nm로 여기시켰을 때 Eu3+ 이온의 5D0→7F1 (595 nm) 자기 쌍극자 전이에 의한 주황색 발광의 세기가 주된 발광이 며 최적의 도핑 농도가 6 mol%임을 보고하였다. Li 등6) 은 고상반응법을 사용하여 Mo/W의 비를 변화시키면서 1,200 ºC에서 2 h동안 소결시켜 Sr2MgMoxW1-xO6:Eu3+ 적색 형광체를 합성하였으며, Mo의 함량비가 40 % 이 상으로 증가함에 따라 615 nm에 피크를 갖는 적색 발 광의 세기가 감소함을 관측하였다. Liao 등7)은 수열법으 로 MWO4:Sm3+ (M = Ca, Sr, Ba) 형광체를 제작하였으 며, 404 nm로 여기시켰을 때 가장 강한 644 nm의 적색 발광을 나타냄을 발표하였다.
본 연구에서는 높은 발광 세기를 갖는 주황색과 적색 형광체를 제조하기 위하여 고상반응법을 사용하여 두 종 류의 활성제 Sm3+와 Eu3+ 이온을 열 및 화학적으로 안 정한 페로브스카이트(perovskite) 물질인 BaSiO3 모체 결 정에 도핑하였다. 두 활성제 이온의 농도를 변화시키면 서 합성한 형광체 분말의 결정 구조, 입자의 크기와 모 양, 흡광과 발광 파장 및 세기, 농도 소광 현상이 발생 하는 활성제 이온 사이의 임계 거리를 조사하였다. 특 히, 가장 강한 주황색과 적색 발광을 방출하는 형광체 를 합성하기 위한 최적의 활성제 이온의 농도를 결정하 였다.
2. 실험 방법
Ba1-1.5xSiO3:xRE3+ (RE = Sm, Eu) 형광체 분말 시료는 초기 물질 BaO (순도: 99.9 %), SiO2 (99.95 %), Sm2O3 (99.9 %), Eu2O3 (99.9 %)를 화학양론적으로 합성하였으 며, 이때 희토류 활성제 이온의 몰 비(x)를 0, 1, 5, 10, 15, 20 mol%로 변화시켰다. 화학 반응은 식 (1)과 같다:
초기 물질은 정밀 저울을 사용하여 측량한 후에, 직경 3 mm의 ZrO2 볼과 함께 몰 비에 따라 분류하여 플라스 틱 통에 넣고, 적정량의 에탄올을 채우고 밀봉하여 볼 밀(ball-mill) 장치를 사용하여 400 rpm의 속도로 24시간 동안 혼합과 분쇄 작업을 수행하였다. 그 후에, ZrO2 볼 을 체(sieve)로 걸러내고 혼합 용액을 비커에 담아 70 ºC 의 건조기에서 20시간 동안 건조시켰다. 건조된 시료는 아게이트 막자 사발에서 미세하게 갈아 80 μm 크기의 체 로 걸러내었고, 몰 별로 알루미나 도가니에 담아 전기 로에 넣어 500 ºC에서 3시간 동안 하소 공정을 실시하 였고 1,100 ºC에서 5시간 동안 소결하여 제조하였다8).
형광체 분말 시료의 결정 구조는 파장 0.15406 nm의 Cu-Kα 복사선을 사용하는 X-선 회절 장치(Ultima IV, Rigaku)를 사용하여 회절각 10~70º 영역에서 조사하였고, 형 광체 분말의 표면 미세 구조는 전계 방출형 주사전자현미 경(FE-SEH, Field effect-Scanning electron microscope, S4300, Hitachi)을 사용하여 촬영하였다. 형광체의 광학 특성은 제논 램프를 광원으로 갖는 형광광도계(FS-2, Scinco)를 사용하여 상온에서 측정하였다.
3. 결과 및 고찰
Fig. 1(a)와 1(b)는 모체 결정 BaSiO3에 도핑되는 활 성제 Sm3+와 Eu3+ 이온의 몰 비 (x)를 각각 x = 0, 1, 5, 10, 15, 20 mol%씩 변화시키면서 합성한 BaSiO3 형광체 분말 시료에서 측정한 X-선 회절 결과를 나타낸 것이 다. 두 종류의 활성제 Sm3+와 Eu3+ 이온의 몰 비에 관 계없이, 모든 형광체 분말 시료는 회절각 2θ = 26.07°에 서 최대 회절 세기를 갖는 주 피크와 상대적으로 약한 세기를 갖는 17.31º, 21.29o, 24.08o, 26.69o, 39.27o, 40.32o, 44.42o, 48.13o에 중심을 둔 회절 피크들로 구성 되었다. 전자는 (111)면에서 발생한 회절 피크이며, 후자 는 (011), (012), (102), (013), (200), (122), (115), (124) 면에서 발생한 회절 피크들이다. 합성한 형광체 분말의 결정 구조는 ICDD #01-070-2112에 제시된 회절 상과 일치하는 사방정계(orthorhombic system) 임을 확인할 수 있었다. Fig. 1(a)에서 보듯이, BaSiO3:Sm3+ 형광체 분말 시료의 경우에 주 회절 (111) 피크의 반치폭(full width at half maximum)은 5 mol%에서 최소값인 0.11º이었고, Sm3+의 몰 비가 증가함에 따라 반치폭의 크기는 증가 하였다. 한편, Fig. 1(b)에서 보듯이, BaSiO3:Eu3+ 형광 체 시료의 경우에 반치폭의 크기는 10 mol%에서 최소 값 0.11º을 나타내었고, Eu3+ 이온의 몰 비가 증가함에 따라 반치폭의 크기는 증가하였다. 주 회절 (111) 피크 에서 얻은 데이터와 Scherrer의 식9)을 사용하여 구한 BaSiO3:Sm3+ 형광체 결정 입자의 평균 크기는 78~84 nm 이었고, Sm3+의 몰 비가 5 mol% 일 때 최대 크기를 보 였다. BaSiO3:Eu3+ 형광체 분말 시료의 경우에 결정 입 자의 평균 크기는 76~85 nm이었고, 10 mol%에서 최대 값을 나타내었다.
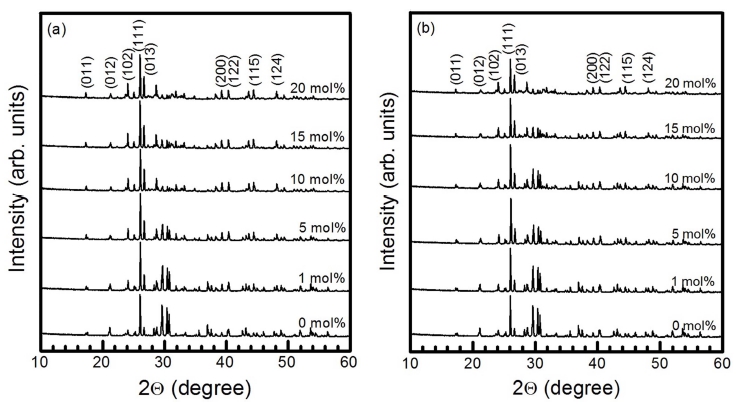
Fig. 1
XRD patterns of BaSiO3 phosphors doped with different concentrations of (a) Sm3+ and (b) Eu3+ ions.
Fig. 2는 Sm3+ 이온의 몰 비(x)를 (a) x = 0, (b) 1, (c) 5, (d) 10, (e) 15, (f) 20 mol% 도핑한 Ba1-1.5xSiO3:xSm3+ 형광체와 Eu3+ 이온의 몰 비를 (g) x = 0, (h) 1, (i) 5, (j) 10, (k) 15, (l) 20 mol% 도핑한 Ba1-1.5xSiO3:xEu3+ 형광 체 분말에서 형성된 결정 입자의 표면 미세 구조를 주 사전자현미경으로 촬영한 것이다. Fig. 2(a)에서 보듯이, Sm3+ 이온이 도핑되지 않은 BaSiO3 시료의 경우에 결정 입자의 평균 크기는 500 nm이었으며, Sm3+의 몰 비가 10 mol%로 증가함에 따라 결정 입자는 서로 용해되어 증 가하는 추세를 나타내었고, 20 mol%로 증가함에 따라 입 자의 크기는 크게 감소하였다. Fig. 2(h)에서 보듯이, Eu3+가 1 mol% 도핑된 BaSiO3 시료의 결정 입자는 불 규칙하게 서로 용해되어 사슬 모양을 형성하고 있으며, 크기는 약 2 μm이었다. Eu3+ 이온의 몰 비가 더욱 증가 함에 따라 결정 입자는 큰 덩어리를 형성하며 증가하는 추세를 보이다가 20 mol%에서 결정 입자의 크기는 현 저히 감소하였다.

Fig. 2
SEM surface images of the Ba1-1.5xSiO3:xSm3+ phosphors doped with (a) x = 0, (b) 1, (c) 5, (d) 10, (e) 15, and (f) 20 mol%, and the Ba1-1.5xSiO3:xEu3+ phosphors doped with (g) x = 0, (h) 1, (i) 5, (j) 10, (k) 15, and (l) 20 mol%.
Fig. 3(a)와 3(b)는 활성제 이온 Sm3+와 Eu3+의 몰 비 를 각각 변화시켜 합성한 BaSiO3 형광체 분말에서 측정 한 여기(photoluminescence excitation) 스펙트럼의 결과 를 나타낸 것이다. Fig. 3(a)에서 보듯이, 방출 파장 604 nm에서 모니터링 하면서 측정한 BaSiO3:Sm3+ 형광체의 경우에 두 종류의 흡광 스펙트럼이 관측되었다. 238 nm 에 피크를 갖고 210~260 nm에 걸쳐서 넓게 분포하는 Sm3+ 양이온과 O2- 음이온들 사이에 발생한 전하 전달 밴 드(charge transfer band; CTB)에 의한 신호와 Sm3+ 이 온의 4f5 전자 배열 내에서 발생한 4f→4f 전이 신호이 다.10) 특히, 347, 365, 377, 406, 476 nm에 피크를 갖는 흡광 스펙트럼은 Sm3+ 이온의 낮은 에너지 상태인 6H5/2 준위에서 4H9/2, 4D3/2, 6P7/2, 4G7/2, 4I11/2 에너지 준위로 각각 전이하면서 발생한 신호이다.11,12) Sm3+ 이온의 몰 비가 1 mol%에서 5 mol%로 증가함에 따라 Sm3+ 이온에 의한 4f 전이 신호의 흡광 세기가 증가하여 5 mol%에 서 최대가 되었으며, Sm3+ 이온의 몰 비가 더욱 증가함 에 따라 모든 흡광 신호의 세기는 점차적으로 감소하여 20 mol%에서 최소를 나타내었다. 이 경우에, 주 흡광 파 장이 406 nm이므로 자외선 혹은 청색 발광 다이오드 표 면에 도포하여 황녹색 발광 소자 개발에 응용할 수 있 다. Fig. 3(b)에서 보듯이, 방출 파장 621 nm에서 모니 터링 하면서 측정한 BaSiO3:Eu3+ 형광체 분말의 흡광 스 펙트럼은 276 nm에 피크를 갖고 240~330 nm 영역에 걸 쳐 넓게 분포하는 Eu3+ −O2- 이온들 사이에 발생한 CTB 신호와 상대적으로 밴드폭이 좁고 파장 영역 350~500 nm에서 Eu3+의 4f6 전자 배열 내에서 발생하는 4f→4f 전이 신호로 구성되었다.13) 이중에서, 366, 386, 397, 468 nm에 피크를 갖는 흡광 파장은 Eu3+ 이온의 낮은 에 너지 상태인 7F0 에너지 준위에서 여기 상태인 5D4, 5G2, 5L6, 5H2 에너지 준위로 각각 전이하면서 발생한 스펙트 럼이다.14) Eu3+ 이온의 몰 비가 1 mol%에서 15 mol%로 증가함에 따라 모든 흡광 스펙트럼의 세기는 순차적으로 증가하여 15 mol%에서 최대를 나타내었으며, 20 mol%에 서 급격하게 감소하였다.
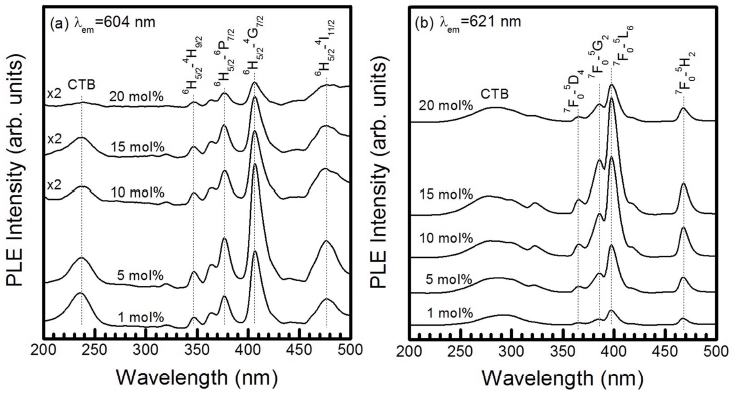
Fig. 3
Excitation spectra of BaSiO3 phosphors doped with different concentrations of (a) Sm3+ and (b) Eu3+ ions.
Fig. 4(a)는 서로 다른 파장(238, 377, 406, 476 nm)으 로 여기시킨 Sm3+ 이온이 5 mol% 도핑된 BaSiO3:Sm3+ 형광체 분말에서 측정한 발광(photoluminescence) 스펙트 럼을 나타낸 것이다. 여기 파장의 종류에 관계없이, 형 광체는 네 종류의 발광 스펙트럼을 나타내었다. 발광 세 기가 가장 강한 604 nm에 피크를 갖는 Sm3+ 이온의 4G5/2→6H7/2 자기 쌍극자 전이에 의한 주황색 발광, 상대 적으로 약한 567 nm에 피크를 갖는 4G5/2→6H5/2 자기 쌍 극자 전이에 의한 황색 발광, 4G5/2→6H9/2 전기 쌍극자 전 이에 의한 651 nm의 적색 발광, 4G5/2→6H11/2 전기 쌍극 자 전이에 의한 711 nm의 적외선 발광이 관측되었다.15) 상기의 발광 스펙트럼 중에서, 4G5/2→6H7/2 (604 nm) 자 기 쌍극자 전이에 의한 주황색 발광 스펙트럼의 세기가 최대이었다. 이 결과는 Sm3+ 이온이 도핑된 Sr3Bi(PO4)3 형광체에서 관측된 결과와 동일하였다.16) 여기 파장의 변 화에 따른 발광 파장의 위치는 이동하지 않았지만, 발 광 스펙트럼의 세기는 큰 변화를 보였다. 청색 파장 406 nm로 여기시켜 발생한 604 nm의 주 발광 스펙트럼의 세 기는 238 nm로 여기시켰을 때 발생한 주 발광 세기의 크기 보다 3배 증가하였다. Fig. 4(b)는 파장 406 nm로 여기시켰을 때, Sm3+ 이온의 몰 비를 1~20 mol%로 변 화시키면서 합성한 BaSiO3:Sm3+ 형광체 분말의 발광 파 장과 세기를 나타낸 것이다. Sm3+ 이온의 몰 비가 1 mol% 에서 5 mol%로 증가함에 따라 네 종류의 발광 스펙트 럼의 파장 이동은 관측되지 않았지만, 발광 세기는 급 격히 증가하여 5 mol%에서 최대값을 나타내었으나, Sm3+ 이온의 몰 비가 10, 15, 20 mol%로 증가함에 따라 모든 발광 피크의 세기는 현저히 감소하여 20 mol%에서 최 소값을 나타내었다. 604 nm 주황색 발광의 경우에, Sm3+ 이온이 5 mol% 도핑되었을 때 발광 세기에 비하여 20 mol% 일때의 발광 세기는 약 8.7배 감소하였다. Sm3+ 이온의 몰 비가 5 mol% 이상으로 증가함에 따라 발광 세기가 감소하는 현상은 발광 센터의 역할을 하는 활성제 Sm3+ 이온의 몰 농도가 임계 농도(critical concentration) 인 5 mol% 이상으로 증가함에 따라 활성제 Sm3+ 이온 들 사이의 거리가 가까워져서 활성제 이온들 사이에 발 생하는 비복사선 에너지 전달로 인하여 발광 세기가 감 소하는 농도 소광(concentration quenching) 현상으로 해 석할 수 있다.17) 모체 결정 내에 위치하는 활성제 Sm3+ 이온들 사이의 임계 거리(critical distance) Rc는 Blasse 의 식,
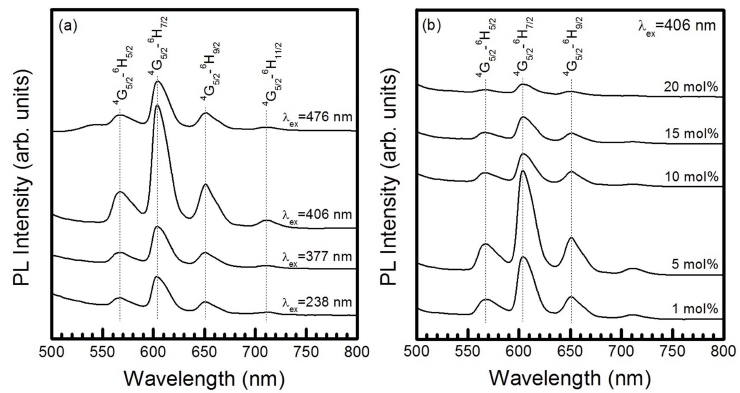
Fig. 4
(a) photoluminescence spectra of BaSiO3:Sm3+ phosphors under different excitation wavelengths and (b) emission spectra as a function of Sm3+ doping concentration.
를 사용하여 계산할 수 있다.18) 여기서 χc는 Sm3+ 이온 의 임계 농도, V는 단위 셀의 체적, N은 단위 셀당 모체 양이온의 수이다. 본 연구의 경우에, BaSiO3 모체 결정의 체적과 단위 셀당 양이온의 수는 각각 V = 319.457Å3, N = 4이고, 농도 소광 현상이 발생하는 임계 농도 χc는 5 mol%이므로, 상기의 값을 식 (2)에 대입하여 계산한 임 계 거리 Rc의 값은 Rc = 14.5 Å 이었다. 활성제 Eu3+ 이 온의 임계 농도는 15 mol% 이므로 Eu3+ 이온들 사이의 임계 거리는 Rc = 10.1 Å이었다.
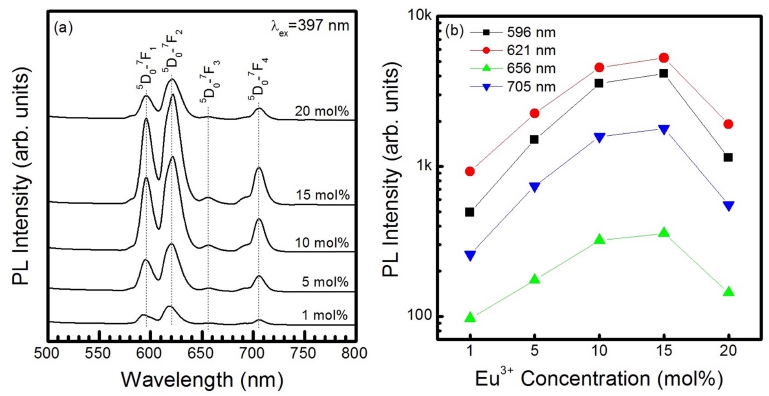
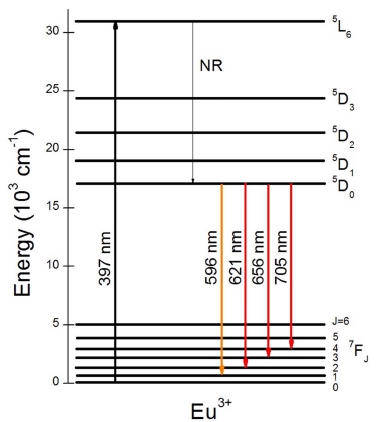
Fig. 5(a)는 활성제 Eu3+ 이온의 몰 비를 변화시켜 합 성한 BaSiO3:Eu3+ 형광체 분말에서 측정한 발광 스펙트 럼을 나타낸 것이다. 파장 397 nm로 여기 시킨 모든 BaSiO3:Eu3+ 형광체 분말의 발광 스펙트럼은 비복사선 (nonradiative, NR) 과정을 거친 후에 Eu3+ 이온의 5D0→ 7F2 전기 쌍극자 전이에 의해 발생한 발광 세기가 가장 강한 621 nm의 적색 발광 신호을 포함하여 5D0→7F1 자 기 쌍극자 전이와 5D0→7F4 전기 쌍극자 전이에 의한 각 각 596 nm의 주황색 발광 신호와 705 nm의 적외선 발 광 신호, 발광 세기가 미약한 5D0→7F3 전기 쌍극자 전 이에 의한 656 nm의 적색 발광 스펙트럼으로 구성되었 다(Fig. 6 참조).19) Fig. 5(b)에서 보듯이, Eu3+ 이온의 몰 비가 1~15 mol%로 증가함에 따라 모든 발광 스펙트럼 의 세기는 점차적으로 증가하여 15 mol% 일 때 최대를 나타내었으나, 20 mol% 일 때는 농도 소광 현상에 의 하여 발광 세기가 현저히 감소하였다. 일반적으로 형광 체의 경우에, 최대 발광 파장과 세기는 모체 결정에 도 핑되는 활성제 이온을 둘러싸는 국소적인 환경이 대칭 자리에서 변형되는 정도에 따라 달라지고, 전기 쌍극자 전이인 경우에 모체 결정 내에 위치하는 활성제 이온은 비반전 대칭 자리(non-inversion symmetry sites)에 위치 하며, 자기 쌍극자 전이의 경우에 활성제 이온은 반전 대칭 자리(inversion symmetry sites)에 위치하는 것으로 보고되고 있다.20) 본 연구의 경우에, Eu3+ 이온의 몰 농 도가 1, 5, 10, 15, 20 mol%일 때, Eu3+ 이온의 5D0→ 7F2 (621 nm) 전기 쌍극자 전이에 의한 적색 발광의 세 기가 5D0→7F1 (596 nm) 자기 쌍극자 전이에 의한 주황 색 발광의 세기에 비하여 각각 1.9, 1.5, 1.3, 1.3, 1.7 배 증가하였다. 그러므로 Eu3+ 이온은 BaSiO3 모체 격자 내 에서 비반전 대칭 자리에 위치하는 것으로 판단할 수 있 다. 실험 결과를 종합하면, 본 연구에서 합성한 BaSiO3:Eu3+ 적색 형광체의 경우에 Eu3+의 몰 비가 15 mol%일 때 최 대 발광 세기를 갖는 최적의 조건임을 알 수 있다.
4. 결 론
활성제 Sm3+과 Eu3+ 이온의 몰 비를 조절하면서 BaSiO3:Sm3+ 주황색 형광체와 BaSiO3:Eu3+ 적색 형광체 분말을 고상반응법으로 합성하였다. 활성제 이온의 몰 비 와 종류에 관계없이, 모든 형광체는 26.06°에서 최대 세 기를 갖는 주 회절 (111) 피크가 관측되었으며, 결정 구 조는 사방정계이었다. 결정 입자는 활성제 이온의 몰 비 가 증가함에 따라 서로 뭉치면서 비대칭적인 모양을 보 였다. BaSiO3:Sm3+ 형광체의 흡광 스펙트럼은 CTB 신 호와 Sm3+ 이온의 4f→4f 전이 신호로 구성되었고, 주 발광 스펙트럼은 604 nm에 피크를 갖는 주황색 발광 신 호이었다. BaSiO3:Eu3+ 형광체 분말의 경우에 주 흡광 스 펙트럼은 397 nm에 피크을 갖는 Eu3+ 이온의 7F0→5L6 전이 신호이었으며, 주 발광 스펙트럼은 621 nm의 적색 발광 신호이었다. 실험 결과로부터 최대 발광 세기를 갖 는 주황색과 적색 형광체 제조를 위한 최적의 Sm3+과 Eu3+ 이온의 몰 농도는 각각 5 mol%와 15 mol%임을 확 인할 수 있었다.