1. 서 론
2. 실험 방법
2.1. 전해질 제조
2.2. 전지 제작
2.3. 측정 및 분석
3. 결과 및 고찰
3.1. 재료 특성
3.2. 전기화학적 임피던스 측정
3.3. 방전 거동
4. 결 론
1. 서 론
현대 사회는 다양한 형태의 산업혁명을 거치며 급속도로 발전하는 기술로 인해 삶의 질이 크게 향상되었으나 그 과정에서 환경의 오염과 파괴를 야기해왔다. 특히, 휘발유나 경유를 연료로 사용하는 내연기관으로 작동하는 자동차의 경우 지구 온난화의 주 원인으로 꼽히고 있다. 내연기관을 탑재한 자동차는 엔진의 구동을 위해 연료를 소모하는 과정에서 유해 물질의 배출로 인해 온실가스, 미세 먼지 등과 같은 환경 문제를 초래한다. 그 결과, 가뭄, 폭우, 기온 상승 등 이상기후 및 지구온난화가 가속화되고 있다. 또한 화석연료의 고갈로 인해 발생되는 다양한 문제에 대한 대응 방안도 마련되어야 한다. 결과적으로 다양한 문제의 해결을 위해 차세대 자동차에 많은 연구가 진행되고 있으며, 하이브리드 자동차, 연료전지 자동차, 전기 자동차 등에 대한 관심이 증가하고 있다. 특히 에너지의 효율성을 향상시키고 환경의 유해 물질의 배출을 최소화할 수 있는 전기 자동차의 생산과 소비가 전 세계적으로 증가하고 있는 추세이다.
전기 자동차의 주 동력원은 이차전지라고 할 수 있다. 더불어 이차전지는 스마트폰이나 태블릿PC 등의 차세대 모바일 기기가 등장함으로써 에너지 저장장치로 많은 관심을 받고 있다. 또한 차세대 기기의 발전으로 다양한 형태 및 구조를 갖추며 무게 및 부피당 높은 용량을 갖도록 발전해 가고 있다.
현재 가장 대표적으로 사용되는 이차전지는 리튬이온 전지이다. 리튬이온 전지가 가장 널리 사용되는 이유로는 우수한 충방전 효율과 높은 비용량, 낮은 자가 방전율 및 기억효과 등이 있다. 하지만 리튬이온 전지는 인화성 및 가연성이 높은 전해질로 구성되어 있어 화재와 폭발의 위험이 존재해 안전성 측면에서 단점이 있다.1) 또한 리튬이온 전지에 사용되는 소재인 리튬의 매장량 감소로 인한 비싼 가격과 제조 과정에서 환경에 유해한 물질이 사용된다는 문제가 있다. 결과적으로 리튬이온 전지를 대체할 수 있는 차세대 전지의 개발 및 연구가 필요하다.
최근 개발 및 연구되는 차세대 전지로는 리튬-황, 나트륨이온, 전고체, 금속-공기 전지 등이 있다. 이중 금속-공기 전지는 가벼운 무게를 가지고 양극을 공기로 사용해 친환경적이며, 재충전이 가능하고 높은 에너지 밀도를 갖는다는 장점이 있다.2) 또한 금속의 종류에 따라 마그네슘-공기, 알루미늄-공기, 철-공기, 아연-공기 등의 다양한 전지로 구성되어 있다. 하지만 마그네슘-공기 전지와 알루미늄-공기 전지는 낮은 안전성과 가역성으로 연구 단계가 더디며, 철-공기 전지는 비싼 제작 비용으로 인해 상용화의 어려움이 있다.3) 금속-공기 전지의 종류 중 하나인 아연-공기 전지는 높은 용량을 가지고 있고 리튬이온 전지보다 대략 5배 정도의 저렴한 제조비용과 약 4배 높은 에너지 밀도를 가지며, 수계 전해질을 사용하기 때문에 화재와 폭발의 위험성도 적다. 또한 음극으로 사용되는 아연은 독성이 낮고 환경에 미치는 부정적인 영향이 적어 환경 친화적이다. 특히 아연의 매장량이 충분하고 화학적으로 안전성을 가지고 있다.4)
아연-공기 전지의 방전 반응식을 식(1), (2), (3), (4)에 나타냈다.5)
하지만 수계 전해질을 사용하기 때문에 음극과 전해질과의 반응으로 부식을 초래하고 음극으로의 불균일한 증착으로 생성되는 수상돌기에 의해 전지의 성능이 감소한다.6) 또한 수계 전해질이 증발되는 문제가 있으며, 공기 중의 산소를 양극으로 사용하기 때문에 완전한 밀봉이 어려워 전해질의 증발을 촉진시켜 배터리의 수명이 감소되는 단점이 존재한다. 최근 아연-공기 전지에 관한 연구동향으로 Douka et al.7)의 전이금속 촉매를 이용해 oxygen reduction reaction (ORR)및 oxygen evolution reaction (OER) 성능을 향상시켜 배터리의 효율성을 최적화하는 연구가 진행되고 있다. 또한 Jiao et al.8)은 폴리아크릴아미드와 구연산 나트륨을 사용하여 젤 전해질을 제조했으며, 젤 전해질에 극성기인 -COO가 다량 함유되어 있어 수분의 동결 및 증발을 억제해 높은 수분 유지율을 보고했다. 따라서 아연-공기 전지의 단점을 해결하기 위해 젤 형태의 전해질 혹은 첨가제를 이용하는 연구가 진행되는 중이다.9)
젤 형태의 고분자 전해질은 액체 전해질에 비해서 불필요한 화학적 반응의 빈도가 적고 분리막이 따로 필요 없으므로 수상돌기의 형성으로 인해 분리막이 찢어지는 현상을 방지할 수 있다. 또한 가교된 고분자 물질은 액체를 흡수 및 저장하는 팽윤이라는 특징도 가지고 있다.10) 이처럼 고분자 물질에 액체 전해질을 흡수시켜 저장하는 방법도 가능하다. 아연-공기 전지에 사용되는 고분자 전해질의 소재로는 폴리비닐 알코올, 폴리(아크릴산), 셀룰로오스 등이 있다. 이들 중 폴리비닐 알코올은 극성기(-OH)를 가지고 있어 쉽게 수분과 혼합되는 높은 친수성을 가진다. 또한 폴리비닐 알코올은 분자 내부의 변화와 환경적인 요인 등으로 산화 및 분해를 하는 생분해성 물질이라서 일회용 플라스틱의 대체가 가능한 친환경적인 소재 중 하나이다.11) 결과적으로 수계 전해질을 사용하며 친환경적이라는 장점을 가진 아연-공기 전지에 가장 어울리는 고분자물질은 폴리비닐 알코올이라고 할 수 있다.
폴리비닐 알코올은 경직된 물성을 가지고 있어 높은 기계적 강도를 지니고 있다. 하지만 고분자 전해질은 경직됨에 따라 감소된 이온전도도를 제공하기 때문에 전지의 성능을 저하시키는 원인이 된다. 또한 폴리비닐 알코올은 알칼리성 수용액의 농도가 증가될수록 인장강도도 증가된다. 따라서 높은 농도의 알칼리성 수용액을 흡수 및 저장하는데 어려움이 있다.12,13) 결과적으로 폴리비닐 알코올로만 고분자 전해질을 제조하는 방법은 한계가 존재하기 때문에 이러한 측면을 개선하기 위해서 첨가제를 사용하는 방법도 연구되고 있다. 최근 연구에서는 금속염 중 하나인 아세트산 아연이 고분자의 기계적 안정성과 기계적 성질 등을 향상시키며, 이온전도도 향상에 도움을 줄 수 있다는 결과가 나타나 있다.14,15)
본 연구에서는 폴리비닐 알코올과 아세트산 아연을 혼합해 고분자 전해질을 제조하였다. 제조 후 전해질 내부의 저항을 통해 이온전도도를 측정과 함께 전해질의 결정구조 및 온도에 따른 질량 변화를 통해 고분자 전해질의 합성 여부를 확인하였다. 더불어 충전/방전 테스트를 통해 전지의 수명 및 방전용량 또한 확인하였다.
2. 실험 방법
2.1. 전해질 제조
초순수 30 mL에 아세트산 아연 이수화물(98.0 %, DUKSAN, Korea)을 1.3 g, 2.6 g, 4 g (0.2 M, 0.4 M, 0.6 M) 씩 각각 500 rpm으로 용해하였다. 용해된 액체에 폴리비닐 알코올(Mw 89,000~98,000, SIGMA-ALDRICH, USA) 4 g을 천천히 첨가해 95 °C에서 1,000 rpm으로 2시간 동안 혼합하였다. 혼합된 용액에 글루타르알데히드 용액(GL, Technical ~50 %, SIGMA-ALDRICH, USA) 0.1 g과 글리세린(GC, 98.0 %, DAEJUNG, Korea) 0.1 g을 첨가한 후 500 rpm으로 대략 20초간 교반하였다. 그 다음 염산(HCL, 35.0 %, DAEJUNG, Korea) 10 mL와 초순수 100 mL를 혼합한 액체를 첨가하고 다시 500 rpm으로 대략 20초간 교반하였다. 혼합된 용액을 ABS 수지로 제작된 몰드(20 mm × 40 mm × 4 mm)에 담아 0 °C 이하인 환경에서 12시간 이상 보관해 gel polymer를 제조하였다. 제조된 젤 고분자를 초순수 100 mL에 수산화 칼륨(KOH, 85.0 %, DAEJUNG, Korea) 39.6 g을 첨가해 만든 6 M의 KOH 용액에 24시간 동안 함침 시켰다. 이렇게 제조된 젤 고분자 전해질(gel polymer electrolyte, GPE)은 첨가된 아세트산 아연 이수화물의 양에 따라서 Table 1에 나타내었다.
Table 1.
Information regarding the GPE synthesis.
| Materials |
Polyvinyl alcohol (g) |
Zinc acetate dihydrate (g) |
Concentration (M) |
| GPE | 4 | 0 | 0 |
| 0.2 GPE | 4 | 1.3 | 0.2 |
| 0.4 GPE | 4 | 2.6 | 0.4 |
| 0.6 GPE | 4 | 4 | 0.6 |
2.2. 전지 제작
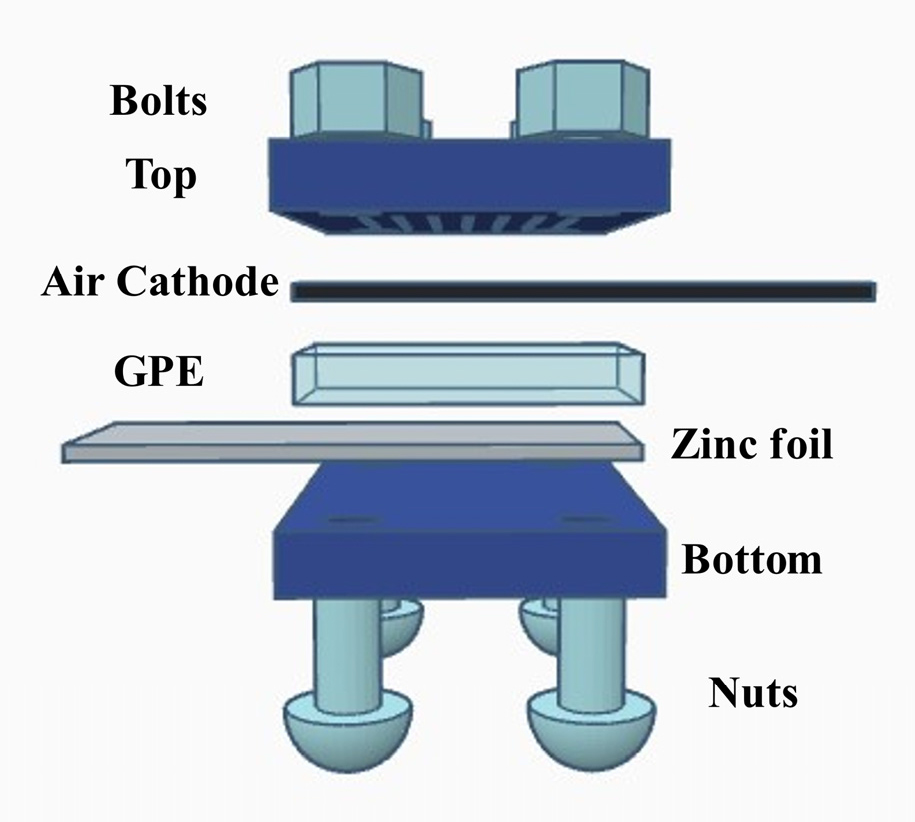
본 연구에서 사용된 아연-공기 전지는 음극과 양극 사이에 제조된 GPE를 적층하여 샌드위치 형태로 제작되었다. 먼저 teflon 소재로 만든 bottom의 모서리 끝에 4개의 bolts를 연결하고 가로 20 mm 세로 50 mm로 절단된 zinc foil (99.98 %, THERMO SCIENTIFIC, USA)을 bottom 중앙에 적층한다. zinc foil 위에 GPE를 도포하고 air cathode (MnO2 Based, DUCK JIN, Korea)를 zinc foil과 같은 넓이로 절단해 GPE 위에 적층한다. 마지막으로 teflon 소재로 만든 top part를 적층해 nuts로 조여서 아연-공기 전지를 제작하였다. 제작된 아연-공기 전지의 모식도를 Fig. 1에 나타내었다.
2.3. 측정 및 분석
2.3.1. 충전/방전 수명, 방전용량 측정
GPE의 아세트산 아연 이수화물 첨가에 따른 아연-공기 전지의 충전/방전 수명과 방전용량을 관찰하기 위해서 GPE, 0.2 GPE, 0.4 GPE, 0.6 GPE를 제조해 24시간 동안 6 M의 KOH용액에 함침시킨 후 4개의 전지를 제작하였다. 전지의 충전/방전 수명은 전기화학분석기(WBC3000L, WonAtech, Korea)를 사용하여 6 mA의 정전류로 10분 주기마다 충전/방전을 진행시켜 시간에 따른 최종 방전전압을 비교해 전지의 충전/방전 수명을 측정하였다. 또한 전지의 방전용량은 10 mA의 정전류로 0.2 V 전압까지 방전시켜 측정하였다.
2.3.2. 전기화학적 저항 측정
제조된 GPE, 0.2 GPE, 0.4 GPE, 0.6 GPE의 저항과 이온전도도를 측정하기 위해 임피던스 분광법이 가능한 전기화학 분석기(ivium, Netherlands)를 사용하였다. 측정은 10 kHz에서 0.1 Hz 사이의 주파수 범위에서 10 mA 진폭으로 진행되었다. 아세트산 아연 이수화물이 첨가된 양에 따라 제조된 GPE의 저항특성을 비교하였으며, 충전된 저항값을 토대로 식 (5)를 통해 이온전도도를 계산하였다.
여기서, σ는 전해질의 이온 전도도, A는 전해질의 면적, Re는 전해질의 저항, l은 전해질의 두께를 나타낸다.16)
3. 결과 및 고찰
3.1. 재료 특성
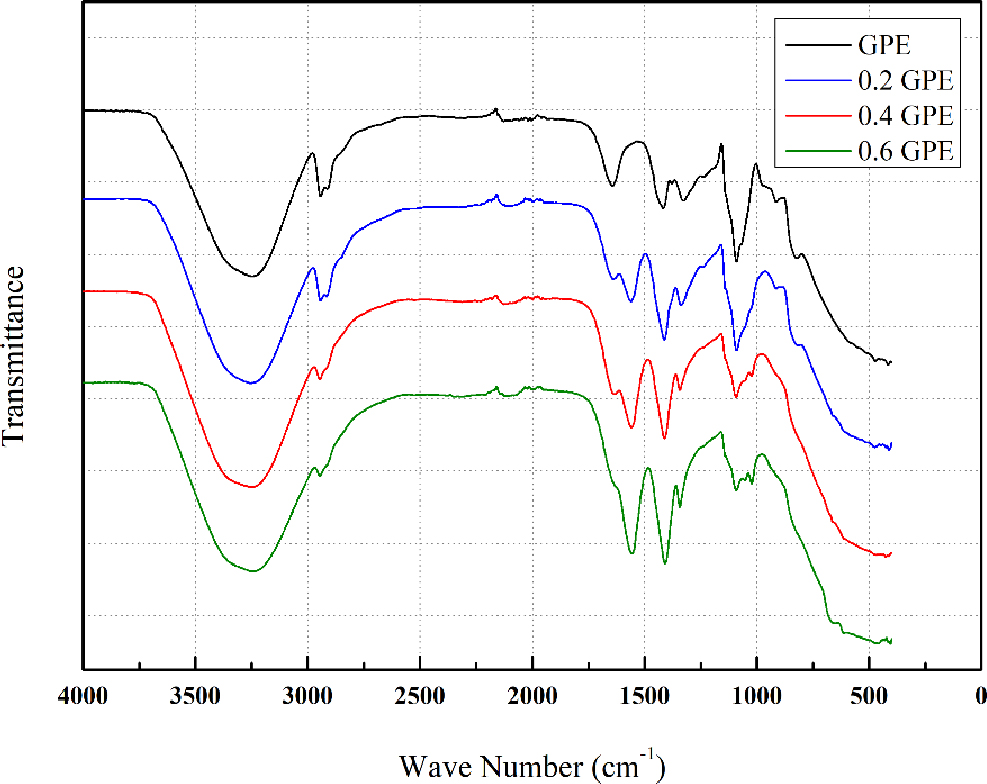
제조된 모든 GPE의 결합 구조적 특성을 확인하기 위해 FT-IR을 통해 분석하였고, Fig. 2 및 Table 2에 결과를 나타내었다. 2,940 cm-1 부근의 피크는 -CH3를 나타내며, 1,090 cm-1 부근에서는 C-O결합을 나타내는 피크를 보인다.17) 아세트산 아연 이수화물의 농도가 증가함에 따라 -CH3와 C-O결합세기의 감소로 피크의 크기가 줄어드는 것이 확인됐다. 또한 1,410 cm-1과 1,550 cm-1 부근에서 보이는 피크는 아세테이트에 포함된 COO-의 대칭 신축운동 및 비대칭 신축운동에 관한 피크로 볼 수 있다.18,19) 하지만 폴리비닐 알코올로만 이루어진 GPE에서도 1,410 cm-1부근에 해당하는 피크를 보이는데 이 영역의 피크는 C-H결합을 나타내므로 COO-결합과는 무관하다. 결과적으로 아세트산 아연 이수화물의 첨가된 사실과 첨가량이 증가함에 따라 결합세기의 감소를 확인할 수 있었다.
Table 2.
FT-IR characteristic of GPE for different irradiation doses.
| Materials |
Electrolyte resistance (Re, Ω) |
Ionic conductivity (σ, S/cm) |
| GPE | 0.394 | 0.013 |
| 0.2 GPE | 0.338 | 0.015 |
| 0.4 GPE | 0.290 | 0.017 |
| 0.6 GPE | 0.213 | 0.023 |
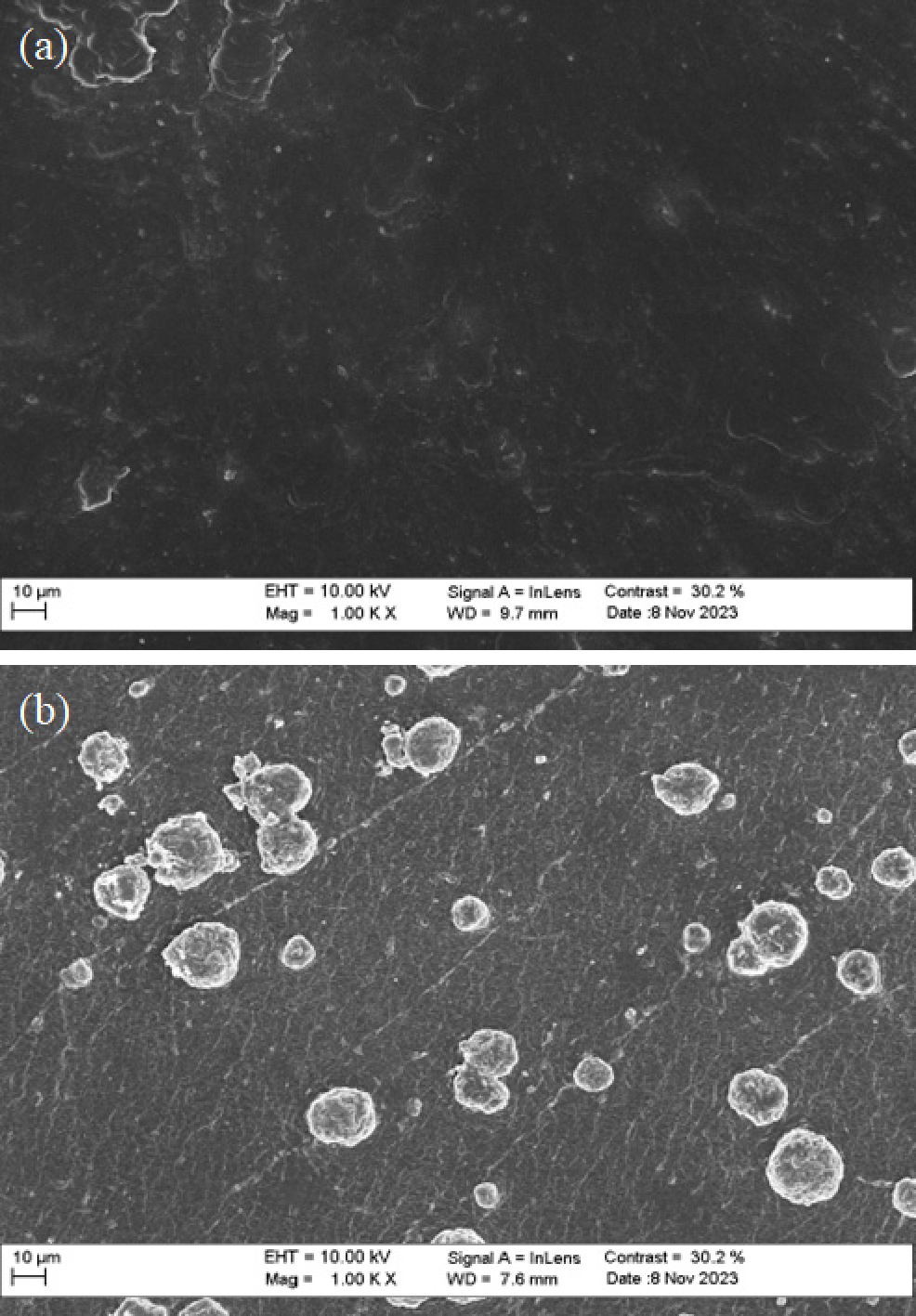
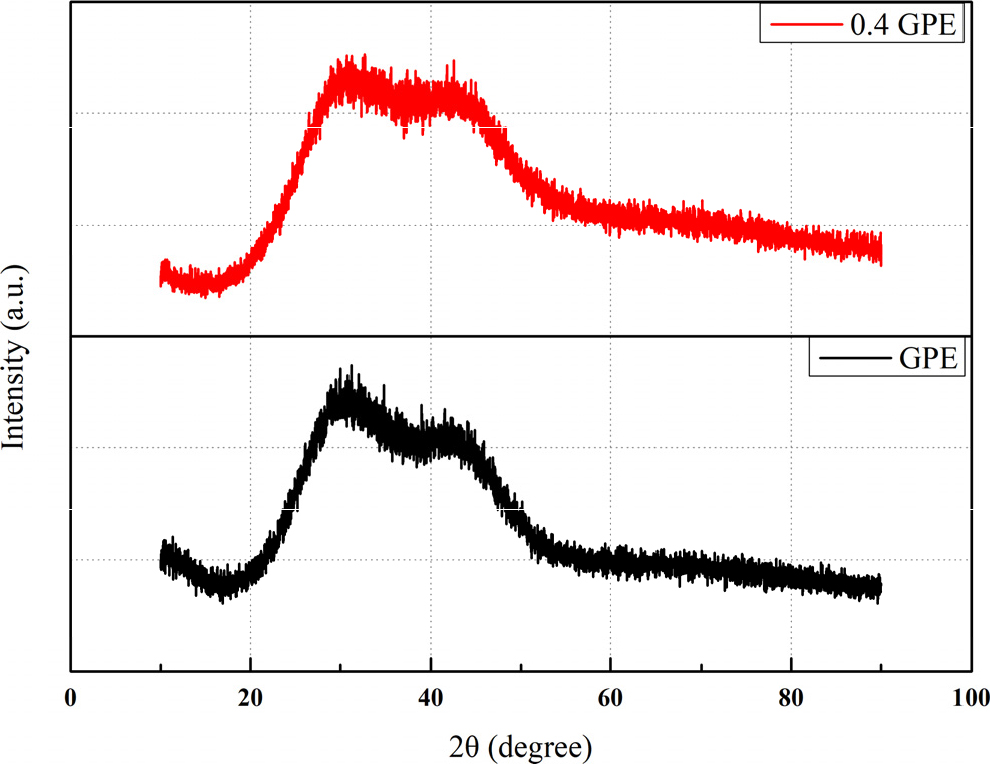
Fig. 3은 제조된 GPE를 FE-SEM으로 분석한 결과이다. 이를 통해 GPE에 아세트산 아연 이수화물이 첨가됨에 따라 GPE 표면에 부분적으로 입자가 형성되는 것을 알 수 있었다. 결과적으로 GPE 표면에 아세트산 아연이 증착되어 구 형태의 입자가 형성됨을 확인할 수 있었다. 더불어, GPE와 0.4 GPE의 결정구조를 확인하기 위해 XRD 측정을 수행하였다. 아세트산 아연 이수화물을 첨가해 제조된 GPE 중 중간에 위치한 조성을 가진 0.4 GPE로 측정하였다. Fig. 4는 XRD를 통해 측정된 결과이다. GPE와 0.4 GPE가 서로 흡사한 회절피크를 보였다. 이러한 회절피크는 전형적인 폴리비닐 알코올의 결정구조를 가진 것으로 나타났다. 이를 통해 폴리비닐 알코올과 아세트산 아연 이수화물의 합성 과정에서 아세트산 아연 이수화물이 폴리비닐 알코올 구조에 영향을 미치지 않았다는 것을 확인하였다. 또한 GPE 내부에 중량퍼센트 80 % 이상이 수분이 함유되어있어 XRD 회절피크가 오른쪽으로 이동됨을 확인할 수 있었으며, 0.4 GPE의 경우 아세트산 아연 이수화물 소량 첨가로 인해 관련된 회절피크가 나타나지 않았다.20,21) 결과적으로 GPE와 0.4 GPE 모두 폴리비닐 알코올 구조를 가지고 있어 팽윤이 가능하다는 것을 확인할 수 있었다.
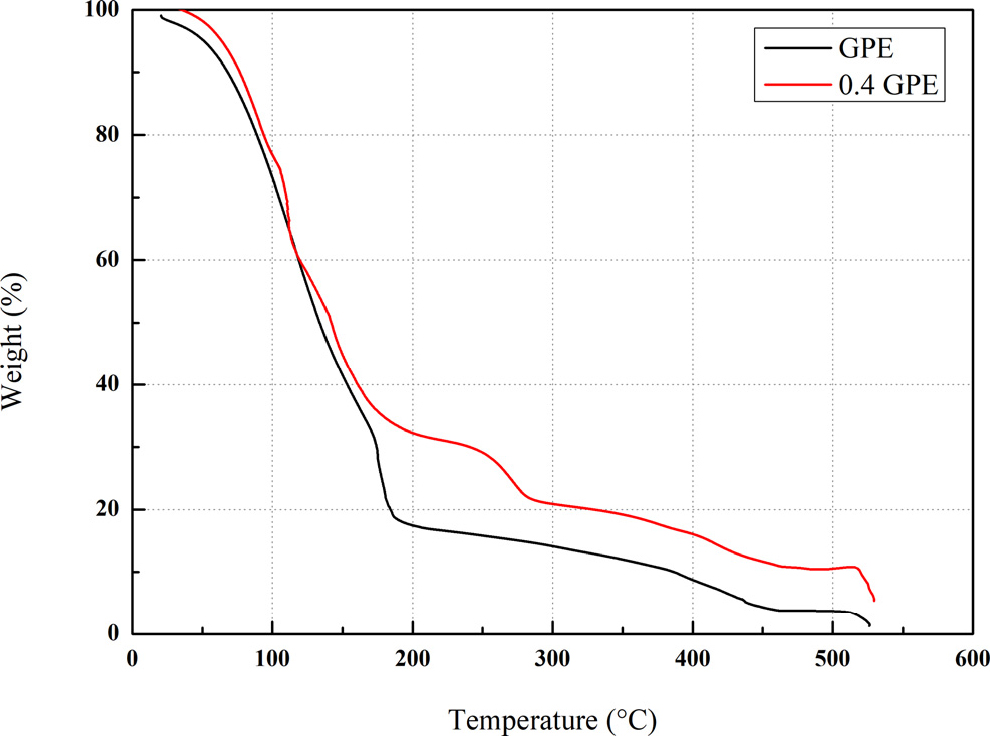
Fig. 5는 GPE와 0.4 GPE를 TGA측정을 통해 질량%를 분석한 결과이다. 본 실험은 산소기체의 기류 하에서 유량속도 40 mL/min, 승온 속도 20 °C/min로 상온에서 500 °C까지 분석하였다.
GPE는 상온에서 200 °C 범위까지 열에 의한 수분증발이 일어나게 되고, 총 82.55 %의 중량감소율을 보였다. 또한 200 °C에서 462 °C 범위까지 13.82 % 중량감소율을 보이며 이 온도 범위에서 폴리비닐 알코올의 열분해 과정을 통해 GPE의 중량이 감소됨을 나타냈다.22)
0.4 GPE는 상온에서 200 °C 범위까지 열에 의한 수분증발이 일어나게 되고, 총 68.16 %의 중량감소율을 보였다. 또한 200 °C에서 462 °C 범위까지 21.05 % 중량감소율을 보이며 이 온도 범위에서 아세트산 아연과 폴리비닐 알코올의 열분해 과정을 통해 0,4 GPE의 중량이 감소됨을 확인하였다. 특히, 200 °C에서 280 °C 부근에서 9.76 % 중량감소율이 나타남으로써 아세트산 아연의 분해반응을 관찰 수 있었고 이를 통해 GPE에 아세트산 아연 이수화물의 첨가가 이루어진 것을 나타냈다.23)
따라서 GPE와 0.4 GPE의 TGA 분석 그래프를 비교해봤을 때 상온에서 200 °C 범위에서 일어나는 중량감소율이 82.55 % (GPE), 68.16 % (0.4 M GPE)이므로 0.4 GPE가 GPE보다 수분 증발 중량이 더 낮다는 것을 알 수 있고, 또한 상온에서 462 °C 범위까지의 중량감소율이 96.32 % (GPE), 89.21 % (0.4 M GPE)이므로 열안정성 또한 우수함을 확인할 수 있었다.
3.2. 전기화학적 임피던스 측정
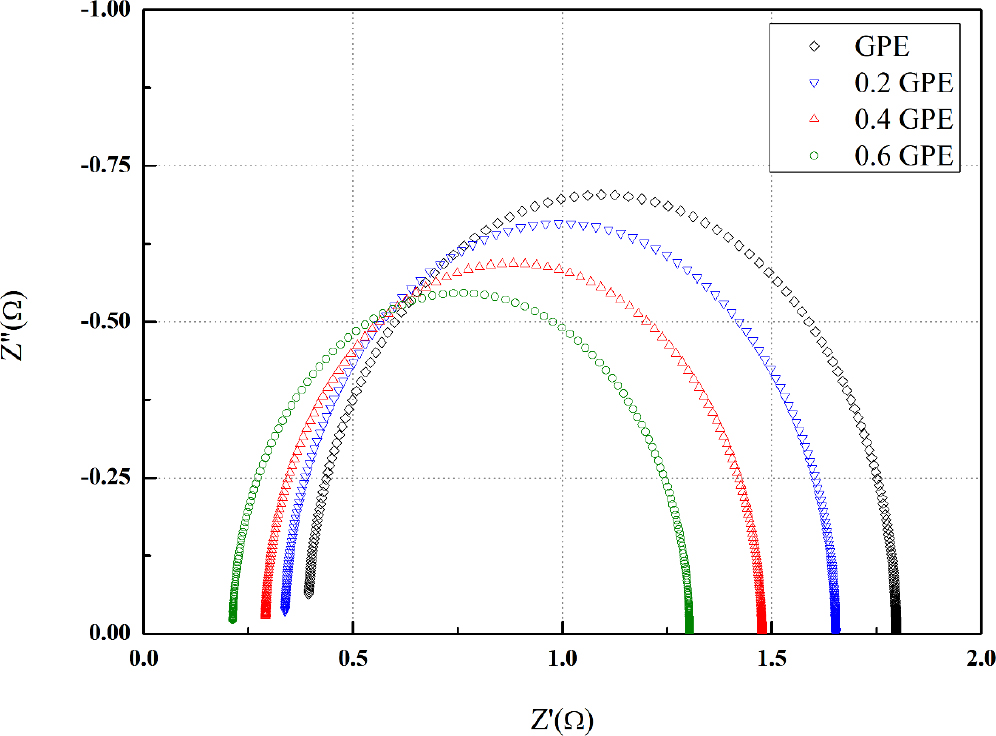
아세트산 아연 이수화물 농도에 따라 제조된 GPE의 이온전도도와 저항을 알아보기 위해 임피던스 분석을 이용해 측정하였다. 각각의 GPE에 대한 nyquist plot을 Fig. 6에 나타내었다. 더불어 전해질 내부의 저항과 이온 전도도의 결과를 Table 3에 나타내었다.
Table 3.
The ionic conductivity (σ) and electrolyte resistance (Re) of GPE with different ratios of zinc acetate dihydrate.
| Wave number (cm-1) | Bands |
| 1,090 | C-O |
| 1,410 | COO- |
| 1,300 | -CH2- |
| 1,550 | COO-, C-H |
| 2,940 | -CH3 |
| 3,200 | O-H |
아세트산 아연 이수화물이 첨가되지 않은 GPE가 0.013 S/cm 값으로 가장 낮은 이온 전도도를 보였다. 가장 낮은 이온전도도를 기록한 원인은 가장 높은 0.394Ω의 전해질 저항값에 기인한다. 반대로 전해질 저항이 가장 낮은 0.213Ω인 0.6 GPE는 가장 높은 0.023 S/cm의 이온 전도도를 보였다. 이처럼 각각의 GPE는 같은 면적과 같은 두께인 몰드에 제조되었기 때문에 전해질 저항값에 따라서 이온 전도도의 결과가 결정된다. 0.2 GPE의 이온전도도는 0.015 S/cm의 값으로 GPE의 이온 전도도와 큰 차이가 없다. 하지만 0.4 GPE는 0.017 S/cm의 점점 증가하는 이온 전도도를 보였다. 더불어 0.6 GPE는 기존에 GPE에 비해 약 2배 향상된 이온 전도도를 보였다. 결과적으로 아세트산 아연 이수화물을 첨가한 0.2 GPE, 0.4 GPE, 0.6 GPE인 모든 전해질은 첨가하지 않은 GPE 보다 높은 이온 전도도를 보였다. 이를 통해 전해질 내부에 이온의 이동은 아연염의 농도 증가로 향상됨을 나타내었다. 결과적으로 아세트산 아연 이수화물에 포함된 아연염의 첨가는 전해질 내부에 저항을 저하시킴으로서 향상된 이온전도도를 초래한다고 판단된다.24)
3.3. 방전 거동
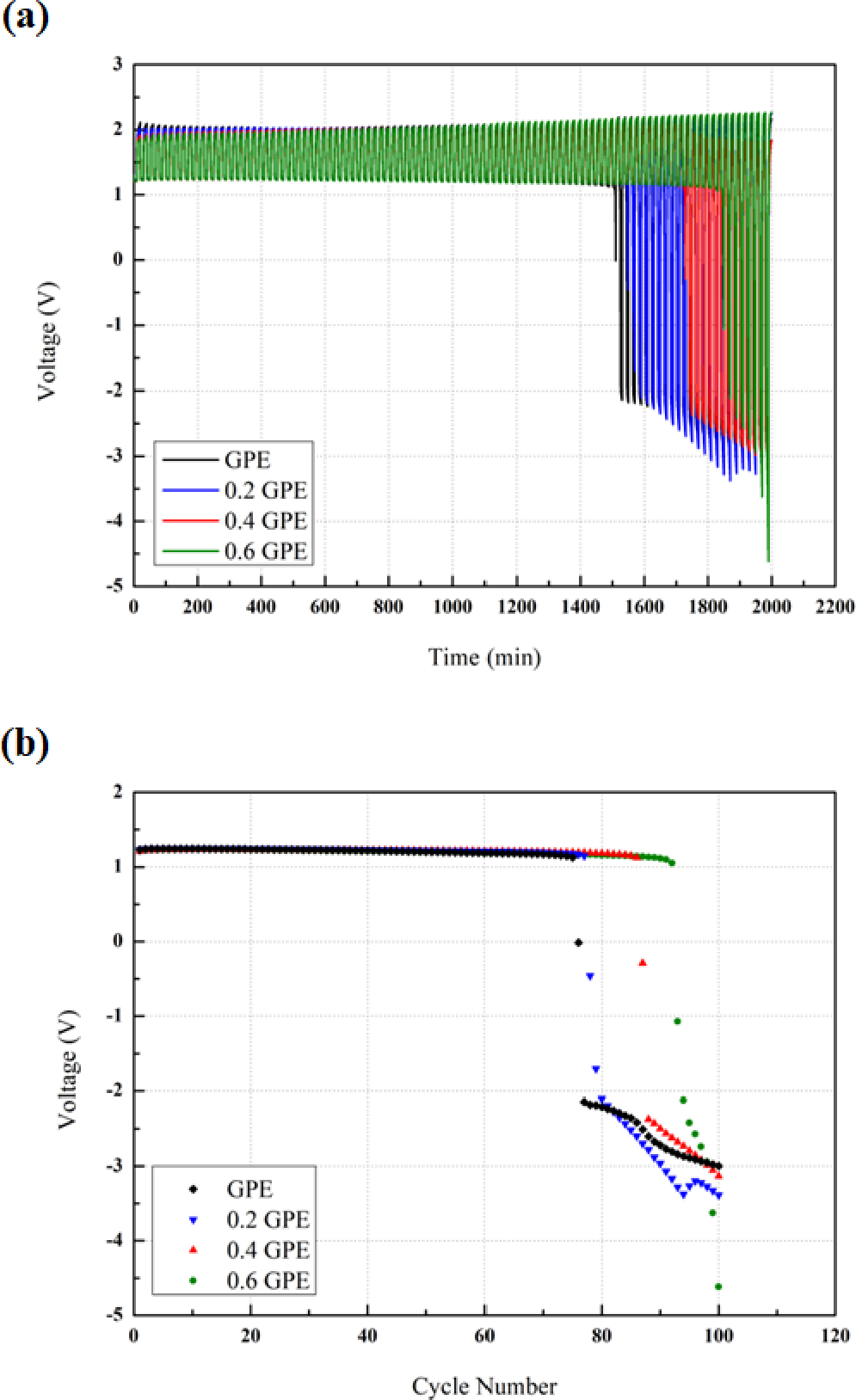
Fig. 7(a)는 GPE의 아세트산 아연 이수화물 첨가에 따른 아연-공기 전지를 6 mA로 충전/방전 수명을 측정하여 그래프로 나타내었다. 각 전지의 수명 판단은 Fig. 7(b)의 사이클 수에 대한 최종방전전압이 1 V 이하로 측정되는 지점을 기준으로 판단하였다. Fig. 7(a)에서는 0.6 GPE가 92사이클 동안 충전/방전이 지속되면서 총 1,840분 동안 작동됨을 나타내며 이는 다른 GPE들에 비해 가장 우수한 충전/방전 수명을 보여주었다. 또한, 0.4, 0.2 GPE는 각각 86, 77 사이클 동안 충전/방전이 지속됨을 나타내었고 GPE의 경우 75번째 사이클까지 충전/방전이 지속되면서 총 1,500분 동안 작동됨을 나타내었으며 가장 낮은 충전/방전 수명을 보여주었다.
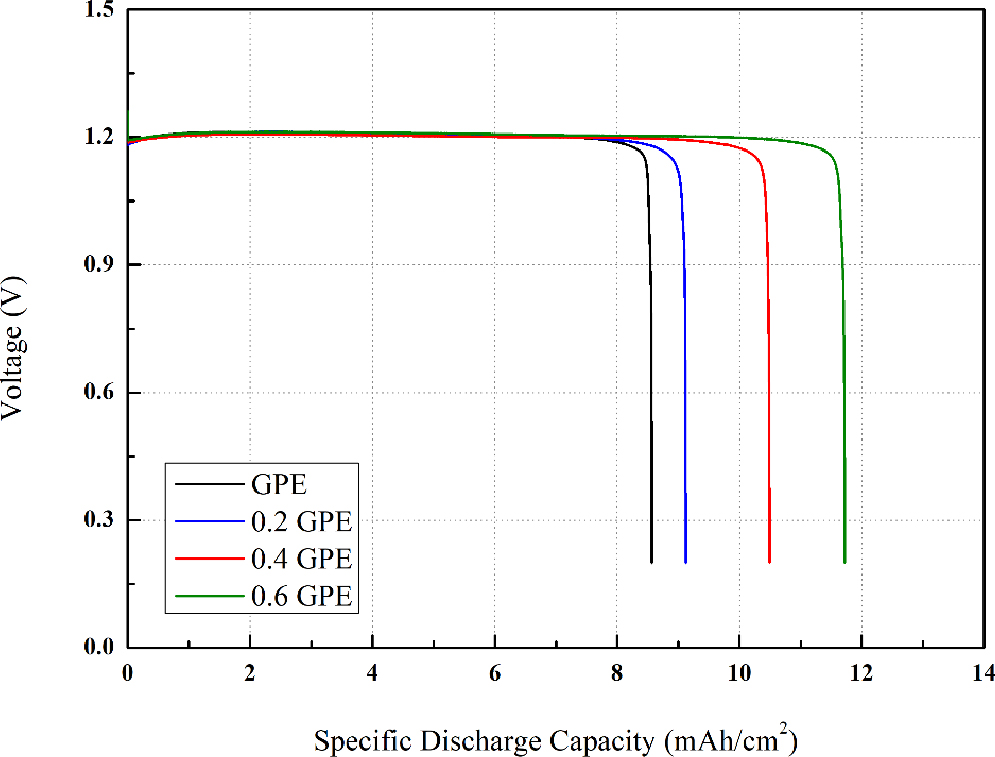
Fig. 8은 GPE의 아세트산 아연 이수화물 첨가에 따른 아연-공기 전지의 방전 용량을 10 mA로 측정하여 그래프로 나타냈다. Table 4는 측정된 방전 비용량을 정리하여 나타내었다. Fig. 8에서 0.6 GPE는 11.73 mAh/cm2의 방전 비용량을 나타내었으며 다른 GPE에 비하여 가장 우수한 비용량을 보였다. 0.4, 0.2 GPE는 각각 10.49, 9.12 mAh/cm2의 방전 비용량을 나타내었고 GPE의 경우 8.57 mAh/cm2의 방전 비용량을 나타내며 다른 GPE에 비하여 가장 낮은 비용량을 보여주었다.
Table 4.
Specific discharge capacity of GPE with different ratios of zinc acetate dihydrate.
| Materials | Discharge capacity (mAh/cm2) |
| GPE | 8.57 |
| 0.2 GPE | 9.12 |
| 0.4 GPE | 10.49 |
| 0.6 GPE | 11.73 |
따라서, Fig. 7에서는 아세트산 아연 이수화물의 함량이 증가할수록 폴리비닐 알코올의 결합력이 약해져 전자의 이동이 활발해지기 때문에 0.6 GPE가 가장 우수한 충전/방전 수명과 높은 비용량을 보여주었다. 결과적으로 0.6 GPE로 전지를 제작할 때 가장 우수한 효율의 전기화학적 특성을 나타냄을 확인할 수 있었다.
4. 결 론
본 연구는 폴리비닐 알코올과 아세트산 아연 이수화물을 혼합해 고분자 전해질을 제조하여 전기화학적 특성을 개선하고자 하였다. 아세트산 아연 이수화물 1.3 g, 2.6 g, 4 g과 폴리비닐 알코올 4 g을 가교제인 GL 0.1 g과 GC 0.1 g, HCl 10 mL, 초순수 30 mL로 혼합해 GPE를 만들었다. 재료특성을 판단하기 위해 각각의 GPE를 FT-IR, SEM, XRD, TGA로 분석하였다. FT-IR 분석을 통해 아세트산 아연 이수화물이 첨가된 사실과 첨가량이 증가함에 따라 결합세기의 감소를 확인할 수 있었고, SEM 분석을 통해 GPE 표면에 아세트산 아연이 증착됨을 확인하였다. 그리고 XRD 분석을 통해 GPE와 0.4 GPE 모두 폴리비닐 알코올 구조를 가지고 있어 팽윤이 가능함을 확인하였다. 또한 TGA 분석을 통해 0.4 GPE가 GPE보다 수분증발 중량이 낮고 열안정성이 우수함을 확인하였다. 각각의 GPE를 사용하여 전지를 만들었고, 충전/방전 수명 및 방전용량을 측정하였고, 임피던스 분광법을 통해 저항특성과 이온전도도를 비교하였다. 비교된 GPE는 각각의 아세트산 아연 이수화물 함량의 차이로 인하여 전기화학적 특성에 차이를 보였다. 그 중 0.6 GPE가 92사이클 동안 충전/방전이 지속되고, 10 mA에서 11.73 mAh/cm2의 가장 높은 방전 비용량을 보였으며 이는 아세트산 아연 이수화물의 첨가가 증가할수록 폴리비닐 알코올 고분자의 결합구조를 약화시키기 때문이다. 또한 0.213Ω의 가장 낮은 전해질저항을 보였고 이를 통하여 계산된 이온전도도는 0.023 S/cm의 가장 높은 값을 보였다. 따라서 0.6 GPE가 비교된 GPE가운데 가장 우수함을 확인하였다.