1. 서 론
최근 차세대 기기와 디스플레이가 등장함으로써 플렉 서블 전지에 대한 관심이 증가하고 있다. 현재 상용화되어 가장 널리 사용되고 있는 리튬 이온 전지를 비롯하여 다양 한 차세대 전지에 대해 플렉서블화에 대해 많은 연구가 이 루어지고 있다.1,2) 리튬 이온 전지는 우수한 충방전 효율 과 높은 에너지 밀도를 가지고 있으며 자가방전 측면에서 장점을 가지고 있으나 전기 자동차(electric vehicle, EV), 에너지 저장 시스템(energy storage system, ESS) 등에 적용 시 충전속도 및 용량 측면에서 불편함이 존재한다.3) 더불 어 비교적 낮은 안전성과 구성 소재의 높은 가격으로 인한 단점이 있다. 이러한 단점을 보완하기 위해 알루미늄, 마 그네슘, 아연 등의 금속-공기 전지 등 차세대 전지에 대한 연구가 활발히 이루어지고 있다.4-6) 아연-공기 전지는 공 기 양극을 사용하여 환경 친화적인 소재와 낮은 가격을 가 지고 있고, 높은 에너지 밀도를 수반하기에 일차 전지 형 태로는 상용화 되어 있다. 하지만 저전압과 낮은 충방전 효율, 자가방전 등의 단점이 있어 이것을 극복하기 위한 연구가 선행되어야 한다.7,8)
아연-공기 전지는 산소 공급이 가능한 양극, 아연 기반 의 음극, 수계 전해질로 구성된다. 방전 과정에서 양극과 음극에 다음과 같은 산화, 환원 반응이 일어난다.9)
음극 : Zn + 4OH- → Zn(OH)42- + 2e- Zn(OH)42- → ZnO + H₂O + 2OH-
양극 : O₂ + 2H₂O + 4e- → 4OH-
전체반응식 : 2Zn + O₂ → 2ZnO
아연-공기 전지의 전해질은 이온전도도가 상대적으로 높은 potassium hydroxide를 사용한다. 리튬이온 전지와 다르게 수계 젤 전해질을 사용하는 아연-공기 전지는 화 학적 안전성이 뛰어나다.10) 하지만 수계 젤 전해질을 사용 함으로써 음극과 전해질 계면에서의 부식과 수소 발생 반 응으로 인한 자가방전이 가속화된다.11)
Zn + 2H₂O → Zn(OH)2 + H₂ ↑ : 수소 발생 반응
2H₂O + 2e- → 2OH- + H₂ : 전기분해 반응
2OH- → 12O₂ + H₂O + 2e- : 전기분해 반응
따라서 이러한 부반응들을 억제하기 위하여 첨가제 또 는 젤 형태의 전해질에 대한 연구가 이뤄지고 있다. 현재 아연-공기 전지의 플렉서블화를 위하여 전해질은 고분자 젤 전해질, 케이블 타입, 섬유형식 등 다양한 방향으로 연 구되고 있으며, 대부분 고분자기반의 젤 전해질을 이용하 는 방식으로 진행되고 있다.12) 일반적으로, 고분자 젤 전 해질은 화학적 가교를 이용하여 고분자 매트릭스를 형성 하고 이후 수계 전해질을 흡수하여 제작된다. 이것은 분리 막의 역할을 대체할 수 있고 수분 증발을 억제할 수 있으 며, 고분자 매트릭스로 인해 수계 전해질보다 더 우수한 기계적 성질을 가진다. 대표적으로 사용되는 고분자로는 PAA, PVA 등이 있으며,13,14) Cellulose, Agar와 같은 천연 고분자 역시 적용이 가능하다. 그 중 대표적인 천연고분자 인 전분은 가격이 매우 저렴하고 친환경적인 고분자 물질 로, 감자, 고구마 등 그 종류가 매우 다양하다. 전분은 열적 특성, 용해도 등이 우수하여 다양한 전지의 고분자 젤 전 해질 첨가제로 적용이 되고 있다. 아연-공기 전지에는 아 연 음극에 cassava, sago를 코팅하여 부반응을 줄이거나,15) Agar로 전지의 용량을 늘리는 방향으로 적용이 되고 있다. 하지만 젤 전해질로의 적용은 많은 연구가 이뤄지지 않아 전분 종류에 따른 전기화학적 특성에 대한 연구가 필요 하다.
본 연구에서는 플렉서블 아연-공기 전지를 위하여 여러 종류의 전분을 이용하여 젤 전해질을 제작하였다. 제작된 전분기반 젤 전해질의 전기화학적 방전거동을 비교하기 위하여 방전 용량 및 bending 후 방전 용량을 측정하였다. 또한 임피던스 분광법을 통해 전분 기반 젤 전해질의 이온 전도도를 분석하였다.
2. 실 험
2.1. 전분 기반 젤 전해질 제조 및 아연-공기 전지 조립
플렉서블 아연-공기 전지를 위하여 감자 전분(Chemical pure, Daejung), 고구마 전분(99 %, Oherb), 옥수수 전분 (Chemical pure, Daejung)을 이용하여 젤 전해질을 제작하 였다. 각각의 전분을 1.0 g씩 증류수 10 ml에 용해시킨 후, 가교제인 N,N’-Methylenebisacrylamide (MBA, 99 %, Daejung) 를 0.05 g첨가하여 교반하였다. 젤화가 진행된 후, 6 M KOH (85 %, Daejung) 10 ml를 첨가하여 30분간 교반하 여 전해질을 제작하였다. 그 후 mold에 넣고 60 °C에서 90 분 건조하였다. 각각의 젤 전해질은 2.0 mm 두께로 제작 되었고, 감자 전분, 고구마 전분, 옥수수 전분을 각각 P, SP, C로 명명하였으며 두께와 함께 나타내었다.
본 연구 측정에 사용된 아연-공기 전지는 zinc foil (99.98 %, 0.25 mm, Alfa Aesar) 위에 젤 전해질을 적층하고 그 위 에 air cathode (ADE-72B, MEET)를 결합하여 제작하였다. 제작된 아연-공기 전지의 모식도를 Fig. 1에 나타내었다.
2.2. 측정 및 분석
2.2.1. 방전 용량 측정
플렉서블 아연-공기 전지의 각 천연 고분자의 전기화학 적 특성을 비교하기 위해 P 2.0 mm, SP 2.0 mm, C 2.0 mm 을 젤 전해질로 사용하여 3개의 전지를 제작하였다. 제작 한 전지의 방전 용량을 측정하여 비교하였다. 전지의 방전 용량은 전기화학 분석기(WonAtech, WBC3000L)를 사용 하여 30 mA, 20 mA 두 정전류로 0.2 V의 전압까지 방전시 켜 방전 용량을 측정하였다.
제작된 전지의 유연성과 그에 따른 방전 용량을 비교하 기 위하여 P 2.0 mm, SP 2.0 mm, C 2.0 mm를 젤 전해질로 사용하여 100° 구부린 전지를 제작하였다. 전지의 방전 용 량은 10 mA의 정전류로 0.2 V의 전압까지 방전시켜 방전 용량을 측정하였다.
2.2.2. 전기화학적 저항 측정
제작된 전분 기반 전해질의 이온전도도 및 저항을 알아 보기 위해 임피던스 분광법을 이용하여 저항특성을 비교 하였다. 0.01 V 진폭으로 10 kHz에서 10 Hz 사이의 주파수 범위에서 진행되었다. 이온전도도는 측정된 결과값을 이 용하여 다음의 식을 통해 계산하였다.16)
여기서, σ는 이온전도도, l, Re와 A는 각각 전해질의 두께, 전해질저항과 전해질의 면적을 나타낸다.
3. 결과 및 고찰
3.1. 재료 특성
Fig. 2에 감자, 옥수수, 고구마 전분을 기반으로 합성된 젤 전해질을 나타내었다. 각 전해질은 2 cm × 4 cm의 규격 으로 제작되었다. 합성에 사용한 mold는 실제 보다 조금 더 큰 규격으로 3D 프린터를 이용하여 제작하였다. 합성 된 전해질은 모두 우수한 점착성을 보였으며 셀 조립 시 양극 및 음극과의 밀착성이 우수한 것으로 나타났다. 하지 만 건조 과정에서 온도, 습도에 따른 부피의 변화가 관찰 되었고 실제 셀을 구성하는 과정에서는 규격에 맞게 재단 하여 적용하였다.
3.2. 방전 거동
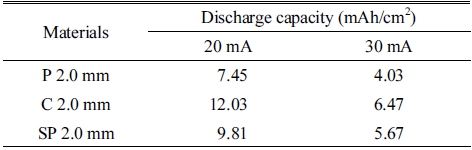
Fig. 3은 전분기반 젤 전해질로 만든 각각의 전지의 방전 용량을 20 mA와 30 mA로 측정하여 그래프로 나타냈다. Table 1은 소재 및 전류밀도에 따른 전기화학적 방전 비용 량을 정리하여 나타내었다. Fig. 3(a, b)에서 C 2.0 mm는 20 mA에서 12.03 mAh/cm2, 30 mA에서 6.47 mAh/cm2의 방전 비용량을 나타내며 다른 전분에 비하여 가장 우수한 비용 량을 보였다. P 2.0 mm의 경우 20 mA에서 7.45 mAh/cm2, 30 mA에서 4.03 mAh/cm2를 나타냈고, SP 2.0 mm는 20 mA에서 9.81 mAh/cm2, 30 mA에서 5.67 mAh/cm2로 감자 전분으로 제작된 젤 전해질이 가장 낮은 특성을 보였다. 비교된 전분은 그들의 구성 성분 비율이 각각 다르며, 이 것은 젤 전해질의 전기화학적 거동에 영향을 줄 수 있다. 전분은 아밀로오스와 아밀로펙틴으로 구성되어 있고 대 부분의 비율은 20:80이다. 아밀로오스는 직선형의 형태로 포도당의 한 형태인 α-D-glucopyranose가 α-1,4 결합을 하 고 있고, 아밀로펙틴은 가지를 친 형태로 같은 물질이 α -1,4 결합을 95 %, α-1,6 결합을 5 % 하고 있다.17,18) 옥수수, 고구마, 감자 전분 중 옥수수가 상대적으로 아밀로오스의 함량이 가장 높았다. 이에 따라 구조상 특징으로 인하여 이온이 이동이 수월하여 우수한 거동을 보였다.
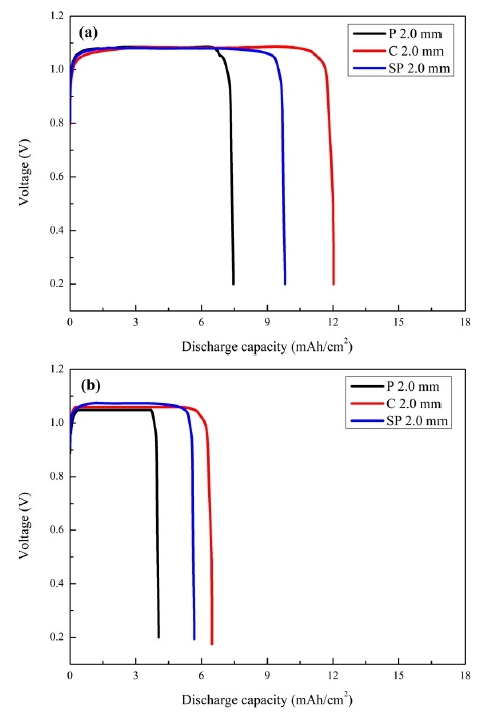
Fig. 3
Electrochemical potential profiles of starch based gel electrolyte in different current (a) 20 mA, (b) 30 mA.
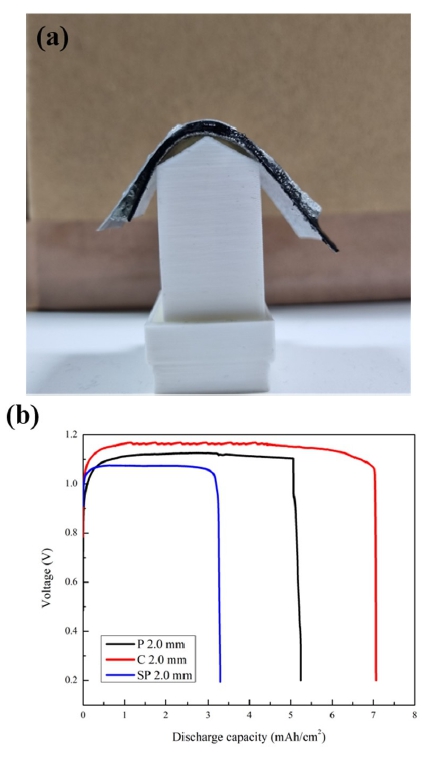
Fig. 4는 젤 전해질로 만든 각각의 전지를 100°만큼 구 부려 방전 용량을 10 mA로 측정하여 그래프로 나타냈다. 또한 측정된 방전 비용량을 Table 2에 나타내었다. Fig. 4(a)는 전분기반 젤 전해질의 bending discharge 측정 방법 을 나타냈으며, 제작된 전해질은 매우 우수한 유연성을 보 임이 확인된다. 또한 Fig. 4(b)에 나타난 방전 비용량은 SP 2.0 mm가 5.24 mAh/cm2을 보였으며, P 2.0 mm는 3.29 mAh/cm2로 가장 낮은 값을 보였다. C 2.0 mm는 방전 과정 중, 높은 방전 전압과 7.06 mAh/cm2의 비용량을 나타내며 가장 우수한 특성을 보였으며, bending 되지 않은 30 mA 전류에서 측정된 방전 비용량보다 높은 값을 나타낸다. 이 는 방전 실험과 다른 조건임에도 옥수수 전분 기반의 젤 전해질이 방전과정에서와 같이 높은 아밀로오스 함량을 가져 다른 전분 기반의 젤 전해질에 비해 우수한 구조적 이점을 가지기 때문이다. 따라서 100° 구부린 후에도 안정 적인 비용량을 나타낸 것으로 확인된다.
3.3. 전기화학적 임피던스 특성
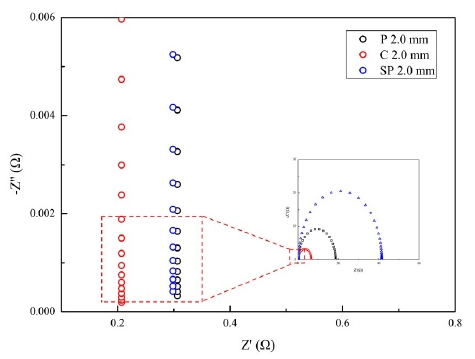
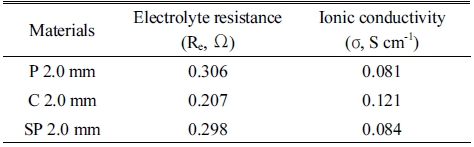
제작된 전분 전해질의 저항 특성 및 이온전도도를 알아 보기 위하여 임피던스 분석법을 이용하여 저항을 측정하 였다. Fig. 5는 각 전해질의 대한 Nyquist plot을 나타내었 고, 전해질저항 및 이온전도도 계산 결과를 Table 3에 나 타내었다. P 2.0 mm는 0.306 Ω의 높은 전해질저항으로 인 하여 0.081 S cm-1의 낮은 전도도를 보였다. P 2.0 mm의 높 은 전해질저항은 전해질의 전기화학적 특성과 이온전도 도에 영향을 미쳐 방전거동에서 특성이 저하될 수 있다. 그러나 SP 2.0 mm는 0.298 Ω의 전해질저항을 나타내어 비교된 젤 전해질 중에서 중간 값을 가지며 0.084 S cm-1의 전도도를 보여 계산된 이온전도도에서 감자 전분과 큰 차 이를 보이지 않았다. C 2.0 mm는 0.207 Ω로 가장 낮은 값 을 나타내었고, 0.121 S cm-1로 가장 높은 전도도를 보였 다. 동일한 면적과 두께의 젤 전해질에서 전해질저항은 전 해질의 전기화학적 거동에 가장 큰 영향을 미치며, 전해질 저항이 낮을수록 높은 이온전도도를 나타낼 수 있다. 제작 된 C 2.0 mm의 경우, 다른 전분에 비하여 낮은 전해질저항 으로 인하여 전극과 전해질 계면에서의 이온 이동이 상대 적으로 원활하게 이루어졌으며, 이것은 높은 이온전도도 와 우수한 방전거동을 나타내는 것으로 이어졌다.
4. 결 론
본 연구는 아연-공기 전지용 젤 전해질에 천연 고분자 를 첨가하여 전기화학적 거동을 개선하고자 하였다. 감자, 고구마, 옥수수 전분 1 g을 각각 가교제인 MBA 0.05 g과 증류수 10 mL, 6 M KOH 10 mL로 혼합해 젤 전해질을 만 들었다. 각각의 젤 전해질을 사용하여 전지를 만들었고 방 전 거동 및 구부린 후 방전 거동을 측정하였고, 임피던스 분광법을 통해 저항특성과 이온전도도를 비교하였다. 비 교된 전분은 각각의 아밀로오스 함량의 차이로 인하여 전 기화학적 특성에 차이를 보였다. 그 중 옥수수 전분은 20 mA에서 12.03 mAh/cm2, 30 mA에서 6.47 mAh/cm2의 방전 비용량을 보였으며, 이는 옥수수 전분이 다른 전분에 비해 높은 아밀로오스 함량을 가지며 이로 인한 구조적 이점을 가지기 때문이다. 또한 0.207 Ω의 낮은 전해질저항을 보 였고 이를 통하여 계산된 이온전도도는 0.121 S cm-1의 매 우 높은 값을 보였다. 따라서 옥수수전분이 비교된 전분 가운데 젤 전해질로 가장 우수함을 확인하였다.