1. 서 론
형광체는 자외선 영역에서의 발광되는 적, 녹, 청 세 가지 주요색으로 3차원 디스플레이, 광저장 장치, 의료 진단, 센서, 태양전지 등 다양한 응용분야에 적용되고 있 다.1) 특히, 디스플레이와 같은 분야에 적용될 경우에는 형광체 입자의 크기가 스크린 두께에 직접적인 영향을 미치기 때문에 형광체의 크기를 줄이는 개발이 필수적 이며, 이러한 관점에서 광범위하게 연구되고 있다.2)
다양한 형광체 중에서 Gd2O3:Eu3+는 열적.화학적 안정 성이 높은 가장 대표적인 적색 형광체로 알려져 있다.3) Gd2O3는 적색형광체 Y2O3와 유사하며 결정성을 가지기 때문에 응용하기 유용한 형광체일 뿐만 아니라, Eu3+를 첨가하는 경우에는 우수한 적색을 보이기 때문에 다양 한 산업에서 응용하기 적합하다.4)
적색형광체 Gd2O3:Eu3+와 같은 형광체를 제조하는 방 법은 크게 고상,5,6) 액상7-9) 및 기상합성법1)으로 분류할 수 있다. 현재 상용화된 공정은 고상법으로 형광체의 대 량 생산에 적합한 공정으로 널리 활용되고 있으나, 이 방법으로는 형광체의 입도 크기 및 형상 조절에 대한 어 려움이 있다고 알려져 있다. 이에 반해 액상 및 기상합 성법은 비교적 공정이 간단하고 형광체의 형상조절이 용 이하며, 특히 액상합성법은 다른 방법보다 저온에서 형 광체의 합성이 가능하다는 장점을 가지며, 나노 크기의 형광체의 합성에 많은 연구가 진행되고 있다. 액상법에 는 졸겔법, 공침법, 주형법 등이 있으며, 그 중에서 주 형법은 액체 시료를 형틀에 함침시킨 후, 소성 공정을 통해 입자를 만드는 방법으로 균일한 나노입자와 높은 결정성을 얻을 수 있으나, 소성 과정에서 다소 응집된 입자가 생성된다.9) 주형법을 사용하기 위해서는 밀링과 정이 필수적이며, 본 연구에서는 형광체 나노입자 및 분 산졸 제조는 휴대용 UV 장비로 시인성이 확보되는 나 노입자코팅형 보안안료에 적용하기 위하여 연구하고 있다.
일반적으로 형광체와 같이 응집된 입자를 나노 크기의 균일한 분산졸로 제조하기 위해서는 비드밀을 이용한 습 식밀링이 주로 사용하고 있으며, 이는 용매 속에서 정 전기적 인력을 반감하여 재응집을 막고 분산안정성을 높 여준다고 알려져 있다.10,11) 밀링과정을 통해 형광체의 분 산은 용이해지나, 밀링조건에 따라 형광체의 구조가 파괴 되어 형광체의 특성이 나타나기 어려운 경우가 있다. 따 라서 형광체 특성을 유지하기 위해 적절한 밀링조건을 찾고, 이를 이용하여 보안안료에 적용하기 위하여 연구 가 필요하다. Lee 등은 기상합성법으로 Y2O3:Eu3+ 형광 체를 합성하였으며, 합성된 입자는 응집된 5 μm의 입자 로 이를 30분 밀링하여 300 nm 이하의 균일한 입자를 만드는 연구를 수행하였다.2) 본 연구자들도 주형법으로 Y2O3:Eu3+ 적색형광체를 제조한 후, 밀링하여 134 nm의 적색형광체 나노분산졸을 합성하였다.9) Antic 등과 Lin 등은 졸겔법으로 적색형광체 Gd2O3:Eu3+를 제조하여 서 브마이크론 크기의 응집된 나노형광체를 제조하였다.3,4) Song 등은 약 10 μm의 형광체 Y3Al5O12:Ce3+를 비드의 종류와 시간에 따라 밀링함으로써 나노크기의 다양한 형 광체 입자를 제조하였다.12) 또한, 본 연구자들은 형광체 이외의 나노분산졸에 관하여 15 μm의 fumed silica 응 집분말을 수계에서 밀링하여 58 nm의 실리카졸을 제조 하는 연구를 진행하였다.10) 이와 같이 밀링공정으로 형 광체와 같은 다양한 입자를 나노입자 및 나노분산졸을 제조하는 연구는 널리 진행되고 있으며, 본 연구에서와 같이 나노분산된 적색형광체 Gd2O3:Eu3+에 관한 연구는 진행되지 않고 있으며 나노분산졸은 입자표면 코팅 매 체 또는 코팅제용으로 적용이 용이할 것으로 고려된다.
본 연구에서는 주형법으로 Gd2O3:Eu3+ 적색형광체 분 말을 제조한 후, 비드밀을 이용하여 형광체 나노분산졸 을 제조하였다. 주형법을 이용한 Gd2O3:Eu3+ 적색형광체 분말은 소성온도와 Eu3+ 함량을 변화하여 제조하여 입자 의 형상, 결정성 및 형광특성을 평가하였다. Gd2O3:Eu3+ 적색형광체 나노분산졸은 밀링 시간에 따른 입자 형상 및 크기의 영향과 밀링 후 나노분산졸의 형광특성을 살 펴보았다. 또한, Gd2O3:Eu3+ 적색형광체 나노분산졸의 수 열처리하에서 제조된 자기조립형 막대기형 입자 제조에 관하여 살펴보고자 한다.
2. 실험 방법
2.1. 주형법에 의한 Gd2O3:Eu3+ 적색형광체 분말의 제조
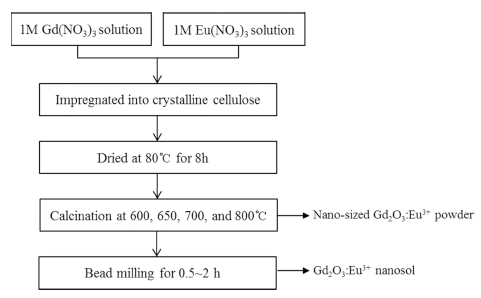
본 연구에서는 주형법으로 Gd2O3:Eu3+ 적색형광체 분 말을 제조하기 위해 gadolinium oxide(Aladdin, 99.99 %)와 europium oxide(Aladdin, 99.9 %)를 질산(Daejung Chem, 60 %)에 각각 녹인 후 Gd(NO3)3와 Eu(NO3)3의 형태로 사용하였다. 이때, Gd(NO3)3와 Eu(NO3)3의 함량 은 Gd(2-x)EuxO3에서 Eu3+의 몰비(x)를 0.1, 0.2, 0.3 및 0.4로 변화시켰다. 20분간 초음파를 이용하여 두 용액을 혼합한 후, 결정성 셀룰로오스에 함침하여 80 °C에서 8 시간 건조 후 소성시켜 Gd2O3:Eu3+ 분말을 제조하였다. 소성온도에 따른 형광특성과의 상관성을 관찰하기 위해 서 소성온도를 600, 650, 700 및 800 °C로 변화시켰으 며, 승온속도 5 °C/min와 열처리 시간은 2시간으로 하여 실험을 진행하였다. Fig. 1은 주형법을 이용하여 적색 형 광체를 제조하는 모식도를 나타내었다.
2.2. Gd2O3:Eu3+ 적색형광체 분말로부터 나노분산졸 제조
주형법으로 제조된 Gd2O3:Eu3+ 적색형광체 분말(약 32 μm)을 습식밀링에 의한 나노분산졸을 제조하기 위해 배 치식 비드밀 분산기(Alesco Co., Japan)를 사용하였다. 분 산성을 높이기 위해서 아크릴계 공중합체를 분산제로서 일정량을 넣은 후, 밀링 시간을 15~180분 동안 변화시 키며 분산성을 관찰하였다. 비드밀 장치는 가운데 축에 장착된 임펠러가 회전하면서 용매내에서 비드와 밀링시 료가 분쇄/분산되는 방식으로 비드밀에 장착되는 임펠러 는 7 cm의 크기를 지닌 flat disc를 사용하였다.10) 지르 코니아 비드 크기는 0.3 Φ를 사용하였으며, 밀링 속도 는 2100 rpm 조건으로 진행하였다. 또한, Gd2O3:Eu3+ 적색형광체는 수계에서 고형분 함량 2 wt% 조건에서 실 험을 진행하였다.
2.3. 자기조립형 Gd2O3:Eu3+ 적색형광체 제조
자기조립형 Gd2O3:Eu3+ 적색형광체를 제조하기 위하여 500 mL 삼구플라스크에 밀링하여 제조한 2 wt%의 적색 형광체 나노분산졸과 일정량의 증류수를 넣어 나노분산 졸의 농도는 1.2 %로 조절하였다. 나노분산졸의 반응온 도는 85 °C로 유지하여 시간에 따른 Gd2O3:Eu3+ 적색형 광체 입자형상의 변화를 확인하였다.
2.4. Gd2O3:Eu3+ 적색형광체의 특성 분석
Gd2O3:Eu3+ 적색형광체 분말의 결정구조는 XRD(X-ray Diffraction, D/MAX-2500V, Rigaku)를 이용하여 측정조 건 400 kv, 20 mA, scan speed 5°/min으로 2θ = 5~90°에 서 관찰하였다. XRD 결과로부터 제조한 입자의 결정립 크기는 Scherrer’s equation을 이용하여 계산하였다.13)
여기서, D는 결정립 크기(nm), K는 shape factor, λ는 파장, β는 반가폭, 그리고 θ는 피크각도이다. 적색형광 체의 밀링 전후의 입자 형상은 FE-SEM(Field Emission Scanning Electron Microscope, JSM-6700F, Jeol)을 이 용하여 관찰하였다. 적색형광체의 분산된 졸의 입도분포 는 입도분석기(ELS-Z, Otsuka)을 이용하여 전기영동광산 란 및 동적광산란 방식으로 측정하였다. 이때 입도분포는 총 5회 측정한 평균값으로 나타내었다. 또한, 적색형광 체의 밀링 전후와 밀링 후 재소성에 따른 형광특성의 변 화는 형광분석기(Fluorescence spectrometer, LS 55, Perkin Elmer)를 이용하여 파장 400~800 nm 범위에서 발광하는 빛의 스펙트럼을 측정하였고, 2% 필터를 장착한 후 측 정하였다. 또한 Gd2O3:Eu3+ 적색형광체 나노분산졸의 수 열처리 과정에서 얻어진 Gd(OH)3:Eu3+ 분말의 특성분석 도 상기의 기기를 이용하여 분석하였다.
3. 결과 및 고찰
3.1. 소성온도와 반응 몰비에 따른 Gd2O3:Eu3+ 적 색형광체의 제조
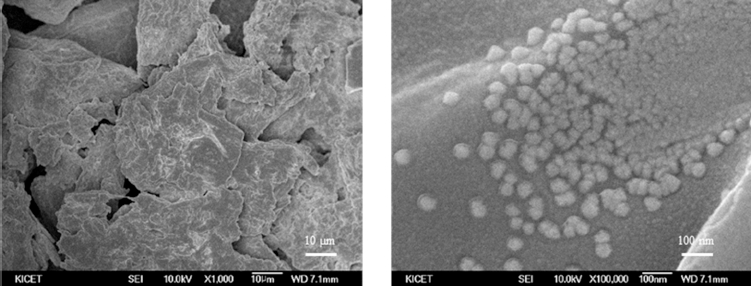
본 논문에서 적색형광체를 합성하기 위하여 사용한 주 형법은 결정성 셀룰로오스에 Gd와 Eu 이온을 함침한 후, 이를 소성하여 Gd2O3:Eu3+ 형광체를 얻는 방법이다. Fig. 2는 Gd와 Eu가 함침된 결정성 셀룰로오스를 1,000 배와 100,000배 확대한 FE-SEM 이미지를 나타낸 것으 로, 결정성 셀룰로오스 내에 20~50 nm의 형상을 지닌 함 침염들이 분포되어 있는 것을 관찰하였다. 이때 상기염 함침된 셀룰로오스를 고온에서 소성하여 Gd2O3:Eu3+ 형 광체를 합성하였다.
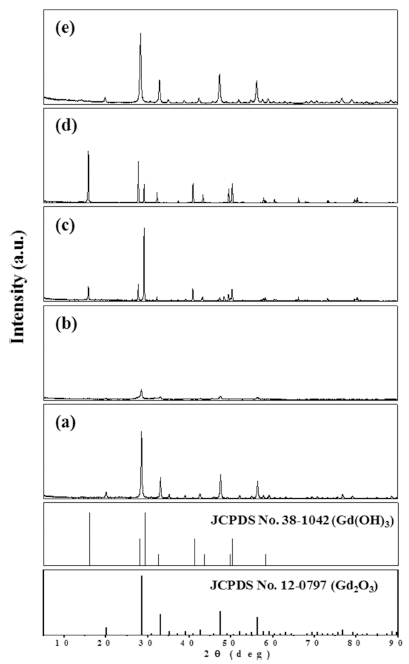
주형법으로 Gd2O3:Eu3+ 적색형광체 합성 시, 소성온도 에 따른 형광체 입자의 특성을 알아보기 위하여 온도를 600, 650, 700 및 800 °C로 변화시켰으며, 소성온도에 따 른 XRD 패턴 결과를 Fig. 3에 나타내었다. 이때, Eu3+ 의 함량은 Gd(2-x)EuxO3에서 x = 0.2로, 소성시간은 2시간 으로 고정하여 제조하였다. 그림에서 보듯이 모든 Gd2O3: Eu3+ 적색형광체는 JCPDS No. 12-0797의 Gd2O3의 패 턴에 일치하였으며, 이로부터 주형법으로 Gd2O3의 적색 형광체가 합성되었다는 것을 확인하였다. 또한, 소성온도 가 600에서 800 °C로 증가할수록 XRD 패턴에서 intensity도 증가하였는데, 이는 온도가 높을수록 결정성이 높 아지기 때문으로 생각된다. Roh 등과 Lin 등도 Gd2O3: Eu3+ 적색형광체를 합성한 후 XRD 결과를 확인한 결 과, 소성온도가 증가함에 따라 intensity가 증가한다고 하 여 본 연구의 결과와 동일한 결과를 보였다.14,15)
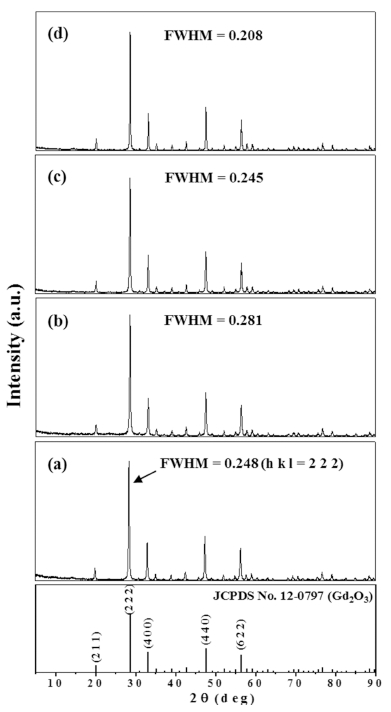
Fig. 3
XRD patterns of Gd2O3:Eu3+ red phosphor powders prepared at (a) 600 °C, (b) 650 °C, (c) 700 °C, and (d) 800 °C for 2 h.
Fig. 4는 소성온도를 600~800 °C로 증가시킴에 따라 합 성한 Gd2O3:Eu3+ 적색형광체의 photoluminescence(PL) 세기를 나타낸 것으로, 2 % filter를 장착한 후 측정된 결 과를 보정한 값이다. Fig. 4(a)는 Gd2O3:Eu3+ 적색형광체 의 소성온도에 따른 PL 세기를 나타낸 것으로 광역대 254 nm 파장대에서 400~800 nm 사이의 최대 중심파장 에서의 발광강도이다. 약 613 nm에서 주피크가 관찰되는 데, 이는 red emission을 의미하는 것으로 알려져 있다. 일 반적으로 613 nm 피크는 Eu3+ site에서 inversion symmetry 부족으로 인한 Eu3+의 전자쌍극자 전이(5D0→ 7F2) 때문 으로 사료된다.15) Fig. 4(b)는 소성온도에 따른 Gd2O3: Eu3+ 적색형광체의 PL 세기를 나타낸 것으로, Fig. 4(a) 와 달리 613 nm 파장대에서 220~500 nm 사이의 최대파 장에서의 발광강도이다. 그림에서 보듯이 약 254 nm에서 높은 값을 보이는데, 이는 Eu-O의 상호작용으로 인한 전 하의 이동때문으로 사료된다.15) 더욱이, Lin 등은 4f level 이 바닥상태에서 들뜬상태로의 변화로 Eu-O의 전하이동 이 발생한다고 하였다.15) Fig. 4에서 보듯이 XRD 패턴 의 결과와 마찬가지로 소성온도가 600에서 800 °C로 증 가함에 따라 최대 파장에서의 PL 세기도 증가하여 800 °C > 650 °C > 600 °C 순으로 증가하는 경향을 보였다. 이 는 온도가 증가할수록 Gd2O3의 결정성의 높아지기 때문 으로 생각된다. Roh 등과 Lin 등의 연구에서도 소성온 도가 증가함에 따라 PL 세기가 증가하여 본 연구와 유 사한 결과를 보였다.4,14,15) 한편, Moura 등은 Gd2O3: Eu3+ 적색형광체를 합성하는 경우 소성온도 500~700 °C 에서는 형광체의 형태가 hexagonal Gd(OH)3:Eu3+에서 cubic Gd2O3:Eu3+로 변화한다고 하였다.16) 이러한 온도는 형광체의 결정구조가 무질서(structural order-disorder)하게 변화하는 범위로 소성온도와 PL 특성을 이해하는 것이 중요하다고 하였다. 본 연구에서는 소성온도가 700 °C인 경우 PL 특성이 다소 낮은 특성을 보였는데, 이는 형 광체가 Gd2O3:Eu3+로 변하는 과정에서 무질서하게 결정 구조가 변화하며 이로인해 XRD intensity가 다소 감소 하였고, PL 특성도 낮게 나온 것으로 생각된다. 따라서 이후 본 연구에서는 나노분산졸을 제조하기에 어려움이 없고, PL 특성도 우수한 조건인 소성온도를 650 °C로 고 정하여 Gd2O3:Eu3+ 적색형광체 제조하였는데 이는 입자 간의 응집으로 인한 분산특성을 고려하였다.
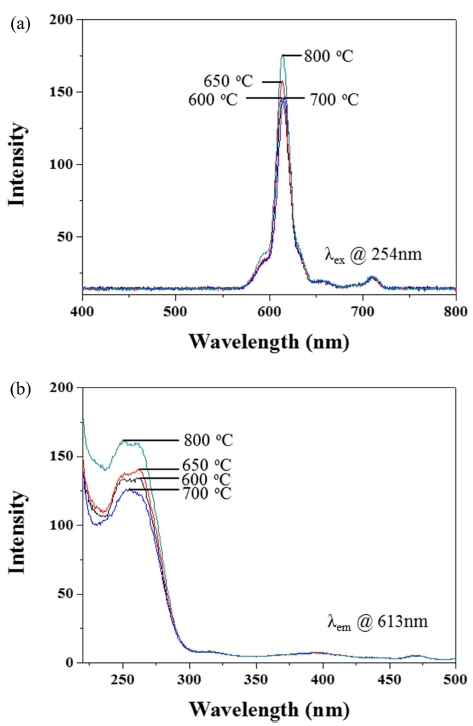
Fig. 4
(a) Emission and (b) excitiation spectra of Gd2O3:Eu3+ red phosphor powders prepared at 600 °C, 650 °C, 700 °C, and 800 °C for 2 h.
Gd3+와 Eu3+의 몰비에 따른 Gd2O3:Eu3+ 적색형광체 입 자의 응집성과 결정립 크기의 상관관계를 알아보기 위 하여 소성온도를 650 °C로 고정한 후, Gd(2-x)EuxO3에서 Eu3+의 몰비인 x의 값을 0.1, 0.2, 0.3 및 0.4로 변화시 켜 Gd2O3:Eu3+ 적색형광체를 합성하였다. x의 값(Eu3+의 몰비)을 0.1에서 0.4로 변화시킨 경우에 XRD를 분석한 결과, 모든 Gd2O3:Eu3+ 적색형광체는 JCPDS No. 12- 0797의 Gd2O3의 패턴에 일치하였다. 이를 식(1)에 적용 하여 Eu3+의 함량에 따른 Gd2O3:Eu3+ 형광체의 결정립 크기를 Fig. 5에 나타내었다. 그림에서 보듯이 Eu3+의 함 량이 0.1, 0.2 및 0.3으로 증가함에 따라 적색형광체의 결정립 크기는 32.4 nm, 30.2 nm 및 23.8 nm로 감소하 다가, 0.4인 경우에는 결정립의 크기가 27.5 nm로 다소 증가하는 결과를 보였다. Eu3+의 함량이 0.1~0.3으로 증 가함에 따라 결정립 크기가 감소하는데, 이는 Gd와 Eu 원소 사이의 반경 차이에 의한 격자 왜곡현상으로 인해 입자의 성장을 방해하는 것으로 보인다. 또한, Eu3+ 0.4 인 경우에는 Eu 원소가 Eu 산화물과 같은 불순물이 생 성되어 결정립 크기가 증가하는 것으로 생각된다. Lin 등 은 Gd2O3:Eu3+ 적색형광체를 소성온도에 따라 제조한 결 과 형광체의 결정립크기는 12~34 nm이었으며,15) Flores- Gonzalez 등도 소성온도에 따라 Gd2O3:Eu3+ 적색형광체 를 제조하였고, 소성온도가 600 °C인 경우에는 결정립크 기가 약 25 nm라고 하여 본 연구의 결과와 유사하였다.17)
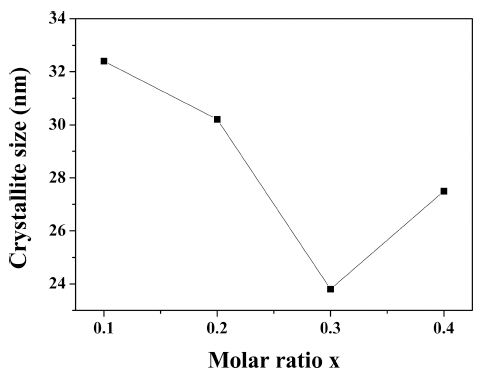
Fig. 5
Crystallite size of Gd2O3:Eu3+ red phosphor powders prepared by different molar ratio x in the Gd(2-x)EuxO3.
Fig. 5의 Eu3+의 몰비를 0.1~0.4로 변화시켜 합성한 Gd2O3:Eu3+ 적색형광체의 실제 형상을 관찰하기 위하여 FE-SEM 이미지 Fig. 6에 나타내었다. 그림은 50,000배 확대한 것이다. Fig. 6(a)는 Eu3+의 몰비가 0.1인 경우의 적색형광체를 나타낸 것으로 약 50~150 nm의 불균일한 구형의 입자들이 응집되어 있는 것을 확인하였다. Eu3+가 0.2인 경우(Fig. 6(b))에는 0.1의 경우보다 입자가 다소 감 소하여 약 20~150 nm의 구형입자가 응집되었다. 이에 반 해 Eu3+가 0.3인 경우(Fig. 6(c))에는 약 20~50 nm의 균 일한 구형입자가, Eu3+가 0.4인 경우(Fig. 6(d))에는 약 100 nm의 균일한 입자가 응집된 것을 확인하였다. 몰비 가 0.1에서 0.3으로 증가할수록 응집된 각각 입자의 크 기는 감소하다가, 몰비가 0.4인 경우에는 입자의 크기가 다소 증가하였는데, 이는 XRD로 계산된 결정립크기의 결 과와 유사하였다. Antic 등, Tamrakar 등, Lin 등은 나 노크기가 응집된 서브마이크론 크기의 구형의 Gd2O3:Eu3+ 적색형광체 입자를 합성하였다.3,15,18)

Fig. 6
FE-SEM images (X 50,000) of Gd2O3:Eu3+ red phosphor powders obtained at different molar ratio x in the Gd(2-x)EuxO3: (a) x = 0.1, (b) x = 0.2, (c) x = 0.3, and (d) x = 0.4 (white scale bar = 100 nm).
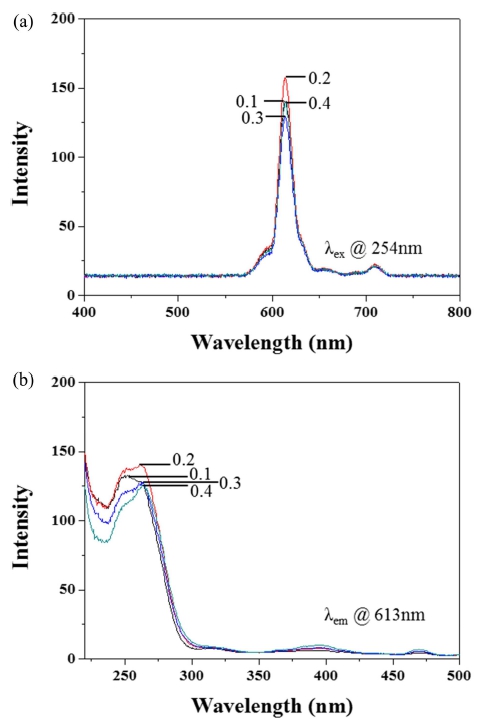
Fig. 7은 Eu3+의 몰비를 0.1~0.4로 변화시켜 합성한 Gd2O3:Eu3+ 적색형광체의 PL 세기를 나타낸 것이다. Fig. 7(a)는 광역대 254 nm 파장대에서, Fig. 7(b)는 광역대 613 nm 파장대에서의 최대 중심파장의 발광강도를 각각 나타내었으며, PL 세기는 0.2 > 0.1 > 0.4 > 0.3 순으로 증 가하였다. 일반적으로 PL 세기는 Eu3+의 농도와 각 원 자사이의 결정학적 위치의 분포에 따라 결정된다.3) 한 편, Eu3+의 몰비가 0.2 이상으로 증가하여도 형광특성은 오히려 감소하는 결과를 보이는데 이는 농도 소광 현상 (concetration quenching phenomena) 때문이다.3) 이로부 터 Eu3+의 몰비가 0.2인 경우 가장 우수한 형광특성을 나타내는 것을 확인하였다. Kang 등의 연구에서도 Eu3+ 의 함량을 0.04~0.24로 변화시켜 Gd2O3:Eu3+를 합성하는 경우에 Eu3+의 몰비가 0.2일 때, 가장 우수한 PL 특성 을 보여 최적의 합성조건이라고 하였다.19) 또한, 입자 크 기와 PL의 상관성은 FE-SEM 결과에서 입자의 크기가 다소 크게 보였던 Eu3+의 몰비가 0.2인 경우의 형광체 의 PL 세기가 가장 높았으며, 입자가 가장 작은 0.3으 로 합성한 형광체가 가장 낮은 PL 세기를 보였다.
3.2. Gd2O3:Eu3+ 적색형광체의 비드밀링에 의한 분 산졸의 분산인자 연구
주형법으로 합성한 Gd2O3:Eu3+ 적색형광체는 응집되어 실제 다른 분야에 응용하기 어려움이 있어 본 연구에서 는 Eu3+의 몰비를 0.1~0.4로 변화시켜 합성한 형광체를 비드 밀링하여 형광체가 분산된 나노분산졸을 합성하는 연구를 수행하였다. Gd2O3:Eu3+ 적색형광체 나노분산졸을 제조하기 위해 비드는 0.3 Φ 지르코니아, 용매는 증류 수를 사용하였으며, 밀링 시간은 15~180분으로 조절하였 다. 이때, 형광체 나노분산졸은 본 연구자들의 논문9)을 참고하여 아크릴계 공중합체 분산제를 넣어 pH 8에서 제 타포텐셜 값을 40 mV로 조절하여 수행하였다.
Fig. 8은 PL 세기가 가장 우수하였던 Eu3+ 몰비가 0.2 인 Gd2O3:Eu3+ 적색형광체 나노분산졸의 밀링시간에 따 른 입자크기(D50, D90)를 나타낸 것이고, Table 1은 몰비 (0.1~0.4)에 따라 제조한 적색형광체 나노분산졸의 밀링 시간에 따른 입자크기를 나타낸 것이다. Fig. 8에서 보 듯이 Gd2O3:Eu3+ 적색형광체 나노분산졸에서 입자의 크 기는 밀링 전 약 32 μm에서 밀링 15분 이후에 약 120 nm로 급격히 감소하다가 그 이후에는 약 110 nm로 거 의 일정한 입자 크기를 보였다. 또한, 그림에서 보듯이 D50과 D90의 그래프가 동일한 경향으로 감소되며, 각 경 우의 입자 크기도 거의 유사한 것을 관찰하였다. 이로 부터 형광체 나노분산졸의 분산이 잘 되었다는 것을 확 인하였다. Table 1에서 보듯이 Eu3+의 몰비를 0.1~0.4로 변화시킨 경우에도 밀링시간이 증가함에 따라 형광체 나 노분산졸의 입자가 급격하게 감소하여 0.2의 결과와 유 사한 결과를 보였다. 한편, 180분 이후에는 오히려 입자 크기가 300 nm로 증가하는 것을 볼 수 있는데 이는 시 간이 경과함에 따라 비드 밀링으로 에너지가 가해져 입 자가 응집된 것이라고 생각된다. Lee 등은 Y2O3:Eu3+ 형 광체를 합성한 후, 30분 밀링하여 약 300 nm 크기의 입 자를 얻었다고 하였는데,2) 이들의 연구로부터 본 연구에 서 합성한 Gd2O3:Eu3+ 적색형광체는 Y2O3:Eu3+보다 강 도가 약하여 밀링 효과가 우수하기 때문에 코팅에 사용 하기 적합하다고 생각된다. 이러한 결과로부터 Gd2O3: Eu3+ 적색형광체 나노분산졸은 밀링시간은 30분 이후에 안정화되는 것을 확인하였으며, 이후 실험은 30분 밀링 한 나노분산졸로 수행하였다.
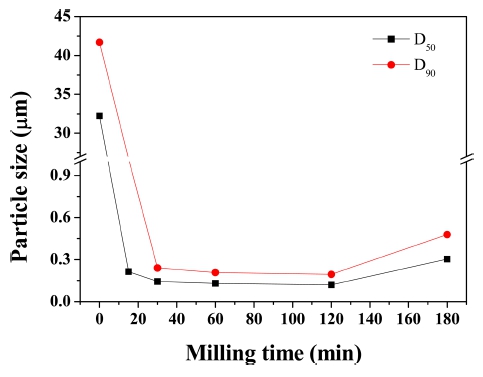
Fig. 8
Median particle size (D50) of slurries or nanosol of Gd(2-x) EuxO3 (x = 0.2) red phosphor prepared by varing milling time.
Table 1
Median particle size (D50) of slurries or nanosol of Gd(2-x) EuxO3 (x = 0.1, 0.2, 0.3, and 0.4) red phosphor prepared according to milling time.
Fig. 9는 Eu3+의 몰비를 0.1~0.4로 변화시켜 합성한 Gd2O3:Eu3+ 적색형광체를 120분 밀링한 나노분산졸의 FE-SEM 이미지를 나타낸 것이다. Fig. 9(a~d)에 나타난 밀링한 나노분산졸은 Eu3+의 몰비와 관계없이 100~150 nm의 균일한 구형 입자인 것을 확인하였다. 밀링 전과 비교하였을 때, 응집된 입자가 없이 고르게 분산되었다.

Fig. 9
FE-SEM images (X 50,000) of Gd2O3:Eu3+ red phosphor nanosol obtained by 120 min milling at different molar ratio x in the Gd(2-x)EuxO3: (a) x = 0.1, (b) x = 0.2, (c) x = 0.3, and (d) x = 0.4 (white scale bar = 100 nm).
밀링 후 Gd2O3:Eu3+ 적색형광체의 안정성을 확인하기 위하여 밀링 30분과 120분의 입자의 XRD를 분석하였다 (Fig. 10). 밀링 이후에도 JCPDS No. 12-0797의 Gd2O3 의 패턴에 모두 일치하나, 밀링시간이 120분으로 경과함 에 따라 결정구조가 깨지면서 XRD 패턴에서 intensity가 감소하여, Gd2O3:Eu3+ 적색형광체의 결정성이 줄어드는 것으로 관찰되었다. 이에 반해 밀링한 나노분산졸을 650 °C에서 2시간 소성한 이후에는 XRD 패턴에서 intensity 가 증가하였고, 이는 밀링 전의 intensity와 비교하였을 때 약 70 % 수준으로 회복되었다. 본 연구에서 제조한 Gd2O3:Eu3+ 적색형광체 나노분산졸은 무기소재 위에 코 팅하는 형태로 사용되는 것으로, 코팅 공정에서 소성과정 은 필수적인 것이다. 따라서 본 연구에서 합성한 Gd2O3: Eu3+ 적색형광체 나노분산졸은 밀링전과 비교하여 XRD 의 intensity는 다소 감소하나, 코팅공정에 사용하기에는 적절한 것으로 판단된다. Song 등의 연구에서도 형광체 Y3Al5O12:Ce3+를 합성한 후, 나노크기의 형광체를 제조하 기 위하여 밀링공정을 거치는데, 밀링 한 경우 시간과 밀링 횟수가 증가할수록 XRD 피크의 intensity는 감소 한다고 하여 본 연구의 결과와 유사하였다.12)
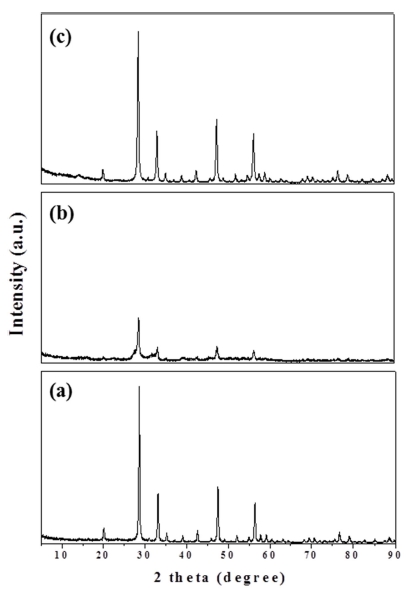
Fig. 10
XRD patterns of Gd2O3:Eu3+ red phosphor powders (x = 0.2): (a) before milling (x1/3), (b) milling for 120 min, and (c) calcination at 650 °C for 2 h.
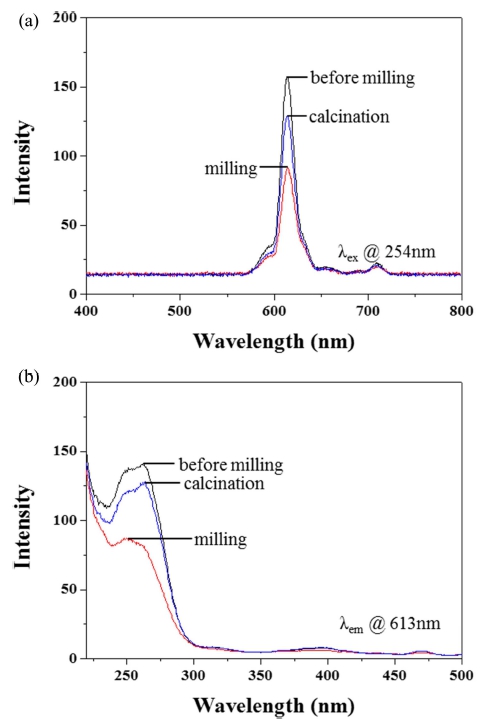
Fig. 11은 Gd2O3:Eu3+ 적색형광체(x = 0.2)의 밀링 전 입자와 형광체 나노분산졸의 밀링 후, 그리고 밀링 후 소성과정을 거친 적색형광체의 PL 세기를 각각 나타낸 것이다. Fig. 11(a)에서 보는 것과 같이 254 nm 파장대 에서의 주피크인 약 613 nm에서 밀링전의 경우에는 157 인데 반해 밀링 후에는 91으로 intetnsity의 높이가 약 60 % 감소하였다. 한편, 소성과정 후의 적색형광체의 경 우에는 130으로 밀링 전의 약 83 %까지 PL 세기가 회 복되었다. Fig. 11(b)의 경우에도 Fig. 11(a)의 결과와 마 찬가지로 적색형광체의 밀링전과 비교했을 때, 밀링 후 가 다소 감소하였으나 소성 후에는 밀링전과 유사한 세 기로 되돌아왔음을 확인하였다. 이러한 결과는 XRD 패 턴의 결과와 유사하였으며, 본 연구에서 합성한 적색형 광체 나노분산졸은 무기소재에 코팅하기에 적합한 소재 임을 확인하였다.
3.3. 자기조립형 Gd2O3:Eu3+ 적색형광체 제조
상기에서 주형법으로 합성한 후 밀링하여 제조한 Gd2O3: Eu3+ 적색형광체 나노분산졸은 일정한 조건하에서 자기 조립하여 막대기형의 입자로 성장하는 특징이 있다. 형 광특성 Gd2O3:Eu3+ 적색형광체 나노분산졸의 농도는 1.2 %, 온도는 85 °C로 조절한 후, 시간에 따른 Gd2O3:Eu3+ 적색형광체 입자형상의 변화를 확인하였다.
Fig. 12는 수열 반응시간에 따른 자기조립형 Gd2O3: Eu3+ 적색형광체의 FE-SEM 이미지를 나타낸 것이다. 그 림에서 보는 것과 같이 가열하기 전의 입자는 100~150 nm의 균일한 구형 입자였으며, 1시간 이후에도 변화없 이 일정한 구형의 형광체임을 확인하였다. 이에 반해 시 간이 3시간에서 12시간으로 경과함에 따라 구형의 입자 는 막대기형으로 성장하였다. 가열시간이 3시간인 경우에 는 구형입자와 막대기형의 입자가 혼재되어 있었으나, 시 간이 지남에 따라 모든 입자가 막대기형으로 형성되었 고, 12시간일 때는 막대기형의 입자들끼리 응집이 발생 하었다. 또한, 시간에 따른 막대기형의 입자는 시간이 3~12시간으로 경과함에 길이는 1233~1650 nm, 두께는 233~367 nm로 증가하였다.

Fig. 12
FE-SEM images of self-assembled Gd2O3:Eu3+ red phosphor obtained according to the variation of reaction time at 85 °C: (a) 0 h, (b) 1 h, (c) 3 h, (d) 6 h, (e) 9 h, and (f) 12 h (white scale bar = 1 μm).
Fig. 13은 FE-SEM 결과에서 확인된 자기조립형 입자 의 시간에 따른 길이와 두께 비를 나타낸 것이다. 그림 에서 보듯이 0~1시간일 때는 구형 입자의 각형비(aspect ratio)를 1로 고려하였을 때, 3시간 이후로는 막대기형의 입자가 생성되어 길이와 두께의 비가 1 이상으로 증가 하였다. 가열시간이 3시간에서 12시간으로 증가함에 따 라 각형비는 5.3, 4.8, 4.3, 4.5로 증가하다가 일정시간 이후로는 시간이 일정한 비율을 가지는 것을 확인하였다.
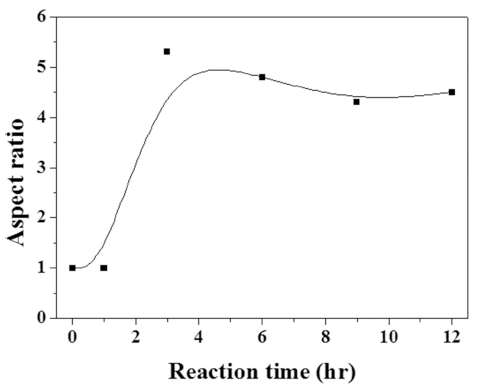
Fig. 13
The aspect ratios of self-assembled Gd2O3:Eu3+ red phosphors obtained according to the variation of reaction time at 85 °C.
합성된 막대기형 입자의 결정구조 및 자기조립현상을 확인하기 위하여 XRD를 분석하였으며, 그 결과를 Fig. 14에 나타내었다. 앞서 설명한 바와 같이 밀링 전과 후 의 적색형광체는 모두 Gd2O3를 나타내며, 밀링 후의 intensity는 밀링 전과 유사수준으로 회복되었다. 이에 반 해 가열온도 85 °C에서 3시간과 12시간씩 반응한 경우 (Fig. 14(c~d))에는 Gd2O3가 아닌 JCPDS No. 38-1042 의 Gd(OH)3의 회절패턴을 보였다. 이는 수열조건에서 Gd2O3:Eu3+ 구형 입자가 Gd(OH)3로 수화되면서 Gd(OH)3 입자간의 표면의 OH기의 축합으로 인해 막대기형으로 성 장하는 것임을 알 수 있다. 즉 이때는 적색 형광특성이 나타나질 않으나, 650 °C에서 2시간 소성한 경우에는 적 색 형광특성을 보이는 Gd2O3:Eu3+의 형광체로 PL 특성 이 회복되는 것을 확인하였다. 추가 연구를 통하여 나 노형광체 입자를 마이크론 크기의 판상 세라믹 입자에 코팅하여 보안특성을 가진 안료로 제조하기 용이하며 나 노입자로 코팅된 입자가 자기조립현상에 의해 표면에 막 대기형으로 성장시 형광 특성이 향상되었다.
4. 결 론
주형법을 이용하여 나노입자 코팅형 보안안료 적용을 위한 형광체 나노분산졸을 제조하기 위하여 소성온도와 Eu3+의 몰비에 따라 Gd2O3:Eu3+ 적색형광체 분말을 합 성하고, 이를 습식밀링 과정을 통해 적색형광체 나노분 산졸을 제조하였다. Gd2O3:Eu3+ 적색형광체 분말 합성시 소성온도는 650 °C, Eu3+의 몰비는 Gd(2-x)EuxO3에서 x가 0.2인 경우가 최적의 조건이었다. 또한, 적색형광체 나노 분산졸을 합성하는 경우에는 밀링시간은 30분이 가장 적 합하였으며, 효과적인 밀링으로 인해 입도는 32 μm에서 100 nm까지 감소하는 것을 알 수 있었다. 나노분산졸을 만드는 과정에서 밀링과 분산을 통해 합성한 Gd2O3:Eu3+ 적색 형광체는 밀링 전과 비교하였을 때, 결정성과 PL 세기가 감소하는 문제점이 있지만, 이는 소성과정을 통 해 결정성과 PL 세기가 밀링전의 유사수준으로 회복됨 을 확인하였다. 또한, 밀링하여 제조한 Gd2O3:Eu3+ 적색 형광체 나노분산졸을 85 °C에서 12시간 가열하여 막대기 형의 자기조립형 입자를 제조하였다. 합성한 자기조립형 형광체는 Gd(OH)3의 결정구조로 변화하였지만, 소성 후 Gd2O3:Eu3+ 형광체로 회복되었다. 또한 추후 연구로 적 색형광체 나노분산졸을 코팅 매체로 사용하여 Gd2O3:Eu3+ 적색형광체 나노분산졸 또는 자기조립형 입자를 판상형 입자에 코팅 및 소성하여 보안안료로 적용하고자 한다.