1. 서 론
2. 실험 방법
2.1. 시료
2.2. PZC 합성
2.3. ZrO2 제조
2.4. PIP 활용한 ZrB2-ZrO2 복합재 제조
2.5. 분석
3. 결과 및 고찰
3.1. ZrO2 전구체 합성 전략 및 특성
3.2. PZC-12의 분자 구조 분석
3.3. 온도에 따른 ZrO2의 결정 구조 변화
3.4. ZrO2의 미세구조
3.5. PZC-12의 열적 특성 및 세라믹화 거동
3.6. PIP 공정을 이용한 ZrB2-ZrO2 복합재 제조
4. 결 론
1. 서 론
극한소재(extreme environment materials)는 초고온, 초저온, 초고압과 같이 통상적인 범주를 벗어나는 환경에서 신뢰성을 보장하는 소재를 의미한다. 특히 최근 정부와 민간 주도의 우주항공 산업 규모가 증대됨에 따라, 태양 탐사선이나 대기권 재진입체와 같이 초고온에 노출되는 부품을 위한 극한소재의 중요성이 그 어느 때보다 부각되고 있다.1) 이러한 요구에 부응하는 핵심 소재로 초고온 세라믹(ultra-high temperature ceramics, UHTCs)이 주목받고 있다.1,2)
UHTCs는 일반적으로 지르코늄(Zr)이나 하프늄(Hf)의 붕화물 및 탄화물(예: ZrB2, ZrC, HfC)을 기반으로 하며, 2,500 °C 이상의 매우 높은 융점을 바탕으로 초고온 환경에서도 구조적 안정성을 확보할 수 있다.2,3) 그러나 UHTCs는 고온에서 산화에 취약하고, 단일 상(phase)으로 사용될 경우 고유의 취성(brittleness)으로 인해 기계적 강도와 파괴인성(fracture toughness)이 낮아 열충격에 의한 파손 위험이 크다는 본질적인 한계를 내포한다. 따라서 실제 적용을 위해서는 UHTCs 기지에 제2상(second phase)을 도입하여 기계적 특성과 내산화성을 보완한 복합재 형태의 연구가 필수적이다.4,5)
복합재의 제2상 후보군 중, 지르코니아(ZrO2)는 높은 융점(2,715 °C), 우수한 내산화성, 그리고 높은 기계적 강도(압축강도 약 2,000 MPa, 굽힘강도 약 1,000 MPa)를 겸비하여 가장 유망한 보강재로 평가받는다.6,7,8,9,10) 특히, 외부 응력에 의해 정방정계(tetragonal)에서 단사정계(monoclinic)로의 상변태가 일어나면서 균열 전파를 억제하는 상전이 강화(transformation toughening) 특성이 발현되어 복합재의 파괴인성을 크게 향상시킬 수 있다.4,9,11,12) 또한 고온에서의 산화저항성도 뛰어나기 때문에 이에 따라 SiC-ZrO2, SiO2-ZrO2, ZrB2-ZrO2, ZrB2-SiC-ZrO2, ZrC-ZrO2 등 다양한 다상 복합재 연구가 활발히 진행되고 있다.11,13,14,15,16,17) 하지만 UHTCs는 소결성이 매우 낮은 난소결성 물질이어서, 기존의 고온 소결 공정으로는 미세구조가 균일하고 치밀한 복합재를 제조하기 어렵고 과도한 에너지가 소모된다는 공정상의 난점이 존재한다.4,15,18)
이러한 소결 공정의 대안으로 고분자 전구체 함침 및 열분해(polymer infiltration and pyrolysis, PIP) 공정이 제시되었다. PIP 공정은 저점도의 액상 고분자 전구체를 다공성 기지(matrix)에 함침시킨 후, 고온에서 열분해하여 세라믹으로 전환시키는 방식이다.19,20) 이 방법은 복잡한 형상의 부품 제조가 용이하고, 나노 수준의 균일한 복합재를 구현할 수 있다는 장점이 있다.19,20) 그러나 PIP 공정의 성공은 전구체의 특성에 절대적으로 좌우된다. 지르코늄 알콕사이드 기반의 지르코니아 전구체(polyzirconium compound, PZC)는 졸-겔(sol-gel) 반응을 통해 합성이 가능하고 이는 나노사이즈의 ZrO2 제조에 유용한 공정이다.21,22,23) 그러나 Zr계 전구체로 sol-gel 반응 진행시 반응성이 지나치게 높아 쉽게 겔화(gelation)되어 액상 상태를 안정적으로 유지하기 어렵다. 이를 해결하기 위해 아세틸아세톤(acetylacetone)과 같은 킬레이트제(chelating agent)를 도입하여 반응 속도를 제어하지만, 이 경우 전구체의 분자량이 낮아져 세라믹으로 전환되기 전에 상당량이 분해되어 최종 세라믹 수율(ceramic yield)이 저하되는 또 다른 문제를 야기 할 수 있다.24,25)
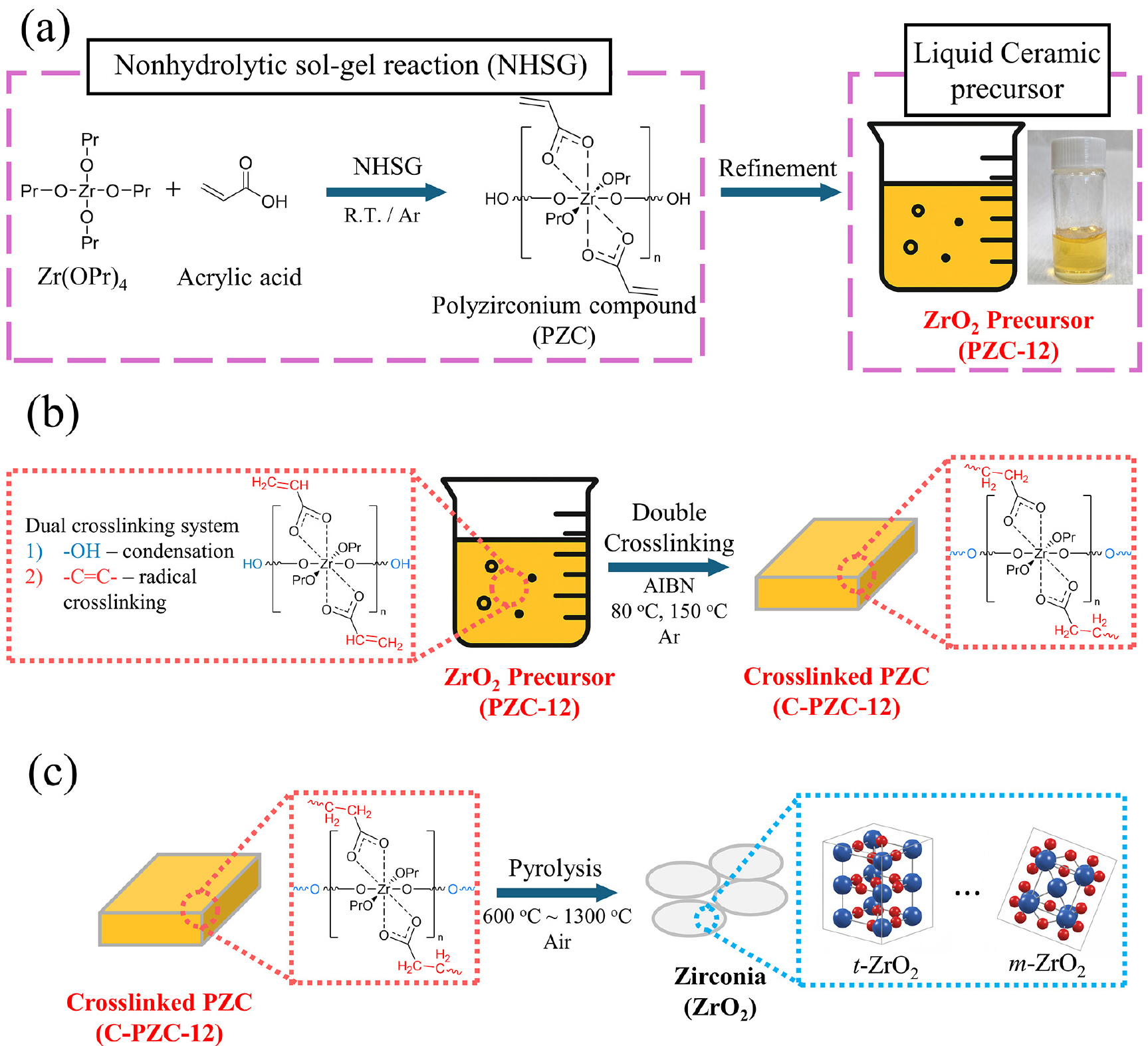
본 연구에서는 선행 연구들이 가진 한계를 극복하고자 새로운 액상 PZC 전구체를 개발하였다. Zirconium propoxide와 acrylic acid를 용매 없이 반응시켜 액상 상태를 안정적으로 유지하는 신규 전구체(PZC-12)를 합성하였고, 개시제(azobisisobutyronitrile, AIBN)를 이용한 이중 가교(dual crosslinking) 메커니즘을 통해 세라믹 수율을 극대화할 수 있는 가능성을 확인하였다. 더 나아가, 개발된 PZC-12 전구체를 ZrB2 성형체에 함침시켜 ZrB2-ZrO2 복합재를 제조함으로써, 본 전구체가 실제 UHTC 복합재 제조를 위한 PIP 공정에 효과적으로 적용될 수 있음을 입증하였다.
2. 실험 방법
2.1. 시료
Zirconium (IV) propoxide 용액(Zr(OPr)4 dissolved in 1-Propanol 70 wt%)은 Thermofisher Scientific(미국)에서 구입하였다. 킬레이트제로 사용된 Acrylic acid는 TCI(일본)에서 구입하였으며, 라디칼 개시제로 사용된 AIBN은 삼천화학(대한민국)에서 구입하였다.
2.2. PZC 합성
PZC는 자기 교반기가 장착된 200 mL 삼구 플라스크를 이용하여 아르곤 분위기 하에서 합성하였다. Zirconium (IV) propoxide (Zr(OPr)4, 0.01 mol)를 각 플라스크에 투입한 후, Acrylic acid (AA)를 Zr(OPr)4 대비 1:1, 1:2, 1:3의 몰 비가 되도록 각각 0.01, 0.02, 0.03 mol씩 첨가하였다. 각 반응물은 몰 비에 따라 PZC-11, PZC-12, PZC-13으로 명명하였다. 반응은 상온의 아르곤 분위기에서 24 h 동안 500 rpm으로 교반하며 진행하였다. 반응이 완료된 후, 75 °C에서 2 h 동안 가열하여 미반응물 및 잔류 용매를 제거하였다. 이 중 몰 비가 1:2인 PZC-12만이 후속 공정에 적합한 황색의 점성 액체로 얻어져 이후 실험에 사용하였다.
2.3. ZrO2 제조
모든 ZrO2는 상기 합성된 PZC-12를 전구체로 사용하여 제조하였다. 먼저, 라디칼 개시제인 AIBN (0.15 g)을 메틸렌 클로라이드(methylene chloride, MC)에 용해시켜 균일한 용액을 준비하였다. 이 용액에 PZC-12 6 g을 투입하여 완전히 혼합하였다. 혼합물은 알루미나 도가니에 옮긴 뒤, 아르곤 분위기 하 80 °C에서 12 h 동안 가열하여 가교 반응(cross-linking)을 통해 경화시켰다. 이렇게 얻어진 고체 중간 생성물은 c-PZC-12이라 명명하였다.
경화된 밝은 황색의 고체(c-PZC-12)를 산화로를 활용하여 공기 분위기에서 각각 500, 600, 700, 800, 1,000, 1,300 °C의 온도로 열분해하여 최종 생성물인 ZrO2를 제조하였다. 각 열분해 온도를 따라 얻어진 백색 분말은 ZrO2-500, ZrO2-600, ZrO2-700, ZrO2-800, ZrO2-1000, ZrO2-1300으로 명명하였다. 각 조건에 대한 상세 내용은 Table 1에서 확인할 수 있다.
Table 1.
Ratio of starting materials and fabricating condition of ZrO2.
2.4. PIP 활용한 ZrB2-ZrO2 복합재 제조
지르코늄 다이보라이드(zirconium diboride, ZrB2, ZrB2-F, d50: 2.12 µm, Japan New Metal Co., Osaka, Japan) 펠릿(직경 10 mm)은 50 vol% ZrB2 슬러리를 건조한 후, 진공 분위기에서 1,900 °C로 1 h 동안 가열(승온 속도: 50 °C/min)하여 제조하였다. ZrB2 슬러리 및 펠릿의 제조 방법은 본 연구 그룹에서 진행하였던 이전 연구에 실험 절차를 따라서 제조하였고 최종 제조된 ZrB2 성형체는 55 %의 상대밀도를 나타내었다.26,27) 제조된 ZrB2 펠릿은 흑연 몰드에 넣은 후, AIBN을 섞은 PZC-12 전구체를 부어 펠릿이 완전히 잠기도록 하였다. 이후 흑연 몰드를 금속 용기에 넣고 10-2 atm의 진공 하에서 20 min 동안 배기하여 진공 침투(vacuum infiltration)를 수행하였다.28) 이어 5 bar의 고압 아르곤 분위기를 20 min 동안 적용하여 전구체의 추가 침투를 유도하였다.28)
진공침투 과정을 거친 후 시편은 아르곤 분위기에서 80 °C로 12 h 동안 가교 반응을 수행한 뒤, 소결로에서 공기중에서 600 °C로 열분해를 진행하였다(승온 속도: 5 °C/min, 600 °C에서 4 h 유지). 위 과정을 3회 반복하여 ZrB2-ZrO2 복합체 시편을 제조하였다.
2.5. 분석
액상 PZC 전구체의 작용기(functional group)는 감쇠전반사 푸리에 변환 적외선 분광법(attenuated total reflectance fourier-transform infrared spectroscopy, ATR-FTIR, Spectrum 2, PerkinElmer, Waltham, MA, USA)을 이용하여 분석하였고, 스펙트럼은 분해능 1 cm-1 조건에서 16회 누적 스캔하여 얻었다. 전구체의 상세 화학 구조는 핵자기공명분광법(nuclear magnetic resonance spectroscopy, NMR, AVANCE Neo, 400 MHz, Bruker, Billerica, MA, USA)을 통해 확인하였으며, 점도는 Cone Spindle이 장착된 점도계(Brookfield, USA)를 사용하여 측정하였다. 전구체의 열분해 거동과 최종 세라믹 수율은 열중량-시차주사열량 동시분석기(thermogravimetric analysis-differential scanning calorimetry, TGA-DSC, LABSYS Evo, SETARAM, Caluire-et-Cuire, France)로 확인하였는데, 분석은 대기 분위기 하에서 상온부터 1,300 °C까지 분당 5 °C의 승온 속도로 진행하였다. 이렇게 열분해를 통해 제조된 ZrO2 분말의 결정 구조는 X선 회절 분석기(X-ray diffraction, XRD, D-Max 3, Rigaku, Tokyo, Japan)로 분석하였다. Cu-Kα 방사선을 사용하여 2θ = 10°부터 90°까지의 범위에서 회절 패턴을 측정하였고, 주 피크의 반치전폭(full width at half maximum, FWHM)과 Scherrer 식을 이용하여 결정상별로 결정립 크기를 계산하였다. 또한 HighScore Plus 소프트웨어를 사용하여 리트벨트(Rietveld) 분석을 수행함으로써 결정상의 비율과 평균 결정립 크기를 정량 분석하였다. 최종적으로 분말의 형상과 미세구조는 주사전자현미경(scanning electron microscopy, SEM, S-4300, Hitachi, Tokyo, Japan)을 이용하여 관찰하였으며, 저배율(5,000×)과 고배율(200,000×)에서 이미지를 각각 획득하였다.
3. 결과 및 고찰
3.1. ZrO2 전구체 합성 전략 및 특성
본 연구에서는 PZC 합성을 위해 Zirconium propoxide (Zr(OPr)4)와 Acrylic acid (AA)를 이용한 졸-겔 경로를 채택하였다. 일반적으로 지르코늄 알콕사이드는 반응성이 매우 높아 의도치 않은 겔화(gelation)를 제어하기 위해 킬레이트제(chelating agent)의 사용이 필수적이다. 본 연구에서는 AA를 킬레이트제로 선정하였는데, 이는 세 가지 주요 이점을 가지기 때문이다. 첫째, AA의 카복실기는 Zr 중심과 킬레이션 반응을 통해 반응성을 조절함과 동시에, 분자 자체의 산성(acidity)으로 인해 별도의 산 촉매 없이 졸-겔 반응을 개시할 수 있다. 둘째, 친수성의 카복실기와 소수성의 비닐기(vinyl group)를 모두 가져 반응물과의 상용성을 증진시킨다.29) 마지막으로, 비닐기는 후속 경화 단계에서 라디칼 연쇄 중합의 반응점으로 활용하여 가교 밀도를 극대화할 수 있다(Fig. 1).
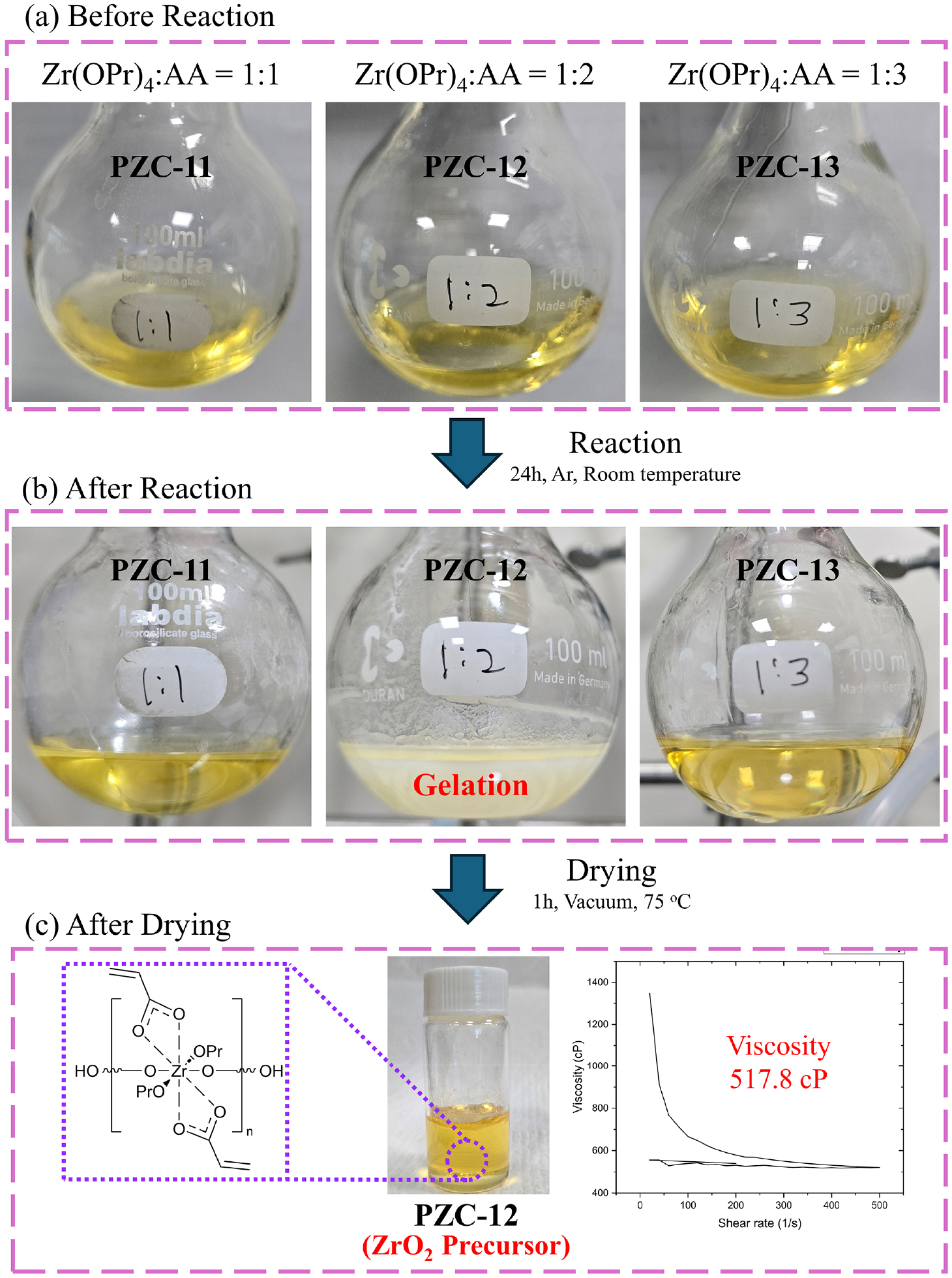
최적의 전구체 조성을 찾기 위해 Zr(OPr)4와 AA의 몰 비를 1:1 (PZC-11), 1:2 (PZC-12), 1:3 (PZC-13)으로 달리하여 상온에서 24 h 반응시킨 후 그 거동을 비교하였다. 반응 초기에는 세 조건 모두 Zr(OPr)4가 프로판올 용매 내에서 AA와 균일하게 혼합되어 투명한 황색 용액을 형성하였다[Fig. 2(a)]. 하지만 24 h 후, PZC-12 용액에서만 백탁 현상(milky white phenomenon)이 관찰되어 졸-겔 반응을 통한 겔화가 진행되었음을 확인하였다[Fig. 2(b)]. 이후 반응 부산물과 용매를 제거하기 위해 75 °C에서 1 h 동안 진공 증류를 실시한 결과, PZC-11과 PZC-13은 고체상으로 남은 반면, PZC-12는 유동성을 지닌 균일한 황색 액상 전구체로 최종 합성되었다[Fig. 2(c)].
이러한 결과는 AA의 두 가지 역할, 즉 i) 반응을 개시하는 산 촉매 역할과 ii) 반응성을 제어하는 킬레이트 역할 사이의 균형이 몰 비에 따라 결정적으로 작용했기 때문으로 해석된다. PZC-11 (1:1)의 경우, 졸-겔 반응을 개시하기에 산의 양이 불충분하여 의미 있는 고분자화가 일어나지 못했다. 반면 PZC-13 (1:3)은 반응을 개시할 산은 충분했으나, 과량의 AA가 Zr 중심에 배위하여 반응 자리(reaction site)를 지나치게 차폐함으로써 오히려 겔 네트워크를 형성할 만큼의 분자량 성장이 억제된 것으로 판단된다. 이와 달리 PZC-12 (1:2) 조건에서는 반응 개시에 충분한 산 농도를 제공함과 동시에, 적절한 수준의 킬레이션 효과로 과도한 축합 반응을 억제하여 결과적으로 액상으로 안정한 올리고머(oligomer) 형태의 전구체가 형성된 것으로 보인다.
합성된 PZC-12의 점도는 약 517.8 cP로 측정되었으며[Fig. 2(c)], 이는 다소 점성이 있으나 PIP 공정의 함침 단계에 적용하기에 충분한 수준이다. 따라서 본 연구에서는 PZC-12를 ZrO2 제조를 위한 최적 전구체로 선정하고, 이후 모든 경화 및 열분해 공정에 적용하였다.
본 연구에서 설계한 전구체는 경화 단계에서 독특한 이중 가교(dual cross-linking) 메커니즘을 통해 높은 세라믹 수율을 확보할 수 있다는 장점이 있다. 일반적인 졸-겔 전구체는 하이드록시기(-OH) 간의 축합 반응만으로 경화되는데, 이때 킬레이트제를 완전히 제거하려면 180 °C 이상의 고온이 필요하며 이 과정에서 전구체의 일부가 분해 또는 휘발되어 질량 손실을 야기한다.18) 그러나 본 연구의 PZC-12는 -OH기 축합 반응에 더하여, AIBN 개시제를 통해 AA의 비닐기 간 라디칼 연쇄 중합을 80 °C의 비교적 낮은 온도에서 유도하였다. 이러한 이중 경화 방식은 세라믹화 이전에 가교 밀도를 극대화하여 승온 과정에서의 질량 손실을 효과적으로 억제하므로, 최종 세라믹 수율을 크게 향상시키는 핵심적인 역할을 한다.
3.2. PZC-12의 분자 구조 분석
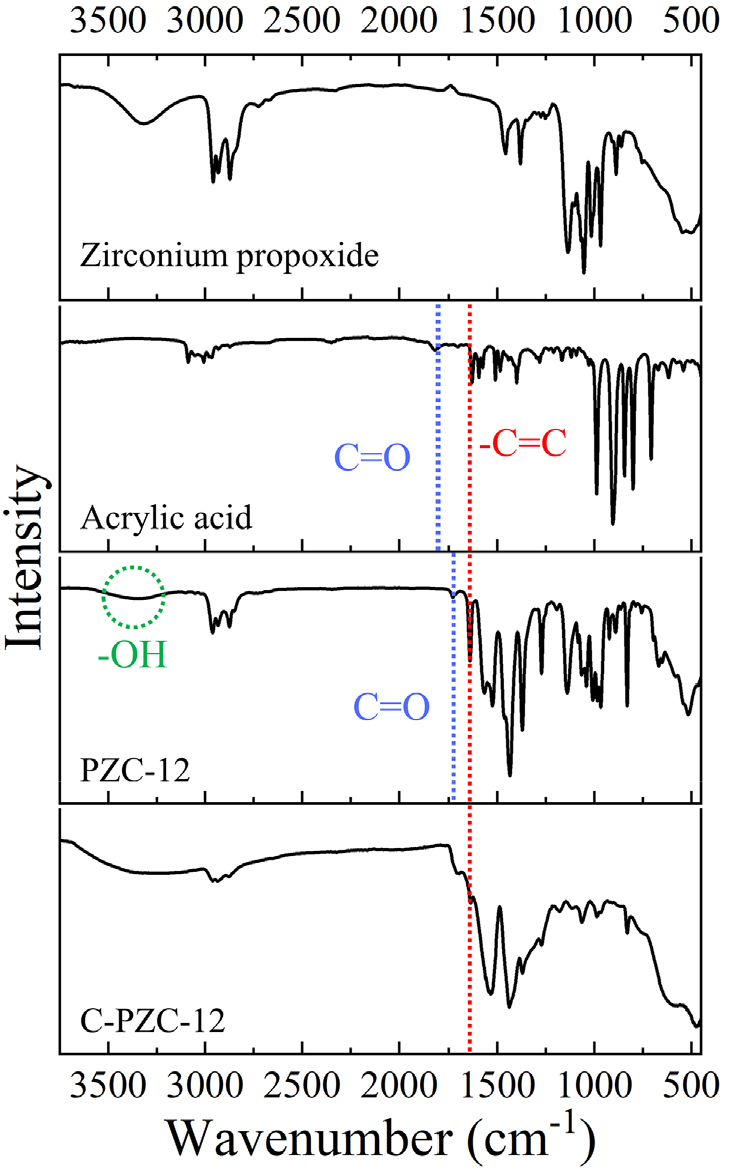
합성된 PZC-12 전구체의 분자 구조와 경화 메커니즘을 규명하기 위해 FT-IR 및 NMR 분석을 수행하였다. Fig. 3은 반응물, 액상 전구체(PZC-12), 그리고 경화된 전구체(c-PZC-12)의 FT-IR 스펙트럼을 보여준다. PZC-12 스펙트럼에서는 C-H 신축 진동(2,920, 2,861 cm-1), C-O 신축 진동(1,121 cm-1), Zr-O 결합(646 cm-1), 그리고 Zr-O-C 결합(1,548 cm-1)에 기인하는 피크들이 공통적으로 관찰되었다.30,31,32) 핵심적으로, 순수 아크릴산(AA)에서 1,764 cm-1에 나타나던 C=O 신축 진동 피크가 PZC-12에서는 1,728 cm-1로 이동(red-shift)하였는데, 이는 AA의 카복실기가 Zr 원자에 성공적으로 킬레이션(chelation)되었음을 의미한다.30) 이 결과는 AA가 Zr(OPr)4의 과도한 졸-겔 반응을 효과적으로 억제하는 킬레이트제로 작용했음을 명확히 뒷받침한다.
경화 후 c-PZC-12의 스펙트럼에서는 주목할 만한 변화가 관찰되었다. PZC-12에서 보였던 광범위한 -OH 피크(약 3,300 cm-1)와 AA의 C=C 이중 결합 피크(1,644 cm-1)가 거의 소멸한 것을 확인하였다. 이는 각각 -OH기의 축합 중합과 비닐기의 라디칼 연쇄 중합이 모두 성공적으로 진행되어, 의도했던 이중 가교(dual crosslinking) 메커니즘이 효과적으로 구현되었음을 증명하는 결과이다.33)
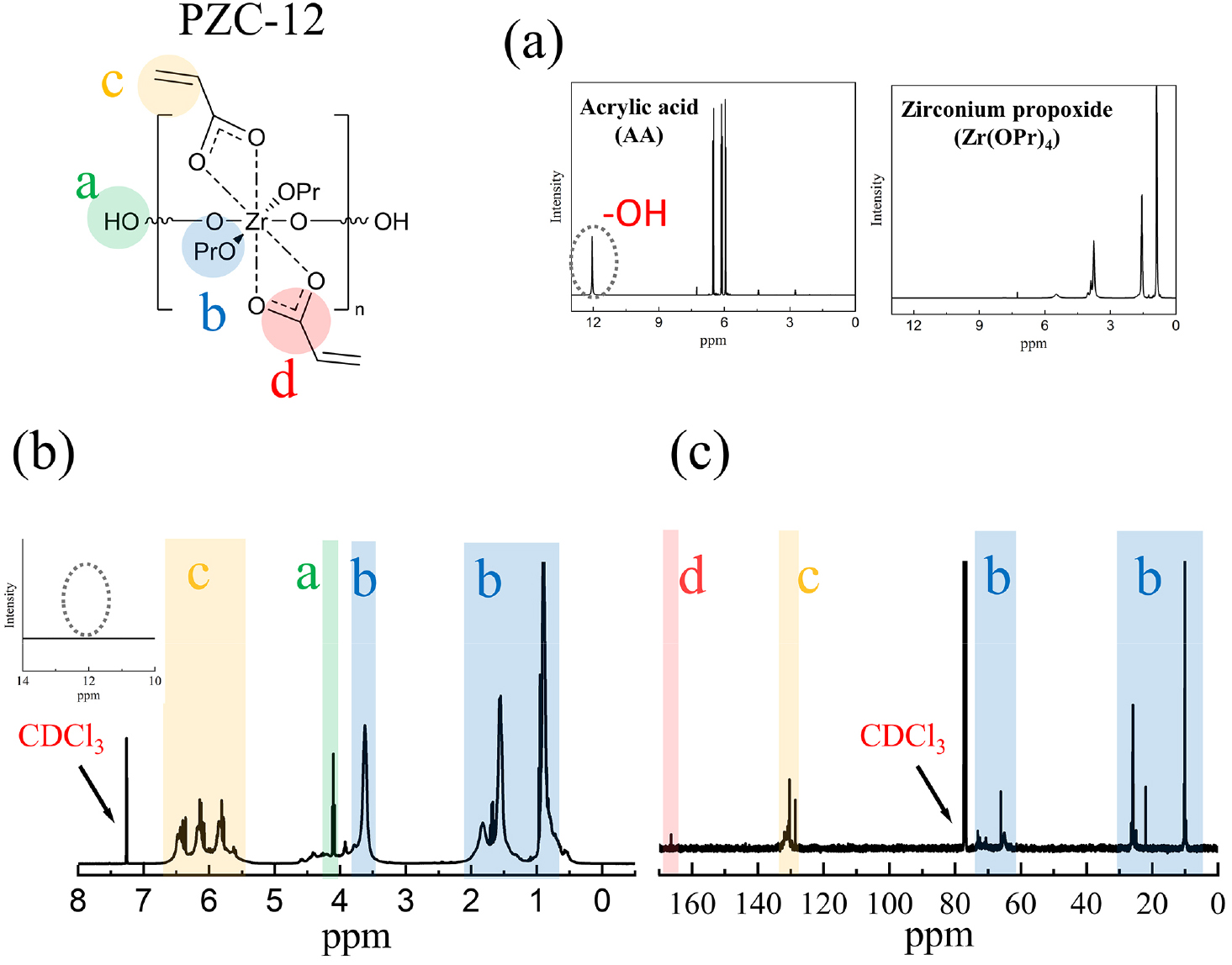
PZC-12의 분자 구조를 더욱 상세히 분석하기 위해 1H 및 13C NMR 분석을 진행하였다(Fig. 4). Fig. 4(b) PZC-12 1H-NMR 스펙트럼에서, AA의 비닐 양성자 피크(5.5-6.8 ppm)가 여전히 뚜렷하게 관찰되었다. 반면, 순수 AA에서 12 ppm 부근에 나타나던 카복실산의 -OH 양성자 피크[Fig. 4(a)]는 PZC-12에서 완전히 사라졌는데, 이는 단순 혼합물이 아닌 킬레이션 결합이 형성되었음을 명확히 보여준다. 또한, 반응물인 Zr(OPr)4의 프로폭사이드기 피크(0.5-4.0 ppm)가 PZC-12 스펙트럼에도 대부분 남아있는 것이 확인되었다. 이는 AA의 킬레이션 효과로 모든 프로폭사이드기가 반응하지 않고 일부가 잔존하도록 반응성이 적절히 제어되었음을 의미한다. 이와 함께 4.2 ppm 부근에서는 졸-겔 반응으로 생성된 말단 -OH기의 새로운 피크도 관찰되었다. 이러한 구조는 13C-NMR 스펙트럼[Fig. 4(c)]에서도 프로폭사이드기에 해당하는 피크(0-30, 65-75 ppm)가 관찰됨으로써 재차 확인되었다.
3.3. 온도에 따른 ZrO2의 결정 구조 변화
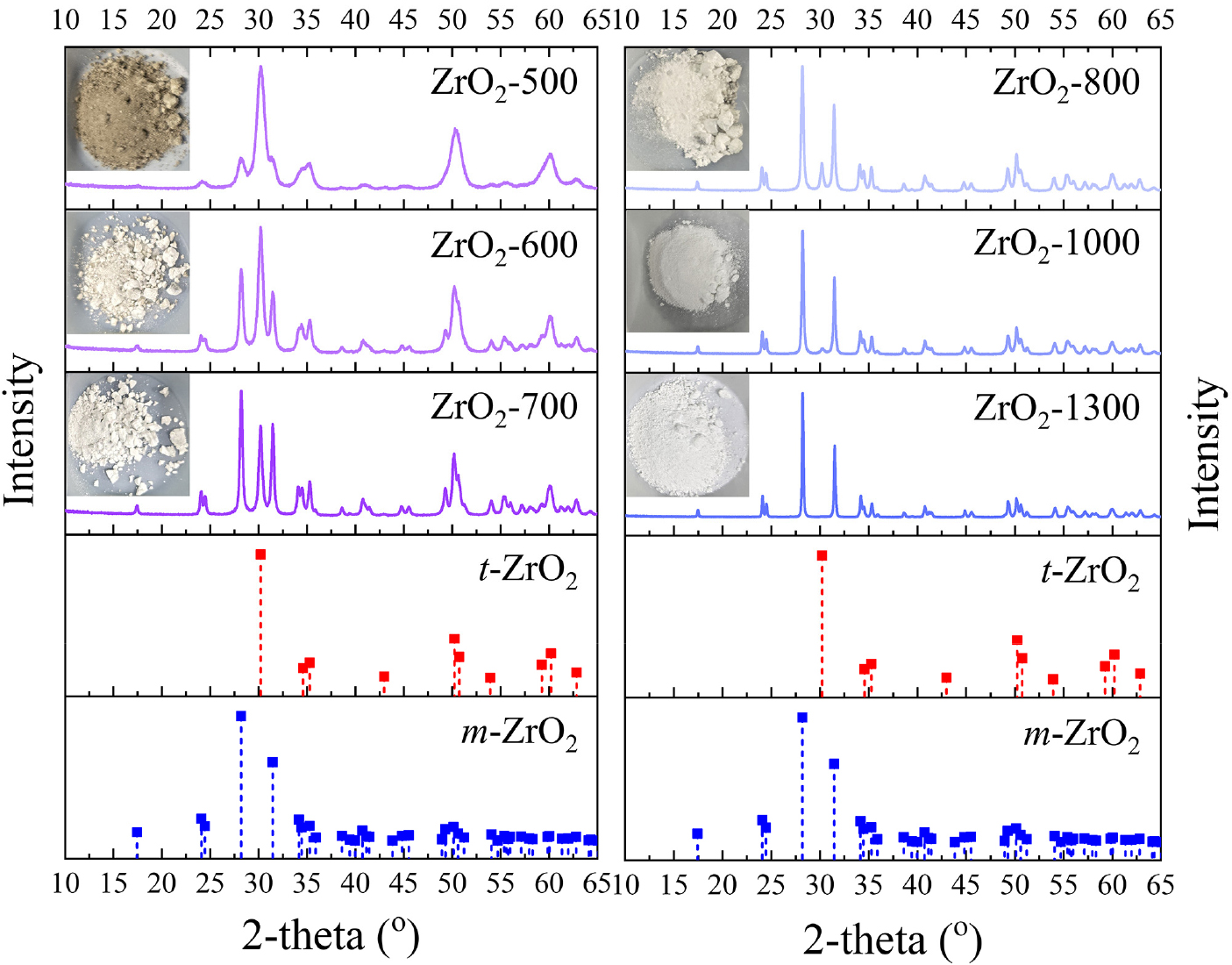
PZC-12 전구체로부터 ZrO2를 제조하기 위한 최적의 열분해 조건을 확립하고, 온도에 따른 결정 구조 변화를 분석하였다. Fig. 5는 각기 다른 온도에서 열분해하여 얻은 ZrO2 분말의 사진과 XRD 패턴을 보여준다. 500 °C에서 제조된 ZrO2-500은 잔류 탄소로 인해 어두운 회색을 띤 반면, 600 °C 이상의 온도에서는 모두 완전한 백색 분말이 얻어졌다. 이는 500 °C 조건에서는 전구체의 세라믹화가 불완전했음을 시사한다. 이러한 결과는 XRD 패턴에서도 명확히 확인되는데, ZrO2-500은 결정립 크기가 매우 작을 때 관찰되는 넓고 뭉툭한 피크를 보이는 반면, 600 °C 이상에서 제조된 시료들은 모두 날카로운 결정성 피크를 나타내어 대부분 ZrO2로 전환되었고 온도 증가에 따라 ZrO2 결정립이 성장했음을 알 수 있다.
XRD 패턴의 상세 분석 결과, 열분해 온도에 따른 뚜렷한 상변이(phase transformation)가 관찰되었다. 저온에서 합성된 ZrO2-500은 정방정계(tetragonal, t-ZrO2) 상에 해당하는 주 피크(2θ ≈ 30.1°)가 우세하게 나타났다. 그러나 소결 온도가 증가함에 따라 이 피크는 점차 감소하고, 단사정계(monoclinic, m-ZrO2) 상의 고유 피크(2θ ≈ 28.2°, 31.5°)가 강하게 발현되었다. 최종적으로 1,300 °C에서 합성된 ZrO2-1300에서는 거의 순수한 m-ZrO2 결정상만이 관찰되었다.
이러한 상변화와 결정립 크기를 정량적으로 분석하기 위해 리트벨트 분석 및 Scherrer 식을 이용하였으며, 그 결과는 Table 2에 정리하였다. 분석 결과, ZrO2-500은 약 70.4 %의 t-ZrO2와 29.6 %의 m-ZrO2로 구성되었으며, 온도가 상승함에 따라 t-ZrO2 분율은 지속적으로 감소하고 m-ZrO2 분율은 증가하여 최종적으로 ZrO2-1300에서는 m-ZrO2로 구성된 것을 확인하였다. 평균 결정립 크기 또한 ZrO2-500의 9.37 nm에서 시작하여 온도가 증가함에 따라 입성장(grain growth)으로 인해 꾸준히 증가하였고, ZrO2-1300에서는 74.07 nm에 도달하였다.
Table 2.
Crystalline phase of all ZrO2 samples and grain size calculated by Scherrer equation.
이러한 결과에서 가장 흥미로운 점은 저온에서 t-ZrO2가 준안정상으로 안정화된 것이다. 일반적으로 벌크 ZrO2는 상온에서 m-ZrO2가 열역학적으로 안정하며, 1,170 °C 이상에서만 t-ZrO2로 상변이하는 것으로 알려져 있다.8) 하지만 나노 크기 영역에서는 표면 에너지 효과로 인해 상 안정성이 달라진다. 즉, 특정 임계 크기 이하에서는 t-ZrO2의 표면 에너지가 낮아지고 m-ZrO2의 표면에너지는 증가하여 상온에서도 t-ZrO2가 안정하게 존재할 수 있다.34,35,36,37) 본 연구에서 AA를 통해 분자량이 제어된 PZC-12 전구체는 저온 열분해 시 나노미터 크기의 미세한 결정립 형성을 유도한다. 실제로 ZrO2-500과 ZrO2-600의 평균 결정립 크기는 각각 9.37 nm와 13.99 nm로, t-ZrO2 결정립을 안정화 시킬수 있는 충분히 작은 크기임을 확인하였다. 이후 소결 온도가 상승하면서 발생하는 입성장으로 인해 결정립 크기가 임계 크기를 초과하게 되면, ZrO2는 다시 벌크 상태처럼 열역학적으로 안정한 m-ZrO2로 상변이하게 된다.29,34,35,36) 결과적으로, 전구체 설계를 통한 초기 나노 결정립 형성과 후속 열처리에 의한 입성장의 조합이 ZrO2의 온도에 따른 결정상 변화를 제어하는 핵심 메커니즘임을 확인하였다.
3.4. ZrO2의 미세구조
열분해 온도에 따른 ZrO2 분말의 미세구조를 SEM으로 관찰하였으며, 그 결과를 Fig. 6에 나타내었다. 5,000배의 저배율 관찰에서는 모든 시료가 불규칙한 형태의 응집체(agglomerate) 표면 구조를 보여, 온도에 따른 거시적 형상의 유의미한 차이는 발견되지 않았다.
그러나 200,000배의 고배율 관찰에서는 뚜렷한 미세구조 변화가 확인되었다. ZrO2-500의 경우, 입자 간의 경계가 불분명하고 매우 미세한 나노 입자들이 비정질(amorphous) 상으로 덮여 있는 듯한 구조를 보였다. 이는 앞선 분석 결과와 일치하게, 500 °C의 낮은 온도에서는 세라믹화가 불완전하여 나노 결정과 비정질 세라믹스, 그리고 미반응 전구체 물질이 혼재하기 때문으로 판단된다. 반면, 완전한 세라믹화가 이루어진 ZrO2-600 이상의 시료들에서는 명확한 입자(grain)들을 관찰할 수 있었다. 특히 열분해 온도가 600 °C에서 1,300 °C로 증가함에 따라, 입자들의 크기가 눈에 띄게 커지는 현상이 관찰되었다. 이러한 SEM을 통한 직접적인 미세구조 관찰 결과는, 앞서 XRD 패턴의 Scherrer 식을 통해 계산된 결정립 크기 증가 경향과 정확히 일치하는 것으로, 온도 상승에 따른 입성장이 일어났음을 명확하게 보여준다.
3.5. PZC-12의 열적 특성 및 세라믹화 거동
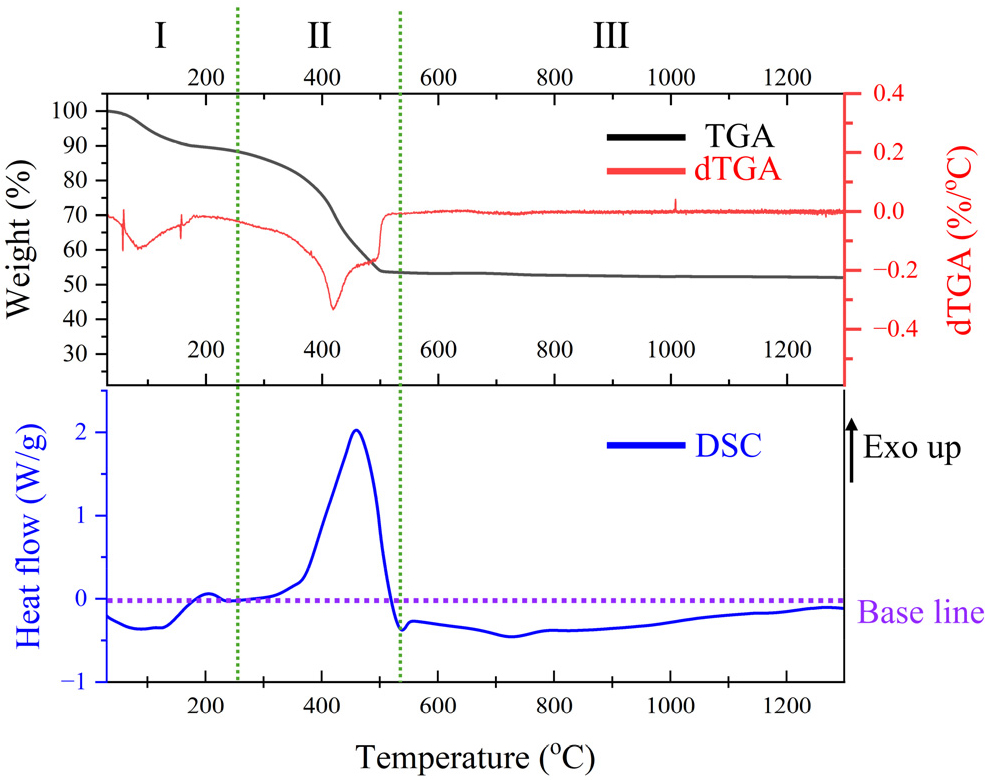
합성된 PZC-12 전구체의 열분해 거동, 세라믹화 과정 및 최종 수율을 분석하기 위해 TGA-DSC을 수행하였으며, 그 결과를 Fig. 7에 나타내었다. 분석은 실제 열분해 공정과 유사하게 공기 분위기에서 1,300 °C까지 분당 5 °C의 승온 속도로 진행하였다.
TGA 곡선은 크게 세 구간으로 나눌 수 있다. 첫 번째 구간(I, 30~250 °C)에서는 약 10 %의 질량 감소가 관찰되었으며, 이는 전구체에 잔류하는 용매, 흡착된 수분 및 미반응 AA와 같은 저분자량 물질의 휘발에 기인한다.38,39)
두 번째 구간(II, 250~530 °C)에서는 전구체의 주된 열분해가 일어난다. 약 250 °C부터 킬레이션 결합 또는 중합체 사슬에 포함된 유기 리간드(ligand)의 분해가 시작되며, 300 °C를 기점으로 급격한 질량 감소가 발생한다. 이 구간에서 가장 주목할 만한 현상은 DSC 곡선에서 관찰되는 458 °C의 강한 발열(exothermic) 피크이다. 이 피크는 비정질(amorphous) 상태의 지르코늄 산화물이 결정질인 t-ZrO2로 상전이하는 결정화(crystallization) 과정에 해당한다.38,39) 이 결정화는 약 522 °C에서 완료되는 것으로 나타났으며, 이는 500 °C에서 열분해한 ZrO2-500 시료가 불완전한 결정성을 보였던 앞선 XRD 및 SEM 분석 결과의 직접적인 원인이 낮은 열분해 온도임을 명확히 설명해준다.
세 번째 구간(III, 530~1,300 °C)에서는 열적 거동이 안정화된다. 600 °C 이후부터 1,300 °C까지의 질량 감소는 약 0.5 %에 불과하여, 대부분의 유기물이 제거되고 안정한 산화물로 전환되었음을 알 수 있다. 1,300 °C에서의 최종 잔류량은 52.7 %로, 이는 본 연구에서 개발된 PZC-12 전구체의 세라믹 수율을 의미한다. 타 전구체의 수율과 비교하기 위하여, 다양한 세라믹 전구체의 세라믹 수율을 Table 3에 제시하였다.40,41,42,43,44) PIP 공정에 직접 적용 가능한 액상 ZrO2 전구체에 대한 연구는 현재까지 거의 보고된 사례가 존재하지 않는다. 따라서 본 연구에서는 PIP용으로 개발된 전구체가 아닌, 타 용도로 보고된 고분자 기반 전구체들과의 수율 비교를 통해 상대적 성능을 검토하였다. 그럼에도 불구하고, 본 연구에서 개발한 ZrO2 전구체의 세라믹 수율은 비교적 우수한 수준을 나타내었다. 일반적으로 보고된 대부분의 전구체는 고체상으로 존재하므로, 이를 액상으로 활용하기 위해서는 별도의 용매를 첨가하여 용해 과정을 거쳐야 하며, 이러한 과정에서 실질적인 수율 저하가 불가피하다. 반면, 본 연구의 PZC-12 전구체는 용매를 포함하지 않는 저점도 액상임에도 불구하고, 높은 세라믹 수율을 확보하였다. 이는 PZC-12 가 PIP 공정 적용을 위한 액상 ZrO2 전구체로서 우수한 공정적 적합성과 높은 전환 효율을 동시에 갖추고 있음을 보여준다.
Table 3.
Ceramic Yields of reported polymer precursors for ZrO2.
| Precursor | Yield | Pyrolysis temperature | Reference |
| ZC13 | ≈ 30 % | 1,200 °C | 40) |
| YSZ precursor | ≈ 15 % | 800 °C | 41) |
| PZCS-2 | 43.9 % | 900 °C | 42) |
| PZSA | 53.5 % | 1,375 °C | 43) |
| BCZr-1100-air | 58% | 1,100 °C | 44) |
한편, 이 고온 영역의 DSC 곡선에서는 흡열 부분에 넓고 완만한 열적 변화가 관찰되는데, 이는 고온에서의 입성장 및 이에 수반되는 ZrO2의 상변태와 같은 복합적인 미세구조 변화에 의한 것으로 판단된다.
3.6. PIP 공정을 이용한 ZrB2-ZrO2 복합재 제조
합성된 PZC-12 전구체의 실제 공정 적용 가능성을 검증하기 위해, 상대밀도 55 %의 다공성 ZrB2 성형체를 이용하여 PIP 공정 기반의 ZrB2-ZrO2 복합재를 제조하였다. 공정은 Fig. 8에 나타낸 바와 같이 PZC-12 함침 후 600 °C에서 4 h 동안 열분해하는 사이클을 총 3회 반복하여 수행하였다. 열분해 온도를 600 °C로 설정한 이유는, 500 °C 이하에서는 전구체의 세라믹화가 불완전하고, 이보다 너무 높은 온도에서는 ZrB2 기지(matrix)의 과도한 산화가 우려되므로, 완전한 결정화를 이루면서도 기지의 손상을 최소화하는 최적의 조건으로 판단하였기 때문이다.
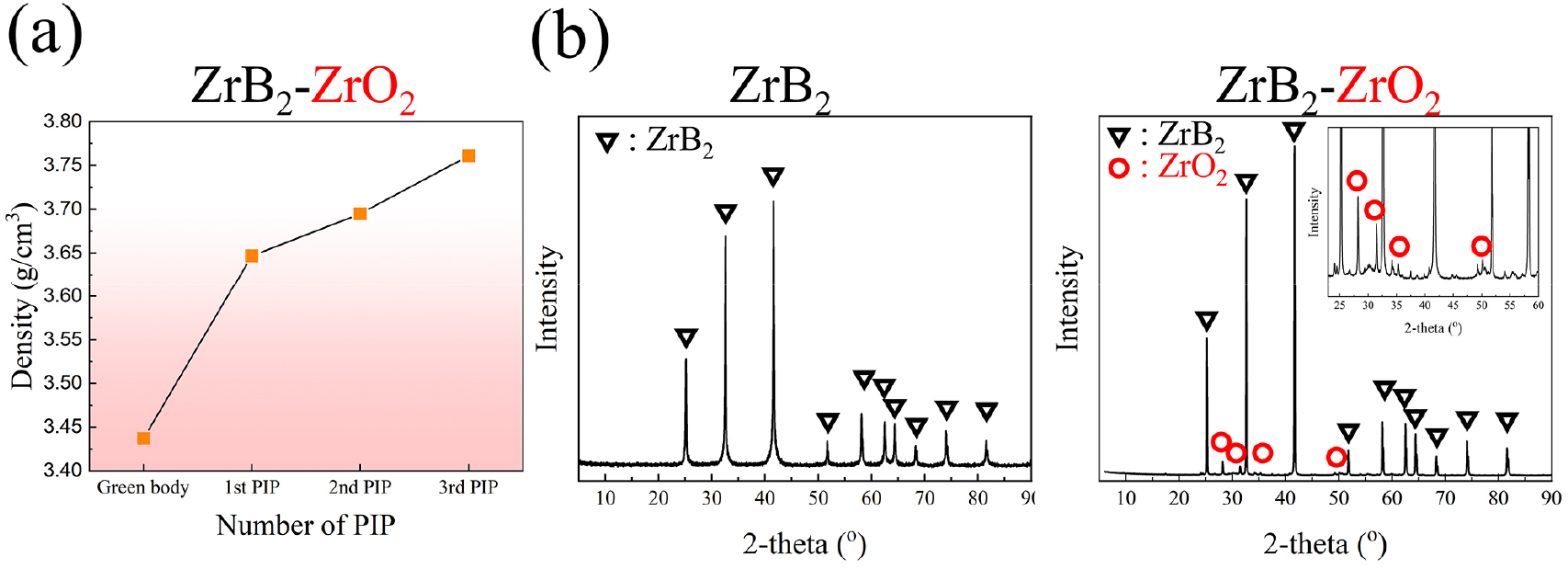
3회의 PIP 공정을 통해 ZrB2-ZrO2 복합재가 성공적으로 제조되었으며, 초기 성형체의 밀도는 3.43 g/cm3에서 3.77 g/cm3까지 유의미하게 증가하여 효과적인 치밀화(densification)가 진행되었음을 확인하였다[Fig. 9(a)]. 또한, XRD 분석을 통해 3회 PIP 공정 후 ZrB2 기지 내에 ZrO2가 성공적으로 형성되었음을 명확히 확인하였다[Fig. 8(b)]. 비교적 높은 상대밀도(약 55 %)를 가지는 ZrB2 성형체임에도 불구하고, 본 연구에서 합성된 전구체는 낮은 점도를 나타내어 용매의 첨가 없이도 안정적인 함침이 가능함을 확인하였다. PIP 공정을 단 3회 반복한 경우에도 복합재의 상대밀도는 약 63 %에 도달하였으며, PIP 횟수를 추가로 증가시킬 경우 상대밀도 80 % 이상의 고밀도 세라믹 제조가 가능할 것으로 판단된다. 이러한 결과는 본 연구에서 개발한 PZC-12 전구체가 PIP 공정에 적합한 ZrO2 기반 액상 전구체로서 우수한 공정성을 지님을 보여주며, 이를 활용하여 2성분계 세라믹 복합재의 복잡 형상 제조 및 밀도 향상이 충분히 가능함을 입증한다.
한 가지 흥미로운 점은 복합재 내에서 형성된 ZrO2의 결정상이다. 앞선 분말 실험에서는 600 °C 열분해 시 t-ZrO2와 m-ZrO2가 약 5:5 비율로 혼재하였으나, ZrB2 기지 내에서 형성된 ZrO2는 대부분 m-ZrO2 상으로 존재하였다. 이는 ZrB2 기지 내의 ZrB2 성형체가 표면산화로 인하여 생성된 ZrO2 때문으로 파악된다. ZrB2가 공기중에 노출되었을시 상온에서도 표면 산화로인한 얇은 ZrO2층이 생성되며 이 ZrO2 층이 전구체 열분해시의 비정질 ZrO2의 결정화 및 입성장의 핵으로 작용하여 600 °C에서 열분해시에도 순수한 전구체 열분해 대비 프리폼 내부에서 형성된 ZrO2의 결정 크기를 성장시킨 것으로 판단된다.45) 그 결과 결정립 크기가 t-ZrO2 상을 안정화시키는 임계 크기 이상으로 성장하여 열역학적으로 안정한 m-ZrO2로 상변태가 일어난 것으로 추정된다[Fig. 9(b)].
4. 결 론
본 연구에서는 zirconium propoxide와 acrylic acid를 활용한 sol-gel 반응을 통해 이중 가교를 활용 가능한 새로운 저점도, 고수율의 액상 지르코니아 전구체(PZC-12)를 합성하고, 이를 기반으로 ZrO2 및 ZrB2-ZrO2 복합재를 제조하여 전구체의 특성과 PIP 공정 적용 가능성을 검토하였다.
지르코니아 전구체 합성 과정에서 Zr:AA 몰비에 따른 거동을 비교한 결과, 1:2 조건(PZC-12)에서만 안정적인 액상 전구체가 형성되었다. 이는 acrylic acid의 산성에 의한 반응 개시 효과와 카복실레이트 킬레이션에 의한 반응 제어 효과가 균형을 이루었기 때문으로 해석된다. 합성된 PZC-12는 약 517.8 cP의 점도를 나타내어 PIP 공정에서 충분한 함침성을 확보하였으며, 전구체로서 최적 조성임을 확인하였다. 합성된 PZC-12의 분자 구조를 FT-IR과 NMR로 분석한 결과, acrylic acid의 카복실기가 Zr과 킬레이션을 형성하고, 비닐기가 전구체 내에 잔존함을 확인하였다. 특히 경화 과정에서 AIBN을 개시제로 도입하여 vinyl기의 연쇄중합을 유도함으로써, -OH 축합 반응과 더불어 이중 가교(dual crosslinking) 메커니즘이 구현된 것을 FT-IR로 확인하였다. 이러한 이중 경화 전략은 열분해 과정에서 전구체 질량 손실을 억제하여 최종 세라믹 수율(약 52.7 %)을 확보한 것을 TGA 분석을 통해 확인하였다.
온도별 열분해를 통해 제조된 ZrO2의 결정 구조와 미세구조를 분석한 결과, 500 °C에서는 비정질 상이 일부 존재하였으나, 600 °C 이상에서는 완전한 세라믹으로의 전환 및 결정화 진행을 확인하였다. 또한 승온에 따라 평균 결정립 크기가 점진적으로 증가하였고, 이에 따라 t-ZrO2가 감소하고 m-ZrO2가 증가하는 전형적인 상전이 거동이 관찰되었다. 이는 나노 크기 영역에서는 t-ZrO2가 상대적으로 안정하나, 결정립 성장이 임계 크기를 초과하면서 m-ZrO2로 전환된다는 기존 보고와 일치하였다.
또한 합성한 전구체의 PIP 적용성을 검증하기 위하여 ZrB2 성형체에 PZC-12를 침투・경화・열분해하여 ZrB2-ZrO2 복합재를 제조하였다. 3회의 PIP 사이클을 거친 복합재는 밀도가 3.43 g/cm3에서 3.77 g/cm3로 증가하였고, XRD 분석 결과 ZrB2 기지상 내에 m-ZrO2 상을 검출하였고 이를 통해 ZrB2-ZrO2 복합재를 성공적으로 제조한 것을 확인하였다. 이러한 결과들로부터 PZC-12가 액상 전구체로서 우수한 함침성 및 세라믹화 능력을 보유하며, 실질적인 PIP 공정에 적용 가능한 전구체임을 입증하였다.
종합하면, 본 연구에서 개발한 PZC-12 전구체는 i) 용매 사용 하지 않고 적절한 액상 유지 안정성과 점도, ii) 이중 가교에 의한 수율 향상, iii) ZrO2 나노결정 제조 가능성을 충족하고 액상이기에 PIP 기반 복합재 제조에 적합한 것으로 확인되었다. 이는 기존 zirconium alkoxide 기반 전구체의 한계를 극복할 수 있는 전략으로, 향후 초고온 세라믹 복합재의 고수율・고신뢰성 제조에 효과적으로 기여할 수 있을 것으로 기대된다.