1. 서 론
알루미나는 세라믹 원료 중에서 내마모성, 내식성, 열 적 안정성, 전기절연성 및 비교적 높은 열전도율(약 30 Wm−1K−1)등과 같은 우수한 물리적 특성이 탁월하기 때 문에 내마모제, 스파크 플러그, 연마제, 촉매담체, 절연 애자, 수지의 필러 등 여러 산업분야에 광범위하게 사 용되고 있다.1,2)
알루미나는 소성온도가 높아짐에 따라 γ-, δ-, θ-, α- Al2O3로 상전이가 일어나며, 이러한 상전이 과정에서 표 면적 변화는 급격하게 수반되는데, γ상에서 α상으로 갈 수록 비표면적은 급격하게 감소한다. 따라서 용도별로 적 절하게 상이 조절된 알루미나 제조기술이 필요하다.3,4) 일 반적인 알루미나 제조법으로는 졸-겔(sol-gel)법, 수열(hydrothermal) 법, 균일침전(co-precipitation)법, 기계적 밀링 (mechanical milling), 증기상 반응(vapor-phase reaction) 법, 그리고 화염을 이용하는 연소(combustion)법 등 다양 한 방법이 있다.5,6) 이 중에서 황산알루미늄암모늄(AlNH4 (SO4)2)을 이용한 열분해법은 정제 비용이 많이 들고, 부 산물로 발생하는 NH3와 SO3 가스를 제거해야 하는 단 점을 가지고 있지만 열분해시 발포성을 갖고 있기 때문 에 매우 작은 입자가 응집된 형상의 알루미나를 제조할 수 있는 장점이 있다.7) 그러나 입자의 크기가 나노화 될 수록 입자의 표면에너지가 증가하여 분산을 저해하는 입 자 간의 응집(agglomeration)을 일으키게 된다.8) 따라서 안정한 콜로이드 나노졸의 제조는 일반적으로 높은 에 너지를 갖는 습식 비드 밀링의 사용이 요구된다.9-11)
Peukert 등은 응집은 입자 간 정전기적(electrostatic) 상 호작용, 입체장애(steric hindrance) 또는 정전기적-입체장 애(electro-steric hindrance)등의 입자 간 반발력에 의해 감소시킬 수 있으며,12) Kiyoshi 등은 나노 분산졸의 안 정성 향상을 위해 입자간 정전기적 반발력의 활용, 계 면활성제를 사용한 분산매와의 친화성 향상, 입자 자체 의 표면개질 등을 제시하였으며, 입자의 등전점 부근에 서의 입자응집을 방지할 목적으로 분산매체의 이온강도, pH를 제어하는 것이 중요하다고 보고하였다.13) 특히 실 란 커플링제를 이용한 입자의 표면개질은 유·무기하이 브리드 소재로의 적용 시 혼화성을 극대화시키며, Jiang 등은 에폭시 수지에 α-Al2O3를 필러로 적용하였을 때 향 상된 특성에 대해 논의한 바 있다.14)
본 연구에서는 나노입자 제조에 용이한 황산알루미늄 암모늄 열분해법을 통해 비정질을 포함하는 γ(amor + γ로 축약하여 표기) 및 α 상의 Al2O3를 제조하였다. 습식 비 드 밀링을 통해 비드 크기 및 배합비, 밀링시간, 산 첨 가제의 종류와 양에 따른 분산 영향을 관찰하였다. 산 첨가제의 종류에 따라 분산된 Al2O3 졸은 농축하여 분 산 안정성을 관찰하였고, 제조된 Al2O3 나노졸은 실란 커 플링제로 표면개질하여 표면에 흡착된 양과 표면 특성 을 관찰하였다. 또한, 유·무기하이브리드 코팅제로 적용 하기 전 단계 과정인 NMP(N-Methyl-2-pyrrolidone) 용매 하에서 실란 표면개질된 amor + γ 및 α 상의 Al2O3의 분 산 특성을 관찰하였다.
2. 실험 방법
2.1 Al2O3 분말 제조
본 연구에서는 출발원료로 사용된 황산알루미늄암모늄 (암모늄명반, AlNH4(SO4)2, (주)에이치엠알)을 10 °C/min 의 승온 속도로 1000 °C에서 3시간 또는 1200 °C에서 1 시간 동안 산소분위기로 각각 하소하여 amor + γ상과 α 상의 Al2O3를 제조하였다.
2.2 Al2O3 나노졸 제조
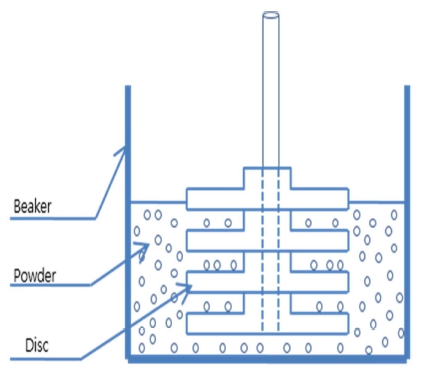
균일한 입도분포를 갖는 알루미나 분산졸 제조를 위해 Scheme 1과 같이 직경 70 mm의 알루미나 디스크가 장 착된 고속의 배치식 비드밀(Alesco)을 사용하여 응집된 입자를 분리하였다. 밀링은 무수에탄올(대정화금, 99.9 %) 을 용매로 사용하고 직경 0.1, 0.3 mm의 지르코니아 비 드(쎄노텍(주))를 사용하였으며, Al2O3 분말과 용매, 비드 의 양 등의 밀링 조건을 Table 1과 같이 진행하였다. 또 한 분산 특성을 향상시키기 위한 산 첨가제로 질산(대 정화금, 60 %)을 1~2 %, 아세트산(J.T.Baker, 99.7 %)을 1~6 wt% 사용하여 Al2O3 나노졸을 제조하였다.
2.3 Al2O3 나노졸의 표면개질
에탄올 용매하에서 분산된 Al2O3 나노졸의 표면에 소 수성의 APTMS(N-phenyl aminopropyltrimethoxysilane, Sigma-Aldrich, 99 %)가 도입된 Al2O3로 표면개질하기 위해 환류냉각관을 부착시킨 삼구 플라스크에 고형분 함 량 5 wt%의 Al2O3 분산졸을 옮기고, 자일렌(대정화금, 80 %) 400 ml를 첨가하였다. 그 다음 APTMS의 첨가량 은 아래 식15) 과 같이 Al2O3의 비표면적과 APTMS의 최 소 피복면적 의해 계산되었다.
이 반응물은 120 °C까지 승온시켜 에탄올을 제거 후 6 시간 동안 교반하면서 반응시켰다. 반응이 끝난 후 10000 rpm에서 자일렌을 넣고 원심분리시키는 과정을 3~4회 반 복하여 미반응물을 제거하였다. 세척이 끝난 Al2O3는 120 °C에서 12시간 동안 진공오븐에서 건조시켰다. 유·무기하 이브리드 코팅제로 적용하기 위한 전단계로 NMP(대정 화금, 99 %)용매하에서 분산하기 위해 회전식 감압증발 기(Rotary-evaporator, Heidolp)를 이용해 용매치환하였다.
2.4 특성평가
Al2O3의 결정상은 X-ray diffraction(XRD, Rigaku)를 통해 확인하였고, Sherrer’s equation에 의해 결정자 크 기를 계산하였다. 제조된 Al2O3의 성분 분석을 위해 Inductively coupled plasma optical emission spectroscopy (ICP-OES, Perkin Elmer, OPTIMA 5300DV)로 조성을 확인하였으며, 입자의 형상 및 크기는 Field emission scanning electron microscope(FE-SEM, JEOL)을 사용하 여 관찰하였다. 입자의 평균 입경 및 분포도를 관찰하 기 위해 동적 광산란(Dynamic Light Scattering, ELS-Z, Otsuka Electronics)방식의 장비를 사용하여 측정하였다. 입자의 비표면적은 180 °C에서 12시간 전처리 후 비표면 적 측정기(Specific Surface Area analyzer, Tristar3000, Micromeritics)를 사용하여 BET법으로 측정하였다. 표면 개질 전, 후에 따른 입자 표면에 흡착된 실란의 함량변 화를(Thermo Gravimetric Analyzer, Mettler Toledo STARe System)를 통해 분석되었다. 분석방법은 Air 분 위기에서 승온 속도 5 °C/min으로 25~1000 °C 범위에서 백분율로 환산하여 함량변화를 관찰하였다. 또한 표면개 질에 따른 입자의 표면특성을 Fourier transform infrared (FT-IR, Agilent) 스펙트럼 분석을 통해 확인하였다.
3. 결 과
3.1 황산알루미늄암모늄으로부터 열분해법에 의한 Al2O3 분말 제조
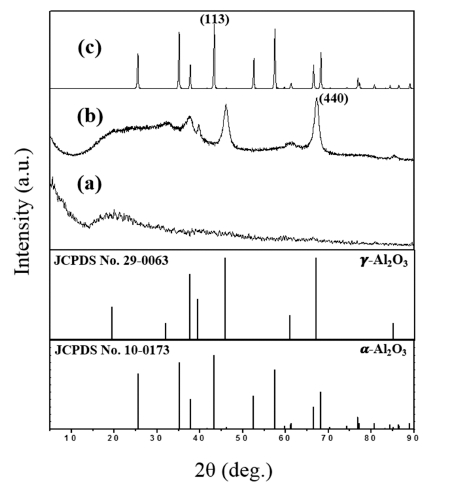
황산알루미늄암모늄(AlNH4(SO4)2)으로부터 하소온도에 따라 생성된 Al2O3의 X-ray 회절 분석 결과를 Fig. 1에 나타내었다. Fig. 1(a)는 하소 전 황산알루미늄암모늄은 비정질 구조를 나타내며, Fig. 1(b)는 황산알루미늄암모늄 을 1000 °C에서 하소한 경우 비정질이 포함된 γ상(amor + γ) Al2O3로서 비정질을 제외한 관찰된 회절패턴은 Cubic 결정상 구조(JCPDS No.29-0063)를 갖는 γ-Al2O3 피크와 일치하였다. Fig. 1(c)는 1200 °C에서 하소한 경우 Al2O3 의 최종상인 α-Al2O3 (JCPDS No.10-0173)의 Hexagonal 결정상 구조를 갖는 피크로 정확히 일치하는 것이 확인 되었다. 일반적으로 α-Al2O3로 상전이가 일어나는 동안 일부 남아있는 비정질상에 의해 비표면적이 감소하고, 결 정의 크기가 커진다고 알려져 있다. XRD 패턴으로부터 amor + γ-Al2O3 의 hkl (440)면과, α-Al2O3 hkl(113)면의 회절 피크를 Sherrer’s equation에 의해 1차 결정립 크기 를 계산한 결과 amor + γ-Al2O3는 분말 중에 γ-Al2O3 부 분이 10 nm, α-Al2O3는 34 nm로 확인되었으며, 질소 흡· 탈착에 의한 비표면적은 amor + γ-Al2O3는 92.1 m2/g, α- Al2O3는 9.8 m2/g의 값을 나타내었다.
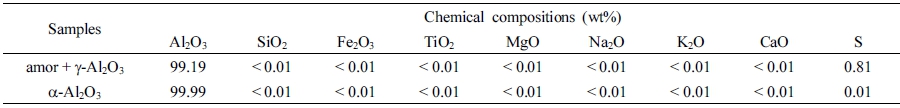
제조된 알루미나의 정확한 조성을 파악하기 위해 ICPOES 분석을 실시하였으며, Table 2에 결과를 나타내었 다. 99.19 % 순도를 갖는 amor + γ-Al2O3는 불순물로 황 이 0.81 %로 검출되었으며, α-Al2O3는 99.99 %의 순도로 불순물 없이 제조된 것을 확인할 수 있었다.
Fig. 2는 황산알루미늄암모늄으로부터 제조된 amor + γ- Al2O3와 α-Al2O3의 FE-SEM 이미지이다. 제조된 알루미 나의 1차 결정립 크기는 약 10~30 nm의 크기를 보였지 만 FE-SEM으로 관찰하였을 때 (a) amor + γ-Al2O3는 약 100 nm이하, (b) α-Al2O3는 약 300~400 nm 이하로 작 은 입자들이 응집된 형태로 관찰되었다. 이러한 응집 무 기산화물 입자는 유·무기하이브리드 코팅제로 적용 시 유 기 고분자 내에서 분산이 되지 않고 응집된 상태로 남아 물성을 저하시키는 원인이 될 수 있으므로 밀링에 의 한 응집된 입자의 분산이 필요함을 알 수 있다.
3.2 비수계 용매하에서의 분산인자에 따른 Al2O3 나 노졸 제조
분산졸 제조에서 중요한 인자는 비드의 크기 및 비드 의 배합비, 분산매체의 속도 등의 물리적 인자와, 입자 가 분산되면 입자가 재응집되는 것을 방지해야 하므로 이를 위해 입자 표면을 분산제에 의해 흡착시켜 입자 간 인력을 약화시키는 화학적 인자가 있다. 이러한 인자들 은 입자의 분산거동에 큰 영향을 주고 있다.
여러 인자 중 물리적 인자에 대한 영향을 확인하기 위 해 Fig. 3에서와 같이 amor + γ-Al2O3를 사용하여 비드 크기에 따른 밀링을 통해 제조된 amor + γ-Al2O3 슬러리 또는 졸의 입도분포를 관찰하였다. 0.1 mm, 0.3 mm 크 기의 지르코니아 비드를 각각 사용하거나 1:1로 혼합하 여 사용하였으며, 질산을 알루미나 입자 대비 1 wt% 첨 가하고, 밀링 시간은 3시간으로 동일하게 진행하였다. 0.3 mm 비드를 사용하여 밀링한 경우 평균입경(Davg)은 1.6 μm, 최대입경(Dmax)은 22.8 μm를 지닌 슬러리로 분쇄 및 분산되었다. 반면에 0.1 mm 비드를 사용하여 밀링한 경 우 평균입경은 0.2 μm, 최대입경은 7.7 μm로 입도가 상 대적으로 낮아지는 것을 보인다. 한편 0.1 mm의 비드는 입자와 충돌할 수 있는 경우의 수가 낮고 입자와 접촉 하는 면적이 0.3 mm 비드에 비해 낮기 때문에 보다 효 과적인 분산을 위해 0.1 mm 비드와 0.3 mm 비드를 1:1 로 혼합하여 밀링을 진행하였다. 이 경우 평균입도는 0.07 μm, 최대입경은 0.13 μm로 급격히 낮아지면서 단일 비드를 사용한 것 보다 분쇄 및 분산에 시너지 효과가 나타남을 알 수 있었다.
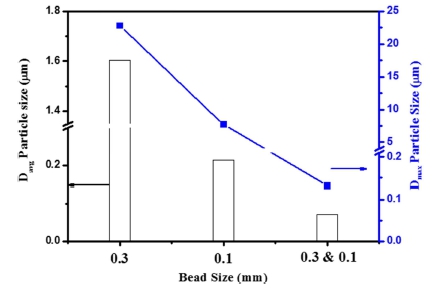
Fig. 3
Davg and Dmax particle size of amor + γ-Al2O3 slurry or sol prepared by the variation of bead size under ethanol solvent.
Fig. 4는 밀링 시간에 따른 amor + γ-Al2O3의 입도분포 를 나타낸 그래프이다. 비드 크기는 Fig. 3의 결과를 토 대로 0.1 mm, 0.3 mm 크기의 비드를 1:1로 혼합하여 사 용하였고, 질산을 알루미나 입자 대비 1 wt% 첨가하여 입도변화를 관찰하였다. 밀링 전 입자는 응집된 입도 분 포를 나타내었다. 밀링 1시간부터 응집된 입자가 점차 감 소하면서 3시간부터 5시간까지 응집된 입자 없이 70 nm 이하의 비교적 좁은 입도분포를 가지는 것을 알 수 있 었다. 여기서 결과가 명시되지 않았으나 4, 5시간 밀링 된 졸의 평균입도가 1 ~ 2 nm로 극소한 차이를 보이므로 밀링을 4시간으로 고정하여 진행하였다.
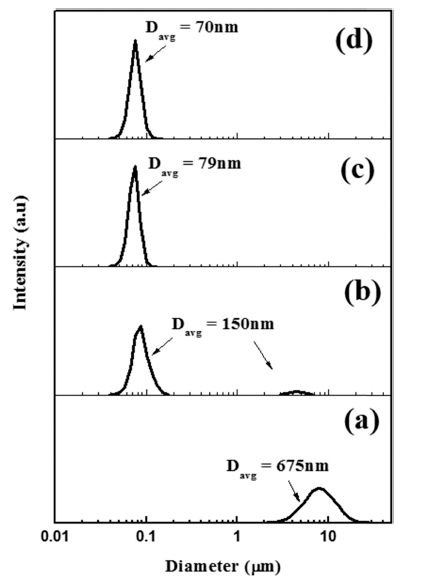
Fig. 4
Particle size distribution of amor + γ-Al2O3 sol prepared by the variation of milling time for (a) 0 h, (b) 1 h, (c) 3 h and (d) 5 h under ethanol solvent.
화학적 요인에 의한 분산성을 관찰하기 위해 질산과 아 세트산의 첨가량에 따라 변화하는 입도 분포를 Fig. 5 에 나타내었다. 밀링조건은 0.1 mm, 0.3 mm 크기의 지 르코니아 비드를 1:1로 혼합하여 사용하였고, 질산을 1~2 wt%, 아세트산을 1~6 wt%로 첨가하여 입도 변화를 관 찰하였다. Fig. 5(A)와 같이 질산을 1.5 wt% 첨가한 경 우 평균입경은 67 nm이고, Fig. 5(B)와 같이 아세트산을 4 wt% 첨가한 경우 평균입경은 68 nm로 가장 낮은 입 도의 나노졸이 제조되는 것을 확인되었다. 이는 질산과 아세트산의 첨가에 의해 pH 변화와 함께 Al2O3 입자 표 면에 H+ 양이온이 증가하면서 제타전위값이 증가하게 된 다. 이로 인해 입자간의 정전기적 반발력을 줄 수 있다.
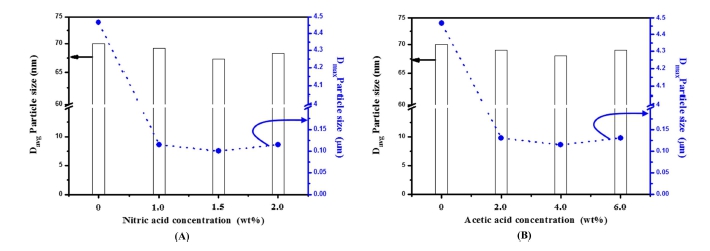
Fig. 5
Davg and Dmax particle size of amor + γ-Al2O3 sol dispersed by the added concentration of (A) nitric acid and (B) acetic acid under ethanol solvent.
분산 졸의 안정성을 비교하기 위해 Fig. 6과 같이 점 도를 측정하였다. 초기 5 wt% 농도에서 산을 첨가하지 않은 졸의 점도가 가장 높았으며, 질산과 아세트산을 첨 가한 경우 큰 차이가 나지 않았다. 그러나 10 wt% 농도 로 농축하였을 때 첨가되지 않은 졸은 겔화되었으며, 아 세트산을 첨가한 졸에 비해 질산이 첨가된 졸은 점도가 약 2.3배 증가하였다. 또한 15 wt%로 농축시킨 경우 아 세트산이 첨가된 졸은 변화가 적었으며, 질산이 첨가된 졸은 겔화되었다. 이는 아세트산이 첨가되었을 때 Fig. 5에서 언급한 바와 같이 양이온과 음이온에 의한 정전 기적-입체장애에 의한 반발력의 시너지 효과에 기인된 것 으로 보인다.
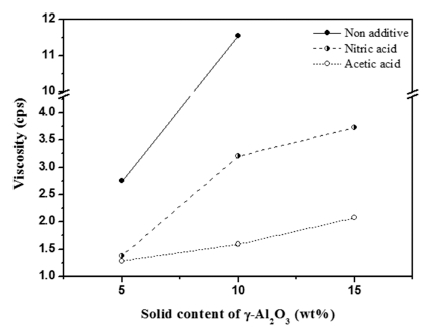
Fig. 6
Viscosity graphs of the amor + γ-Al2O3 sols prepared by acid additives with increasing the solid content.
위 결과로부터 도출된 amor + γ-Al2O3 졸의 최적화된 조건을 α-Al2O3 나노졸에 적용한 밀링 전후의 입도 분 포를 Fig. 7에 나타내었다. 밀링 전의 평균입도 약 608 nm에 비하여 밀링 후에는 약 70 nm의 좁은 입도 분포 를 갖는 것을 확인하였다.
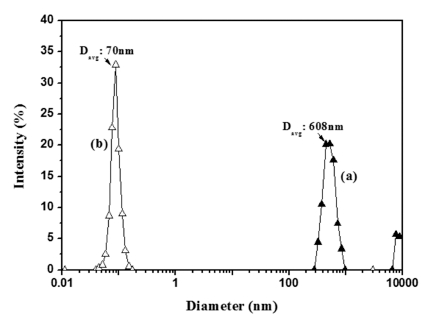
Fig. 7
Particle size distribution of α-Al2O3 slurry or sol obtained (a) before and (b) after milling under ethanol solvent.
최적화 조건에서 제조된 amor + γ-Al2O3과 α-Al2O3 분 산졸의 FE-SEM 이미지를 Fig. 8에 나타내었으며, Fig. 8(a)의 amor + γ-Al2O3는 30 nm 이하의 입자들이 대부분 이며, 일부 60 nm 이하의 큰 입자가 관찰된다. Fig. 8(b) 의 α-Al2O3는 50 nm 이하의 입자들이 대부분이며, 일부 100 nm 이하의 큰 입자가 관찰된다.
밀링에 의해 에탄올 용매하에서 분산된 Al2O3 나노졸 은 실란 표면개질을 통해 비수계용매인 NMP하에서 분 산하기 위해 사용되었다.
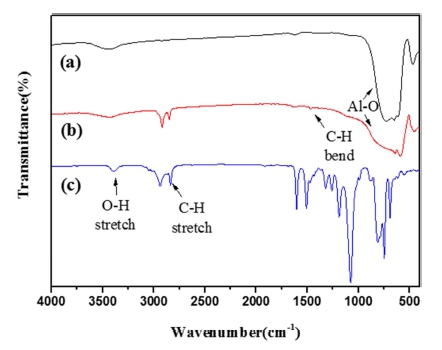
APTMS 실란으로 표면개질된 α-Al2O3 입자 표면의 실 란화 반응을 확인하기 위한 FT-IR 스펙트럼을 Fig. 9에 나타내었다. 500 cm−1 부근과 1000 cm−1 부근에서 나타난 피크는 Al-O 결합의 피크이며 3400 cm−1 부근에서 나타 난 피크는 Al-OH 피크이다. 표면개질을 처리한 경우에서 나타난 2800 cm−1 부근의 피크는 APTMS에 의한 C-H stretching에 의한 피크로 뚜렷하게 나타났으며 Al2O3 표 면에 APTMS의 흡착에 따라 3400 cm−1 부근의 OH피크 가 점차 감소함을 알 수 있었다.
Fig. 10은 표면개질된 Al2O3 표면에 흡착된 실란의 양 을 TGA로 분석한 결과를 나타내며, 표면에 흡착된 수 분을 제외한 200~600°C에서의 열감량을 관찰하였다. Fig. 10(A)는 표면개질 전후의 amor + γ-Al2O3는 각각 5.39 %, 0.84 %로 약 4.55 %의 감량을 보였고, Fig. 10(B)는 표 면개질 전후 α-Al2O3는 각각 3.00 %, 0.40 %로 약 2.6 %의 감량으로 amor + γ-Al2O3보다 α-Al2O3가 표면에 흡 착된 실란의 양이 많은 것으로 나타났다. 이는 amor + γ- Al2O3의 경우 α-Al2O3보다 낮은 온도에서 제조되어 입 자의 결정성의 차이로 입자 표면에 드러난 –OH group 의 수가 많이 남아있고, 상대적으로 단일 입자의 크기가 작고, 비표면적이 크기 때문에 표면에 흡착된 양이 다 르게 나타난 것으로 보인다. 그러므로 입자 자체의 크기 와 표면특성에 의해 표면개질 특성이 다르게 나타나고, 이 는 실란 표면개질에서 직접적인 영향을 주고 있다.
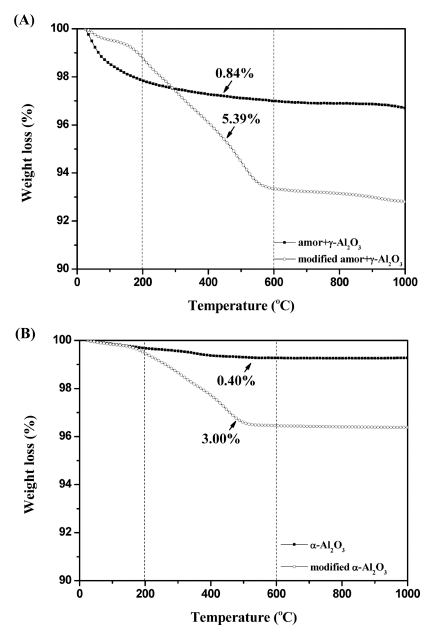
Fig. 10
TGA curves of (A) amor + γ-Al2O3 and (B) α-Al2O3 treated with or without silane modification.
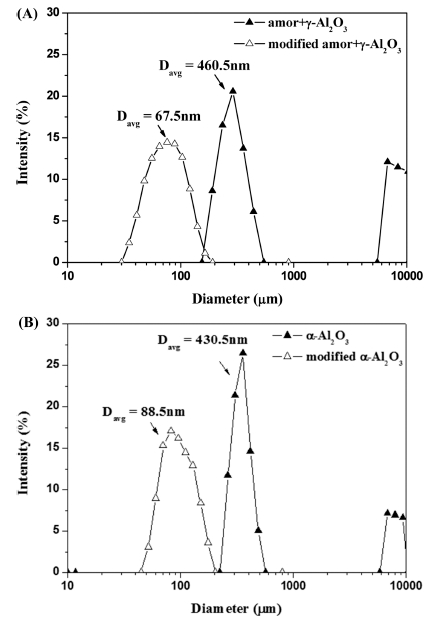
Fig. 11은 표면개질 전후의 amor+ γ -Al2O3와 α-Al2O3 를 유·무기하이브리드 소재로 적용하기 위한 전 단계 과 정으로 NMP상으로 용매치환한 후의 입도분포를 보여주 고 있다. NMP 용매하에서 표면개질 전 amor + γ-Al2O3 와 α-Al2O3는 약 ~450 nm로 입자 간 응집이 발생하였 으나, 표면개질 후에는 각각 약 67 nm와 89 nm로 입자 간 응집 없이 비교적 안정한 입도 분포를 나타내었다. 차후 본 연구를 토대로 절연 및 열전도도가 향상되는 유 ·무기하이브리드 코팅제 제조를 위해 α-Al2O3 입자 자체 의 표면특성과 실란에 의한 표면개질 정도에 따라 변화 하는 유·무기 간 계면에서의 상관성 및 특성분석에 관 한 추가적인 연구를 진행할 예정이다.
4. 결 론
본 연구에서는 비수계 용매인 에탄올과 NMP 용매하 에서 분산특성이 최적화된 amor + γ-Al2O3와 α-Al2O3 나 노졸을 제조하였다. 나노입자 제조가 용이한 황산알루미 늄암모늄의 열분해법을 이용하여 amor + γ-Al2O3와 α- Al2O3 분말을 제조한 후, 비드밀링하에서 분산인자로 밀 링시간, 비드크기 및 비드배합비, 산 첨가제의 종류 및 양에 따른 분산특성을 연구하였다. 최적 밀링조건은 0.1 mm 비드와 0.3 mm 비드를 1:1로 혼합, 밀링시간 4시간, 질산 1.5 wt% 또는 아세트산 4 wt% 첨가 시에 amor + γ-Al2O3와 α-Al2O3 나노졸의 평균 입도가 약 68 nm로 분산특성이 가장 우수했다. 특히, 질산과 아세트산을 첨 가했을 때 평균 입도 변화는 유사한 결과를 나타냈으나, 아세트산이 첨가된 분산졸은 고농도에서 보다 안정하였 다. 이는 질산 첨가 시 Al2O3 입자간의 정전기적 반발 력에 의한 분산 역할보다, 아세트산 첨가에 의한 입자 간 정전기적 입체장애 반발력으로 인한 시너지 효과에 기인하는 것으로 보인다. 제조된 Al2O3 나노졸은 실란 커 플링제인 APTMS 실란의 표면개질을 통해 NMP 용매하 에서 평균입도가 각각 약 67 nm와 89 nm를 지닌 amor + γ-Al2O3와 α-Al2O3 나노졸을 제조하였다.