1. 서 론
고도 산화 처리기술(advanced oxidation processes, AOPs) 중 광촉매(photocatalyst) 기술은 무한한 에너지로 간주할 수 있는 태양광을 이용하여 대기질 및 수질을 친 환경적으로 정화할 수 있는 경제적인 방법이다.1-3) 광촉 매에 의한 정화 과정은 선택된 소재의 띠 간격 에너지 (band gap energy)보다 크거나 비슷한 에너지를 갖는 빛 의 조사(irradiation)에서부터 시작된다. 조사된 빛은 광촉 매 내에 전자의 여기(excitation)를 유도해 전자(e−)와 정 공(h+) 쌍을 형성시키고, 생성된 전하운반체(charge carrier) 는 각각 표면으로 이동해 흡착된 오염 물질과 산화환원 반응을 일으켜 무해한 물질로 변화시키는 역할을 한다. 이 와 같은 반응 기전(mechanism)을 통해, 광촉매의 양자 효 율(quantum efficiency)은 촉매의 띠 간격과 띠 끝(band edge), 생성된 전자와 정공의 재결합 속도(recombination rate)와 비표면적에 의해 결정된다는 것을 알 수 있다.
다양한 산화물과 황화물이 광촉매 특성을 갖지만, 이 산화티타늄(titanium dioxide, titania, TiO2)은 준수한 광 반응성, 높은 광화학적 및 열적 안정성과 무독성 등으 로 인하여 가장 널리 활용되고 있다.4-6) 전술한 반응 기 전을 고려하면, TiO2의 띠 간격은 3.0 eV(rutile phase) 또는 3.2 eV(anatase phase)로 자외선(ultraviolet ray) 영 역의 빛만을 흡수하여 이용할 수 있다. 이를 극복하기 위 해, 다양한 양이온 또는 음이온을 TiO2에 도핑하거나, 금 속의 표면공명(surface plasmon) 현상을 이용해 흡수 스 펙트럼을 가시광선(visible light) 영역으로 확장하는 연구 가 활발하게 진행되고 있다.7-9) 반면에 생성된 전자와 정 공의 분리는 고가의 귀금속 공 촉매(co-catalyst)를 표면 에 형성하는 기술에 의존하고 있으며, 효과적으로 분리 되지 못한 전자와 정공의 재결합은 효율 저하의 주요 원 인으로 작용하고 있다.
띠 구조(band structure)가 상이한 소재를 복합화한 이 종접합구조(heterostructure)는 전하 분리(charge separation) 과정을 가속화할 수 있는 효과적인 대안이다.10-11) 이는 생성된 전자와 정공이 상대적으로 높거나 낮은 에너지 준위를 갖는 상호 접합된 이종 재료의 가전자대(valence band) 또는 전도대(conduction band)로 이동하기 때문이 다. SnO2, SrTiO3, Bi2WO6, ZnO, CeO2, V2O5 등 다 양한 소재가 TiO2와 이종접합구조를 형성하여 광촉매 효 율을 개선한 보고가 있었지만, 이종접합구조를 구현하기 위해 두 가지 이상의 공정을 필요로 하여 공정이 복잡 하고, 각 상의 분율을 제어하기 어려운 한계가 있다. 또 한 접합된 재료의 고유 특성이 TiO2의 장점을 상쇄시켜 광반응성의 감소 및 안정성의 저하 등의 문제가 발생할 수 있다.
본 연구에서는 TiO2와 산소불화 티타늄(titanium oxyfluoride, TiOF2)이 이종 접합된 복합체 분말을 합성하여, 기존 소재의 한계를 극복하고자 하였다. TiOF2는 우수한 전기화학적 및 광화학적 특성과 대기 중에서 안정하고 독성이 없다는 장점으로 리튬이온 배터리(Li-ion battery, LIBs), 전기변색 소자(electrochromic display), 광촉매 (photocatalyst) 등 다양한 분야에 적합한 소재이다.12-14) 또한 TiOF2와 TiO2는 상호 화학적 변환(chemical transformation) 이 용이한 소재로 합성 과정에서 온도, 분위기 및 반응 시간을 제어하여 단일 공정으로 동시에 제조할 수 있다는 장점을 가지고 있다. TiO2/TiOF2 복합체 분 말은 초음파 분무 열분해법(ultrasonic spray pyrolysis, USP)을 이용하여 합성하였고, 합성 온도를 변화하여 상 분율의 제어를 시도하였다. 합성된 분말의 형상, 입도 및 결정 구조를 체계적으로 고찰하였으며, 자외선-가시광선 영역에서의 흡광도와 Kubelka-Munk식을 통해 띠 간격 에너지를 측정하여, 상 분율에 따른 광학적 특성을 분 석하였다. 최종적으로 합성된 분말의 광촉매 특성을 광 조사에 의한 Rodamine B의 탈색(decolorization) 실험을 통해 확인하여 응용 가능성을 고찰하였다.
2. 실험 방법
TiO2/TiOF2 이종접합구조 기반 분말을 제조하기 위 해, 100 mM의 불화티탄산 수용액(hexafluorotitanic acid solution, 60 wt% H2TiF6 in H2O, Sigma-Aldrich)을 초 순수(de-ionized water)에 용해하여 전구체 용액을 준비 하였다. 준비된 용액은 미세 정량 펌프를 통해 1.2 ml/ min의 유량으로 초음파 분무 장치로 공급되었으며, 1.7 MHz로 설정된 초음파 진동자에 의해서 미세 액적의 형 태로 관상 로(tube furnace) 내부로 분무되었다. 미세액 적을 관상 로 내부로 이동시키기 위한 운반가스(carrier gas)는 고 순도 산소 가스를 선택하여 사용하였고, 2 lpm 의 속도로 공급하여 미세액적을 운반하였다. TiO2/TiOF2 의 상 분율을 제어하기 위해 관상 로의 내부 온도는 400 °C에서 800 °C까지 각각 100 °C 간격으로 설정하여 미 세 액적내의 용매 증발 및 출발 물질의 열분해 그리고 결정화를 유도하였고, 최종적으로 관상 로의 상부에 필 터페이퍼(filter pater)가 삽입된 유리 필터를 위치시켜 합 성된 분말을 취득하였다.
합성된 분말의 형상과 직경은 전계 방사형 주사 현미 경(field emission-scanning electron microscopy, FE-SEM, JSM-6700F, JEOL, Japan)을 이용하여 관찰하였고, 결정 구조와 상 분율 및 결정 크기(crystallite size)는 X-선 회 절분석기(X-ray diffractometer, XRD, X'Pert3 Powder, PANalytical, Netherlands)를 사용하여 분석하였다. 또한 분말의 흡광도와 확산 반사율을 측정하기 위해, 자외선 /가시광선 분광광도계(UV-vis spectrophotometer, UV-2600, SHIMADZU, Japan)를 이용하였고, 확산 반사율을 이용 하여 Kubelka-Munk 식을 기반으로 띠 간격 에너지를 계 산하였다.15) 제조된 분말의 광촉매 특성을 측정하기 위 해, 100 ml의 Rhodamine B 수용액(1 × 10−5M)에 0.05 g 의 합성된 분말을 분산하여 준비하였다. 광원은 Xenon lamp(300W, PE300BF)를 사용하였으며, 200W의 세기 로 빛을 조사하고, 시간별로 탈색 정도를 분광광도계를 이용하여 측정해 광촉매 특성을 평가하였다.
3. 결과 및 고찰
초음파로 분무된 액적의 열분해 온도를 변화하여 제조 된 분말의 결정구조와 상 분율을 확인하기 위해 XRD 분석을 실시하였고, 그 결과를 Fig. 1에 나타내었다. Fig. 1에서와 같이, 400 °C에서 합성을 실시한 경우, cubic 구 조를 갖는 TiOF2(JCPDS #:08-0060)의 회절패턴만이 관 찰되어 단일상을 갖는 것으로 확인되었으며, 500 °C 이 상에서는 anatase 상 TiO2(JCPDS #:21-1272)의 회절패 턴을 확인할 수 있어 TiO2/TiOF2 이종접합구조 분말이 합성되었음을 알 수 있다. 합성온도가 높아짐에 따라 상 대적으로 TiO2 회절패턴의 강도가 상승하였으며, 이를 통 해 제조된 분말에서의 상 분율이 변화하는 것을 확인할 수 있었다. 각 합성온도에서의 TiOF2에 대한 TiO2의 상 대적인 피크 강도를 ITiO2/(ITiO2+ITiOF2) 식으로 계산한 결 과, 400 °C에서 800 °C로 온도가 증가함에 따라 각각 0(400 °C), 0.267(500 °C), 0.315(600 °C), 0.488(700 °C), 0.548(800 °C)로 TiO2의 분율이 증가되었다. 또한 관찰된 회절 패턴의 강도와 반가폭을 고려할 때, 제조된 분말 의 결정성(crystallinity)은 합성 온도가 높아짐에 따라 개 선되는 것을 알 수 있다.
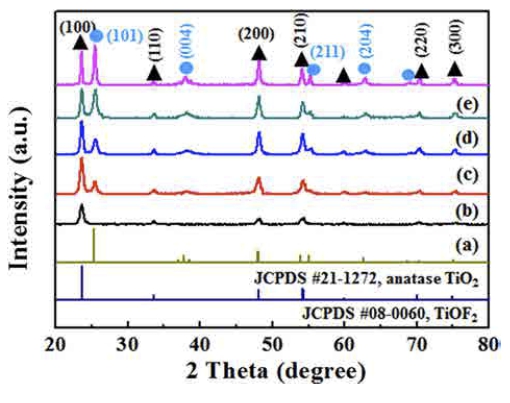
Fig. 1
X-ray diffraction patterns of the products synthesized by the ultrasonic spray pyrolysis process at (A) 400 °C, (B) 500 °C, (C) 600 °C, (D) 700 °C and (E) 800 °C.
일반적으로 USP로 합성된 분말은 미세한 1차 입자가 응집된 조대한 2차 입자의 형태를 갖는다. 1차 입자의 크기는 분말의 전체 비표면적을 결정하는 요인이며, 비 표면적은 광촉매 특성에 영향을 미치는 주요 인자 중 하 나이다. 각각의 온도에서 합성된 분말의 X-선 분석 결 과로부터 얻은 반가 폭(Full width at half maximum, FWHM)과 Scherrer equation (식 1)을 이용하여 1차 입 자의 크기를 계산하였고, 이를 Table 1에 정리하였다.
Table 1
Average crystallite sizes of TiO2/TiOF2 powders synthesized by the ultrasonic spray pyrolysis at different temperatures.
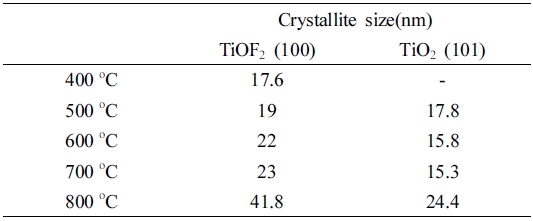 |
식 (1)에서 λ는 X-선 회절 분석 시 이용한 파장 (1.5406 Å)이고, θ와 B는 각각 특정 회절 피크의 각도 와 반가 폭을 나타내며, 23.64°에서 관찰된 TiOF2 (100) 면과 25.28°에서 나타난 TiO2 (101)면의 회절 각도와 반 가 폭을 선택해 식 (1)에 대입하였다. TiOF2의 경우, 온 도가 증가함에 따라 2차 입자를 구성하는 1차 입자의 크 기가 증가하였으며, 이는 온도 증가에 따른 결정 성장 에 의한 것으로 해석할 수 있다. 반면에 TiO2의 경우, 1차 입자의 크기가 500 °C에서 700 °C까지의 합성 온도 에서는 유사하였고, 800°C에서만 증가되었다. 이는 TiO2 의 분율이 700 °C 이하에서는 핵 생성에 의해, 800 °C 에서는 결정성장에 의해 증가했다고 해석할 수 있다.
Fig. 2은 USP 공정을 통해 다양한 온도에서 합성된 분 말의 주사전자현미경 사진이며, 수 백 나노미터에서 1 마 이크로미터 수준의 입도를 갖는 입자들을 관찰할 수 있 다. 분말의 형상은 구형이었으며, 이는 분무된 액적이 표 면장력을 최소화하기 위해 구형을 형성한 후, 용매의 증 발, 전구체의 분해 및 결정화 과정을 거쳐 분말로 합성 되기 때문이다. 합성 온도의 증가에 따른 분말의 형상 및 입도 변화는 관찰되지 않았다.

Fig. 2
(A-E) Low and (F-J) high magnification FE-SEM images of the TiO2/TiOF2 powders synthesized by the ultrasonic spray pyrolysis at (A, F) 400 °C, (B, G) 500 °C, (C, H) 600 °C, (D, I) 700 °C and (E, J) 800 °C.
TiO2/TiOF2 복합체의 상 분율에 따른 광학적 성질은 자 외선/가시광선 분광광도계를 이용하여 분석하였고, 각 분 말의 흡광도와 확산 반사율(diffuse reflection)을 Kubelka- Munk 식으로 변환한 그래프를 Fig. 3에 나타내었다. Fig. 3(A)에서 보여주듯이, 모든 분말이 400 mm 이하의 자외 선 영역에서 강한 흡광도를 나타내었지만, 합성 온도의 증가, 즉 TiO2의 분율 증가에 따라 가시광에 대한 흡광 이 증가하는 것을 관찰할 수 있다. 이는 TiOF2로부터 TiO2가 형성되는 과정에서, F이온이 TiO2 결정격자 내로 도핑(doping)되어 TiO2의 띠 간격 내에 불순물 에너지 준 위가 형성되었기 때문이다.16-17) 이러한 결과는 자외선으 로만 국한되는 TiO2의 광 활성을 가시광 영역으로 확장 하는 데 응용할 수 있다. 합성된 분말의 띠 간격은 합성 온도와 관계없이 약 3.15 eV 이었으며, 이는 3.2 eV로 알 려진 anatase TiO2와 TiOF2의 띠 간격 에너지(약 3.2 eV)와 유사한 값으로 확인되었다.
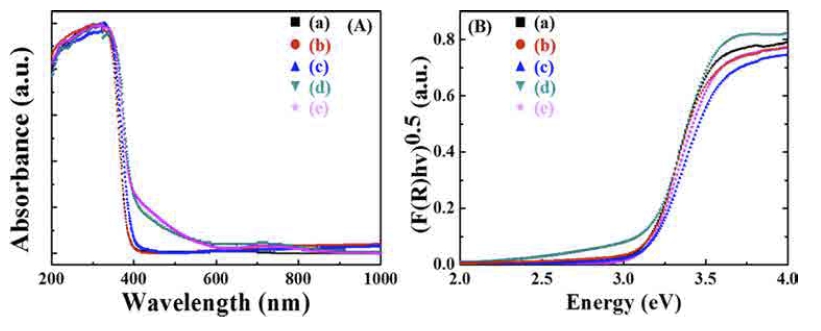
Fig. 3
(A) UV-Vis diffuse absorption spectra and (B) the plots of the transformed Kubelka-Munk function versus the absorbed light energy of the TiO2/TiOF2 composite powders synthesized at (a) 400 °C, (b) 500 °C, (c) 600 °C, (d) 700 °C and (e) 800 °C.
제조된 분말의 광촉매 특성을 확인하기 위해, Rhodamine B에 대한 탈색(degradation)효율을 광 조사(irradiation) 시 간에 따라 측정하였다. 일반적으로 유기물질의 광분해 반 응은 식 2와 같은 Langmuir-Hinshelwood 속도식을 따 르고, 이를 적분해 식 3과 같이 유사 1차 속도식으로 표 현할 수 있다.18) 식 (3)에서 Co와 C는 각각 반응 유기 물의 초기 및 특정 반응시간(t) 후의 농도이며, kapp는 유 사 1차 속도 상수이다. 이 속도상수는 온도 및 pH 등의 반응 조건에 영향을 받으며, 이 값이 커질수록 촉매는 큰 효율을 갖는다는 것을 의미한다.
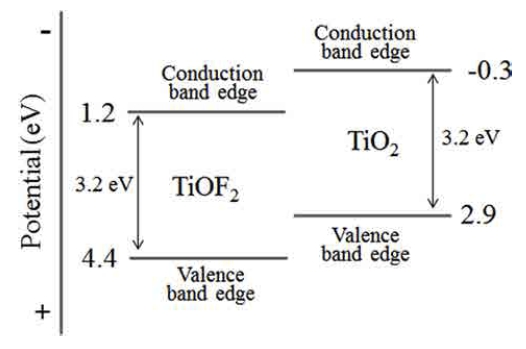
Fig. 4는 Rhodamine B 수용액에 합성된 분말을 첨가 하고 Xenon 램프를 이용해 광 조사를 실시하여, 5분 단 위로 Rhodamine B의 농도를 자외선/가시광선 분광광도 계를 이용해 분석한 결과이다. 그래프에서 dark에서 0 min 까지는 광이 조사되지 않은 상태에서 분말과 Rhodamine B의 흡착 정도를 나타내며, 모든 분말에서 유사한 수준 을 나타내었다. 이는 합성된 분말의 크기 및 형상의 차 이가 미비해 유사한 비표면적을 갖기 때문이라고 해석 할 수 있다. 광 조사가 실시된 이후에는 모든 분말에서 Rhodamine B의 농도 감소를 확인할 수 있었다. 특히, 400 °C에서 700 °C까지는 온도 증가에 따라 농도 감소의 폭이 증가하였지만, 800 °C에서는 700 °C와 비교하여 상 대적으로 농도 감소가 적게 관찰되었다. Fig. 5는 Fig. 4에서 관찰된 농도 변화를 식 (3)으로 변환해 표현한 그 래프이며, Table 2는 유사 1차 속도 상수를 계산해 정 리한 값을 보여준다. 700 °C에서 합성된 분말이 가장 빠 른 농도 감소를 나타내었으며, 유사 1차 속도 상수는 6.02 × 10−2/min으로 확인되었다. 유사 1차 속도 상수는 순수한 400 °C에서 합성된 TiOF2가 가장 낮은 값을 가 졌으며, TiO2의 분율 증가에 따라 점차적으로 증가하였 고, TiO2와 TiOF2의 분율이 1:1에 가장 가까운 값인 0.488을 갖는 700 °C에서 합성된 분말에서 가장 높은 값 을 나타내었다. 하지만 TiO2의 분율이 0.548로 증가하면 유사 1차 속도 상수는 감소하는 경향을 보였다. 이를 통 해 광촉매 특성이 합성 온도의 증가에 따른 결정성의 개 선 또는 비표면적의 감소에 의한 영향보다는 TiO2와 TiOF2의 분율에 크게 의존한다는 것을 알 수 있다. 이 러한 결과는 Fig. 6과 같이, TiOF2와 TiO2가 갖는 띠 끝 의 위치에 의해 전자-정공 쌍의 효율적인 분리가 이루 어지고, 그 결과, 재결합이 효과적으로 방지되었기 때문 이라고 해석할 수 있다.
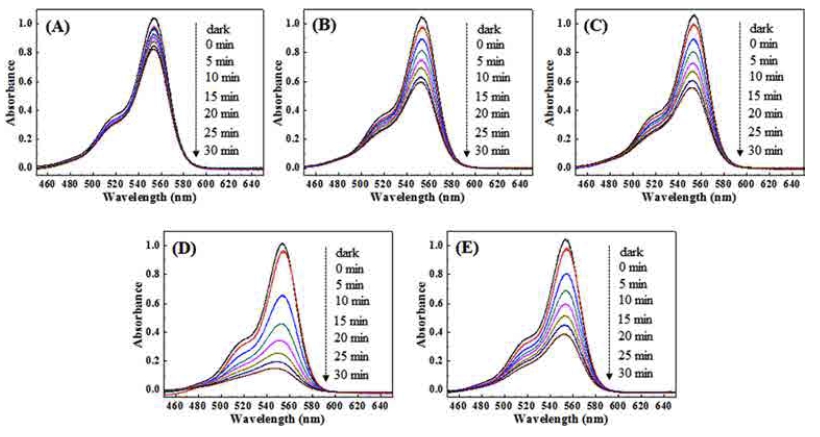
Fig. 4
Graphs showing the change in the concentration of Rhodamine B by the photocatalytic reaction of the TiO2/TiOF2 composite powders and the Rhodamine B as a function of light irradiation time.
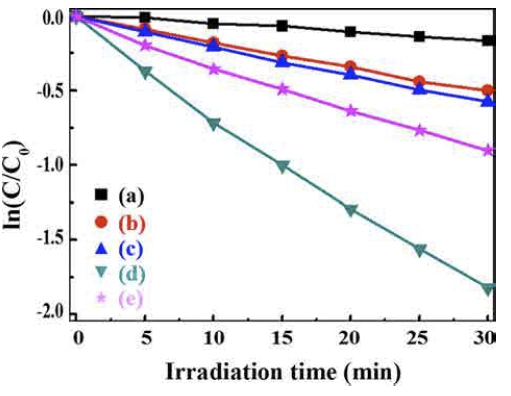
Fig. 5
Kinetic profile on the photocatalytic degradation of aqueous Rhodamine B solution under light irradiation in the presence of the TiO2/TiOF2 composite powders synthesized at (a) 400 °C, (b) 500 °C, (c) 600 °C, (d) 700 °C and (e) 800 °C.
4. 결 론
본 연구에서는 TiOF2와 TiO2의 이종접합 복합체 분말 을 합성함으로써, 광 조사에 의해 생성된 전자-정공 쌍 의 효율적인 분리를 유도하여 재결합을 억제하고 이를 통해 광촉매 효율을 개선하였다. 특히, USP 단일 공정 을 이용하여 TiO2/TiOF2의 이종접합 복합체 분말을 합 성함으로써, 분말 제조공정의 단순화와 연속 합성 및 대 량생산의 가능성을 확보하였고, TiO2/TiOF2의 상 분율을 공정 변수인 열분해 온도만을 변화하여 효과적으로 제 어하였다. 제조된 분말은 서브 마이크론 크기의 구형 입 자였으며, 열분해 온도가 증가함에 따라 순수 TiOF2 분 말에서 anatase TiO2의 분율이 증가된 TiO2/TiOF2 이종 접합 복합체 분말을 형성하였다. 합성된 복합체 분말의 띠 간격 에너지는 약 3.15 eV로 확인되었다. 각각의 온 도에서 합성된 분말의 광촉매 특성을 확인한 결과, 각 상의 분율이 1:1에 가까운 700 °C에서 합성한 분말이 가 장 효율적으로 rhodamine B를 분해하였으며, 이를 통해 TiO2/TiOF2의 이종접합 구조가 전자-정공 쌍을 효과적으 로 분리하여 재결합을 억제하고, 광촉매 효율을 개선하 는 데 주요한 인자로 작용하였다는 것을 확인하였다.