1. 서 론
기후 변화에 대한 위기와 함께 친환경 에너지 생산 기술에 대한 관심과 수요가 증가하면서 수소 연료전지는 미래 에너지 전원으로서 수송, 건물, 분산 발전 등 다양한 산업 분야에서 적극 활용될 것이라 예상되고 있다.1,2,3) 수소를 연료로 사용하여 전기화학 반응을 통해 전기를 생산하는 수소 연료전지는 이산화탄소를 배출시키지 않는 청정 기술로 많은 연구가 진행 중에 있다.2,3,4,5,6,7) 다양한 연료전지 시스템 중, 수송 및 분산발전용으로 활용되고 있는 양성자 교환막 연료전지(proton exchange membrane fuel cells, PEMFCs)에서는 양 전극 사이에서 수분을 함유한 고분자 막을 통해 양성자가 전달되므로 일반적으로 60~80 °C에서 작동되어 저온형 연료전지로 분류된다.1) 한편, 이러한 저온 작동 조건은, 전기화학 촉매 반응의 활성화 에너지 측면을 고려할 때 매우 느린 반응 환경을 제공하게 되는데 이러한 촉매 반응 특성의 문제점을 해결하기 위해 주로 Pt 기반의 귀금속 나노 입자를 촉매로 사용하고 있다.
특히, 캐소드에서의 느린 산소 환원 반응은 연료전지 시스템 효율에 큰 영향을 미치기 때문에 매우 중요한데, 전기화학 반응 효율을 높이기 위해 PtFe, PtCo, PtNi, PtCu 등과 같은 합금 구조 촉매를 개발 중에 있다.8,9,10) 이러한 합금 촉매는, Pt 보다 격자 상수가 작은 제 2의 전이금속을 합금 시킴으로써 Pt 전자 구조 수축 및 d 밴드 중심의 이동 등 전자 구조의 변형으로 인해 산소 결합에너지를 순수 Pt에 비해 낮출 수 있어 매우 높은 산소 환원 반응 성능을 나타낼 수 있다고 보고되었다.10) 더 나아가, 금속간 화합물(intermetallic) 합금 구조를 갖는 fct-PtFe와 같은 합금은 단순한 무작위(random) 합금 구조 촉매에 비해 산소 환원 반응 활성과 내구성이 상대적으로 높다고 알려져 있다.9,10,11)
그러나 이러한 금속간 화합물 합금 구조 나노 입자를 제조하기 위해서는 700~1,000 °C 정도의 고온 열처리 공정이 필요하다. 이러한 고온 열처리는 합금 나노 입자 내부에 원자 배열의 변형을 유도하기 위한 충분한 열에너지를 제공하지만, 원자 및 입자의 이동도가 높아지고 구조적으로 불안정해져 서로 뭉치게 되는 sintering 현상이 자연적으로 발생하게 된다. 따라서 기체 분위기와 온도 만을 제어하는 기존 열처리 공정을 통해서는 이러한 문제점을 피해갈 수 없다.12,13)
따라서 본 연구에서는 기존 열처리 공정의 한계를 극복하기 위한 전략으로서, 공정 그 자체 보다는 열처리를 위한 촉매 소재 구조를 새롭게 설계하는 새로운 시각을 제안하고자 한다. 특히, 카본쉘이 코팅된 무작위 합금 입자를 활용하여 1차 고온 열처리를 통해 금속간 화합물 합금 구조를 먼저 만든 뒤, 2차 열처리 공정을 통해 카본쉘을 etching 시켜 촉매 활성점을 확보하는 기술을 소개하고자 한다. 구체적으로, 카본쉘을 템플레이트로 활용하여 금속간 화합물 합금 구조를 가진 나노 입자의 크기를 3~4 nm 수준으로 매우 작게 유지하면서 촉매 활성 면적을 효과적으로 제어하며, 이를 통해 최적의 연료전지용 합금 촉매 구조를 찾는 전략이라고 할 수 있다. 이러한 촉매 제조 공정은 전기화학 촉매의 구조적 제어에 대한 아이디어를 제공하면서도, 열적 안정성이 요구되는 열화학 촉매 시스템에서의 활용이 가능할 것으로 기대된다.
2. 실험 방법
2.1. 촉매 합성 및 열처리 공정
카본쉘이 코팅된 20 wt% Pt3Fe1 합금(Pt3Fe1@C/C) 촉매를 합성하기 위해 카본 소스를 제공해줄 수 있는 유기 리간드로 알려진 아세틸아세토네이트(acetylacetonate, acac)를 포함하고 있는 Pt(acac)2 (97 %, Sigma-Aldrich, USA) 및 Fe(acac)3 (97 %, Sigma-Aldrich, USA)를 금속 전구체로 사용하였다.10,14) Pt와 Fe의 원소 비율을 3:1로 하여 각 전구체를 준비한 후, 촉매를 담지시키기 위한 카본 블랙(Vulcan XC-7, Cabot, USA) 0.1 g과 함께 160 mL의 1-octadecene (90 %, Sigma-Aldrich, USA)에 분산시켰다. 산소 및 수분과 같은 불순물을 제거하기 위해 Ar 분위기, 120 °C에서 추가적으로 1시간 동안 교반한 뒤 용액의 온도를 300 °C까지 증가시키고 열분해 반응이 잘 일어날 수 있도록 교반과 함께 반응 온도를 2시간 동안 유지했다. 반응 종료 후, 용액을 80 °C로 냉각하고 과량의 헥산(n-hexane, 95 %, Sigma-Aldrich, USA)과 에탄올(ethanol, 95 %, Sigma-Aldrich, USA)로 세척하였다. 여과 후에는 남겨진 분말을 60 °C 진공 오븐에서 건조시켜 열처리 전 촉매 샘플(Pt3Fe1@C/C-ASP)을 얻었다. Pt3Fe1@C/C-ASP 샘플에 비활성 기체인 Ar을 흘려주며 1,000 °C에서 1시간 동안 카본쉘 형성 및 촉매 구조 전환을 위한 1차 열처리를 수행하여 Pt3Fe1@C/C-Ar1000 샘플을 얻었다. 이후, 카본쉘의 두께 및 기공 구조를 변형시키기 위해 Pt3Fe1@C/C-Ar1000 샘플을 나누어 air를 흘려주며 180 °C에서 30분(0.5 시간), 300 °C에서 1시간, 300 °C에서 3시간을 2차 열처리 공정으로서 각각 진행하였다. 이렇게 제조된 최종 촉매 샘플을 각각 Pt3Fe1@C/C-Ar1000/0.5air, Pt3Fe1@C/C-Ar1000/1.0air, Pt3Fe1@C/C-Ar1000/3.0air로 명명하였다.
2.2. 촉매 구조 및 전기화학 특성 분석
제조된 Pt3Fe1@C/C 샘플들의 구조 및 입자 크기를 확인하기 위해 투과 전자 현미경(transmission electron microscope, TEM, Tecnai G2 F30 S-Twin, FEI, Netherlands) 분석을 실시하고, X-ray diffraction (XRD, SmartLab, Rigaku, Japan)을 활용하여 Pt3Fe1@C/C 샘플들의 결정 구조를 분석하였다. 촉매의 전기화학 특성은 potentiostat (Metrohm, Autolab, Netherlands)에 연결된 rotation disk electrode (RDE)를 이용한 3 전극 전기화학 셀을 사용하여 실온에서 수행하였다. 전기화학 셀은 기준 전극으로 Ag/AgCl 전극, 상대 전극으로 Pt sheet, 그리고 작동 전극으로 0.196 cm2의 면적을 갖는 glassy carbon 전극으로 구성하였다. 측정된 전압은 모두 reversible hydrogen electrode (RHE)로 나타내었고 전류는 전극의 기하학적 면적을 사용하여 전류 밀도로 표기하였다. 균일한 촉매 잉크를 제조하기 위해, 5 mg의 촉매를 34.4 µL의 Nafion 용액(5 wt%, Sigma-Aldrich, USA)과 2-propanol (99.5 %, Sigma-Aldrich, USA) 500 µL에 교반한 후 15분 동안 초음파 처리하여 분산시켰다. 그런 다음 촉매 잉크 4 µL를 RDE의 카본 전극 표면에 올려놓고 실온에서 건조시킨 다음 전기화학 측정을 시행하였다. 상용 Pt/C (20 wt%, Premetek)는 38.18 µg cm-2)의 Pt 로딩양을 가지며, Pt3Fe1@C/C 샘플들의 경우 Pt/C와 동일한 총 metal 로딩(Pt + Fe)으로 맞추어 Pt 로딩양은 상대적으로 적은 34.9 µg cm-2가 되었다. 촉매 표면 구조를 살펴보고 전기화학적 활성 면적(electrochemically active surface area, ECSA)을 계산하기 위해 0.1 M HClO4 전해질에서 상온, Ar 분위기 하에서 20 mV s-1로 cyclic voltammogram (CV)을 측정하였고, 산소 환원 반응 성능은 CV 측정 후, O2가 포화된 0.1 M HClO4 용액에서 1,600 rpm의 RDE 회전속도, 5 mV s-1의 스캔 속도 조건에서 평가하였다.
3. 결과 및 고찰
Fig. 1은 금속간 화합물 합금으로 알려져 있는 fct-PtFe 나노 입자를 3~4 nm 크기로 작게 제조하기 위한 촉매 제조 공정을 보여준다. 먼저, 카본쉘을 형성하기 위한 카본 소스를 제공해주는 아세틸아세토네이트와 같은 유기 리간드를 포함하고 있는 Pt 및 Fe 전구체를 활용하여 약 300 °C에서 열분해법을 통해 카본 소스를 함유하고 있는 fcc-PtFe 무작위 합금 나노 입자(Pt3Fe1@C/C-ASP)를 제조한다.14,15,16) 이때, 합금 입자의 격자 내 포함되어 있는 카본은 700~1,000 °C의 고온, 비활성 기체 분위기 하에서 1차 열처리하게 되면 표면으로 segregation 되면서 촉매 작용에 의해 금속 입자 표면에 매우 얇은 카본층을 형성하며 초박형 카본쉘이 코팅된 나노 입자가 만들어진다.16,17,18) 한편, 비활성 기체 분위기 하에서의 후 열처리 과정 중에 최초 합성된 무작위 합금 나노 입자 표면에 카본쉘이 코팅되면서 동시에, 그 카본쉘이 템플레이트로 작용하여 입자 크기를 성장시키지 않으면서 합금의 결정 구조를 fcc에서 fct로 변화시킬 수 있을 것으로 예상해볼 수 있다. 이후, 카본쉘 두께를 얇게 만들면서 표면에 결함(defect)을 생성시키기 위해 air에서 2차 열처리를 진행하며 이를 통해 전기화학적 활성 면적을 증대시키게 된다.
먼저, fcc에서 fct 합금으로 구조 변환시킬 때 요구되는 열에너지의 최적화를 위해 1차 Ar 열처리 온도를 700 °C에서부터 100 °C 간격으로 1,000 °C까지 변화를 주었다. Fig. 2는 다양한 열처리 온도 조건 하에서 제조된 Pt3Fe1@C/C 샘플들의 TEM 이미지를 보여준다. 예상한 바와 같이, 금속 격자 내 함유된 카본이 표면으로 나오면서 탄화되어 매우 얇은 카본쉘이 형성된 것을 확인할 수 있으며 카본쉘의 confinement 효과로 합금 입자의 크기는 급격한 열처리 온도 변화에도 불구하고 큰 영향을 받지 않았음을 알 수 있으며 결과적으로 3~4 nm 사이의 크기가 유지되었다.
이렇게 제조된 카본쉘 코팅 합금 촉매의 구조 변화를 살펴보기 위해, XRD 분석을 실시한 결과(Fig. 3), 700 °C에서 1,000 °C로 열처리 온도가 점차적으로 상승함에 따라 fct-PtFe 합금 구조를 확인할 수 있는 (110), (210), (211) peak가 나타나며 그 신호가 점자 강해짐을 알 수 있었다.11,19,20) 따라서 금속간 화합물 합금 제조 시, 제공되는 열에너지가 커질수록 보다 효율적으로 합금 구조를 변화시킬 수 있음을 확인할 수 있으며 준비한 샘플 중 1,000 °C에서 열처리된 Pt3Fe1@C/C-Ar1000 샘플이 금속간 화합물 합금 구조를 가장 잘 형성하였음을 확인하였다.
따라서 다양한 1차 열처리 온도 하에서 제조된 Pt3Fe1@C/C 중, 1,000 °C에서 열처리된 Pt3Fe1@C/C-Ar1000 샘플을 2차 열처리에 활용하였다. 이때 카본쉘의 두께를 얇게 하거나 표면 결함을 생성시키기 위해 열처리 기체는 air를 선택하였으며 촉매 지지체로 사용된 Vulcan의 열화를 방지하기 위해 열처리 온도는 180 °C 또는 300 °C로 고정하였다. 이때, 효율적인 카본쉘 구조 변화를 위해 air 열처리 시간을 30분(180 °C), 1시간(300 °C), 3시간(300 °C)으로 변화시켰으며 이러한 온도 및 시간 변수에 따라 제조된 촉매 구조를 Fig. 4에서 보여주고 있다. TEM 이미지 상에서는 air 분위기 하에서의 2차 열처리 후에도 입자의 크기는 크게 변화하지 않았으나 합금 입자 표면에서 카본쉘이 잘 보이지 않을 정도로 매우 얇아 졌음을 확인했다.
이러한 카본쉘 구조 변화를 보다 명확히 확인하기 위해 CV를 측정한 결과[Fig. 5(a)], air 열처리 온도와 시간이 늘어남에 따라 점차적으로 수소 흡탈착 영역(0~0.35 V)의 면적이 증가됨을 알 수 있으며 특히 180 °C에서 300 °C로의 온도 상승이 큰 영향을 미치는 것으로 판단되었다. 수소 흡탈착 전하량으로부터 전기화학적 활성 면적을 계산한 결과, 180 °C에서 30분(0.5air 샘플) 동안 열처리했을 때는 활성 면적이 0에 가까울 정도로 카본쉘에 결함이 거의 없는 구조를 보였으나 300 °C에서 1시간(1.0air 샘플)에서 열처리 했을 때 약 26 m2 gPt-1으로 넓어졌으며 300 °C 3시간(3.0air 샘플) 후에는 약 32 m2 gPt-1으로 표면 결함이 늘어나고 두께가 더 얇아진 것으로 확인되었다. 일반적으로 이러한 전기화학적 활성 면적의 변화는 촉매 입자의 크기에 반비례한데, 이와 같은 결과는 카본쉘이 코팅된 촉매 입자를 사용한 경우에 입자 크기를 매우 작게 유지하면서도 카본쉘의 두께 및 기공 구조에 따라 노출된 촉매의 표면적을 변화시킬 수 있음을 시사한다[Fig. 5(b)]. 그럼에도 불구하고 300 °C의 온도에서 1시간에서 3시간으로 air 열처리 시간을 늘렸을 때 매우 큰 활성 면적의 증가가 없다는 것은 금속간 화합물 합금 구조 제조 시 수행한 1,000 °C에서의 1차 열처리에 의해 카본쉘 구조가 매우 견고해 짐을 의미한다고 볼 수 있다.
이렇게 변형된 카본쉘 코팅층 안쪽으로 fct-PtFe 합금 입자를 갖는 Pt3Fe1@C/C-Ar1000 샘플들의 산소 환원 반응 활성을 측정한 결과, 0.5air << 1.0air < 3.0air 샘플 순으로 촉매 성능이 증가하였으며 이는 앞서 살펴본 전기화학적 활성 면적과 같은 경향을 나타냄을 알 수 있다[Fig. 5(c)]. 한편, 단일 Pt 나노 입자로 구성되어 있는 상용 Pt/C 촉매의 경우, 전기화학적 활성 면적이 약 77 m2 gPt-1으로 준비된 샘플 중 가장 높은 값을 보이고 있으나 산소 환원 반응 촉매 성능의 경우 Pt3Fe1@C/C-Ar1000/1.0air 샘플과 유사하였다. 따라서 air에서 3시간 동안 2차 열처리를 진행했던 Pt3Fe1@C/C-Ar1000/3.0air 샘플이 상대적으로 적은 전기화학적 활성 면적을 나타내고 있음에도 불구하고 가장 높은 산소 환원 반응 활성을 보였는데, 이는 Pt-Fe 간 합금 효과, fcc에서 fct 구조로 변화된 금속간 화합물 구조 형성 효과 등 복합적인 요인들이 시너지를 보인 것으로 사료된다.19,20) 연료전지 촉매 성능 지표로서 대표적으로 활용되고 있는 0.9 V에서 촉매의 mass activity (질량 활성)와 specific activity (단위면적당 활성) 값을 비교해보면 air 열처리 온도 및 시간이 증가할수록 빠르게 커짐을 알 수 있으며[Fig. 5(d)], 특히, 약 6 m2 gPt-1 정도의 전기화학적 활성 면적 차이로도 3.0air 샘플의 촉매 성능이 1.0air 샘플에 비해 매우 크게 향상되었다. 이는 측정된 전기화학적 활성 면적 값으로부터 드러나지 않는 카본쉘 안쪽의 Pt 활성점이 존재할 수 있음을 시사한다. 정량적으로 살펴보면, air에서 3시간 동안 2차 열처리를 진행했던 Pt3Fe1@C/C-Ar1000/3.0air 샘플은 상용 Pt/C 촉매에 비해 mass activity는 약 2.7 배, specific activity는 약 6.5배 높은 값을 보여 준비된 샘플 중 최적의 촉매 구조를 가진다고 볼 수 있다.
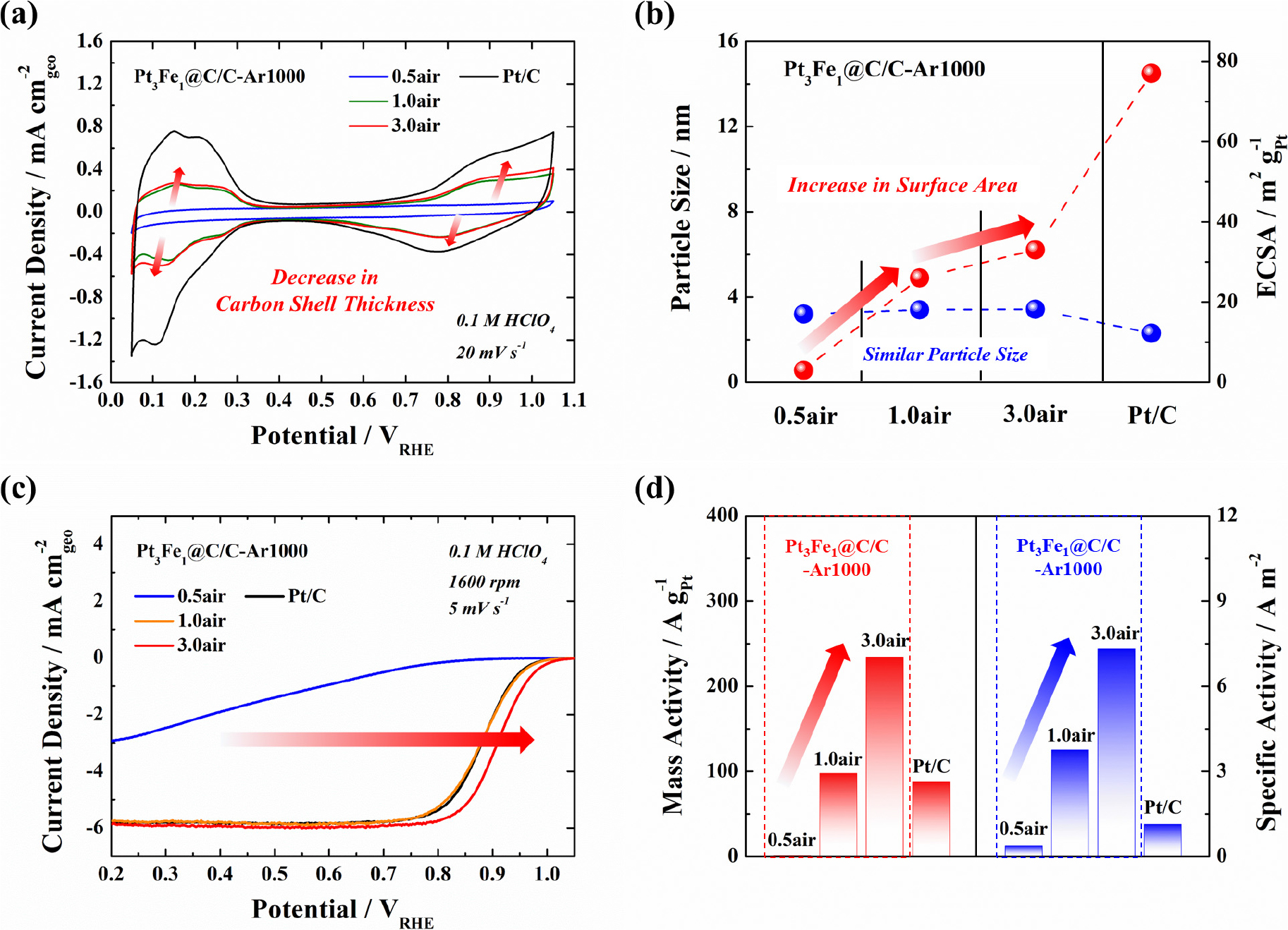
Fig. 5.
Electrochemical properties of Pt3Fe1@C/C-Ar1000/0.5air, Pt3Fe1@C/C-Ar1000/1.0air, Pt3Fe1@C/C-Ar1000/3.0air, commercial Pt/C catalysts: (a) CVs, (b) correlation curves between particle size and electrochemically active surface area (ECSA), (c) ORR polarization curves, and (d) mass activity and specific activity.
4. 결 론
본 연구에서는 연료전지용 산소 환원 반응 촉매로서, 초박형 카본쉘이 코팅된 금속 화합물 합금 나노 입자를 제조하였다. 카본 소스를 제공하기 위한 유기 리간드를 함유하고 있는 금속 전구체를 사용하여 fcc-PtFe 합금 나노 입자를 합성하였고, 1,000 °C, Ar 분위기에서 1차 열처리를 통해 고밀도 카본쉘이 코팅된 fct-PtFe 합금 나노 입자를 제조하였다. 이후, 카본쉘의 두께를 얇게 하면서 동시에 표면 결함(기공)을 만들어내기 위해, air 분위기에서 온도(180~300 °C) 및 시간(0.5~3 시간)을 변화시켜가며 2차 열처리를 진행하였고, 이를 통해 합금 입자의 크기는 3~4 nm로 유사하지만 전기화학적 활성 면적이 서로 다른 초박형, 다공성 카본쉘이 코팅된 fct-PtFe 합금 촉매를 제조하였다. 이렇게 제조된 합금 촉매들의 결정 구조, 카본쉘 특성, 산소 환원 반응 성능을 비교 분석하여 최적의 촉매 구조를 선정하였다. 이를 통해, 극한의 고온 열처리로 인해 입자 크기의 성장 및 뭉침을 피할 수 없었던 기존의 촉매 제조 공정과 달리, 카본쉘을 템플레이트로 활용하여 1,000 °C의 고온에서도 3~4 nm의 크기를 유지하면서 금속간 화합물 합금 나노 입자를 제조할 수 있는 아이디어를 제공하였다. 특히, 상용 Pt/C 촉매 대비, 금속간 화합물 합금 구조를 갖는 fct-PtFe 촉매의 높은 산소 환원 반응 활성이 확인되어 연료전지 촉매로서 활용될 가치가 있음을 확인할 수 있었다. 마지막으로, 본 연구에서 제공하는 카본쉘 코팅층을 템플레이트로 활용한 합금 구조 제어 전략 및 고활성 촉매 제조 공정은 고온 열처리가 필요한 나노 입자 제조 공정, 고온 반응이 요구되는 화학 촉매 시스템 등에도 적용 가능할 것으로 기대한다.








