1. 서 론
발전소, 공장, 자동차 등에서 배출되는 질소산화물(NOx) 은 대기오염의 주요 원인이며 특히 발전소에서 에너지를 얻기 위해 연료와 공기를 연소로에 주입하여 연소시킬 시 배가스가 발생하고 배가스 중 질소산화물 또한 함께 배출 된다.1) NOx는 NO, NO2, N2O 및 N2O3를 포함하는 질소와 산소의 화합물이며 지구온난화, 초미세먼지(PM2.5), 오존 층파괴, 광화학 스모그 등과 같은 환경 문제의 원인이다.2)
이러한 질소산화물을 질소로 분해하기 위해 프로필렌 등의 천연가스, 암모니아 등을 환원제로 이용한 선택적 촉 매 환원법(selective catalytic reduction, SCR)을 사용하며 그중에 NH3-SCR 공정이 상업적으로 널리 적용하고 있는 방법이다. NH3-SCR 공정은 저온(160~300 °C), 중온(280~ 420 °C), 고온(350~450 °C)의 온도영역대로 구분되어 사용 되고 있으며 공정의 배가스 온도는 사용되는 촉매의 유형 과 연료 가스에 따라 달라지는데 바이오 열병합 발전소에 서 400~450 °C, 보일러에서 380~450 °C로 중온에서 고온 영역까지 넓은 온도 범위를 포함하고 있다.3,4) V2O5-WO3 계 촉매는 주로 중온에서 사용되고 있으나 촉매 담체의 차 이 또는 담지되는 활성금속의 차이로 다른 온도에서 적용 이 가능하다. 저온형 촉매로는 VWSbTiO2 촉매, MnCe/ TiO2 촉매 등이 있으며 중고온형 촉매로는 높은 함량의 WO3가 담지된 WO3/TiO2 촉매, N 도핑된 TiO2로 제조한 VW/TiO2계 촉매 등이 있다.5-8)
TiO2는 NH3-SCR용 탈질촉매의 담체로 주로 사용되고 있으며, WO3/TiO2 촉매는 고온에서 높은 탈질 효율과 열 적 안정성을 나타내는 것으로 알려져 있어 가스 터빈의 배 가스에 적용이 가능하나 장기적으로 이용하면 효율이 감 소 등의 어려움이 있다.9) 석탄화력이나 바이오매스 발전 소의 경우 중온형 촉매를 쓰고 있으나, 열교환기 배관의 오염으로 인한 촉매반응기의 온도 상승에 영향을 주어 높 은 내열성을 갖는 중온-고온형 촉매 개발이 필요하기도 하다. 중고온형 촉매로서는 낮은 함량의 V2O5가 담지된 V2O5/TiO2에 CeO2 도핑하였을 때 촉매 표면에 산-염기 특 성이 변화하여 200~500 °C의 온도 영역대에서 촉매 활성 이 향상되었고 V2O5/Al2O3 촉매에 란탄계(La, Sm, Ce)를 담지하였을때도 촉매 산 특성이 변하는 것을 관찰하였 다.10,11) 이와 같이 조촉매를 사용하거나 비표면적을 높여 서 촉매 효율 높이는 등의 경우 담체의 흡착 특성을 향상 시키고, 금속 물질의 분산도 및 촉매의 안정성을 향상시킬 수 있다. 또한, 저온형 탈질촉매의 경우는 높은 함량이 V2O5가 담지된 V2O5/TiO2 촉매나,12) 판상형 V2O5를 비드 밀링하여 나노분산된 판상체 V2O5를 TiO2에 담지하는 방 법으로 촉매를 제조할 수 있다.13) 이는 V2O5의 V4+/V5+ 비 의 제어 및 증가를 통하여 저온에서 높은 탈질 효율을 갖 는 현상을 보고하였다.13)
본 연구에서는 비드밀링하에서 나노분산된 TiO2 담체 (nTi)에 V2O5 및 WO3을 담지하여 NH3-SCR 탈질촉매(VW/ nTi)를 제조하였다. 비드밀링 전의 수계 및 에탄올에서 각 각 분산된 TiO2 평균입도(D50)는 2.4 μm와 582 nm를 나타 내었으며, 에탄올하에서 1~3시간 비드밀링 후의 TiO2는 D50이 159 nm에서 93 nm로 감소하였다. 이 분산특성이 다 른 TiO2 담체들로 제조된 촉매들의 탈질 분해효율 향상과 분해온도가 고온으로 이동하는 원인을 NH3 Temperatureprogrammed desorption (NH3-TPD), Hydrogen Temperatureprogrammed reduction (H2-TPR), Fourier transform infrared spectroscopy (FT-IR), X-ray Photoelectron Spectroscopy (XPS) 등을 통하여 관찰하였다. 여기에서 TiO2 담체상에 함침된 V2O5의 V4+/V5+ 비, NH3 흡착량 및 세기, H2 환원력 차이, 탈질 반응온도에 따른 NO, NH3 분해 및 N2O 생성 현 상을 비교 관찰하여 촉매특성을 규명하였다.
2. 실험방법
2.1. TiO2 담체 및 나노분산 TiO2 제조
NH3-SCR용 탈질촉매용 담체를 제조하기 위해 황산티 타닐 TiOSO4 (66.2 % TiOSO4 7.2 % H2SO4, 26.3 % H2O, Tayca Co.)을 가수분해하여 아나타제 TiO2를 제조하였다. 가수분해가 종료된 TiO2 침전물은 증류수로 2회 세척하 였다. 이 침전물은 암모니아수(ammonia solution, 28~30 %, Sigma-Aldrich)를 이용하여, pH 7~8로 적정하여 수계 TiO2 슬러리를 제조하였다.
상기의 TiO2 슬러리를 에탄올(ethyl alchol, 99.5 %, Samchun) 용매치환 및 분산시킨 후 0.1 Ø 크기의 지르코니아 비드로 밀링하였다. 이때 밀링 조건은 2,100 rpm의 속도에 서 0, 1, 2, 3시간 동안 밀링 하여 에탄올 용매하에서 나노 분산 TiO2 담체를 제조하였다 이 TiO2 담체는 약어로 nTi- 0h, nTi-1h, nTi-2h, nTi-3h로 각각 표기하였다.
2.2. 나노분산 TiO2 담체상에 제조된 V2O5-WO3/TiO2 탈질촉매
에탄올 용매하에서의 나노분산된 TiO2 (nTi-0h~3h) 담체 에 V2O5와 WO3를 담지하여 V2O5-WO3/TiO2 탈질촉매를 다음과 같이 제조하였다. 먼저 WO3를 담지하기 위해 전구 체 AMT (ammonium metatungstate, >99 %, Sigma-Aldrich) 를 증류수에 용해하였다. TiO2 중량 대비 WO3를 2 wt% 담 지하고 2시간 상온에서 교반하여 WO3/TiO2를 제조하였다. 그 이후에 AMV (ammonium metavanadate, >99 %, Sigma- Aldrich)를 60 °C의 증류수에 용해시킨 후, 상온으로 냉각 되면 C2H2O4 (oxalic acid, >99 %, Sigma-Aldrich)를 첨가하 여 pH 2.5 조건에서 용해하였다. TiO2 중량 대비 V2O5를 0.5~1.5 wt% 되도록 담지하고 2시간 동안 교반하여 V2O5- WO3/TiO2 슬러리를 제조하였다. 교반 및 담지가 완료된 V2O5-WO3/TiO2 슬러리는 회전감압증류기를 사용하여 건 조된 V2O5-WO3/TiO2 분말을 제조하였다. 이 분말은 2 °C/ min 속도로 500 °C까지 승온한 후 공기 분위기에서 4시간 동안 소성하였다. 이와 같이 제조한 촉매는 VxWy/nTi로 표기하였으며 x, y는 담지량을 나타낸다. 이 제조한 촉매 는 VxWy/nTi-0h~3h로 표기하였다.
수계에서는 에탄올 용매와의 TiO2 분산성을 비교하였 을 때, TiO2 입자간 응집으로 인한 분산특성이 낮아져서 비 드밀링 없이 단순 분산된 TiO2 슬러리를 사용하였다. 상기 제조 방법과 동일하게 V2O5와 WO3를 함침하는 기존의 방 법으로14) 제조하였으며 VxWy/Ti로 표기하였다.
2.3. NH3 SCR 반응 활성 실험
본 연구의 고온 SCR 반응 실험에 사용한 고정층 반응기 에 공급되는 가스는 N2, O2, NH3, NO로 MFC (mass flow controller)를 사용하여 유량을 조절하였다. 가스관은 NO 와 NH3가 반응하여 생기는 NH4NO3, NH4NO2, NH4HSO4 와 같은 염의 생성을 방지하고 수분이 응축되지 않기 위하 여 열선밴드를 감아 300 °C로 일정하게 유지하였다. 반응 기는 내경이 15 mm 석영관을 사용하였으며 NO 농도는 가스분석기(TESTO 350K)를 사용하였으며 반응 전 투입 되는 가스들은 N2 가스를 이용하여 조정하였다.
본 실험은 공간속도 60,000 hr-1, O2 5 vol.%, NH3 300 ppm, NO 300 ppm, N2 balance에서 수행하였으며 반응 온도는 5 °C/min 속도로 PID 온도 조절기에 의해 상온에서 500 °C 까지 수행하였다. 촉매의 반응 활성도는 다음과 같이 백분 율로 전환하여 나타냈으며 식 (1)과 같이 정의하였다.
여기서, [NO]in 및 [NO]out은 촉매반응기 가스 주입구 및 배 출구에서 측정된 NO 가스농도를 의미한다.
2.4. 촉매 특성분석
TiO2 담체 및 촉매의 결정구조를 관찰하기 위하여 XRD (X-ray Diffraction, D8, ADVANCE, Bruker Co.)분석을 하 였으며 CuKα (l = 0.1506 nm) 방사선원, 40Kw X-ray 발생 기, 2q = 10~90°의 범위에서 5°/min의 주사속도에 의하여 측정되었다.
촉매의 비표면적 및 기공크기 측정은 Tristar 3000 (Micromeritrics Co.)을 사용하였으며 BET (Brunauer-Emmett- Teller)식을 이용하여 비표면적을 구하였다. 기공크기 분 포는 Kelvin식을 통해 유체의 meniscus의 평균반경과 상 대압력에서의 흡착층의 두께를 측정하였고 세공의 크기 를 계산하는 방법인 BJH (Barrett-Joyner-Halenda)법에 의 하여 계산하였다.
TiO2 분산상의 평균 입도와 분포도는 ELSZ (Otsuka Co.) 를 사용하였으며 분석 원리는 시료를 용매에 분산시킨 후 레이저가 통과한 후 입자크기에 따른 레이저의 산란각을 측정하여 분산된 TiO2의 평균입도(D50) 및 입도 분포를 측 정하였다.
촉매로 제조하였을 때 촉매의 형상과 크기를 확인하기 위하여 투과전자현미경(TF30ST, FEI Co.)을 사용하였으 며 가속 전압은 300 kV로 하였다.
수차보정 에너지여과 투과전자현미경(LIBRA 200 HT MC, Carl Zeiss Co.)의 Energy Dispersive Spectrometry (EDS) 기법을 이용하여 제조된 촉매의 Ti, V, W 원소의 성분 및 담 지된 원소의 분산특성을 확인하였다. 200 kV 가속전압의 STEM 모드에서 2 mm 크기의 전자빔 프로브로 EDS Mapping 분석을 실시하였으며 검출기는 X-Max 80T (Oxford Instr.)를 이용하였다.
촉매의 산화 환원 특성을 확인하기 위해 NH3 Temperature- programmed desorption (NH3-TPD)분석을 수행하였으 며 AutoChem II 2920 (Micromeritics)로 분석하였다. 촉매 의 흡착 수분을 제거하기 위해 O2/He을 50 cc/min 흘리며 300 °C까지 10 °C/min으로 승온한 후 30분 유지하였다. 이 후 반응기 온도를 상온으로 내린 후 10 vol.% NH3/He으로 1시간 동안 촉매에 NH3를 흡착시키고, He으로 퍼징하며 물리 흡착된 NH3를 배제시켰다. 이후 10 °C/min의 승온속 도로 500 °C까지 승온하며 탈착되는 NH3를 측정하였다.
촉매의 산화환원능력을 확인하기 위하여 Hydrogen Temperature- programmed reduction (H2-TPR)은 Auctochem 2920 (Micromeritics)로 분석하였다. 농도측정을 위한 검출기는 TCD (thermal conductivity detector)를 사용하였다. 측정에 앞서 O2/He 50 cc/min을 흘리며 300 °C까지 10 °C/min으로 승온하였다. 이후 상온으로 하온하여 10 vol.% H2/Ar 가스 를 50 cc/min을 지속적으로 흘리며 10 °C/min의 승온 속도 로 800 °C까지 승온하였으며 TCD로 소모된 H2의 농도를 확인하였다.
촉매 표면의 원소 및 산화가를 확인하기 위해 XPS (Xray Photoelectron Spectroscopy, Thermo Fisher Scientific, NEXSA Co.)로 관찰하였다. 측정조건은 50.0 eV (step 0.1 eV) 통과에너지, 50 ms 체류시간, 400 μm 스팟 크기에서 관찰하였다. 특히 촉매 내에 존재하는 V, O 원소의 결합에 너지와 피크세기를 비교관찰하였다.
촉매의 탈질반응에서 가스 분해 및 생성을 관찰하기 위 해 FT-IR (Varian 660IR, Agilent Co.)로 관찰하였다. 상기 의 2.3절의 탈질촉매 반응 조건에서 반응 후단에서 나오는 가스를 in situ FT-IR로 KBr이 장착된 유리관을 통과시켜 탈질 반응온도에 따른 NO, NH3, N2O 가스의 분해 및 생성 현상을 관찰하였다.
3. 실험결과 및 고찰
3.1. 촉매 담체로 사용된 나노분산 TiO2 제조 및 물리 화학적 특성 연구
기존의 탈질촉매에서 사용되는 TiO2 촉매 담체는 슬러 리 형태의 응집상을 사용하였으나, 본 연구에서는 비드밀 링을 통한 TiO2를 나노분산하여 제조한 후 분산 용매 및 비드밀링 전후의 분말 및 분산상의 물리화학적 특성을 관 찰하였다.
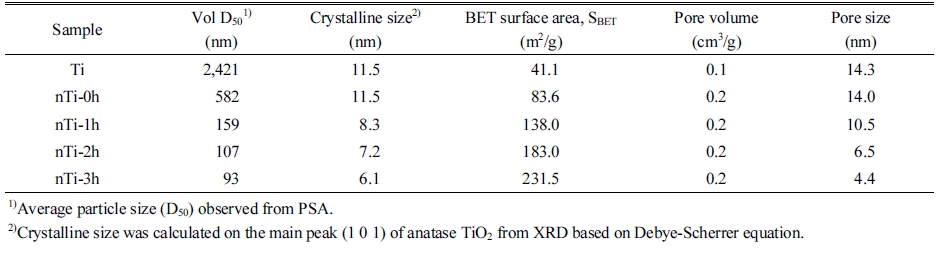
Fig. 1은 수계 및 에탄올 용매하의 TiO2 분산상을 밀링 없이 단순 분산한 Ti 및 nTi-0h와, 에탄올하에서 1~3시간 까지 비드밀링하여 제조된 nTi-1h~3h를 건조한 분말에 대 한 결정상, 결정립크기, 결정성 등을 XRD 피크로 관찰하 였다. 이들 시료의 XRD 피크는 모두 anatse (JCPDS card no. 21-1272)상과 일치하였다. 특히 nTi-1h~3h는 비드밀링 에 의한 물리적 에너지에서도 rutile 구조의 상전이는 없음 을 확인하였다. 모든 시료의 anatase TiO2의 회절면 (101) (2θ ≈ 25.3°)의 FWHM값을 Debye-Scherrer식을 이용하여 결정 크기는 계산하였다. 수계 및 에탄올하에서 밀링없이 단순 분산된 Ti 및 nTi-0h의 TiO2 결정 크기는 11.5 nm로 같이 계산되었으며, 비드밀링의 물리적인 힘에 의해 처리 된 nTi-1h~3h는 에탄올 용매하에서 밀링 시간이 1, 2, 3시 간으로 증가함에 따라 결정 크기는 각각 8.3, 7.2, 6.1 nm로 점차 감소함을 알 수 있었다. 이는 XRD 피크 세기의 감소 와 반가폭이 넓어짐을 통하여 TiO2의 결정 크기 및 결정성 감소가 있음을 확인할 수 있었다.
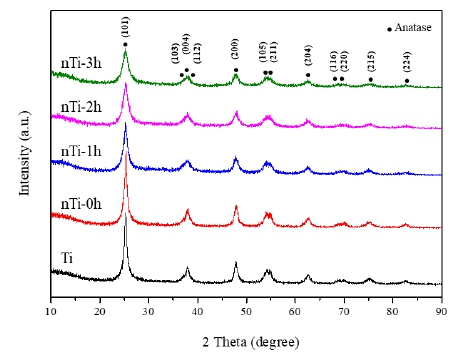
Fig. 1
Powder XRD patterns of TiO2 on [Ti] dispersed under water, [nTi-0h] dispersed under ethanol, and [nTi-1h~3h] bead-milled for 1~3h under ethanol.
Fig. 2는 에탄올 용매하에서 비드밀링 시간에 따라 제조 된 TiO2 (nTi-0h~3h) 분산상을 측정한 입도 분포도를 보여 주고 있다. Fig. 2의 에탄올 용매하에서 단순 분산된 nTi-0h 를 1~3시간 비드밀링하여 얻어진 nTi-1h~3h 분산졸의 평 균 입도를 비교하였다. 밀링 전의 nTi-0h 평균 입도는 582 nm였으며, 1~3시간 밀링 후에는 각각 159, 107, 93 nm 크 기로 평균입도가 감소함에 따라 분산성이 향상됨을 알 수 있다. 용매를 에탄올 대신에 수계하에서도 비드밀링 전후 TiO2 담체의 분산 특성을 비교하였으나, Ti 시료의 평균입 도(D50)는 밀링 전 2.4 μm와 3시간 밀링 후 9 μm로 분산되 지 않고 응집됨을 알 수 있었다(Fig. 2에 미포함). 특히, 수 계에 비하여 알코올계에서 TiO2 입자가 분산이 용이하였 는데 이는 에탄올의 에톡시 작용기가 TiO2 입자 표면에 흡 착되어 알콕시 작용기 간의 입체장해 효과에 영향을 받은 것으로 보인다.15,16)
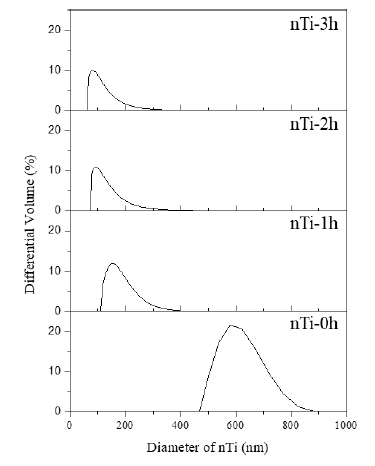
Fig. 2
Particle size analysis of TiO2 dispersion phase before [nTi-0h] and after [nTi-1h~3h] bead-milling for 1~3h under ethanol solvent.
Fig. 3은 수계 및 에탄올 용매하에서 비드밀링 없이 단 순 분산한 Ti 및 nTi-0h와 에탄올 용매하에서 비드밀링 시 간에 따라 제조된 nTi-1h~3h 입자들의 FE-SEM 이미지를 보여주고 있다. 수계의 Ti는 약 100 nm 크기의 입자들이 조밀하게 응집되어 있는 반면에, 에탄올의 nTi-0h는 상대 적으로 응집현상이 완화된 것으로 보인다. 이는 Fig. 2의 결과 설명과 같이 수계에서 2.4 μm 및 에탄올에서 582 nm TiO2 평균입도를 보이는 것과 간접적으로 일치함을 알 수 있다. 그리고, nTi-1h~3h의 1~3시간 동안 비드밀링하여 관 찰된 FE-SEM 사진에서 보는 바와 같이 밀링 전의 100 nm 입자들이 1시간 밀링 후의 nTi-1h는 50~100 nm 크기로 관 찰되었으며, 2시간 후의 nTi-2h는 10~100 nm, 3시간 후의 nTi-3h는 10~150 nm 입자크기 분포를 보였다. 이는 10 nm 크기 입자들의 재응집으로 인해 일부 입자들이 150 nm 크 기로 커짐을 의미한다. 이로 비드밀링에 의해 TiO2 입자크 기가 효과적으로 감소된 것을 확인할 수 있었으며, 적합한 밀링 시간은 XRD상의 결정성과 다음장의 탈질촉매 특성 을 고려하여 2시간이 적절한 것으로 고려하였다.

Fig. 3
FE-SEM images TiO2 powder for [Ti] dispersed under water, [nTi-0h] dispersed under ethanol, and [nTi-1h~3h] bead-milled for 1~3h under ethanol (white scale bar = 100 nm).
Fig. 4는 수계 및 에탄올 용매하에서 밀링 없이 단순 분 산한 Ti 및 nTi-0h와 에탄올 용매하에서 비드밀링 시간에 따라 제조된 nTi-1h~3h 분산상의 건조 분말에 대한 질소 흡탈착 등온선 및 세공분포도를 보여주고 있다. Fig. 4(a)의 Ti, nTi-0h는 질소 흡탈착 등온선이 type 2로 얻어진 반면, 비드밀링을 1~3시간 처리 후에 얻어진 nTi-1h~3h는 type 4 를 보여주고 있다. 이는 TiO2 담체 기공구조가 거대기공에 서 메조기공으로 변함과 동시에 비표면적이 증가함을 알 수 있다.17,18) Fig. 4(b)는 TiO2의 기공크기분포를 나타낸 것 이며, 밀링 전 Ti와 nTi-0h는 10~100 nm의 기공 분포를 보 인 반면에 nTi-1h~3h는 에탄올하에서 밀링된 TiO2의 나노 분말로 각각 10~30 nm, 3~15 nm, 3~6 nm의 기공분포를 보 였으며 밀링시간이 증가할수록 기공분포는 감소하였다. 특히, 비표면적이 높고 기공이 발달한 소재는 NH3-SCR 탈질분해, N2O 분해 등 다양한 분야에서 우수한 성능을 보 이는 촉매로 사용되고 있는 것으로 알려져 있다.19,20)
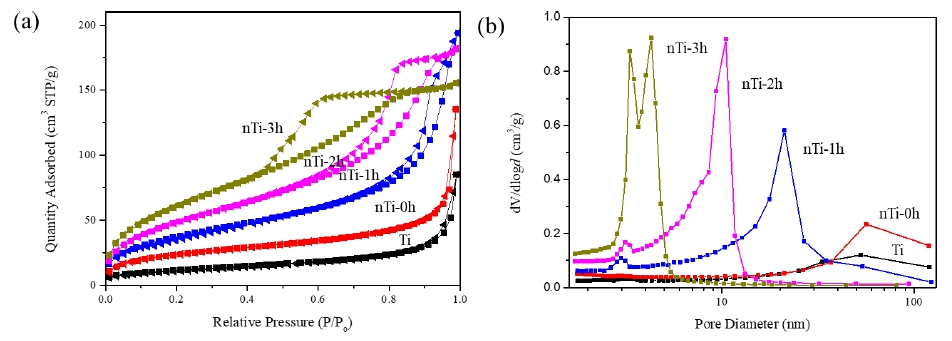
Fig. 4
(a) Nitrogen adsorption-desorption isotherms, and (b) Pore size distribution of TiO2 powder for [Ti] dispersed under water, [nTi-0h] dispersed under ethanol, and [nTi-1h~3h] bead-milled for 1~3h under ethanol.
Table 1은 Fig. 2와 Fig. 4의 TiO2 담체 분산 및 밀링에 의 한 결정 입자크기 및 평균 입도와 비표면적에 관한 물리화 학적 특성을 비교 정리하였다. 수계 및 에탄올 용매하에서 밀링없이 단순 분산한 Ti 및 nTi-0h 담체의 XRD 상의 결정 크기는 11.5 nm로 변화 없었으며, PSA 측정에서 수계 및 에탄올 용매하에서의 TiO2 분산상의 평균 입도는 약 2.4 μm에서 582 nm로 얻어졌다. 또한 이 분말들의 비표면적 특성은 41 m2/g에서 83.6 m2/g으로 증가함에 분산성 역시 에탄올 용매하에서 개선됨을 알 수 있다. 그리고, 에탄올 하의 비드밀링된 nTi-1h~3h의 분말들은 밀링 시간이 증가 함에 따라서 138.0 m2/g에서 231.5 m2/g로 비표면적이 증 가하였으며 측정된 기공 크기는 10.5 nm에서 3시간 밀링 후에는 4.4 nm로 감소함을 알 수 있다. 이는 Fig. 4(b)의 기 공분포와 비례하여 TiO2 담체는 거대기공에서 미세기공 이 형성되며 밀링이 진행됨에 따라 미세기공이 감소한 결 과와 일치하는 것을 확인하였다. 또한 밀링 시간이 증가할 수록 입자의 크기가 작아지면서 촉매에 존재하던 기공들 이 감소하였고 비표면적이 증가하여 촉매가 반응을 할 수 있는 표면적이 넓어짐으로써 촉매의 성능을 향상시킬 수 있음을 유추할 수 있다.
3.2. 나노분산 TiO2 담체로 제조된 V2O5-WO3/TiO2 촉매의 특성분석
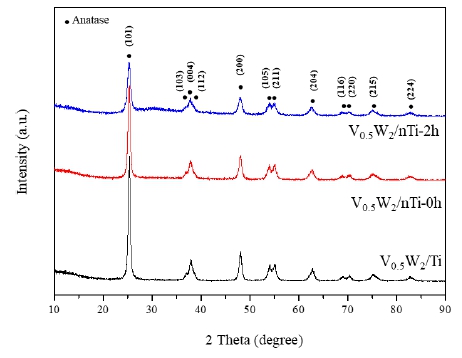
Fig. 5는 수계 및 에탄올 용매하에서 밀링없이 단순 분산 한 Ti 및 nTi-0h와 에탄올 용매에서 1~3시간의 밀링에 의해 제조된 nTi-1h~3h 담체상에 V2O5와 WO3를 함침하여 제 조된 V2O5-WO3/TiO2 (V0.5W2/Ti 또는 V0.5W2/nTi-0h~3h) 탈질촉매의 XRD 패턴을 나타내었다. Fig. 1의 결과와 동 일하게 촉매 제조를 위한 소성 후에도 TiO2 담체는 anatase 결정구조를 지니고 있으며 구조적인 변화는 없었다. 또한 바나듐 및 텅스텐 산화물을 담지한 후에도 균일하게 나노 분산되어 코팅됨으로 인해 V2O5 및 WO3 회절피크를 관찰 할 수 없었으며, TiO2 anatase 표면에 V2O5와 WO3가 무정 형으로 균일하게 담지되었음을 판단할 수 있다.
Fig. 6은 V0.5W2/Ti, V0.5W2/nTi-0h, V0.5W2/nTi-2h 촉매의 TEM 이미지를 보여주고 있다. V0.5W2/Ti와 V0.5W2/nTi-0h 촉매는 촉매 담체 TiO2의 분산 용매인 물과 에탄올을 사용 해서 분산하였으나, 입자 형상은 약 10 nm 크기의 나노입 자가 뭉쳐져서 약 100 nm 크기의 구형입자를 이루고 있으 며 입자 형상 및 크기에 차이가 없다. Fig. 6의 V0.5W2/nTi-2h 촉매는 에탄올하에서 2시간 밀링 및 나노분산 TiO2 담체 에 V2O5 및 WO3를 함침 및 소성하여 제조되었고, 촉매 분 말의 크기가 증가하지 않고 나노크기로 유지하면서 제조 되었음을 확인하였다.

Fig. 6
TEM images of V0.5W2/Ti, V0.5W2/nTi-0h, and V0.5W2/nTi-2h catalysts (white scale bar = 50 nm).
Fig. 7은 V1.5W2/nTi-2h 촉매의 TEM 내의 EDS Mapping 으로 Ti, V, W 원소분포도를 관찰하였다. Fig. 6 및 Fig. 7의 V1.5W2/nTi-2h의 TEM 사진에서 보는 바와 같이 10 nm 크 기의 나노입자들이 소성과정에서 일부 뭉쳐진 형태로 관 찰되며, V, W 원소는 TiO2 나노입자인 nTi-2h 상에 균일하 게 담지되었음을 확인할 수 있다.
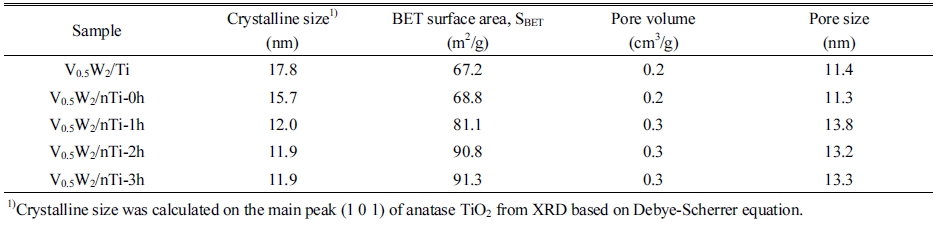
촉매 담체인 Ti, nTi-0h, nTi1h~3h 분산상의 평균 입도 차 이에 따라 촉매를 담지하여 제조한 다양한 촉매의 물리적 성질은 Table 2에 나타내었다. 촉매에서 TiO2 결정 크기는 Table 1과 같이 XRD 패턴에서 Debye-Scherrer식에 의해 anatase TiO2의 (101)면 2q = 23.5°에서 계산하였다. V0.5W2/ Ti 촉매의 결정 크기는 17.8 nm였으며, 밀링시간별로 제조 한 V0.5W2/nTi-0h~3h 촉매는 15.7 nm에서 11.9 nm로 감소하 였다. 촉매의 기공 크기는 소성 과정 중 나노입자가 뭉치면 서 입자 크기가 증가하여 기공 크기가 증가한 것으로 판단 된다. nTi의 밀링시간에 따라 제조된 다양한 촉매의 비표면 적은 68.8 m2/g에서 91.3 m2/g으로 증가하였으며 이로 인해 SCR 반응에 참여하는 활성점이 증가하였음을 알 수 있다.
3.3. 나노분산 TiO2 담체로 제조된 V2O5-WO3/TiO2 촉매의 탈질 효율 및 특성평가
지금까지 많이 알려진 탈질촉매 제조방법으로 활성금 속인 바나듐 및 텅스텐 산화물을 담체인 TiO2에 담지하여 제조해왔다. 본 연구에서는 담체인 TiO2를 비드밀링에 의 해 나노분산시켜 담체 분산상의 평균 입도에 따라 제조된 촉매들의 탈질촉매 활성 및 촉매 특성을 비교 평가하였다.
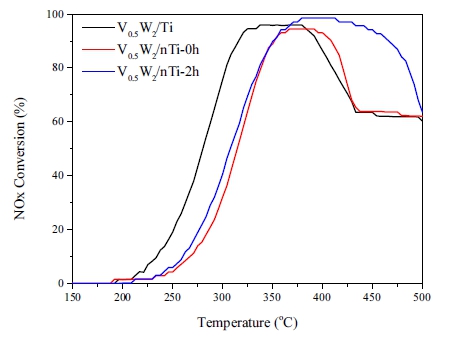
Fig. 8은 탈질촉매 V0.5W2/Ti, V0.5W2/nTi-0h, V0.5W2/nTi- 2h의 반응온도 변화에 따른 NH3-SCR 반응에 의한 NOx 전환율을 그래프로 나타내었으며 세 촉매의 탈질 전환율 은 350~412 °C에서 94 % 이상을 보인다. V0.5W2/Ti는 수계 에서 밀링없이 단순 분산된 TiO2 담체(Ti)로 제조한 V0.5W2/ TiO2 촉매의 경우 상용화된 촉매처럼 350~380 °C에서 96 % 의 최대 탈질 전환율을 보여주고 있다. 그리고 에탄올에서 밀링없이 단순 분산된 TiO2 담체(nTi-0h)로 제조된 V0.5W2/ nTi-0h 촉매는 365~391 °C에서 94.5 %와 2시간 비드밀링 한 TiO2 담체(nTi-2h)로 제조된 V0.5W2/nTi-2h 촉매는 379~ 412 °C에서 98.6 % 최대 탈질 전환율을 각각 보여주고 있 다. 특히, 수계에서 단순 분산한 Ti 담체에 비해 에탄올 용 매하에서 분산한 nTi-0h 및 밀링 2시간으로 나노분산시킨 nTi-2h 담체로 제조한 촉매일수록 NO의 최대 분해온도가 고온으로 이동함을 알 수 있었다. 이에 관하여 촉매의 TiO2 평균 입도와 탈질 효율의 특성과의 상관성을 Fig. 9 에 언급하였다.
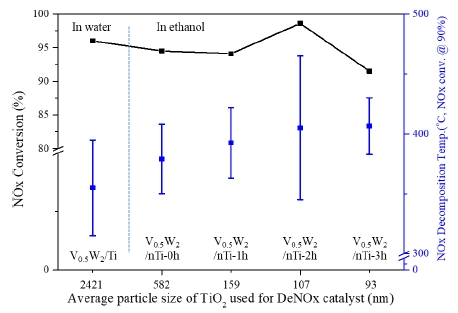
Fig. 9
Graphs of relationship between TiO2 particle size and NOx decomposition temperature at 90 % NOx conversion based on Fig. 8.
TiO2 담체의 평균 입도 (D50)를 달리하여 제조한 V0.5W2/ Ti 및 V0.5W2/nTi-0h~3h 촉매들의 NOx 분해온도 및 효율 에 대한 상관성을 Fig. 9에 나타내었다. 이 촉매들은 90 % 이상 NOx 전환율에서 분해온도는 D50이 2.4 μm인 Ti로 제 조한 V0.5W2/Ti 촉매의 경우 315~395 °C, D50이 582 nm에 서 93 nm인 nTi-0h~3h로 제조한 V0.5W2/nTi-0~3h 촉매는 350~408 °C에서 383~430 °C로 관찰된다. 이는 TiO2 분산 상의 평균 입도가 감소함에 따라 NOx 분해온도 영역대가 높아짐을 알 수 있다. 또한 D50이 107 nm인 nTi-2h로 제조 한 V0.5W2/nTi-2h 탈질촉매의 NOx 분해효율 증가 및 온도 윈도우가 넓어지면서 최적화됨을 알 수 있었다. 여기서 D50이 93 nm인 nTi-3h로 제조한 V0.5W2/nTi-3h 탈질촉매 효율이 서서히 낮아지는 이유는 과밀링으로 인해 TiO2 결 정성 및 비표면적 및 기공제어 등에 서서히 영향을 미치는 것으로 여겨진다. 촉매의 탈질 반응에 참여하는 산소종 중 hydroxyl과 같은 표면 산소종은 촉매 반응에 있어 산소를 쉽게 전달하는 것으로 알려져 있다.21) 이는 촉매 담체인 TiO2의 밀링과정에 의해 TiO2 입도가 감소하고 비표면적 증가함에 따라 hydroxyl 작용기의 밀도가 증가하여 활성 종 V2O5가 담지될 때 분산에 영향을 미치면서 표면산소종 이 많은 V0.5W2/nTi-2h 촉매가 넓은 온도에서 쉽게 산화환 원 반응을 효과적으로 유도한 것으로 판단된다. 따라서 TiO2 담체의 분산이 고온 영역의 SCR 반응 활성에 영향을 미쳤다고 판단할 수 있다. 동일한 양의 바나듐을 담지하여 제조된 촉매는 전구체의 제조방법 및 분산도에 따라 활성 온도에 차이가 있음을 확인하였고 위와 같은 차이의 원인 을 알아보기 위하여 NH3-TPD, XPS, FT-IR로 분석하여 비 교 관찰하였다.
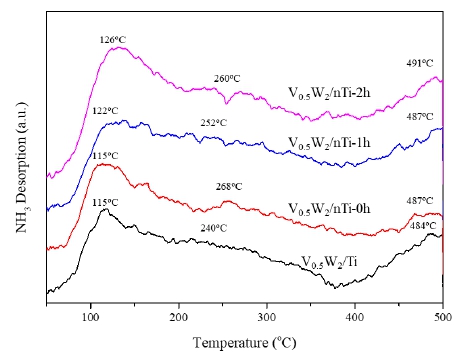
탈질촉매 표면의 산점 특성은 NH3 흡착에 중요한 역할 을 하며 NH3 탈착 피크의 면적과 피크 위치는 촉매 산점의 양과 세기와 관련이 있다. 이를 확인하기 위해 Fig. 8의 탈 질촉매의 특성을 NH3-TPD로 실험하여 Fig. 10에 나타내 었다. 100~500 °C의 탈착 피크는 TiO2에 담지된 활성 금속 에 따라 다르며 이는 산점의 양과 세기에 다른 영향을 미치 는 TiO2 담체와 금속 사이에 강력하고 다양한 상호작용을 의미한다. 또한 Fig. 4(b)에서 비드밀링하에서 제조된 nTi 에서 관찰된 미세기공 TiO2에 담지된 VOx에 대하여, 김도 희 그룹에서는 미세다공성 TiO2상의 VOx 종은 Brønsted 산점을 유지하여 촉매에 흡착된 NH3 종을 고온까지 쉽게 제공할 수 있어 안정적인 DeNOx 효율을 얻을 수 있다고 보고하였다.22) 에탄올에서 밀링한 TiO2로 제조된 촉매의 NH3 탈착 피크는 수계에서 제조한 TiO2 제조 촉매와 비교 해 전반적으로 높은 온도에 나타났으며 400 °C 이후의 피 크 면적을 비교하였을 때 V0.5W2/nTi-2h 촉매는 V0.5W2/Ti 촉매보다 약 2.1배 증가하였고 전체 면적은 1.9배 더 넓었 다. 이는 TiO2 담체를 밀링하여 촉매 표면에 중간-강산의 산점이 증가하여 중고온에서 더 높은 탈질 제거율을 보인 것으로 보인다.23)
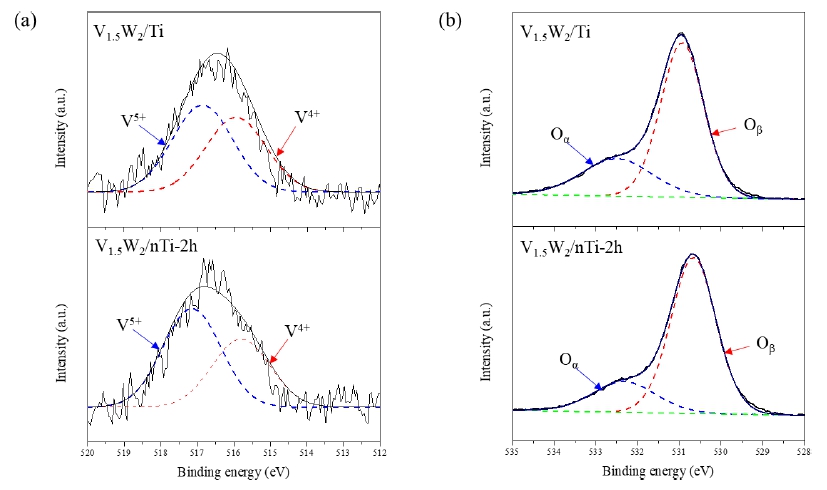
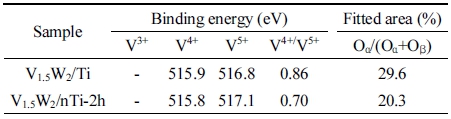
담지된 V 함량이 0.5 %인 촉매로 XPS 분석을 진행하였 으나 피크 분해능이 낮아 피크 확인이 어려워 V 함량을 1.5 %로 높인 V1.5W2/Ti 및 V1.5W2/nTi-2h 촉매의 XPS 분석결 과를 Fig. 11에 나타내었다. 이들 촉매의 탈질 전환율은 Fig. 8과 유사한 결과를 얻었다. Fig. 11(a)의 XPS 분석 결과 V2p 분석에서 V4+의 515.8~515.9 eV 피크와 V5+의 516.8~ 517.1 eV가 피크가 공존하는 것을 확인할 수 있었다. Fig. 11(a)의 V2p의 피크 면적비를 계산하여 Table 3으로 정리 하였으며 V4+/V5+ 비율은 V1.5W2/Ti 촉매 0.86, V1.5W2/nTi- 2h 촉매 0.70로 나노분산된 nTi-2h로 촉매를 제조하였을 때 V5+의 비율이 증가하였다. 본 연구진이 게재한 논문에 서는13) 저온에서 높은 탈질 제거율을 가진 나노플레이크 형태 V2O5를 WO3/TiO2에 담지하여 제조한 촉매의 XPS 분석 결과 V4+의 비율이 V5+보다 높았으며 본 연구와 상반 되는 결과임을 확인하였었다. 촉매 표면의 V5+는 NH3-SCR 반응에 영향을 주는 암모니아 종의 탈수소(dehydrogenation) 과정을 촉진하는 효과를 가지고 있는 것으로 보고되 고 있다.24) NH3의 탈수소로부터 생성된 NH2는 SCR 반응의 중간 생성물로서 촉매에 흡착된 NO와 쉽게 반응하여 N2 및 H2O로 분해되며 V5+는 열적 안정성을 향상시켜 중고온 에서 탈질 효율이 증가한 요인으로 판단된다.25) Fig. 11(b) 의 O1s 분석 결과 두 촉매 모두 화학흡착산소종의 513.3~ 532.0 eV 피크와 격자 산소종의 529.6~530.1 eV 피크가 존 재하였으며 그 면적 비율은 Table 3에 나타내었다.26) 두 촉 매의 피크 면적을 계산한 Oα/(Oα+Oβ) 비율이 V1.5W2/Ti 촉 매의 29.6 %에서 V1.5W2/nTi-2h 촉매의 20.3 %로 감소하여 V1.5W2/nTi-2h 촉매가 더 높은 격자산소종(Oβ)을 가지고 있는 것을 알 수 있다. 또한 격자 산소(Oβ)는 촉매 표면에 서 NH3 또는 NO의 흡착 및 활성을 촉진하여 촉매 효율을 향상시킬 수 있다고 보고되어 V1.5W2/nTi-2h 촉매의 탈질 효율 증진에 영향을 미친 것으로 판단된다.27,28)
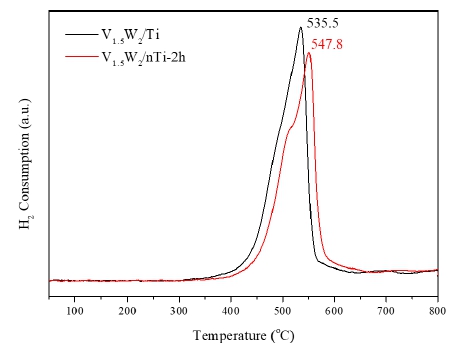
NH3-SCR 반응에서의 촉매의 산화 및 환원 특성을 비교 관찰하기 위해 H2-TPR을 분석하여 Fig. 12에 나타내었다. V1.5W2/Ti 촉매는 535.5 °C와 V1.5W2/nTi-2h 촉매는 547.8 °C에서 환원피크가 관찰되었으며 최대 환원 피크는 TiO2 의 평균 입도가 2.4 μm에서 107 nm로 감소함에 따라 약 12 °C 고온으로 이동되는 것을 확인하였다. 이를 통해 나노분 산상을 지닌 nTi-2h 담체를 적용한 V1.5W2/nTi-2h 촉매가 NH3-SCR 탈질 반응 중 더 높은 온도에서 산소를 쉽게 이용 할 수 있어 고온에서 높은 효율을 얻은 것으로 판단된다.
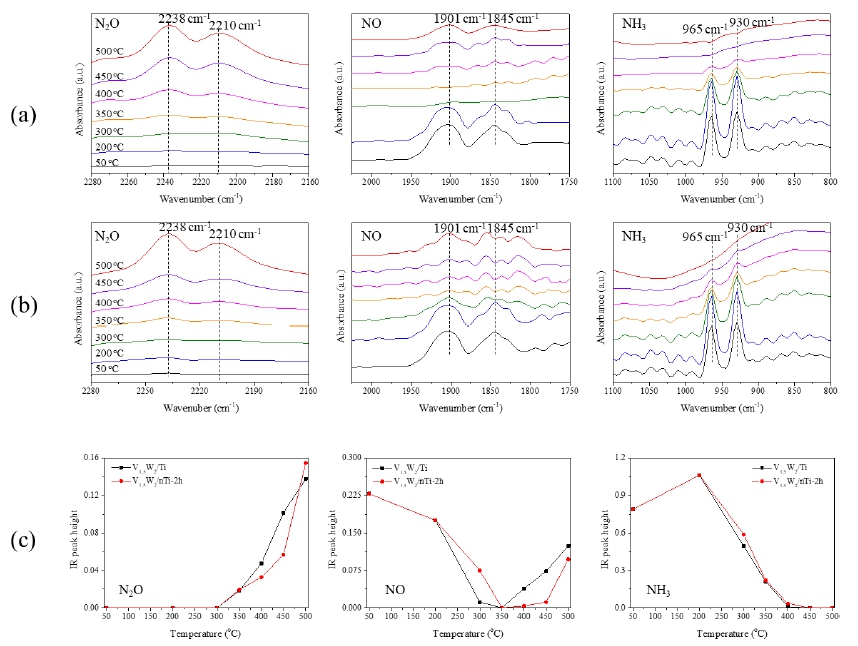
Fig. 13은 V1.5W2/Ti 및 V1.5W2/nTi-2h 촉매의 in situ FT-IR 스펙트럼에서 관찰된 NO, NH3, N2O 가스의 분해 및 생성 됨에 따른 피크를 비교 관찰하였다. V2O5/TiO2계 촉매를 이용하는 NH3-SCR 공정으로부터 발생되는 N2O는 주로 NOx가 NH3와 반응하여 생성되거나 NH3의 산화로 생성 된다.29) 상기 반응을 통한 N2O 발생정도는 촉매의 특성과 반응조건 등에 따라 달라질 수 있으며 촉매 담체의 분산정 도에 따라 N2O 배출 차이를 FT-IR로 확인하였다. 특히, Fig. 13(b)의 나노분산 촉매 담체인 nTi-2h가 적용된 V1.5W2/ nTi-2h 촉매의 경우 400 °C 이후 반응온도에서 N2O가 형 성되면서 450 °C에서 발생량이 Fig. 13(a)의 V1.5W2/Ti 촉 매에 비해 상대적으로 적게 발생하였다. 이는 다공성 TiO2 담체하에서 촉매 표면에 바나듐 종의 특성과 구조제어가 용이하여 bulk-like V2O5 형성을 억제하였고 Brønsted 산 점이 존재하여 열적으로 안정적인 촉매로 NH3-SCR 반응 에서 N2O 형성이 억제되었다고 보고 하였다.22) NO의 경우 Fig. 13(a)의 V1.5W2/Ti 촉매는 300 °C부터 감소하여 350 °C 에서 완전히 분해되었고, Fig. 13(b)의 V1.5W2/nTi-2h 촉매 는 350 °C부터 감소하여 400~450 °C에서는 NO가 완전히 분해되어 피크가 관찰되지 않았다. Fig. 13(c)는 Fig. 13(a) 와 Fig. 13(b)의 두 촉매 반응온도별 NO, NH3, N2O 피크 높 이 차이를 비교하여 정리하였다. Fig. 13(c)의 NO 결과는 Fig. 8의 탈질전환율 그래프와 일치하는 결과를 보이고 있 으며 V1.5W2/nTi-2h 촉매는 400 °C 이상의 고온에서 검출 되는 NO의 농도가 낮아 N2O 생성량이 적어 NO 분해에 효 과가 있음을 확인하였다.
4. 결 론
에탄올 용매하에서 비드밀링으로 나노분산된 TiO2 (nTi) 분산상에 담지된 활성종 V2O5와 WO3 (V0.5W2/nTi) 촉매를 제조하여 기존의 수계에서 단순 분산된 V0.5W2/Ti 촉매와 비교하여 TiO2 분산상의 평균 입도와 최고 탈질 분 해온도와의 상관성을 통해 NOx 활성 특성을 연구하였다. 수계 및 에탄올 용매하에서 분산한 밀링 전 Ti 및 nTi-0h의 평균 입도(D50)는 2.4 μm 및 585 nm을 보였으며, 에탄올하 에서 2시간 비드밀링하였을 때 nTi-2h의 D50은 107 nm로 감소된 나노분산 졸을 얻을 수 있었다. 비드밀링에 의한 TiO2 담체의 물리화학적 특성은 비표면적은 증가하고 기 공구조는 거대기공에서 메조기공으로 변하는 것을 BET 를 통하여 확인하였으며 결정크기도 11.5 nm에서 7.2 nm 로 감소하였다. 이를 담체로 적용하여 촉매를 제조한 후 탈질 효율을 평가하였을 떄, V0.5W2/Ti 촉매는 315~395 °C, V0.5W2/nTi-2h 촉매는 345~465 °C에서 90 % 이상의 탈질 전환율을 나타내어 탈질 효율이 증가하고 최고 분해온도 는 고온으로 이동함을 확인하였다. 이에 대한 탈질 특성을 규명하기 위하여 NH3-TPD, H2-TPR, XPS, FT-IR로 평가 하여 비교 관찰하였다. 이들 촉매의 NH3 흡착량을 NH3- TPD로 확인하였으며 V0.5W2/nTi-2h 촉매의 흡착 면적은 V0.5W2/Ti 촉매보다 약 2.1배 증가하여 TiO2 담체 밀링으 로 인해 촉매 표면의 중간-강산 산점이 증가함을 확인하 였다. H2-TPR에서는 V0.5W2/nTi-2h 촉매가 V0.5W2/Ti 촉매 보다 환원 피크의 위치가 고온으로 이동하였으며 V0.5W2/ nTi-2h 촉매가 더 높은 온도에서 산소를 쉽게 이용할 수 있 어 고온에서 높은 탈질 효율을 얻은 것으로 판단된다. XPS 상의 V2p 분석결과에서 V4+/V5+의 피크면적비가 V1.5W2/Ti 촉매는 0.86과 V1.5W2/nTi-2h 촉매는 0.70로 각각 얻어졌다. V5+의 증가는 촉매의 열적 안정성을 향상시키는 요인이며 암모니아 종의 탈수소 과정을 촉진하기 때문에 V1.5W2/ nTi-2h 촉매의 반응활성 온도 이동과 중고온에서 높은 탈 질 효율을 갖는 요인으로 판단된다. O1s 분석결과에서 Oα/ (Oα+Oβ) 비율은 V1.5W2/Ti 촉매가 29.6 %와 V1.5W2/nTi-2h 촉매는 20.3 %로 각각 얻어졌으며, NH3 및 NO 흡착을 촉 진하는 격자 산소종(Oβ) 양이 증가하여 촉매의 탈질 효율 증가에 기여함을 확인하였다. FT-IR에서 V1.5W2/Ti의 NO 는 300 °C부터 감소하여 350 °C에서 완전히 분해되었고, V1.5W2/nTi-2h 촉매는 350 °C부터 감소하여 400~450 °C에 서 분해되어 촉매의 반응온도에 따른 탈질 전환율과 유사 한 결과를 보이고 있다. 또한 400 °C 이상의 온도에서 N2O 가 발생하는 것을 확인하여 V1.5W2/nTi-2h 촉매가 더 낮은 농도의 N2O를 생성함을 관찰하였다. 이는 비드밀링 과정 에서 제어된 미세기공 TiO2 담체로 인해 촉매 표면의 바나 듐 종이 Brønsted 산점을 유지함과 V1.5W2/nTi-2h 촉매의 열적 특성과 상관성이 있음을 확인하였다. 400~450 °C의 온도에서 검출되는 NO 농도가 낮으므로 N2O 발생량이 적어 NO 분해에 효과가 있음을 알 수 있다. 따라서 TiO2를 비드밀링하여 나노분산된 nTi 적용 탈질촉매는 중고온에 서 활성온도의 증가 및 담체상에 촉매의 분산성을 높여 탈 질 효율에 향상시킬 수 있음을 확인하였다.