1. 서 론
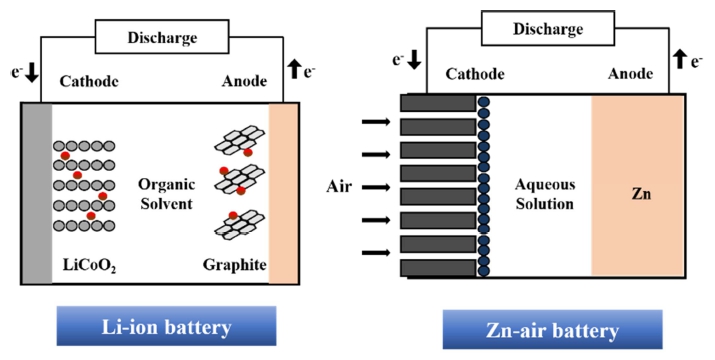
휴대용 전자기기 및 전기 자동차 시장의 성장에 따라 에너지 저장장치에 대한 관심이 높아지고 있으며, 향후 에도 계속 증가할 것으로 전망된다.1,2) 따라서 에너지 저 장 기술은 현대 사회에서 중요한 연구 주제로 각광받고 있다. 전지는 에너지 저장 매체로 활용되고 있으며 현 재 리튬이온 전지가 가장 많이 사용되고 있다. 하지만 리튬 매장량의 한계가 있고 환경에 유해한 물질을 사용 한다는 단점을 가지고 있기에 차세대 전지에 대한 개발 이 필요하다. 차세대 전지로써 나트륨이온 전지, 리튬-황 전지, 리튬-공기 전지, 아연-공기 전지 등이 주목을 받 고 있다. 리튬이온 전지와 아연-공기 전지는 Fig. 1과 같 은 구조를 가지며, 아연은 높은 에너지 밀도, 풍부한 매 장량, 친환경성, 저렴한 가격 등의 이점으로 전지의 음 극으로 널리 사용된다.3,4)
아연-공기 전지는 공기 양극, 아연 음극, 염기성 전해 질과 분리막으로 구성되고, 방전 과정에서 양극과 음극 은 다음과 같은 산화, 환원 반응이 일어난다.5,9)
양극: O2 + 2H2O + 4e− → 4OH− Ecathodic = 0.40 V
음극: Zn + 4OH− → Zn(OH)42− + 2e− Eanodic = 1.25 V 음극: Zn(OH)42− → ZnO + H2O + 2OH−
전체반응식: 2Zn + O2 → 2ZnO Eoverall = 1.65 V
이론 전압의 경우 1.65 V이지만, 실제 개방 회로 전압 측정 시 1.45 V로 떨어지며, 방전 시 1.35 V 이하로 공 급된다. 아연-공기 전지는 양극, 음극, 전해질, 분리막으 로 구성된다. 양극은 catalytic active layer(CAL)와 gas diffusion layer(GDL)로 구성된다. gas diffusion layer로 는 carbon particle과 hydrophobic organic material로 구성된 polytetrafluoroethylene(PTFE)이 쓰인다.6) CAL 에서는 GDL을 통해 확산된 산소와 음극으로부터 방출 된 전자가 만나는 oxygen reduction reaction(ORR)과 oxygen evolution reaction(OER)이 일어난다.7) 공기 중 산 소를 반응물로 사용하는 양극은 ORR과 OER을 위한 다 공성의 구조를 가져야 한다. ORR은 4-electron pathway 와 2-electron pathway의 두 메커니즘을 따르며, 반응이 매우 느리고 높은 과전압이 요구된다.8) 분리막은 젖음성 이 좋아야 하고 OH− 이온만 이동하여야 한다. 또한, 적 절한 기공 크기와 높은 이온 전도성을 나타내지만, 전 기화학 반응에서는 비활성을 띄어야 한다. polypropylene 과 polyethylene재질의 폴리머는 적절한 기공 크기와 저 렴한 가격을 갖기 때문에 분리막으로 널리 사용된다. 전해질은 전지의 보존 수명을 향상시키고 부식 속도를 저하시키며 자가 방전 효과가 있는 hydroxide 용액이 많 이 사용된다. potassium hydroxide, lithium hydroxide, sodium hydroxide가 대표적으로 쓰이며, 이 중 potassium hydroxide가 이온 전도도가 가장 높기 때문에 많이 사 용된다. 염기성 전해질 내에서 아연 음극의 부식 및 hydrogen evolution reaction(HER)은 자연스러운 반응이 다. 이러한 부반응은 아연-공기 전지의 자가 방전을 가 속화시키기 때문에 억제되어야 한다.7,9) 전해질의 농도는 부식 억제뿐만 아니라 전지의 성능에 직접적인 영향을 미친다. 또한, 전해질에서 발생하는 문제점은 점도 외에 도 용매로 사용하는 물에 의해서도 발생한다. 문제를 해 결하기 위해 용매로 사용되는 물을 공급해주거나 전해 질 내에 gelling agent를 첨가해 젤 상태의 전해질을 만 들어 수분 손실을 방지하는 방법이 있다. 이러한 이유 로 전도도와 점도의 영향을 모두 고려하여 전해질의 농 도를 설정해 주어야 한다. 따라서 전해질 농도 제어를 통한 전지의 전기화학적 거동에 미치는 영향에 대해 연 구하였다.
2. 실 험
2.1 전해질 제조
전해질의 농도가 아연-공기 전지의 거동에 미치는 영 향을 파악하기 위해 6 M, 7 M, 8 M, 9 M의 KOH 용 액을 각각 제조하였다. 각각의 제조된 용액에 gelling agent인 polyacrylic acid를 혼합해주었으며 potassium hydroxide용액과 polyacrylic acid를 각각 15.5 g 및 0.5 g으로 정량 후 24시간 동안 magnetic bar와 stirring machine을 이용해 교반 시켜 젤화 된 전해질을 제조하 였다.
2.2 아연-공기 전지 조립
아연-공기 전지의 구성은 Fig. 2와 같으며 다음과 같 은 순서로 진행되었다. bottom part에 볼트를 끼운 후, bottom part 가운데에 음극 집전체인 nickel mesh를 적 층해주었다. 적층한 nickel mesh 위에 가운데가 뚫려있 는 electrode container를 올려주었고, 이후 zinc powder 7 g과 젤화 된 전해질 0.65 ml를 일회용 사발에 넣고 균 일하게 섞어주었다. 혼합한 slurry를 electrode container 를 제외한 nickel mesh 위에 도포해주었고 그 위에 분 리막을 얹어주었다. 분리막 위에 air cathode를 적층해 주 었고, top part를 덮은 후 너트를 조여 아연-공기 전지 를 조립하였다.
2.3 방전 용량 및 자가 방전 용량 측정
아연-공기 전지의 전해질 농도에 따른 방전 용량을 관찰하기 위해 gelling agent가 포함된 전해질 6 M, 7 M, 8 M, 9 M을 이용해 네 종류의 cell을 제작하였다. 제조된 네 종류의 cell을 제조 후 storage 없이 방전시 킨 cell의 용량과 상온에서 6시간 storage를 시킨 이후 방 전 용량을 측정하여 비교하였다. Electrochemical analyzer (COMPACTSTAT, IVIUM technologies)를 이용하여 방 전용량을 분석했으며, 40 mA/cm2의 전류밀도를 사용하여 0.2 V의 전압까지 측정을 진행하였다.
2.4 부식 측정
전극과 전해질 사이에서 발생하는 수소 가스를 포집 하기 위해 Fig. 3과 같이 실험을 진행하였고, 실험 기 구로서 glass vial, rubber septa, syringe를 사용하였다. glass vial 안에 zinc powder를 넣어준 후 6 M, 7 M, 8 M, 9 M의 potassium hydroxide 용액을 채워주었다. 이 후 vial의 입구를 rubber septa로 밀폐시키고 syringe를 체결했다. syringe의 piston을 통해 수소 가스 발생량을 관찰하였으며, 8시간 동안 30분 간격으로 확인하였다.10,11)
3. 결과 및 고찰
3.1 방전 거동
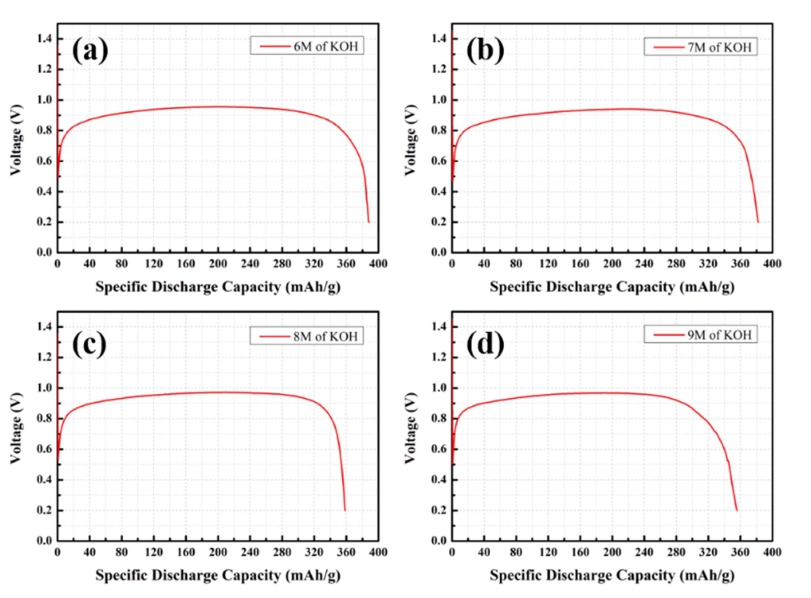
아연-공기 전지의 용량을 측정하기 위해 젤화 된 전 해질의 몰 농도를 변수로 하여 방전 성능을 관찰하였 다. 용액의 농도가 증가할수록 전도도가 증가하여 용량 이 증가할 것 같지만, Fig. 4에서 전지의 방전 용량은 6M의 전해질을 사용했을 때 가장 높고 농도가 증가할 수록 줄어드는 것을 알 수 있다. 선행 연구 논문에 따 르면 25 ºC에서 KOH 용액의 농도에 따른 점도 특성을 보고하였는데, 8 M의 KOH 수용액과 16 M의 KOH 수 용액의 점도는 각각 1.46 mPa 및 4.06 mPa로 약 두 배 가 증가하며, 이는 높은 점도에서 OH−이온의 이동의 어 려움을 말한다.6) 즉, 전해질의 점도가 증가하면 높은 전 류 밀도에서 cell 성능에 부정적인 영향을 주는 것을 알 수 있다.12) 따라서 6 M보다 높은 농도를 갖는 KOH 용 액을 사용하여 cell을 제조할 경우 점도가 증가하여 이 온의 이동이 방해를 받기 때문에 전도도가 감소하여 용 량이 감소함을 알 수 있다.
3.2 자가방전 거동
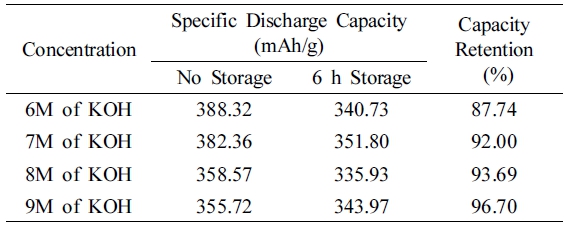
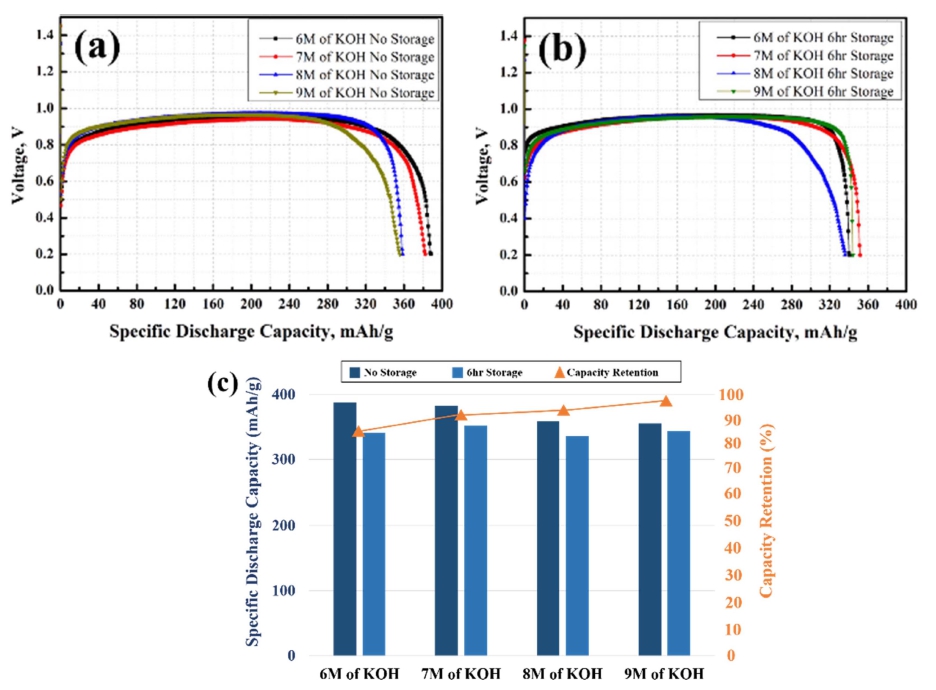
Table 1은 Fig. 5를 통해 6시간 동안 storage를 시킨 cell과 storage를 하지 않은 cell의 방전 비용량과 용량 보존율을 측정하여 비교한 값을 나타낸 것이다. 자가 방 전 거동을 측정하기 위해 storage를 시키지 않은 cell과 6시간 동안 storage를 시킨 cell의 용량을 비교하였다. 9 M의 KOH를 전해질을 사용한 cell의 방전 비용량은 355.72 mAh/g을 보였으며, 6시간동안 저장한 cell은 343.97 mAh/g 의 용량을 나타냈다. 이를 토대로 용량 보존율을 계산하였을 때 96.70 %로 시도된 물질 중 가장 우수한 값을 보였다. 6 M의 KOH를 전해질로 사용한 cell이 방 전 비용량은 388.32 mAh/g으로 가장 높지만, 6시간 저 장 후에는 340.73 mAh/g 의 용량을 나타냈으며 용량 보 존율이 87.74 %로 가장 낮은 값을 갖는다. 전해질의 농 도가 증가할수록 점도가 증가하며, 이에 따라 아연의 부 식이 억제되기 때문에 높은 농도의 전해질을 사용했을 때 우수한 용량 보존율을 나타내는 것으로 판단된다. 자 가 방전에 영향을 미치는 hydrogen evolution reaction (HER) 이 전해질의 농도가 증가할수록 억제되어 자가 방 전이 억제되는 것이라고 추론할 수 있다.
3.3 부식 거동
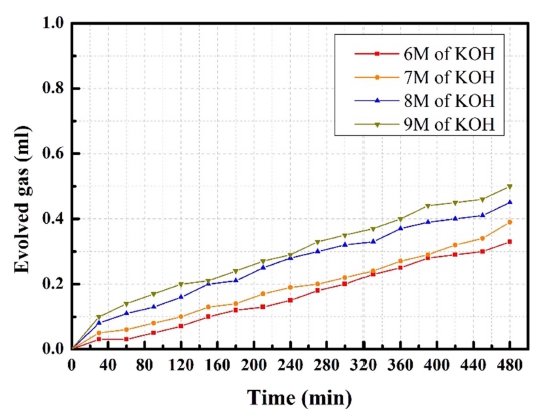
아연 음극은 전해질과 접촉 시 Zn + 2H2O → Zn(OH)2 + H2↑와 같은 수소발생 반응을 수반하며 동시에 음극의 부식을 일으킨다. 이는 아연-공기 전지의 수명을 저해하 는 이유 중 하나이다. 전지의 수명을 향상시키기 위해 수소 가스 발생을 제어할 수 있는 최적의 전해질 농도 를 찾는 것이 필요하다. 부식 속도는 전해질에서 zinc powder의 시간에 따른 수소 가스 발생을 부피 단위로 측 정하여 알 수 있다. 수소 가스를 포집하기 위해 syringe 와 vial을 사용하여 실험을 수행하였으며 그 결과는 Fig. 6에 나타내었다. glass vial 안에 zinc powder를 넣어 준 후 6 M, 7 M, 8 M, 9 M의 KOH 용액을 각각 채워 syringe의 piston을 통해 수소 발생량을 관찰하였다. 8시 간 동안 30분 간격으로 piston의 변화를 기록하였으며, KOH의 농도가 증가할수록 수소 발생량이 증가하는 현 상을 보여준다.10,11) 즉, gelling agent를 포함시키지 않은 전해질을 이용하였을 때 아연의 부식은 9 M의 KOH를 포함하는 vial에서 가장 많이 일어나는 것을 관찰할 수 있었다.
4. 결 론
본 연구는 아연-공기 전지의 전해질의 농도의 조절을 통해 전기화학적 및 자가방전 거동을 개선시키고자 하 였다. 전해질의 농도가 증가할수록 이온 전도도가 높아 지지만, 일정 농도 이상이 되면 점도의 증가로 인해 OH− 이온의 움직임에 저해가 된다는 단점이 존재한다. 일반 적으로 사용되는 수계 전해질이 아닌 전해질과 gelling agent인 polyacrylic acid를 교반시켜 젤화된 전해질을 사 용하였다. gelling agent가 포함되지 않은 KOH와 zinc powder의 부식 반응을 관찰한 결과 농도에 따라 수소 발 생량이 높아지는 경향이 관찰되었다. 또한, 젤화 된 전 해질의 농도에 따른 용량 거동을 관찰하였다. 7 M의 KOH를 전해질로 넣은 cell은 382.36 mAh/g으로 6 M과 유사한 높은 용량을 가지며, 6시간의 storage 이후에도 351.80 mAh/g으로 92.00 %의 우수한 용량 보존율을 보 여주며, gelling agent를 포함하는 전해질로 구성되어 수 분 손실이 적고 안정성 있는 점도로 인해 우수한 이온 전도도를 가져 OH−의 손실이 적은 전해질의 농도는 7 M 임을 알 수 있다. 따라서 종합적 판단 결과, 전해질로 7M의 젤화 된 KOH가 아연-공기 전지의 용량 및 자가 방전 억제 측면에서 가장 적합한 것으로 여겨진다.