1. 서 론
2. 실험 방법
2.1. 시료 준비 및 기체 충전 방법
2.2. 부피 분석법에 의한 충전된 고분자 시료의 기체 방출량 측정
2.3. 압력 분석법에 의한 충전된 고분자 시료의 기체 방출량 측정
2.4. 기체 장입량 및 확산도 분석 프로그램
3. 결과 및 고찰
3.1. 부피 분석법과 압력 분석법에 의한 측정 결과
3.2. 기체 용해도와 기체 임계온도와의 상관관계
4. 결 론
1. 서 론
고분자 재료는 유연한 가공성, 경량성, 화학적 안정성 등의 장점으로 인해 가스 차단막, 연료전지, 센서, 반도체 공정 등 다양한 산업 분야에서 널리 활용되고 있다.1,2,3,4,5,6,7,8,9,10) 특히 고압 가스 시스템에서 기밀성을 확보하기 위해서는 고분자 내 기체의 확산도(diffusivity)와 용해도(solubility) 특성이 핵심적인 물성으로 간주되며, 이는 고분자-기체 간 상호작용뿐만 아니라 기체 자체의 열역학적 특성과도 밀접하게 연관되어 있다.
그중에서도 기체 분자의 임계온도(critical temperature)는 용해도 예측을 위한 유효한 지표로서 주목받아 왔다.11,12,13,14,15,16,17) 기체의 용해도는 기체가 고분자 매트릭스 내에 흡수되는 정도를 의미하며, 이는 일반적으로 기체의 응축성(condensability)에 의해 크게 좌우된다. 응축성이 높은 기체는 고분자 내에 보다 쉽게 용해되며, 이러한 응축성은 기체의 임계온도와 정량적인 상관관계를 갖는다. 실제로 다수의 연구에서 고분자 내 기체 용해도는 임계온도와 선형적인 증가 경향을 나타내며, 이는 비극성 고분자-비극성 기체 시스템에서 특히 뚜렷하게 관찰된다. 예를 들어, 고밀도 폴리에틸렌(high-density polyethylene, HDPE), 폴리디메틸실록산(polydimethylsiloxane, PDMS), 폴리(1-트리메틸실릴-1-프로핀)[poly(1-trimethylsilyl-1-propyne), PTMSP] 등의 고분자에서 CO2, CH4, N2 등의 용해도는 임계온도가 증가함에 따라 지수 함수적으로 증가하는 경향을 보여주었으며, 이는 Henry’s law와 van der Waals 상호작용 모델을 통해 이론적으로도 설명이 가능하다.18,19,20,21)
그러나 이러한 상관관계는 고분자의 결정성, 배합 첨가제, 극성, 온도, 압력 등 외부 요인에 따라 달라질 수 있으며, 각 고분자 시스템별로 이러한 경향을 정량적으로 명확히 제시한 연구는 아직 제한적이다. 특히 수소(H2) 및 헬륨(He)과 같은 저임계온도 비극성 기체의 경우, 낮은 응축성으로 인해 고분자 내 용해도가 낮게 나타나며, 이는 실링 성능 저하나 누출 리스크 증가와 같은 문제로 이어질 수 있다.
이러한 기체별 상이한 임계온도에 따른 용해도 특성은 고분자 실링 소재 선정에 있어 중요한 판단 기준이 된다. 실제로 수소 충전소와 같은 고압 수소 시스템에서는 플루오로엘라스토머(fluoroelastomer, FKM), 에틸렌 프로필렌 디엔 모노머(ethylene propylene diene monomer, EPDM), 니트릴 부타디엔 고무(nitrile butadiene rubber, NBR), HDPE 등 다양한 고분자 소재가 사용되고 있으며, 수소의 높은 확산성과, 이에 따른 고분자의 취성(embrittlement) 및 물성변화에 대한 정량적 분석이 요구된다.22,23,24,25,26,27,28,29) 반도체 공정에서는 헬륨 및 질소가 퍼지(purge) 가스나 냉각 가스로 사용되며, 진공 상태에서의 기밀성 유지가 공정 안정성에 직결된다. 또한, 아르곤은 고온·고압 조건에서 보호 가스로 사용되어 장기적인 밀폐 성능 확보가 핵심이다.30)
따라서 다양한 기체에 대한 고분자 내 용해도 특성과 기체의 임계온도 간 상관관계를 정량적으로 분석하는 것은 고분자 재료 설계 및 기체 차단 성능 향상을 위해 매우 중요하다. 이를 위해, 최근 개발된 실린더 기반의 부피 분석법31,32,33,34,35)과 소형 압력계를 이용한 압력 분석 기법36,37)을 활용하여 고분자 내부에 흡수된 기체의 방출량을 정밀하게 측정하였다. 이 방법은 미세한 온도 및 대기압 변화의 영향을 보정할 수 있어, 방출된 기체량을 기반으로 고분자 재료의 기체 용해도를 보다 정확히 평가할 수 있다.38,39,40)
본 연구에서는 서로 다른 임계온도를 가지는 다섯 종류의 순수 기체(H2, He, N2, O2, Ar)를 대상으로, 저밀도 폴리에틸렌(low-density polyethylene, LDPE), HDPE, NBR S60, EPDM MT60 등 밀도와 구조가 상이한 고분자에서의 용해도를 1 MPa부터 10 MPa까지의 고압 조건에서 정량적으로 측정하고 분석하였다. 이를 통해 기체의 임계온도와 고분자 내 용해도 간의 정량적 상관관계를 비평형 격자 유체(Non-Equilibrium Lattice Fluid, NE-LF) 모델에 기반하여 설명하고자 하며, 이러한 결과는 고분자 가스 실링 소재의 최적 설계를 위한 기초 물성 데이터를 제공하는 동시에, 향후 고분자-기체 계면의 물리적 상호작용에 대한 이론적 해석에도 기여할 수 있을 것으로 기대된다.
2. 실험 방법
2.1. 시료 준비 및 기체 충전 방법
본 연구에서는 기체의 임계온도와 고분자 내 용해도 간의 상관관계를 분석하기 위해 네 종류의 고분자 재료를 사용하였다. 사용된 재료는 HDPE, LDPE, NBR, EPDM이다.
HDPE와 LDPE는 각각 수소 연료전지 차량용 Type IV 고압 수소 저장 탱크의 라이너 소재와 수소 배관으로 사용되고 있으며, 수소 기체의 침투를 효과적으로 차단하여 탱크의 경량화 및 내압 안전성 향상에 기여한다. HDPE와 LDPE 시료는 항균 처리가 적용된 특수 사양의 제품이다.
한편 EPDM과 NBR은 각각 고압 가스 저장 시스템의 O-ring 및 기타 밀폐부품 소재로 널리 활용된다.41,42) EPDM은 고온 환경에서도 우수한 화학적 및 물리적 안정성을 유지하며, 가스 누설 방지 및 장기적인 밀봉 효과 측면에서 탁월한 성능을 제공한다. 반면, NBR은 다양한 용매와 가스에 대한 뛰어난 내화학성을 바탕으로 안정적인 물성을 유지하는 특징이 있다. 이 두 재료는 특히 고압 수소 환경에서도 실링 안정성을 확보할 수 있는 탄성 고분자 소재로 평가받고 있다. 실험에 사용된 고분자 시료의 화학적 조성과 밀도는 Table 1과 같다. NBR S60과 EPDM MT60 시료는 첨가제의 영향을 최소화하기 위해, 두 시료의 화학적 조성은 첨가제를 최소한으로 사용하는 방식으로 구성하였다. 충전에 사용된 시료는 2.4절에서 설명한 확산 해석 조건을 만족하고, 두께 대비 충분한 면적을 확보하여 기체 확산 경로의 영향을 최소화할 수 있도록 가로 20 mm, 세로 20 mm, 두께 2 mm의 직사각형 시트 형태로 제작하였다.
Table 1.
Chemical compositions and density of polymer specimens [Unit : phr (parts per hundred rubber)].
기체 장입량 특성 분석을 위해 시료는 고순도(99.99 %)의 기체를 사용하여 고압 충전 후 탈착 과정(desorption)을 거쳤다. 실험에 사용된 기체는 수소(H2), 헬륨(He), 질소(N2), 산소(O2), 아르곤(Ar)이며, 모두 순수 기체 상태로 준비하였다. 고압 충전에는 내부식성과 기밀성이 우수한 스테인리스강(SUS 316)으로 제작된 고압 챔버를 사용하였다. 가스는 1 MPa에서 10 MPa까지의 압력 조건에서 주입되었으며, 이는 순수 고압 기체 봄베의 최대 저장 압력(약 12 MPa)을 고려하여 설정하였다. 고압 기체는 상온에서 24 h 동안 충전하였으며, 이 시간은 시료 내 기체가 확산 평형에 도달하기에 충분한 시간이었다.
충전이 완료된 후, 밸브를 개방하여 내부 압력을 대기압 수준까지 급격히 감소시킨 후, 이를 기준 시점(시간 0)으로 설정하여 탈착 실험을 개시하였다. 이때부터 시료 내부에 흡수되어 있던 기체가 빠르게 방출되며, 시간에 따른 방출량 데이터를 기반으로 용해도 및 확산계수를 측정하여 분석하였다. 기체 방출 거동은 두 가지 측정 기법을 통해 정밀하게 분석되었다. 첫 번째는 실린더를 이용한 부피 분석법(volumetric analysis method, VM)으로, 시료로부터 탈착된 기체가 실린더 내부 부피를 증가시키는 원리를 활용한다. 두 번째는 소형 정밀 압력계를 이용한 압력 분석법(manometric analysis method, MM)으로, 방출된 기체에 의해 발생하는 압력 상승을 실시간으로 기록하여 탈착 거동을 추적하였다. 두 방법 모두 미세한 온도 변화 및 대기압 변화의 영향을 보정하는 알고리즘을 적용하여 신뢰도 높은 데이터를 확보하였다. 두 측정법의 원리 및 방법은 다음절에서 설명하였다.
2.2. 부피 분석법에 의한 충전된 고분자 시료의 기체 방출량 측정
고분자 재료에 고압 기체를 주입한 후, 시료 내 기체의 장입량(uptake) 및 확산도(diffusivity)를 정량적으로 분석하기 위해 부피 기반 탈착량 측정 기술(volumetric desorption measurement technique)이 개발되었다.43,44) 본 측정법은 고압 환경에서 기체가 시료에 흡수된 이후, 감압 시 시료로부터 방출되는 기체의 부피를 직접 측정함으로써, 장입량과 확산도를 추출하는 방식이다.
실험은 다음과 같은 절차로 수행된다. 먼저, Fig. 1에서와 같이 고순도의 기체를 고압 봄베로부터 시료가 장착된 고압 가스 챔버로 공급하여, 설정된 압력 조건(1-10 MPa)에서 24 h 동안 시료에 기체를 충분히 주입(충전)한다. 이때 시료는 평형 상태에 도달하도록 상온에서 유지된다. 기체 충전이 완료된 후, 챔버 내 압력을 빠르게 대기압까지 낮추고, 시료를 꺼내어 물이 일정량 채워진 물통(water container) 속에 수직으로 세워진 눈금 실린더(graduated cylinder)의 상부 공간에 삽입한다.
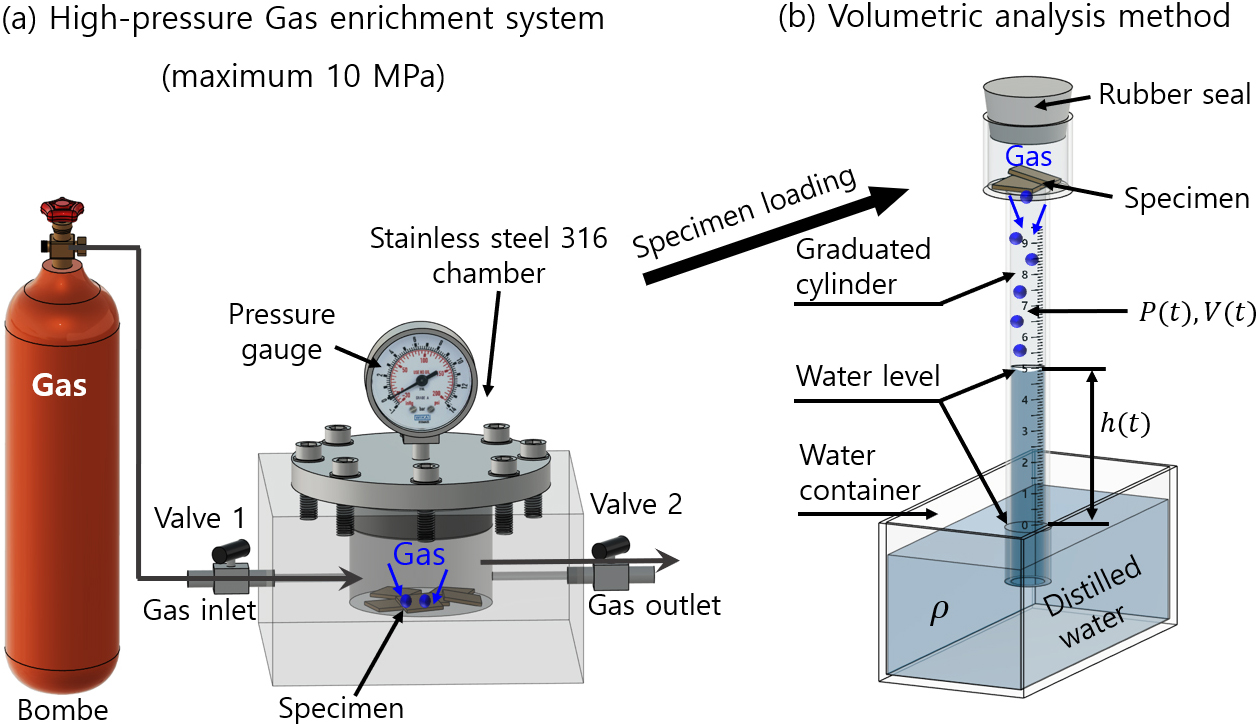
Fig. 1.
A volumetric analysis system was used to measure the gas released by a specimen after exposure to high-pressure gas and decompression. (a) The specimen is charged with gas in the high-pressure chamber supplied from high pressure gas bombe. (b) After decompression, the specimen is placed in the upper air space of the graduated cylinder. The cylinder is submerged in a water container and gas emission measurements are conducted. The blue area in the cylinder represents the water. The ● symbol in (b) indicates the gas emitted from the charged sample.45)
시료 내부에 흡수되어 있던 기체는 외부 압력 변화에 따라 빠르게 탈착되며, 이때 방출된 기체가 실린더 내의 기체 공간을 채우면서 부피가 증가하게 된다. 증가한 부피는 실린더의 눈금을 통해 실시간으로 측정되며, 측정된 탈착 기체 부피는 이상기체 상태방정식을 이용하여 몰 수로 환산할 수 있다. 시간에 따른 기체 방출 몰 수 는 이상기체법칙에 따라 다음과 같이 표현된다.43,44)
식 (1)의 로부터 시료에서 방출된 단위 질량당 기체 질량비 는 다음과 같이 변환된다.43,44)
여기서 는 기체의 몰 질량이고, 아르곤 기체의 경우에 몰 질량은 은 39.95 g/mol이고, 은 시료의 질량이다. 식 (1)과 (2)에서 시간에 따른 방출 기체 몰 수 는 방출된 기체 질량비 로 변환되었으며, 이때 변환 계수는 이다.
2.3. 압력 분석법에 의한 충전된 고분자 시료의 기체 방출량 측정
고분자 시료에 고압 기체를 주입(충전)한 후, 기체의 장입량과 확산도를 측정하기 위한 압력 측정 기술이 개발되었다.36,37) 앞의 부피 분석법과 동일하게 Fig. 2에서와 같이 고압 봄베로부터 기체를 공급받아서 시료에 일정 시간 동안 고압 챔버에서 기체를 충전시킨다. 챔버에서 시료에 기체로 충전한 후, 상용 USB 형 데이터 로거(ELP)가 들어있는 용기에 시료를 넣으면 시료에서 방출된 기체로 인해 압력이 증가하게 된다. 이를 ELP 센서를 이용하여 용기내부의 압력뿐만 아니라 온도의 변화를 측정하여 이상 기체 상태 방정식을 이용하여 방출된 기체의 몰 수를 얻는다. 측정 원리 및 방법은 이전의 논문에 상세하게 서술되어 있고, 용기에서 총 몰 수[]와 아래와 같이 표현된다.36,37)
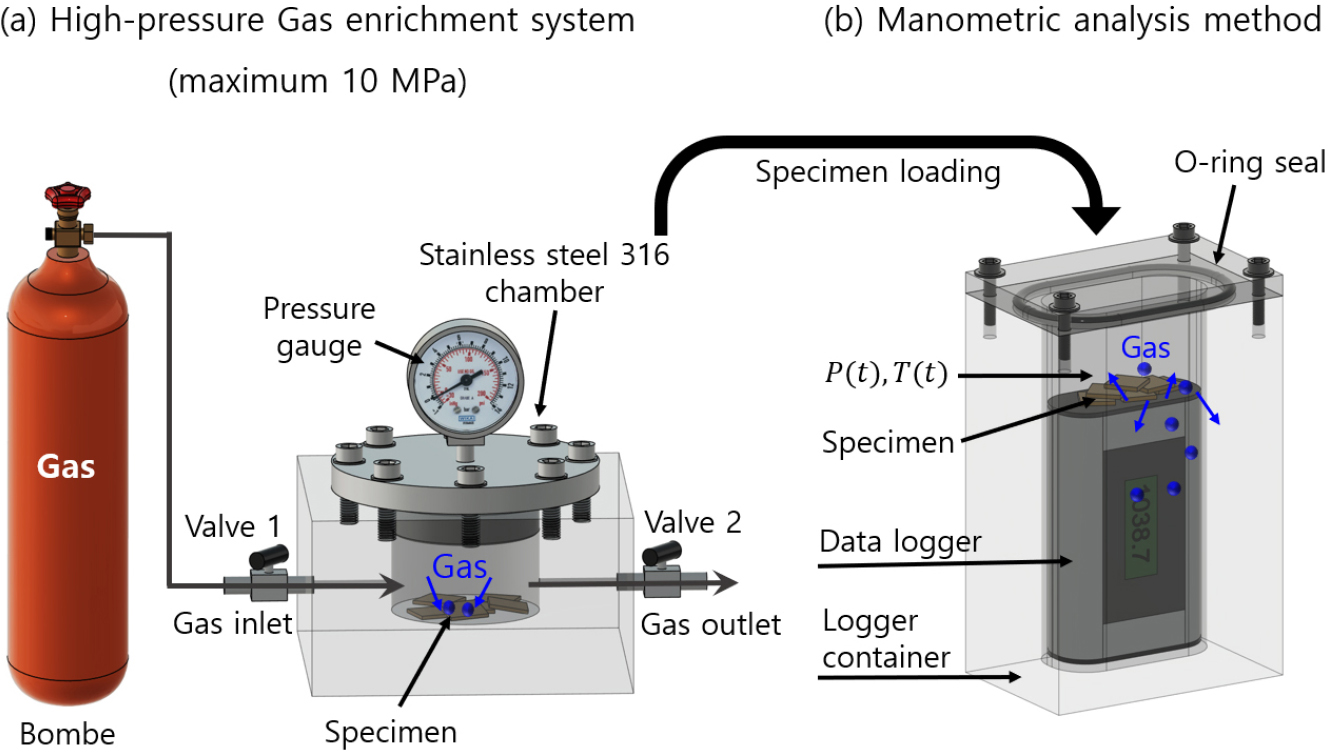
Fig. 2.
A manometric analysis system to measure the gas released by a specimen after exposure to high-pressure gas and decompression. (a) The specimen is charged with gas in the high-pressure chamber supplied from high-pressure gas bombe. (b) After decompression, the specimen is placed in the specimen container together with data logger. The ● symbol in (b) indicates the gas emitted from the charged sample.45)
은 시편 용기 내부의 기체(공기와 기체)의 몰 수를 나타낸다. 는 초기 공기의 몰 수이며, 는 시간에 따른 방출 기체에 의한 몰 수의 증가분이다. 따라서 용기 안의 기체의 총 몰수는 으로 된다. 식 (3)에서 , , 는 각각 시편이 들어 있는 용기 내부 공기의 초기 시간에서의 온도, 초기 부피, 초기 압력을 나타낸다. 는 초기 공기 압력()와 시편에서 방출된 기체로 인해 시간에 따라 증가하는 압력 변화 []의 합으로 표현되며, 즉, 로 나타낼 수 있다. 는 초기 온도 에 대한 시간에 따른 온도의 변화율을 나타낸다. 한편 식 (3)의 는 시편의 단위 질량당 방출된 기체 농도 []로 아래와 같이 변환된다.36,37)
여기서 는 기체의 몰 질량이고, 아르곤 기체의 경우에 몰 질량은 은 39.95 g/mol이고, 은 시료의 질량이다. 식 (3)와 (4)에서 시간에 따른 방출되는 기체의 몰 수 로부터 시료에서 방출된 기체 질량비 로 변환되었으며, 앞의 부피 분석법과 동일하게 변환 계수는 이다.
2.4. 기체 장입량 및 확산도 분석 프로그램
기체가 충전된 시료에서 탈착되는 기체는 Fick’s 확산 제 2법칙을 따른다고 할 때, 방출된 기체의 농도 는 다음과 같이 계산된다.46)
식 (6)은 초기에 일정하고 균일한 기체 농도를 가지고 있고, 또한 시료 표면에서 일정한 농도를 가진 평판 모양의 고분자 시료에 적용되는 Fick’s 확산 제2법칙의 해이다.
는 시트형 시료의 두께를 나타낸다. 식 (6)은 무한급수로서 수 많은 항들이 포함된다. 최적화 알고리즘을 기반으로 한 기체 장입량()와 확산도()를 정확하게 계산하는 전용 확산 분석 프로그램을 개발하였다.47,48) 따라서 식 (2) 와 (4)에 의한 기체질량 농도의 측정결과를 식 (5)를 이용한 계산을 전용 프로그램을 통해 분석함으로써 와 를 정확하게 얻을 수 있다.
3. 결과 및 고찰
3.1. 부피 분석법과 압력 분석법에 의한 측정 결과
4종의 고분자 시료(LDPE, EPDM MT60, HDPE, NBR S60)에 대해 고압 기체를 일정 시간 동안 충전한 후 감압 과정을 거친 뒤, 부피 분석법(VM)과 압력 분석법(MM)을 이용하여 시간에 따른 기체 방출량을 정밀하게 측정하였다. 이를 바탕으로 확산 분석 프로그램을 활용하여 식 (5)에 따라 기체 장입량()을 도출하였다. Fig. 3(a-d)와 Fig. 3(e-h)는 각각 HDPE와 NBR S60 시료에 대해 네 가지 기체(H2, He, N2, Ar)의 기체 장입량을 압력에 따라 분석한 결과를 보여준다. 이 결과들은 부피 분석법과 압력 분석법을 통해 얻은 데이터를 함께 비교 제시하고 있으며, 두 분석법이 이는 이전의 연구에서 반복 측정 3회를 포함한 불확도 요인들을 고려하여37,38,48,49) 불확도 10 % 내에서 서로 잘 일치함을 확인할 수 있다.
HDPE와 NBR S60의 두 고분자 시료에 대해 네 가지 기체 모두에서 기체 장입량은 노출 압력이 증가함에 따라 일정하게 증가하는 경향을 보인다. LDPE와 EPDM MT60에서도 동일한 경향이 나타났다. 즉, 네 가지 고분자 시료 모두에서 기체 장입량은 압력이 증가함에 따라 선형으로 증가하는 경향을 보인다. Fig. 3에서 검은색과 파란색 사선은 각각 부피 분석법과 압력 분석법에 의한 가스 장입량 데이터에 선형으로 피팅한 결과이며, 제곱상관계수(squared correlation coefficient) R2 값이 모두 0.97이상으로 우수한 선형성을 보여준다. 이는 HDPE와 NBR S60이 모든 가스 분자를 분해하거나 화학 반응을 겪지 않고 헨리의 법칙을 따르며 분자 상태로 흡수함을 나타낸다.50,51)
3.2. 기체 용해도와 기체 임계온도와의 상관관계
기체의 용해도 는 Fig. 3에서 압력에 대한 가스 장입량의 기울기로부터 얻어지는데 아래와 같이 구해진다.31,43)
는 해당 가스의 몰 질량으로 수소 가스의 경우 몰 질량은 2.016 g/mol이며, 는 시료의 밀도이다. HDPE, NBR S60, LDPE, EPDM MT60 시료에서 부피 분석법과 압력 분석법 을 사용하여 측정된 기체의 용해도를 식 (6)을 통해 얻을 수 있다.
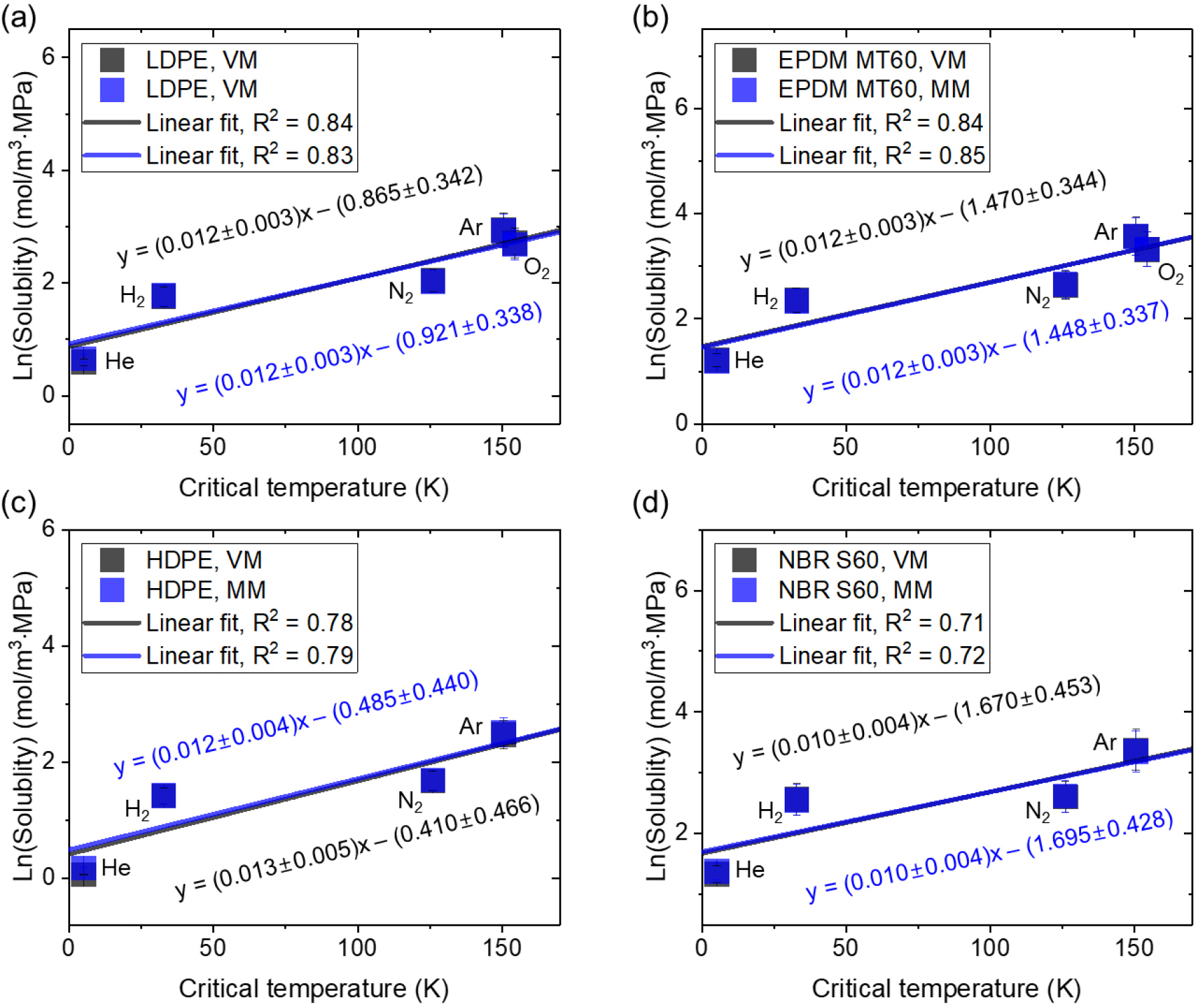
기체의 용해도는 일반적으로 기체 분자의 임계온도와 밀접한 상관관계를 갖는 것으로 알려져 있다.52,53,54,55,56,57) 이러한 이론적 배경을 바탕으로, 본 연구에서는 Fig. 3과 식 (6)을 통해 얻은 용해도 측정값과 기체 임계온도 간의 정량적 관계를 분석하기 위해 다섯 종류 기체(H2, He, N2, O2, Ar)의 임계온도 값을 Table 2에 정리하였다. 이어서, Fig. 4는 LDPE, EPDM MT60, HDPE, NBR S60의 네 종류 고분자 시료에 대해 얻은 기체 용해도와 해당 기체의 임계온도 간의 상관관계를 나타낸 결과이다.
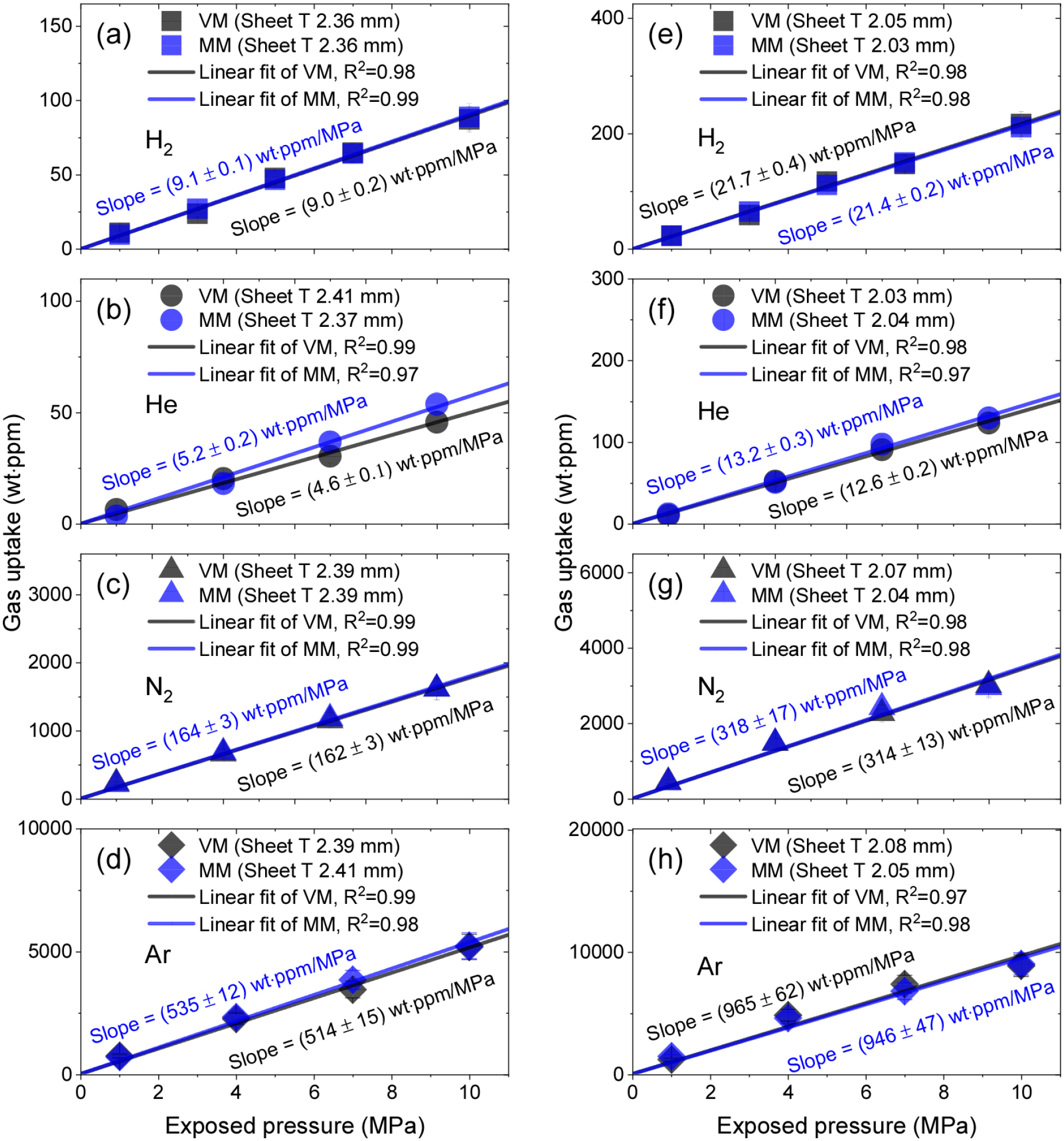
Fig. 3.
(a) H2 gas uptake, (b) He gas uptake, (c) N2 gas uptake and (d) Ar gas uptake versus exposed pressure for HDPE. (e) H2 gas uptake, (f) He gas uptake, (g) N2 gas uptake and (h) Ar gas uptake versus exposed pressure for NBR S60. VM and MM indicates volumetric measurement and manometric measurement, respectively. The black and blue line is linear fitted result with slope value by VM and MM, respectively. T is the thickness of sheet specimen.
Table 2.
Critical temperatures for gas molecules.
| Gas | H2 | He | N2 | O2 | Ar |
| Critical temperature (K) | 33.2 | 5.2 | 126.0 | 154.6 | 151.0 |
Fig. 4의 회귀 분석 결과에 따르면, 모든 고분자 시료에서 상관계수 R2 (squared correlation coefficient)가 0.71 이상으로 나타났으며, 이는 다양한 고분자 매트릭스에서도 기체의 로그 스케일에서 기체 용해도가 분자 기체의 임계온도에 비례하는 경향을 보인다는 점을 정량적으로 시사한다. 이러한 상관성은 시료의 물성(밀도, 결정성, 분자 구조 등)과 무관하게 일관되게 관찰되었으며, 이는 가스의 흡착이 없는 경우의 고분자-기체 계면에서의 물리적 메커니즘이 기체의 열역학적 성질에 의해 주도된다는 해석을 지지하는 결과이다. 특히, 이러한 실험 결과는 NE-LF 모델의 예측과 대체적으로 부합한다. 해당 이론에 따르면, 기체의 용해도()는 다음 식 (7)과 같은 형태로 표현된다.52,53,54,55,56,57)
여기서 는 기준 용해도 항, 는 경험 계수 또는 시스템 상수이며, 는 기체의 임계온도이다. 이 식은 로그 스케일에서 용해도가 기체의 임계온도에 대해 선형적으로 증가함을 나타내며, 본 연구의 실험 결과와 꽤 일치함을 확인하였다.
NE-LF 모델은 유리상 고분자(glassy polymers)에서 기체의 용해도와 확산 거동을 예측하기 위해 개발된 열역학적 모델이다. 이 모델은 고분자의 비평형 상태를 고려하여, 기체의 용해도와 임계온도 사이의 상관관계를 설명하는 데 활용된다. 특히, 무한 희석(infinite dilution) 상태에서의 기체 용해도와 임계온도 간의 관계를 해석하는 데 사용되며, 이는 유리상의 고분자에서 관찰되는 기체의 거동을 보다 정확하게 예측하는 데 사용된다.
4. 결 론
본 연구에서는 고압 가스 시스템에서의 고분자 실링 성능 향상을 위한 기초자료 확보를 목적으로, 서로 다른 임계온도을 가지는 다섯 종류의 순수 기체(수소, 헬륨, 질소, 산소, 아르곤)를 사용하여, 서로 다른 밀도와 구조를 가지는 네 가지 고분자 재료(LDPE, HDPE, NBR S60, EPDM MT60)에 대한 기체 용해도 특성을 1-10 MPa의 고압 조건에서 정량적으로 측정하고 분석하였다. 실험에는 실린더를 이용한 부피 측정법과 소형 압력계를 이용한 압력 측정법을 병행 적용하였고, 측정 정확도 제고를 위해 온도 및 대기압의 변화에 대한 보정을 수행하였다. 부피 분석법은 시각적으로 기체의 부피 변화를 직접 확인할 수 있어 직관적인 측정이 가능하다는 장점이 있다. 다만, 수위를 직접 판독하거나 자동으로 측정하기 위한 추가 장치가 필요하다. 압력 분석법은 상용 센서를 통해 압력 변화를 자동으로 기록함으로써 정밀도가 우수하고, 데이터 수집 및 분석이 자동화되어 효율성이 높다는 특징이 있다. 그러나 용기 내부의 온도 변화에 민감하게 반응하므로 이에 대한 보정이 필수적이다.
그 결과, 네 가지 고분자 시료 모두에서 기체 장입량은 압력이 증가함에 따라 선형으로 증가하는 경향을 보인다. 이는 고분자 내에서 모든 가스 분자를 분해하거나 화학 반응을 겪지 않고 헨리의 법칙을 따른다는 것을 보여준다.
한편 고분자 내 기체의 로그 스케일에서 용해도는 기체 임계온도에 비례하는 경향을 나타내었으며, 이는 NE-LF 모델에 의해 예측되는 거동과 정량적으로 일치함을 확인하였다. 특히, 이 모델은 구조와 밀도가 서로 다른 네 종류의 고분자에 무관하게 적용되어 고분자 시스템에 대한 확장가능성을 보여주었다.
본 연구는 고분자 기반 실링 재료의 기체 용해 및 확산 특성을 고압 조건에서 정량적으로 규명함으로써, 수소 충전소와 같은 고압 수소 인프라뿐만 아니라 반도체 공정, 연료전지 시스템, 정밀 환경 제어 장비 등 고 기밀성이 요구되는 다양한 산업 분야에서의 재료 설계 및 선택에 실질적인 자료를 제공한다. 향후에는 실제 복합가스 혼합계, 반복 압력-온도 사이클 조건 등 실사용 환경을 반영한 용해 및 확산 거동 분석을 통해, 보다 신뢰성 높은 실링 기술 개발로 확장될 수 있을 것으로 판단된다.