1. 서 론
광촉매(photocatalyst)는 태양광을 이용해 상온에서도 유기 오염물질을 효율적으로 분해할 수 있어, 폐수 처리 및 대기 정화 등의 환경 오염 문제 해결을 위한 친환경적 소재로 주목받고 있다.1,2) 현재 대표적인 광촉매 소재인 이산화 티타늄(TiO2)은 높은 화학적 안정성과 강한 산화력을 바탕으로 환경 정화에 널리 활용되고 있으나, 자외선(UV) 영역에서만 활성을 보이는 한계로 인해 실용성이 제한된다.3) 이에 반해, 은 나노입자(AgNPs)는 우수한 광흡수 특성과 높은 촉매 활성을 가지며, 국소 표면 플라즈몬 공명(local surface plasmon resonance, LSPR) 효과를 통해 자외선뿐만 아니라 가시광선 영역에서도 광반응이 가능하다. 이러한 특성 덕분에 AgNPs는 TiO2 기반 촉매에 비해 더 넓은 파장 범위에서 오염물질 분해에 활용될 수 있다.1,2,4)
AgNPs는 주로 환원제를 이용한 화학적 환원법으로 합성되지만, 이 과정에서 사용되는 환원제와 유기 용매의 독성으로 인해 환경 및 생체 분야 응용에 한계가 있다. 최근에는 식물 추출액을 활용한 친환경적 AgNPs 합성법이 주목받고 있으나,5) 용액 내에서 시간이 지남에 따라 나노입자의 응집이 일어나고, 촉매의 회수가 어렵다는 문제가 보고되고 있다. 이에 따라, 식물의 미세 구조를 생체 주형(biotemplate)으로 활용하여 마이크로 및 나노미터 규모의 계층적 구조(hierarchical structure)를 갖는 촉매를 합성하는 방법이 대안으로 제시되고 있다.6) 계층적 구조는 마이크론 규모의 구조를 통해 반응물의 확산을 촉진하고, 나노 구조를 통해 표면적을 극대화하여 높은 촉매 효율을 구현할 수 있다. 그러나, 식물 잎을 생체 주형으로 활용한 연구는 주로 솔-젤(sol-gel)법이나 고온 고체 환원법을 적용한 TiO2, ZnWO4 등 금속 산화물 합성에 국한되어 있으며,7,8,9) AgNPs 합성에 적용된 사례는 아직 보고되지 않았다.
액상 환원법으로 생체 주형에 AgNPs를 형성하고자 할 경우, AgNPs가 주형 표면이 아닌 용액 내에서 형성되는 문제가 있다. 본 연구에서는 이러한 문제를 해결하기 위해, 식물 잎의 큐티클 층에 친환경적인 시트레이트(citrate) 작용기를 도입하여 Ag+ 이온이 잎의 표면에서 선택적으로 환원되도록 설계하였다. 이때, 큐티클 층의 미세 구조가 변형되지 않도록 반응 온도, 시간, 용액의 pH를 조절하였으며, AgNPs가 잎 표면에 균일하게 형성되도록 Ag+ 이온 수용액과의 반응 온도 및 시간을 조절하였다. 이후 소성(calcination) 공정을 통해 주형을 제거함으로써, 마이크로/나노 계층 구조를 갖는 은 광촉매(micro/nano-structured Ag photocatalyst, 이하 MNAg)를 합성하였다.
또한, 시트레이트 작용기 도입 기반의 AgNPs 합성 전략이 다양한 식물 잎에 적용 가능한지 확인하기 위해 연잎, 장미 꽃잎, 스타티스 꽃잎의 세 종류의 잎을 주형으로 활용하였다. 실험 결과, 세 종류의 잎 모두에서 표면의 미세 구조를 따라 AgNPs가 형성됨을 확인하였으며, 소성 후에도 10-30 nm 크기의 AgNPs가 잎 표면의 마이크론 규모의 골격을 따라 계층적 구조를 형성함을 확인하였다.
최근 연구에 따르면, AgNPs의 LSPR 기반 광흡수 특성은 입자의 크기, 형상, 배열 간격 및 응집 상태에 따라 민감하게 변화하는 것으로 보고되고 있다.2,10,11,12,13) 예를 들어, 약 10 nm 크기의 구형 AgNPs는 400 nm 부근에서 뚜렷한 LSPR 흡수 피크를 보이며, 입자 크기가 커질수록 이 피크는 적색 편이되어 더 긴 파장의 가시광선을 흡수한다.12) 또한, 입자 간 거리가 멀어질수록 LSPR 피크의 폭이 감소하며 특정 파장에 집중된 흡수가 나타나는 반면, 거리가 가까워지면 나노입자 간의 플라즈몬 상호작용(plasmonic coupling)에 의해 가시광선 전 영역에 걸쳐 빛을 흡수하는 특성을 보인다.13)
본 연구에서도 이러한 광학적 특성의 변화를 확인하기 위하여, 생체 주형 기반으로 합성한 MNAg의 광흡수 특성을 DRS (diffuse reflectance spectrophotometer)로 측정하고, 이를 Ag powder 및 Ag film과 비교하였다. MNAg는 Ag powder 및 Ag film에 비해 자외선 영역에서 밴드 간 전이에 의한 흡수 피크의 폭이 넓게 나타났으며, 가시광선 영역에서는 LSPR에 의한 흡수가 전 영역에 걸쳐 광범위하게 관찰되었다. 이는 AgNPs의 입자 간격이 매우 가까울 때 특징적으로 나타나는 흡수 양상으로, 계층적 표면 구조를 따라 밀집 배열된 AgNPs 사이의 plasmonic coupling에 기인한 것으로 해석된다.
MNAg의 광촉매 성능을 평가하기 위해 메틸렌 블루(MB) 분해 실험을 수행하였다. Xenon 램프를 이용해 50 W/m2의 광세기로 6 h 동안 빛을 조사한 결과, 잎의 종류에 따라 71.4-90.9 %의 MB 분해율을 보였다. 식물 추출액 기반 AgNPs의 광촉매 효과 연구에서 MB 분해율은 광원, 광 세기, 광 조사 시간, 용액의 pH 등 다양한 조건에서 측정되어 비교가 쉽지 않으며 20-90 %로 다양하다.2) 이 중 높은 분해율을 보인 연구는 태양광(약 1,000 W/m2) 조건에서 98 %의 분해율을 보였으나 72 h이 소요되었으며,14) 3 h 이내로 빠르게 분해되는 효과를 보인 연구에서는 최대 83 %의 분해율을 보였다.4) 반면, 본 연구에서 합성한 MNAg는 50 W/m2의 낮은 광세기에서도 6 h 내에 90 % 이상의 MB 분해율을 보였으며, 이는 생체 주형 기반의 계층적 구조가 광촉매 활성을 향상시키는 데 효과적일 수 있음을 나타낸다.
2. 실험 방법
2.1. MNAg의 합성
실험에 사용된 sodium citrate tribasic dihydrate (Sigma-Aldrich, ≥ 99.0 %), NaOH (SAMCHUN, 98 %), AgNO3 (Sigma-Aldrich, 99.0 %)는 별도의 정제 없이 사용하였다. 스타티스 꽃잎과 장미 꽃잎은 꽃자루를 제거한 후 충분히 자연 건조하여 사용하였으며, 연잎은 건조된 상태로 구매하여 세척 후 사용하였다.
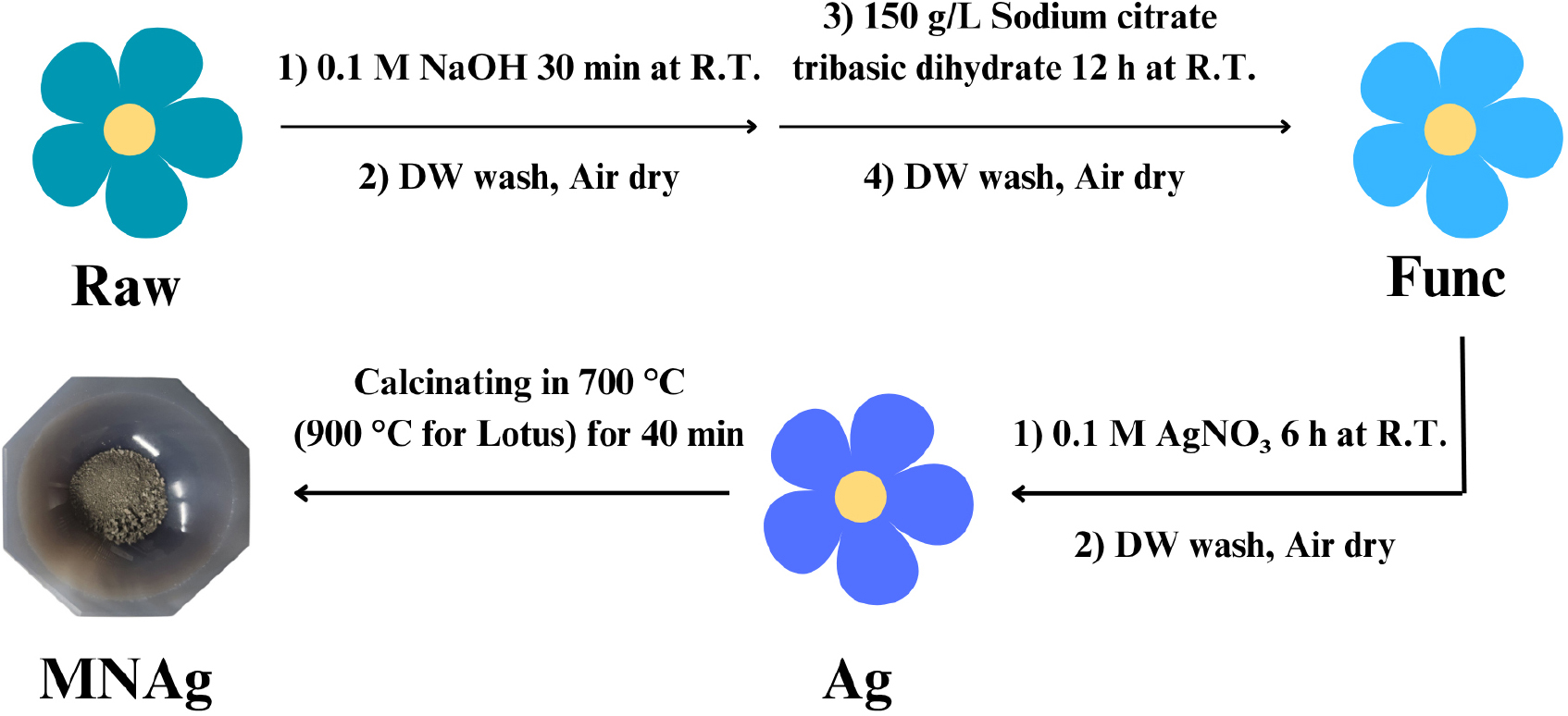
시트레이트 작용기를 잎의 표면에 도입하기 위해 반응 온도, 시간 및 용액의 pH를 조절하였고, AgNO3 수용액과의 반응에서도 온도와 시간을 조절하여 잎의 미세 구조를 보존하면서 표면에 AgNPs가 균일하게 형성되는 조건을 선정하였다. 이 조건을 바탕으로 연잎, 장미 꽃잎, 스타티스 꽃잎을 생체 주형으로 활용하여 MNAg를 합성하였으며, 합성 과정은 Fig. 1의 모식도에 나타내었다. 실험에 사용된 시료는 단계에 따라 세척・건조된 잎(Raw), 시트레이트 작용기가 도입된 전처리 잎(Func), 표면에 은이 형성된 잎(Ag), 소성을 통해 주형이 제거된 시료(MNAg)로 구분하였다.
먼저, 세척・건조된 잎(Raw)을 0.1 M NaOH 수용액에 넣고 상온에서 30 min간 교반 후 걸러내고, 증류수로 세척・건조하였다. 건조된 잎을 150 g/L sodium citrate tribasic dihydrate 수용액에 넣어 상온에서 12 h 교반 후 증류수로 세척・건조하여 전처리 잎(Func)을 얻었다.
전처리 잎(Func)을 0.1 M AgNO3 수용액에 넣고 상온에서 6 h 교반 후 세척・건조하여 은이 형성된 잎(Ag)을 합성하였다. 마지막으로, 은이 형성된 잎(Ag)을 소성로(FB-1310M, Thermo Fisher)에서 장미 및 스타티스 꽃잎은 700 °C, 연잎은 900 °C까지 가열한 후 40 min간 소성을 통해 주형을 제거하여 MNAg 시료를 합성하였다.
합성의 각 단계에 Desktop-SEM (scanning electron microscope, SNE-4500M, SEC)과 FE-SEM (field emission scanning electron microscope, JSM-IT800, JEOL)을 이용해 잎의 표면 구조를 관찰했으며, FT-IR (IR Prestige-21, SHMADZU)로 각 단계에서 시료 표면의 작용기 변화와 소성 후 주형이 남아있는지 확인하였다. EDS (energy dispersive X-ray spectroscopy, Aztec Energy_X-MaxN, OXFORD)를 이용해 은 형성 후 꽃잎 표면에 남아 있는 원소를 확인하였다. 소성 과정에서 온도에 따른 중량의 변화를 확인하고자 공기를 주입하면서 30-800 °C까지 10 K/min의 승온 조건으로 TGA/DSC (thermogravimetric analyzer and differential scanning calorimeter, LABSYS Evo, SETARAM)를 측정하였다. XRD (high resolution powder X-ray diffractometer, SmartLab, RIGAKU)로 소성 후 남은 시료의 성분 및 결정 구조를 분석하였으며, FE-TEM (field emission transmission electron microscope, Talos F200X G2, Thermo Fisher)를 이용해 AgNPs를 관찰하였다.
2.2. 광흡수 특성 및 광촉매 효과 분석
합성한 시료의 광흡수 특성은 DRS (diffuse reflectance spectrophotometer, SolidSpec-3700, SHIMADZU)로 측정하였다. 합성한 세 종류의 MNAg 시료와 Ag powder (Sigma-Aldrich, 99.99 %, < 250 µm)와 Ag film (Nilaco, 99.98 %)을 250-900 nm 파장에서 reflectance를 측정하여 분석하였다.
합성한 시료의 광촉매 효과는 MB 분해 실험을 통해 분석하였다.15) MB 수용액(2 mg/L, 3 mL)에 MNAg 시료(3 mg)를 첨가한 후, 5 min간 초음파 분산(sonication)시켰으며, 암실에서 30 min간 방치하여 흡착-탈착 평형(adsorption-desorption equilibrium)에 도달하도록 하였다. 이후, 석영 셀을 IR-cut 유리를 장착한 Xenon 램프(300 W) 기반 태양광 시뮬레이터(XPN500WA, DY-Tech)에 장착하고, 광원 아래 20 cm 거리에서 50 W/m2의 세기로 광을 조사하였다. 각 실험은 동일 조건에서 3회 반복 수행(n = 3)하였으며, 0 h, 1 h, 2 h, 3 h, 6 h 후 시료를 채취하여 원심 분리 후 상층액의 MB 흡광도를 UV-Vis 분광광도계(UV-2700, SHIMADZU)로 측정하였다. 흡광도의 시간에 따른 변화율은 평균값과 95 % 신뢰수준에서의 확장 불확도(expanded uncertainty)를 함께 계산하여, 막대그래프에 error bar로 표시하였다.
3. 결과 및 고찰
3.1. MNAg의 합성
식물의 꽃잎이나 잎 표면은 고도의 친지질성(lipophilic) 왁스로 이루어진 큐티클층으로 덮여 있으며, 이러한 큐티클층이 고유한 미세 구조를 형성한다.16) 큐티클층은 긴 사슬을 가진 지방족 및 고리형 화합물의 복합 혼합물이며 표면에 드러난 작용기는 OH, COOH, COOR, C=O 등이 존재한다.17,18) 식물의 큐티클층 표면에 존재하는 일부 COOH, COO- 작용기는 식물의 표면에서 환원제로 작용할 수 있다. 본 연구에서는 이러한 시트레이트 작용기를 잎 표면에 균일하게 도입하기 위해 0.1 M NaOH 수용액과의 반응 시간을 조절하고, 시트레이트 작용기를 갖는 citric acid, sodium citrate tribasic dihydrate를 사용하여 산성 및 염기성 조건에서 실험하였다. 표면 작용기 도입을 위한 전처리 과정의 반응 시간과 반응 온도를 조절하여 잎의 구조가 손상되지 않으면서 표면에 시트레이트 작용기가 도입되는 반응 조건을 탐색하였다. 또한 AgNO3 용액과의 반응 온도와 반응 시간을 조절하여 표면에 균일하게 AgNPs가 형성되도록 하였다. 반응 온도를 80 °C로 올렸을 때 식물 잎 본연의 정교한 미세 구조가 사라지고 흔적만 남아 있는 것을 통해 반응 온도가 미세 구조에 중요한 영향을 주는 것을 확인하고 모든 반응은 상온에서 수행하였다.
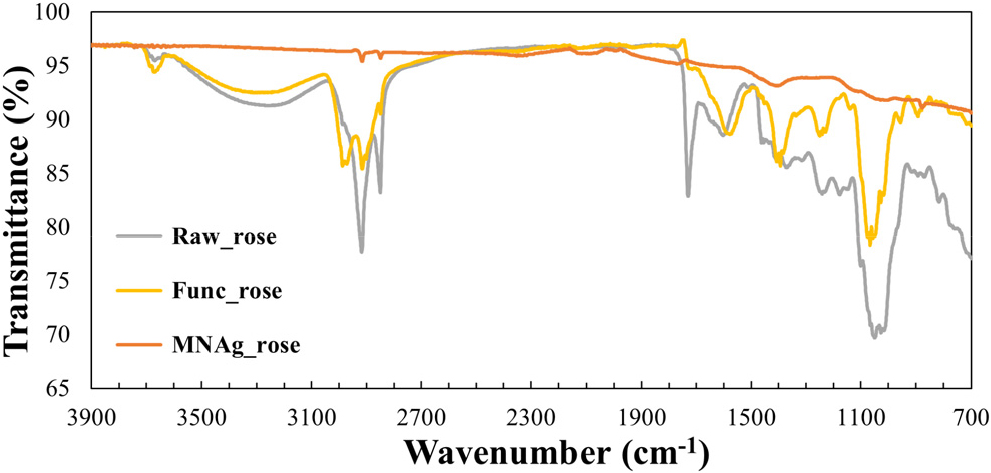
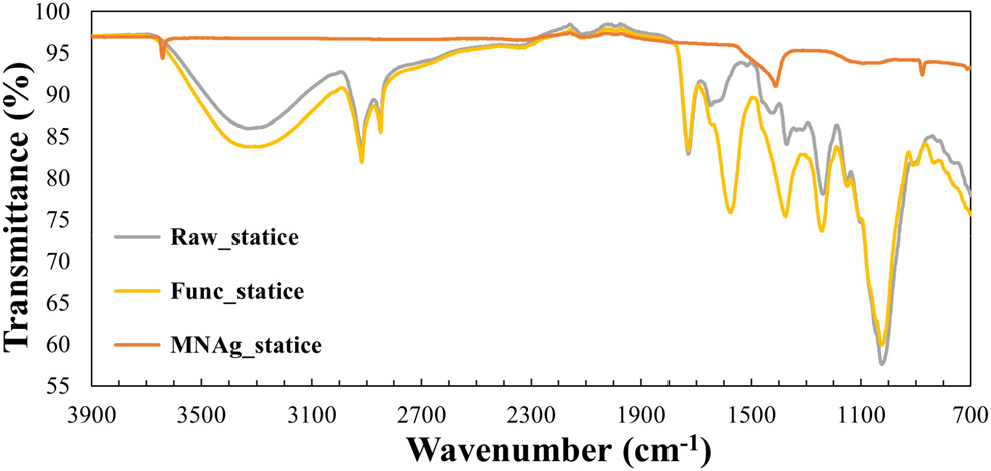
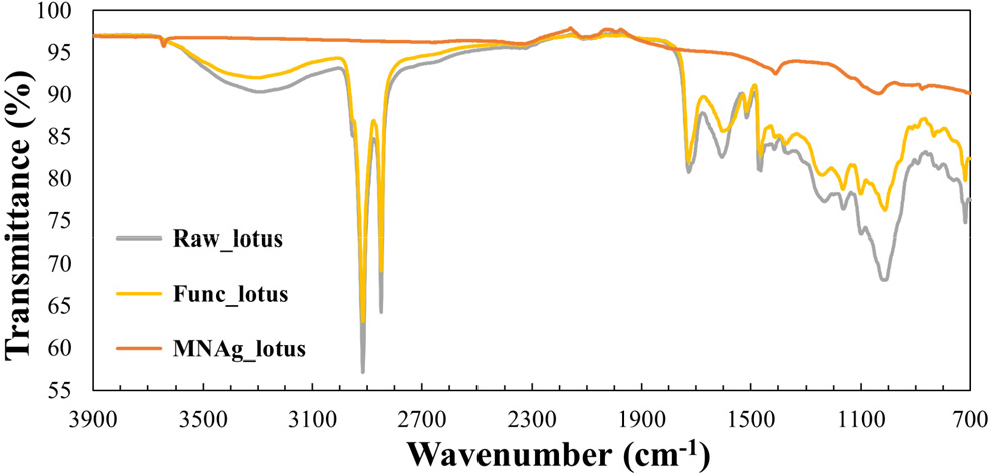
이러한 과정을 거쳐 상온에서 NaOH 용액과 30 min, sodium citrate tribasic dihydrate 수용액과 12 h 반응시키는 조건을 확립하였다. 표면 작용기 도입을 위한 전처리 과정 후 FT-IR 분석을 통해 작용기 변화를 관찰한 결과(Figs. 2, 3, 4), 장미 꽃잎(Raw_rose)은 Fig. 2에서와 같이 3,000 cm-1에서 C-H 피크가 강하게 나타나고 1,600-1,750 cm-1에 걸쳐 C=C, C=O, COO- 등의 다양한 작용기에 의한 피크가 관찰되었다. 1,600-1,750 cm-1 피크들의 상대적 크기에 변화를 통해 표면에 작용기의 변화가 일어났음을 알 수 있다. 이러한 결과는 스타티스 꽃잎에서도 동일하게 관찰되었으며(Fig. 3), 연잎은 작용기의 변화가 다른 두 시료에 비하여 미미하였다(Fig. 4).
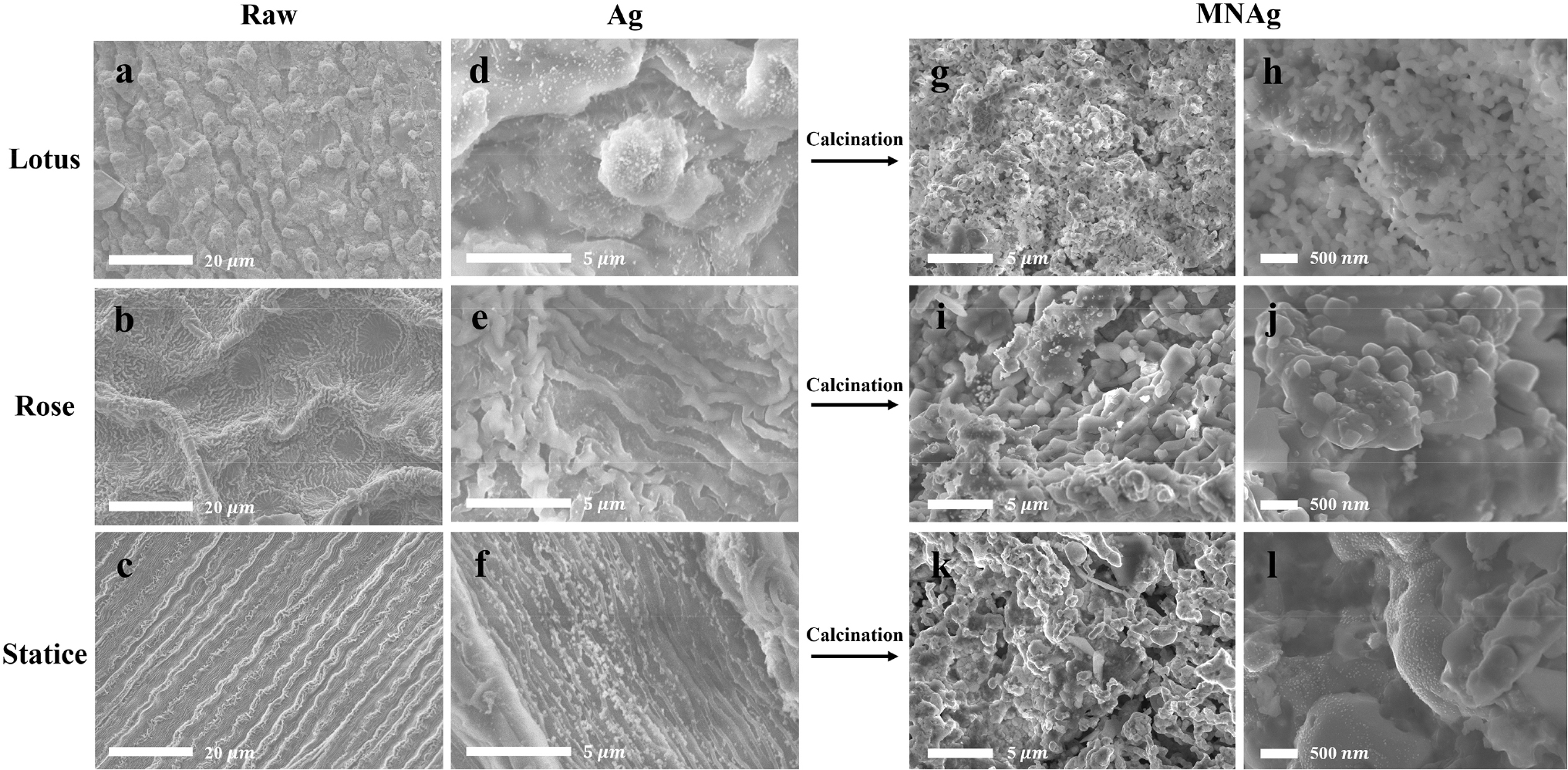
본 연구에 활용된 세 종류의 식물 잎은 각기 다른 미세 구조를 가지며, 연잎(Raw_lotus)은 3-5 µm 크기와 나노 크기의 돌기가 있는 표면 구조를,19) 장미 꽃잎(Raw_rose)은 1 µm 내외의 빽빽한 주름 구조를, 스타티스 꽃잎(Raw_statice)은 10 µm 크기의 골격과 2-3 µm 간격의 주름 구조를 형성하고 있다. 이러한 표면 구조는 주형으로 활용할 경우, 계층적 구조의 형성과 확산 경로 확보 측면에서 촉매로서의 장점을 제공할 수 있다. 전처리 잎(Func)의 표면에 AgNPs를 합성하기 위해 0.1 M AgNO3 수용액과 상온에서 12 h 반응시킨 결과 Ag_lotus, Ag_rose, Ag_statice 모두에서 AgNPs가 균일하게 형성되고, 잎의 원래 구조가 유지되었다[Fig. 5(d)-(f)]. EDS Mapping 결과(Fig. 6), 세 종류의 Ag 시료 모두 잎의 표면 전반에 Ag 성분이 분포함을 확인하였다.
소성을 통해 주형을 제거하기 위해, 장미 및 스타티스 꽃잎은 700 °C에서, 연잎은 900 °C에서 40 min간 소성하였다. 스타티스 꽃잎(Raw_statice)을 공기를 주입하며 800 °C까지 10 K/min의 승온 속도 조건으로 TGA 분석한 결과 중량의 76.6 %가 감소하였으며, 은이 형성된 스타티스 꽃잎(Ag_statice)은 중량의 71.8 %가 감소하였다. 두 시료 모두 650 °C 이상에서 중량의 변화가 나타나지 않았다. 소성 후 각 시료의 FT-IR을 측정하여(Figs. 2, 3, 4) 3,000 cm-1의 C-H 피크가 사라지는 것을 확인하며 소성 온도를 조절하였다. 소성 후 주형이 제거된 시료(MNAg)의 구조는 FE-SEM으로 분석하였다. 세 종류의 MNAg 모두 입자들이 주형의 형태를 유지하며 수 마이크로미터와 수백 나노미터 크기의 주름 또는 돌기를 형성하며 그물처럼 연결되어 있었다. MNAg_lotus는 주형에 있던 돌기를 닮은 수 마이크로 크기의 구조와 수백 나노 크기의 돌기가 관찰되며[Fig. 5(g, h)], MNAg_rose는 주름의 구조를 보이며 500 nm 이하 크기의 돌기들이 관찰되었다[Fig. 5(i, j)]. MNAg_statice는 주형에서 나타는 밭고랑 모양의 구조가 뚜렷하게 나타나지 않으나 입자들이 그물처럼 연결되어 있으며 100 nm 이하의 돌기 구조가 확인되었다[Fig. 5(k, l)].
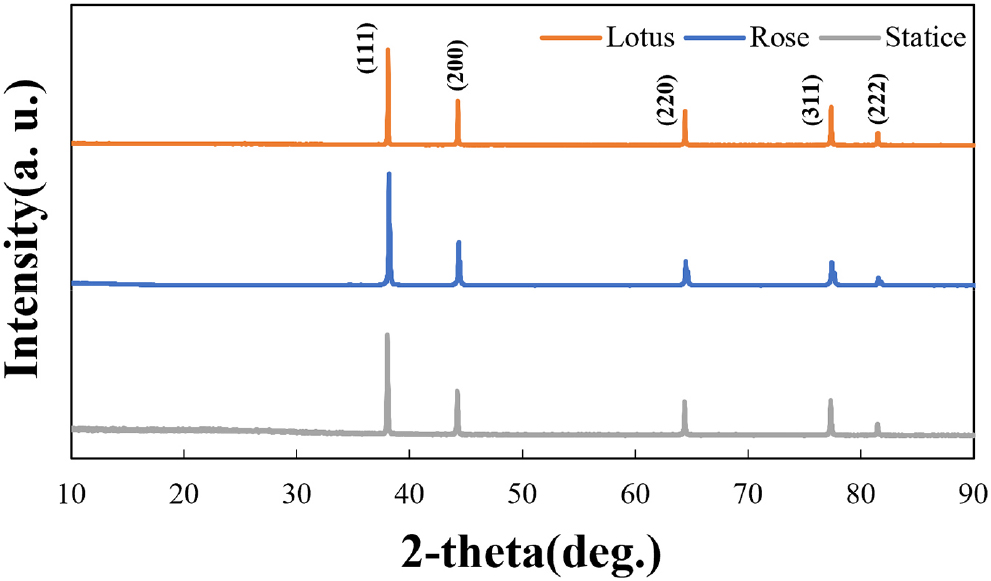
TEM 분석을 통해 세 종류의 MNAg 시료에서 수십 나노미터 크기의 AgNPs가 형성된 것을 관찰할 수 있었다. MNAg_lotus, MNAg_rose, MNAg_statice 모두에서 AgNPs의 크기는 10-30 nm 범위로 분포하였다[Fig. 7(a)-(c)]. HR-TEM 분석 결과 MNAg_lotus에서 AgNPs의 격자 간격 (lattice fringe spacing)은 평균 2.4 Å로 측정되었으며, 이는 문헌에 보고된 FCC 구조 Ag 결정 d-spacing 값과 일치하였다(Fig. 8).20,21) XRD 분석 결과 MNAg 시료는 모두 FCC 구조의 Ag 특성 피크인 (111), (200), (220), (311), (222)를 보였고(Fig. 9),20) Ag2O와 같은 산화물은 검출되지 않았다.
Figs. 5, 6, 7, 8, 9에 나타난 합성 각 단계에서의 식물 잎 표면의 미세 구조와 성분 분석 결과를 종합하면, 수십 나노미터 크기의 은 입자들이 수 마이크로미터 크기의 식물의 미세 구조를 따라 형성됨을 확인할 수 있었다. 또한, 소성 이후 식물의 미세한 구조가 그대로 유지되지는 않지만, 주형의 마이크로미터 크기의 골격을 따라 AgNPs가 응집 및 연결되어 형성됨을 확인할 수 있었다.
3.2. 광흡수 특성 및 광촉매 효과 분석
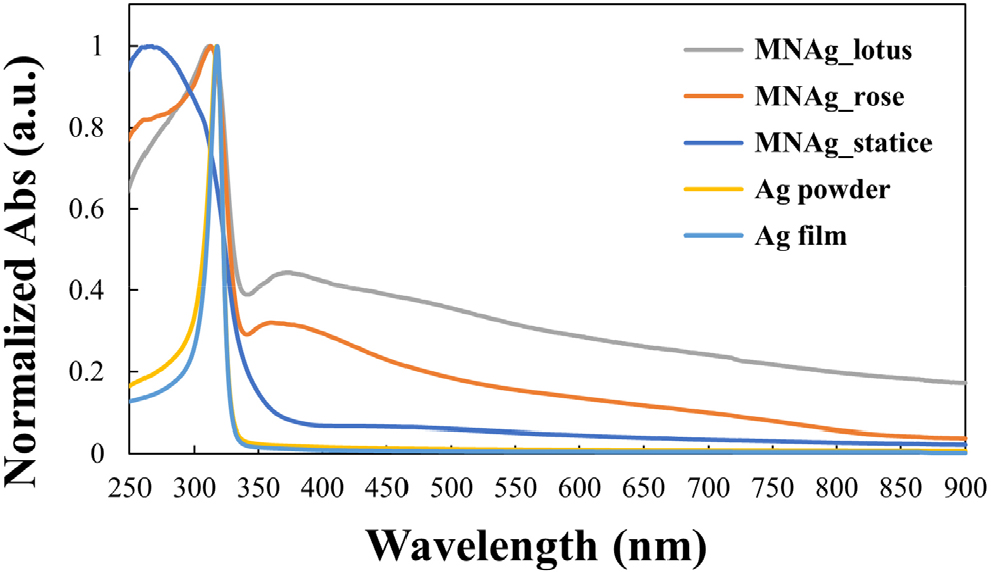
MNAg_lotus, MNAg_rose, MNAg_statice의 광흡수 특성을 분석하기 위해 고체 MNAg 시료의 diffuse reflectance를 측정하였으며, Ag powder와 Ag film을 함께 분석하여 비교하였다. 측정한 reflectance는 Kubelka-Munk 식을 이용해 흡광도로 변환 후 최대 흡수 피크에 대해 정규화하여 파장에 따른 흡광도의 변화를 그래프로 나타내었다(Fig. 10). 세 종류의 MNAg 시료는 모두 320-900 nm의 넓은 가시광선 영역에서의 흡수와 320 nm 이하 자외선 영역의 흡수를 보였다. 가시광선 영역의 흡수는 AgNPs에서 유도되는 LSPR에 기인하며, AgNPs의 LSPR에 의한 흡수는 입자의 크기, 간격, 배열 구조에 따라 특성이 민감하게 영향을 받는 것으로 알려져 있다.10,11,12,13) MNAg_lotus, MNAg_rose, MNAg_statice 모두 가시광선 전영역에 걸쳐 넓고 완만한 흡수 특성을 나타냈으며, 이 중 MNAg_lotus가 가장 높은 흡광도를 보였다. MNAg_rose는 lotus보다 다소 낮은 흡수를 보였고, MNAg_statice는 세 시료 중 가장 낮은 흡광도를 나타내었다. 반면, Ag powder와 Ag film은 약 318 nm 부근의 자외선 영역에서만 날카로운 흡수 피크를 보였으며, 가시광선 영역의 흡수는 거의 일어나지 않았다. 자외선 영역의 흡수는 Ag의 밴드 간 전이(interband transition)에 해당하는 것으로 알려져 있다.2) 세 종류의 MNAg 시료에서도 320 nm 이하에서 유사한 흡수가 관찰되었으나, 피크의 폭이 Ag powder와 Ag film에 비하여 넓게 나타났으며 이러한 특성은 MNAg_statice에서 뚜렷하게 관찰되었다. 이는 입자 응집, 표면 결함, 구조적 불균일성 등의 복합적 요인을 반영한 결과로 해석된다.
일반적으로 AgNPs의 LSPR 흡수는 직경이 약 10 nm인 구형 입자의 경우 400 nm 부근에서 뚜렷하게 관찰되며, 입자 크기가 증가할수록 적색 편이가 일어나 더 긴 파장의 빛을 흡수한다.12) 또한 입자 간 간격이 넓을 경우 흡수 피크가 좁고 선명하게 나타나는 반면, 간격이 좁거나 입자들이 서로 소결(sintered)된 경우 나노입자 간 plasmonic coupling으로 인해 가시광선 전 영역에 걸친 확산된 흡수 특성을 보이는 것으로 보고되어 있다.13)
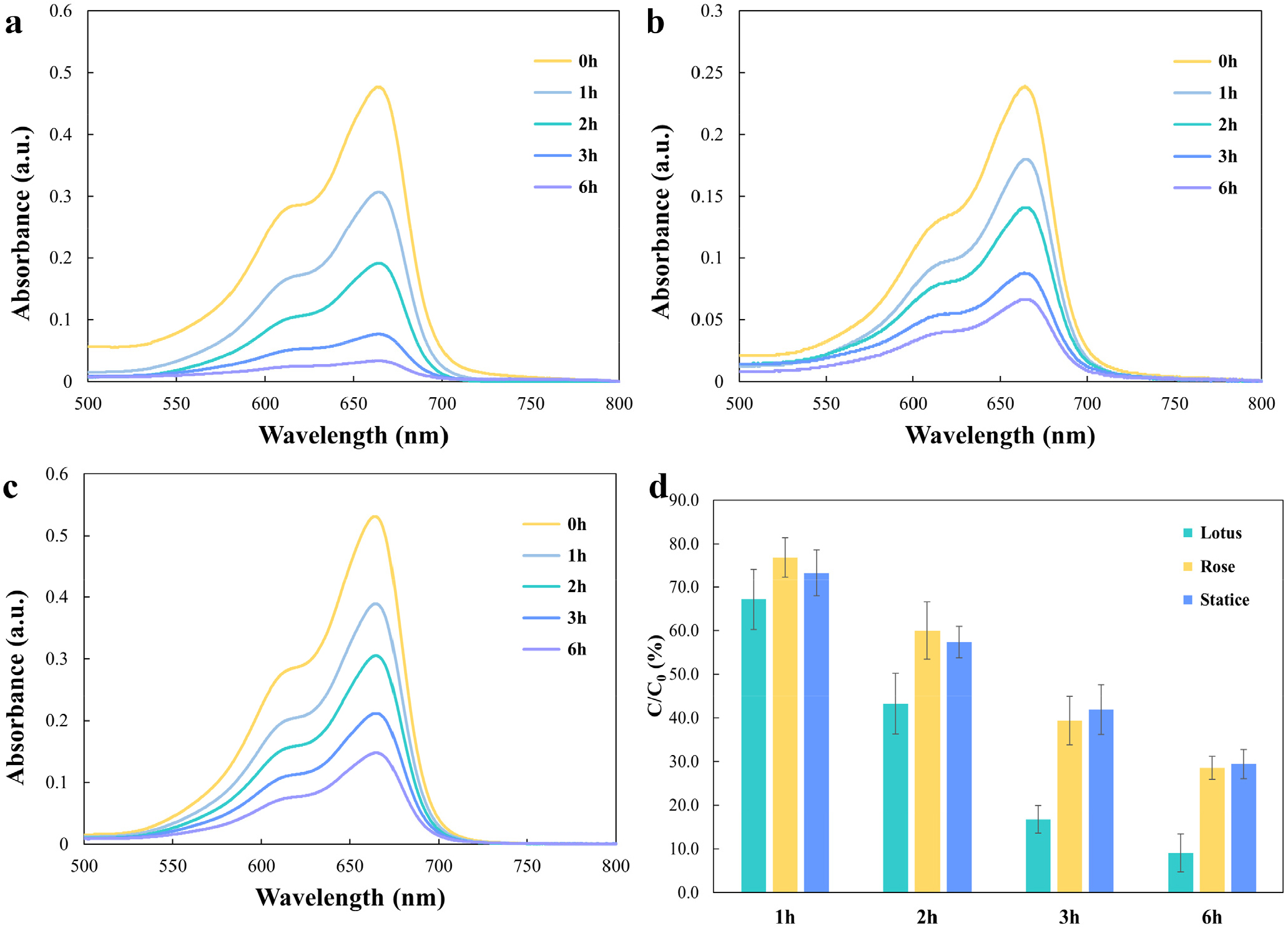
MNAg_lotus, MNAg_rose, MNAg_statice의 광촉매 활성을 평가하기 위해 MB 수용액의 UV-Vis 흡광도 변화를 분석하였다. 광원으로는 IR-cut 유리를 장착한 Xenon 램프를 사용하여 자외선 및 가시광선 영역의 빛을 모두 시료에 조사하였으며, 각 MNAg 시료를 2 mg/L 농도의 MB 수용액에 첨가한 뒤 상온에서 최대 6 h까지 빛을 조사하며 시간에 따른 MB의 흡광도 변화를 측정하였다[Fig. 11(a)-(c)].
광촉매 실험은 동일 조건에서 3회 반복(n = 3) 수행하였다. 시간에 따른 흡광도 감소율의 평균값을 바탕으로 막대그래프를 작성하고, 각 평균값에 대한 95 % 신뢰수준에서의 확장 불확도를 error bar로 표현하였다[Fig. 11(d)]. 세 시료 모두 뚜렷한 광촉매 활성을 보였으며, MNAg_lotus는 평균 90.9 %의 MB 분해율로 가장 우수한 성능을 나타냈다. MNAg_rose와 MNAg_statice는 각각 평균 71.4 %, 70.6 %의 분해율을 보여 유사한 수준의 활성을 나타냈다. 한편, 대조 실험으로 MNAg 없이 6 h 동안 MB 수용액에 빛을 조사한 경우, 29 %의 흡광도 감소만 관찰되어 자외선 및 가시광선에 의한 자연 분해는 제한적임을 확인할 수 있었다.
추가로, 소성 과정에서 주형이 완전히 제거되지 않은 MNAg_lotus 시료에 대해 동일한 조건으로 광촉매 실험을 수행하였을 때, MB 수용액의 흡광도의 감소율은 약 45 %로 확인되었다. 이는 주형 제거 공정을 통해 형성된 AgNPs의 계층적 구조와 응집 상태가 광촉매 활성 향상에 기여함을 보여준다.
MNAg 시료의 광흡수 특성은 각 시료의 광촉매 효과와 밀접한 상관성을 나타낸다. MNAg_lotus는 90.9 %의 MB 분해율을 보여 가장 우수한 광촉매 효과를 보였으며, 이는 가시광선 영역에서 흡광도가 가장 높았던 DRS 결과와 일치한다. SEM 분석 결과, 세 시료 모두에서 AgNPs가 응집되고 서로 연결된 구조를 형성하고 있었으며, 이러한 구조적 특성이 가시광선 전 영역에 걸친 확산된 흡수 특성에 기여한 것으로 보인다.
MNAg_rose와 MNAg_statice는 각각 유사한 수준인 약 71 % 내외의 분해율을 보였다. DRS 결과에서 MNAg_rose는 가시광선 전 영역에서의 흡수 특성이 뚜렷한 반면, MNAg_statice는 가시광선 영역의 흡수는 낮지만, 자외선 영역에서 흡수 피크의 폭이 넓어 더 넓은 범위의 자외선을 강하게 흡수하는 특성을 보였다. 이러한 차이는 두 시료가 유사한 수준의 광촉매 활성을 보이는 데 영향을 준 것으로 보인다.
이처럼 본 연구에서 합성한 MNAg 시료는 생체 주형의 계층적 구조를 따라 AgNPs가 응집·연결된 형태로 배열되어, 광범위한 가시광선 흡수를 가능하게 하며, 이러한 광흡수 특성으로 인해 우수한 광촉매 효과를 보이고 있다.
4. 결 론
본 연구에서는 연잎, 장미 꽃잎, 스타티스 꽃잎의 독특한 미세 구조를 생체 주형으로 활용하여 마이크로/나노 계층 구조를 갖는 MNAg를 친환경적으로 합성하고, 그 광촉매 효과를 분석하였다. 잎의 표면에 환원제 역할을 하는 시트레이트 작용기를 도입하기 위해, 세척・건조된 잎을 상온에서 NaOH 수용액 및 sodium citrate tribasic dihydrate 수용액과 반응시킨 후 AgNO3 수용액과 반응시켰다. 이후 소성 과정을 통해 주형을 제거하여 MNAg를 합성하였다. 소성 전까지 잎의 미세 구조는 유지되었고, 소성 후에도 마이크로 구조를 따라 AgNPs가 응집 및 연결된 구조가 형성됨을 확인하였다.
DRS 분석 결과, 합성된 세 종류의 MNAg 시료는 가시광선 전 영역에서 광범위한 흡수 특성을 나타내었으며, 자외선 영역에서는 밴드 간 전이에 의한 흡수가 함께 관찰되었다. 특히, 가시광선 영역의 광범위한 흡수는 AgNPs 간의 밀집된 응집 구조로 LSPR과 plasmonic coupling에 기인하는 것으로 해석된다. 이는 계층적 표면 구조를 따라 배열된 AgNPs의 구조적 응집이 광흡수 특성을 향상시키고, 결과적으로 광촉매 활성을 증진시키는 데 기여할 수 있음을 보여준다.
본 연구에서 제시한 합성 방법은 연잎, 장미, 스타티스 꽃잎에 모두 적용 가능함을 확인하였으며, 향후 다양한 식물 잎에도 확장 적용될 수 있을 것으로 기대된다. 생체 주형 공법을 활용한 친환경적이고 간단한 MNAg 합성 전략은 지속 가능한 나노소재 합성 기술의 발전과 생체 구조를 모사한 기능성 소재 개발에 기여할 수 있을 것으로 기대된다.