1. 서 론
최근 고성능 Nd-Fe-B계 희토류 영구자석은 가정용·산 업용·국방용으로 사용되는 PC, 노트북, 휴대용 스마트 통신기기, 로봇, 의료기기 등 각종 전기·전자기기는 물 론, 하이브리드 자동차(HEV), 전기자동차(EV), 풍력발전 기 등의 수요가 급증함과 동시에 그들 제품의 고효율화· 소형화·경량화·고성능화 추세에 따라 보다 우수한 자 기적 특성이 요구되고 있다.1-4)
실제로 희토류 영구자석 제품의 자기적 특성향상을 위 해서는 주요 원료인 Nd금속의 순도는 3N(99.9 %)이상의 고순도화가 필수적이며, 특히 Nd금속 중의 산소(O) 농 도를 50 ppm이하로 요구하고 있다. 그러나 원래 Nd금속 은 산소(O2)와의 친화력이 크기 때문에 Nd 잉곳의 표면 산화보다 용존 산소의 제거가 매우 어려운 것으로 알려 져 있다.5)
일반적으로 희토류금속은 Monazite((Ce,Y)PO4), Xenotime( YPO4), Bastnaesite(CeFCO3) 대표적 광물중, Monazite(( Ce,Y)PO4) 및 Bastnaesite(CeFCO3) 등의 광물로부 터 염화물(NdCl3), 불화물(NdF3) 및 산화물(Nd2O3) 등으 로 추출된다. 그러나 원래 물리·화학적 성질이 유사하 기 때문에 원광으로부터 각 원소로 분리하는 것이 매우 어렵기 때문에 고순도(99.9 % 이상) Nd 잉곳 형태로 제 조하기 위해서는 1차적으로 용융염 전해법이나, 금속열 환원법 등에 의해 98~99 % 수준으로 제조된다. 이러한 Nd 잉곳 중에는 Li, Na, Mg, Al, Ca, O, C, N, H, Cl 등의 불순물 원소가 미량 단독으로 존재하지만, 그 밖 에 CO, CO2, SO2 등의 화합물이나 산화물(CeO2, Pr2O3, Nd2O3, Sm2O3, Tb4O7, Dy2O3 등)의 형태로 존재하며, 2 차적인 진공용해정련, 지역용해법 및 고상전해법 등의 정 련을 통해 99.9 % 수준의 고순도 Nd 금속을 제조한다.
따라서 본 연구에서는 용융염 전해법이나 금속열 환원 법에 의해 제조되어 국내에 시판되는 저품위 Nd 잉곳 (99 %)의 고순도화에 필요한 기초 데이터를 확보하기 위 해, 특히 Nd 잉곳의 용존 산소(O)량 저감을 위하여 비 교적 저온(890~970 °C)에서 고체 Nd금속과 용융 Ca 대 신 Ca 증기(vapour)를 접촉시켜 탈산거동을 조사하였다.
2. 실험 방법
본 연구에 사용한 시료는 상용 중국산 Nd잉곳(99 wt%, 산소농도 500 ppm이상)과 금속 Ca chips(98 %)을 사용 하였다. 탈산실험 1회에 사용한 시료 량은 5 × 5 × 7 mm 크기, 중량 약 12 g으로 절단한 Nd 잉곳과 Ca 량은 0.6~1.8 g(Nd의 5~15 %)으로 변화시켜 실험하였다.
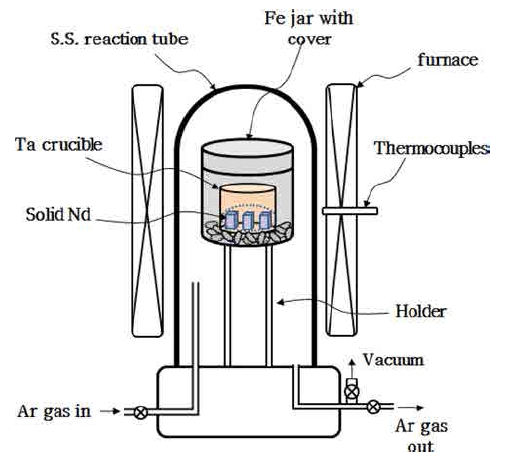
Fig. 1은 본 연구의 탈산실험에 사용한 실험장치의 개 략도를 나타낸 것으로서, 수직 전기저항식 튜브로와 stainless steel제 반응관을 사용하였다. 탈산반응 시 Ca의 증 발을 줄이기 위해 덮개가 달린 저탄소강으로 제조한 용 기를 사용하였으며, 용기 내측에는 Nd금속과의 반응을 억 제하기 위해 금속 Ta제 용기를 사용하였다. 더욱이 Ta 제 용기 내측에는 절단한 Nd 잉곳을 중앙에 넣고, 금 속 Ca는 Nd잉곳과는 액상으로 접촉하지 않고 증기로만 접촉하도록 하였으며, 실험온도는 Ca의 융점(845 °C)이상 이며, Nd잉곳의 융점(1024 °C) 이하인 890~970 °C범에서 1~5h동안 변화시켜 탈산실험을 행하였다. 탈산된 고체 Nd 시료는 소정의 크기로 절단하여 ONH분석기(Eltra Model ONH-2000, Germany)를 이용하여 잔존 산소량을 분석하 였다.
3.1. Ca에 의한 Nd잉곳 중 용존 산소의 탈산에 관 한 열역학적 고찰
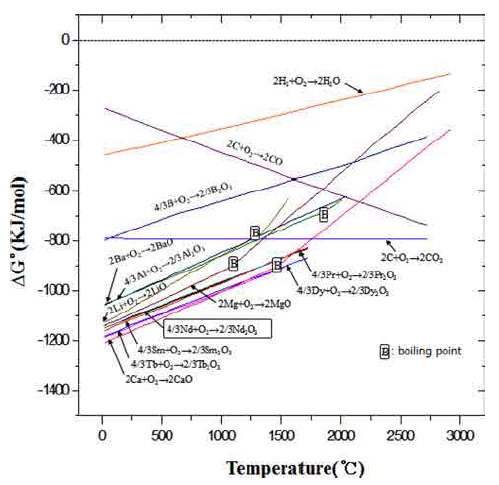
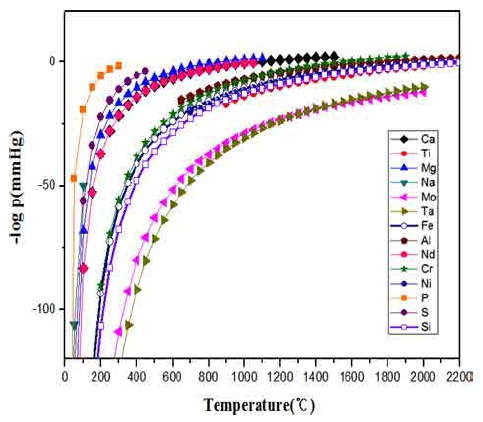
Fig. 2 및 3은 본 연구에서 Nd 잉곳 중의 용존 산소 량을 저감하기 위해 대표적 비금속 활성물질(H, C), 활 성금속(Al, Ba, Li, Mg, Ca) 및 희토류금속(Pr, Nd, Sm, Tb, Dy) 등의 산화물 생성에 대한 ΔGo-T도(Ellingham diagram)6) 및 각 원소의 온도에 따른 증기압 곡선7)을 나 타낸 것이다.
이러한 정성적 고찰로부터 고체상태의 Nd잉곳 중 용 존 산소의 탈산반응과(deoxidation reaction)과 Nd2O3의 환원반응을 위해서는 Ca 원소가 적합함을 알 수 있었으 며, 다음과 같은 반응식으로 나타낼 수 있다. 예를 들 면, 식 (1)은 금속 Ca의 과잉 첨가량에 의한 고체 Nd잉 곳의 탈산반응을 나타낸 것이며, (2)식은 927 °C(1200K) 에서 이론적으로 네오디뮴 산화물(Nd2O3)과 금속 칼슘 (Ca)에 의한 환원반응의 경우 ΔGo1300K= −59.01 kJ/mol로 환원반응이 가능하므로, 식 (1)의 탈산반응이 가능함을 추 정할 수 있다.
특히 희토류원소는 산소(O)와의 친화력이 크기 때문에 용존 산소량이 많아 진공용해정련, 지역용해법 및 고상 전해법 등의 2차적 정련공정을 거쳐 고순도 희토류금속 으로 제조하지만, 99.9 %이상의 고순도 희토류금속을 얻 기 위해서는 전술한 미량 불순물원소의 제거가 필수적 이다. 특히 산소의 잔존량을 50 ppm이하로 저감시키는 것 은 매우 어려운 것으로 알려져 있다.
3.2. Nd-O 및 Nd-Ca 2원계 평형상태도
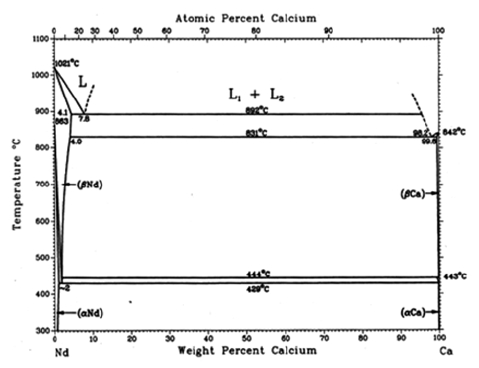
Fig. 4에 나타낸 Nd-Ca 2원계 평형상태도8)로부터 추 측할 수 있는 것은, 우선 Nd-rich 측의 경우, Nd의 융 점(1021 °C)이하의 비교적 저온에서 α-Nd 및 β-Nd 2개 의 고용체(S.S.)가 존재할 뿐만 아니라, 892 °C에서 공정 반응(7.8 wt%Ca)에 의한 Nd-Ca의 액상이 형성된다. 또 한 Ca-rich 측에서는 α-Ca 존재와 함께 Ca융점(842 °C) 보다 낮은 831 °C에서 공정반응(99.6 wt%Ca)으로 Ca-Nd 의 액상이 생성되기 때문에 용융된 Ca에 의해 고체상태 Nd 잉곳 중에 용존하는 산소(O)의 탈산은 어려울 것으 로 예측되었다.
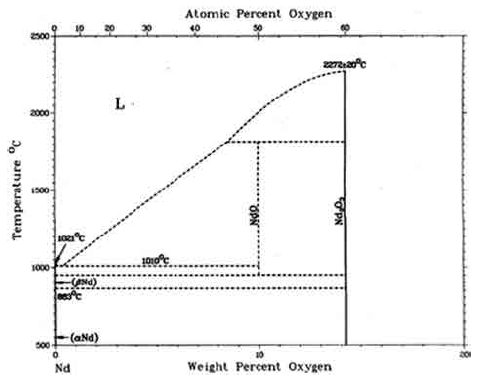
Fig. 5에 나타낸 Nd-O 2원계의 부분 평형상태도는 Massaski 등9)이 보고한 것으로, NdO 및 Nd2O3 2종류의 산화물이 존재하며, Nd금속 융점(1024 °C)보다도 낮은 1010 °C에서 불명료하지만 Nd-O 2원계상태도에서 공정반 응(약 0.05 wt%O)이 발생하여 온도 및 산소농도 상승과 함께 액상이 증가할 뿐만 아니라, 특히 2272 °C의 고융 점인 Nd2O3 산화물이 존재하는 것은 Nd 금속과 산소의 친화력이 매우 큰 것으로 추정이 가능하다.
3.3. 탈산 온도/시간에 따른 산소량의 변화
Fig. 6은 전항에서 고찰한 이론적 결과들로부터 실제 로 금속 Ca증기를 이용하여 Nd 잉곳 중 용존하는 산 소의 탈산에 관한 최적의 반응온도를 조사하기 위해, 우 선 금속 Ca량을 1.2 g, 반응시간을 1 h로 고정하고 890~ 970 °C범위에서 탈산실험을 행한 결과이다. 탈산온도가 높 아짐에 따라 산소량이 감소함을 확인하였다. 특히 970 °C 에서의 Nd 잉곳시료의 경우 잔존 산소량이 15.45 ppm 까지 감소하였으나, 시료 표면에 Nd-Ca 합금의 액상이 약간 형성되는 것이 관찰되어 이하의 모든 실험은 930 °C 에서 실시하였다.
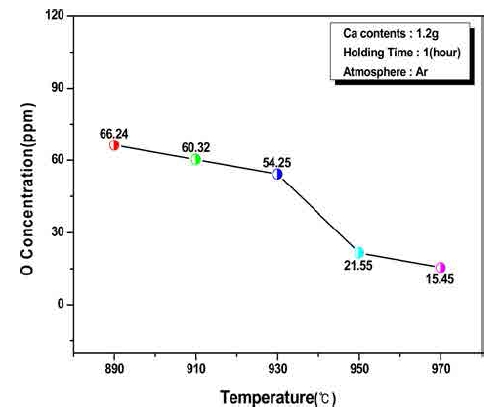
Fig. 6
Variation of residual oxygen for reaction temperature of solid Nd samples were prepared by deoxidation reaction with Ca vapour.
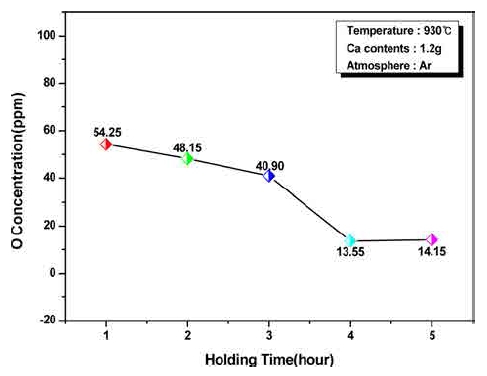
Fig. 7은 반응온도를 930 °C, Ca첨가량을 1.2 g으로 고 정하고, 반응시간을 변화시켜 실험한 결과로서, 반응시간 이 증가함에 따라 산소량이 감소하여 4시간 동안 반응 한 시료에서는 13.55 ppm까지 감소하였지만, 5시간의 시 료에서는 14.15 ppm으로 오히려 약간 증가하였다. 이러 한 결과는 Ca첨가량(1.2 g)이 부족한 상태에서 장시간 가 열로 인해 용융 Ca이 모두 휘발된 후, 반응기 내의 Ar 분위기 중의 미량의 산소가 유입되었기 때문인 것으로 추측되었다.
3.4. Ca 첨가량에 따른 산소량의 변화
Fig. 8 및 Fig. 9는 본 연구에서 최적의 Ca량을 조사 하기 위해 반응온도를 930 °C, 반응시간을 1h으로 고정 하고 Ca첨가량을 0.6~1.2 g(Nd 잉곳 중량의 5~15 %)범 위로 변화시켜 실험한 결과이다. Ca 첨가량이 증가함에 따라 감소하여 0.9 g이상이 되면, 20 ppm이하로 크게 감 소하였으며, 1.5 g 첨가한 시료에서 17.15 ppm으로 가장 적게 나타났지만, 1.8 g에서는 17.56 ppm으로 오히려 약 간 증가하였다.
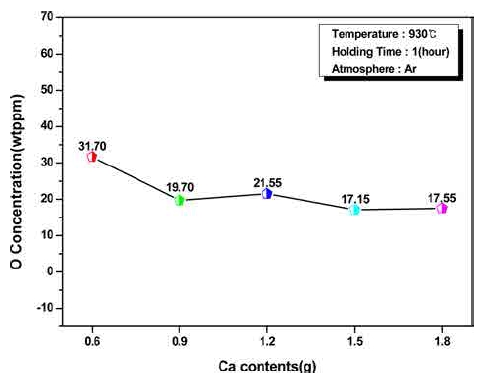
Fig. 8
Variation of residual oxygen for contents of addition Ca of solid Nd samples were prepared by deoxidation reaction with Ca vapour.
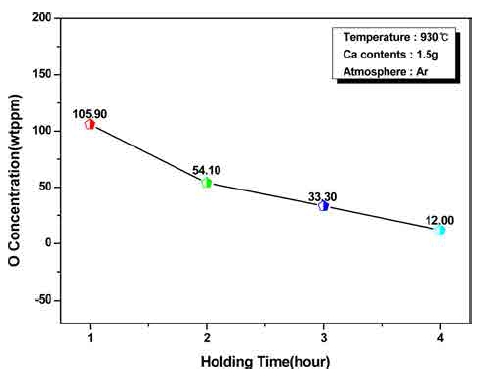
Fig. 9
Variation of residual oxygen for holding time of solid Nd samples were prepared by deoxidation reaction with Ca vapour.
따라서 본 연구에서는 반응온도를 930 °C, Ca첨가량을 1.5 g으로 고정하고, 재차 최적의 반응시간을 조사하기 위 해 실험하였으며, Fig. 9는 그 결과를 나타낸 것으로서, 탄산반응 시간이 증가함에 따라 산소량이 선형적으로 감 소하여 4시간 동안 가열한 시료에서 12.00 ppm까지 감 소함을 확인하였다.
4. 결 론
본 연구는 금속 Ca에 의한 고체 Nd잉곳 중의 용존 산 소량을 저감하기 위한 기초연구로서, ΔG-T도, Nd-O 및 Nd-Ca 2원계 평행상태도 등을 통한 열역학적 고찰과 함 께 Nd 잉곳 시료와 Ca 용액이 직접 접촉하지 않고 Ca 증기를 이용한 탈산반응을 조사하기 위해 반응온도는 890~970 °C, 반응시간은 1~5h 및 Ca첨가량은 0.6~1.8 g (Nd잉곳의 5~15 %)범위로 변화시켜 실험하였다.
1) 927 °C(1200K)에서 Nd 산화물(Nd2O3)과 금속 칼슘 (Ca)의 이론적 반응에 따른 ΔG1300K= −59.01 kJ/mol이므 로 환원반응이 가능할 뿐만 아니라, 고체 Nd 잉곳 중 의 용존 산소의 탈산반응이 가능함을 추정할 수 있다.
2) 금속 Ca에 의한 탈산반응 시, Nd-Ca 2원계 평형상 태도로부터 추측할 수 있는 것은, 우선 Nd-rich 측의 경 우, Nd의 융점(1021 °C)이하에서 α-Nd 및 β-Nd 2개의 고용체(S.S.)가 존재하며, 892 °C에서 공정반응(7.8 wt%Ca) 에 의한 Nd-Ca의 액상이 형성되며, 반면에 Ca-rich 측은 α-Ca존재와 함께 Ca융점(842 °C)보다 낮은 831 °C에서 공 정반응(99.6 wt%Ca)으로 Ca-Nd의 액상이 생성되기 때문 에 용융된 Ca에 의해 고체상태의 Nd 잉곳 중에 용존 하는 산소(O)의 탈산은 어려울 것으로 추측되었다.
3) 또한 Nd-O 2원계의 부분 평형상태도에 의하면, NdO 및 Nd2O3 2종류의 산화물이 존재하며, 1010 °C에서 Nd- O의 공정반응(약 0.05 wt%O) 및 Nd2O3 산화물 존재 등 은 Nd금속과 산소의 친화력이 매우 큰 것으로 추정되 었다.
4) Nd 잉곳 시료와 Ca용액이 직접 접촉하지 않고 Ca 증기를 이용한 탈산반응에 있어서, 최적의 탈산조건으로 반응온도는 930 °C, 4h 동안 그리고 Ca량은 1.5 g(Nd잉 곳의 13 %) 첨가하여 실험한 시료에서 잔존 산소량이 12.00 ppm까지 감소함을 확인하였다.