1.서 론
안정적인 수소 동위원소인 중수소는 화학 추적자(tracer), NMR 분광법에서 중수소화 용매, 대사 속도가 느린 약 물의 합성, 원자로에서 감속재 등으로 사용되고 있으며, 또 다른 동위원소인 삼중수소는 방사성 동위원소로 최 근 핵 폐기물에서 이를 제거하는 것이 큰 이슈가 되고 있다. 중수소와 삼중수소는 경수소 대비 자연적으로 존 재할 확률이 각각 0.0156 %와 10-17 % 이다.1-2) 이러한 수소 동위원소는 크기, 모양 및 열역학적 특성이 서로 매우 유사하므로 동위원소 분리가 매우 어려우며 분리 를 위한 분석 장비도 매우 제한적인 상황이다. 따라서, 본 연구에서는 일반적인 경수소(H2)에서부터 자연계 존 재 확률이 낮은 중수소(D2)와 삼중수소(T2)를 분리하는 측 정기술에 대해서 논하고자 한다.
현재 수소동위원소 분리하기 위해 산업 분야에서 사용 하고 있는 기술은 girdler sulfide (GS) 공정과 극저온 증류법이다. GS 공정은 H2O[일부 중수(D2O) 포함] 및 H2S로부터 중수를 분리하기 위해 수소와 중수소의 화학 반응 속도 차이를 이용한다. 이 공정에는 약 60 m 높 이의 탑에 수 백가지의 분리 공정이 탑재되며, 선택도 는 1.3이고, 1 kg의 중수를 생산하는데 30 GJ의 에너지 가 필요하다. GS 공정은 일반적으로 D2O 함량을 20 % 로 만들고 생성물을 99 mol%까지 농축한 후 전기분해 를 통해서 중수소를 생산하게 된다.3) 이 공정은, 중수소 가스를 직접적으로 생산하는 것이 아니라 중수를 생산 하는 공정이라고 할 수 있다. 극저온 증류법은 동위원 소 간의 끓는점 차이를 이용하여 분리하는 것으로 1.5 정도 수준의 낮은 선택도를 가지는데, GS 공정과 더불 어 에너지 집약적이며 선택도가 낮다는 단점을 가진다.4)
고비용의 GS 공정과 극저온 증류법을 대체하기 위해 서 최근 다공성 흡착제 이용한 수소 동위원소 분리 기 술에 대한 실험 연구들이 수행되고 있다. 여러 다공성 물질 중에서도 주로 결정성을 가진 금속-유기 골격체 (metal-organic frameworks: MOFs), 제올라이트와 같은 재료들을 중심으로 많은 연구들이 진행되어 왔다. 이는 흡착제의 기공 크기가 양자 분리 효과를 향상시킬 수 있는 중요한 요인으로 알려져 왔으며 이러한 효과는 극 저온 분야에서 극대화되는 것으로 알려졌다.5) 다공성 소 재들의 동위원소 분리 성능을 평가하기 위한 대표적인 두 가지 방법으로 이상 흡착 용액이론(ideal adsorbed solution theory: IAST)을 이용하는 간접적인 방법과 열 탈착 분석 장비(thermal desorption spectroscopy: TDS) 를 이용하는 직접적인 측정 방식이 있다. IAST의 경우, 측정된 순수 수소 또는 중수소의 흡착량을 압력에 따른 비율로 변환하여 간접적으로 분리 성능을 비교하는 것 이다. 보통 이력현상(hysteresis)이 없다면 수소와 중수소 의 분리도를 계산할 수 있다. 하지만, IAST의 경우 계 산 과정에 있어서 종종 데이터를 사용할 수 있는 범위 를 넘어서 등온선을 외삽해야 하는 경우가 발생하기 때 문에, 이로 인해 실제 선택도와 차이가 발생하는 한계 점이 있다.6) TDS를 이용하는 경우, 동위원소 혼합기체 를 주입한 후 온도를 극저온 이하로 낮춘 다음 승온 시 키면서 탈착되는 수소 동위원소를 질량 분석기(잔류기체 분석기, RGA)로 분석하여 기체의 정량적 분석을 하는 것 이다. TDS 장비를 이용할 경우, 직접적인 선택도 계산 이 가능하여 활용도가 높으나, 사용 가능한 흡착제의 양 에 한계가 있어서, 대용량 상업화 기술에 바로 적용하 기에는 어려움이 따른다.7) 따라서 개발된 소재를 상업화 공정에 응용하기 위해서는, scale-up 된 규모로 소재 분 리 성능에 대한 평가/분석이 가능한 시스템이 필요하다.
본 논문에서는 실험실 규모에서 최대로 scale-up 한 극 저온 파과(breakthrough) 곡선 측정 장비에 관한 내용에 중점을 두고 있다. 액체 질소 온도인 77 K에서 H2와 D2 의 혼합기체에 대한 분리 공정을 살펴보기 위한 파과 곡 선 측정 장비 시스템을 설계 및 제작하였다.
2.이 론
2.1. Quantum sieving (QS)
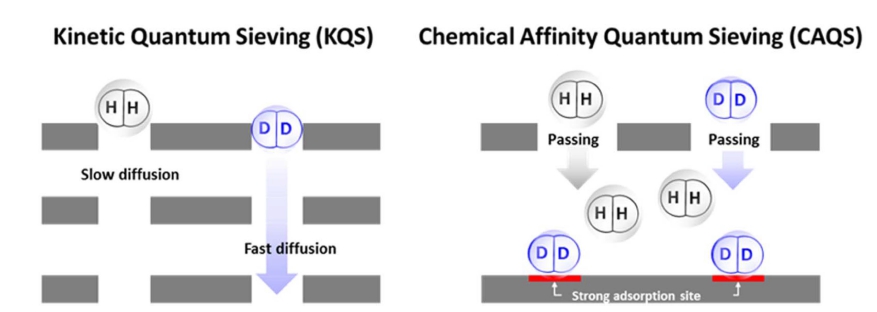
Kinetic quantum sieving (KQS)은 수소 동위원소의 드 브로이(de Broglie) 파장의 차이를 기반으로 하는 분리 메커니즘으로, Beenakker 연구진에 의해서 1995년에 처 음 제안되었다.8) 다공성 물질의 입구 기공 크기가 분리 하려는 분자의 드브로이 파장과 비슷할 경우 KQS를 이 용한 분리에 적합하다. KQS 메커니즘 상에서 더 가벼 운 동위원소에 대한 높은 확산 장벽이 존재하며, 특히, 온도가 매우 낮을 경우 동위원소의 분리에 상당한 영향 을 미칠 정도로 분자 확산도의 차이가 크게 벌어질 수 있다.9) 2013년에 발표된 자료에서는, KQS를 이용하여 H2/D2 혼합 가스를 분리할 경우, 최적의 기공 크기는 3.0 ~ 3.4Å으로 제안하고 있다.10)
또 다른 방식으로는 열역학적인 효과를 이용하는 것이 다. 수소동위원소 분자는 각 질량 차이가 가장 크게 나 고, 이로 인해 서로 다른 친화력을 가지게 된다. 즉, 질 량 차이로 인해서 서로 다른 영점 에너지(ZPE)를 초래 하므로, 각 동위원소에 대해 서로 다른 흡착 엔탈피(ΔH) 가 발생한다. 이러한 흡착 엔탈피 차이로 인해서, 더 무 거운 동위원소를 우선적으로 흡착하여 액체 질소 온도 (77 K) 이상에서도 큰 분리계수를 유발할 수 있다. 이 를 chemical affinity quantum sieving (CAQS)라고 한다 (Fig. 1).
2.2. 파과 곡선 분석(Breakthrough curve analysis)
실제 산업 분야에서의 가스 분리 성능의 평가는 정적 인 평형(static equilibrium) 상태보다는 동적(dynamic) 조 건과 더 가깝다고 할 수 있으므로, 파과 곡선의 분석이 필요하다. 파과 곡선 분석은 frontal chromatography이라 고도 알려져 있는데, 금속-유기 골격체에서의 기체 분리 및 제올라이트에서의 수소 동위원소 분리 연구 분야에 서 사용돼 왔다.
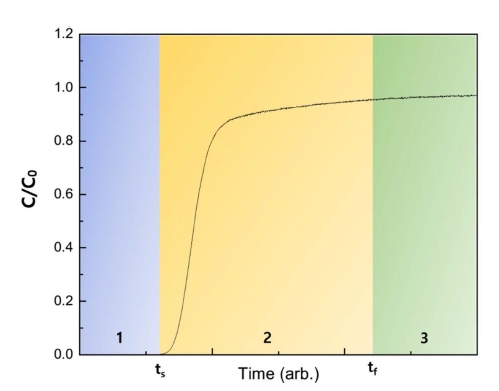
일반적으로, 파과 곡선 측정 실험은 컬럼 혹은 베드 형 태에 채워진 흡착제에 기체를 공급한 후, 흘러나오는 기 체의 성분을 질량 분석기 또는 검출기를 사용하여 측정 하고 있다. 흡착제의 흡착 성능, 선택도, 동역학은 파과 곡선 분석뿐만 아니라 공급된 기체의 유량, 공급된 기 체 및 흘러나오는 기체의 구성 등을 분석하여 측정할 수 있다. Fig. 2은 일반적인 단일 기체에 대한 단일 흡착제 의 파과 곡선이다. 흡착물이 흘러나오는 농도(C) 대비 공 급된 농도(C0)의 비율이 시간에 대한 함수로 나타낸다. 1단계에서, 기체는 흡착제에 정해진, 일정한 유량만큼 흘 러 들어가서 전부 흡착이 되어, C/C0는 0이다. 2단계는 가스가 흡착제 베드를 완전히 통과하기 시작하는 시간인 초기 파과 시간(initial breakthrough time: ts)에서 시작된 다. 2단계를 통해서, C/C0는 완료 파과 시간(complete breakthrough time: tf)에서 1이 될 때까지 증가한다. 3단 계에서 C와 C0의 값은 같게 되며, 시스템은 평형상태에 이르게 된다.
Fig. 2에서 흡착제 컬럼에 흡착된 흡착물의 몰 수는 다 음 식을 이용하여 데이터로부터 계산 가능하다.
여기서, F는 유량[cm3/min], C0는 주입 농도[mol/cm3], C(t)는 시간 t [min]에서 흘러나오는 농도를 말한다. 이 식을 이용하여 유량에 의해 설정된 압력에서 재료의 흡 착 용량을 측정할 수 있게 된다. 이 계산에는 흡착 사 이트의 기체 외에도 흡착제의 불용체적(dead volume)에 머무는 기체가 포함되기 때문에 흡착물의 양에 대한 근 사치라고 할 수 있다.11)
물질 전달 구역(mass transfer region)이라고 하는 2 단계에는 파과 실험에서 동역학에 관한 정보들이 포함 되어 있다. 일반적으로, 파과 실험의 동역학을 이해하기 위해서는 측정된 데이터를 이론적 모델과 비교하는 것 이 중요하다. 주로 세 가지의 파과 동역학 모델이 사용되 고 있는데, Thomas,12) Yoon-Nelson,13) Adams-Bohart14) 모델이 있다. Thomas 모델은 가장 널리 사용되는 모델 중의 하나로서 Langmuir 동역학(kinetics)을 따르며, 컬 럼 흡착에서 축 방향 분산을 무시할 수 있다고 가정하 는 것을 특징으로 한다. Yoon-Nelson 모델은 활성탄에 대한 가스 흡착에 기초한 비교적 간단한 모델로, 흡착 제의 흡착 확률 및 파괴확률 등으로 기술하는 것이 특 징이다. Adams-Bohart 모델에서는 흡착률을 흡착제의 잔 류 용량 및 흡착 종(species)의 농도에 비례한다는 가 정을 기본으로, 파과 곡선의 초기 부분(10 ~ 50 %)을 기 술하는데 사용된다.15) 이 모델들을 이용하여 최대 흡착 용량, 물질 전달 계수, 비율 상수 등을 계산할 수 있게 된다.
혼합기체 주입에 관한 파과 실험은 흡착제의 분리 능 력을 평가하는 데 응용할 수 있다. Fig. 3은 두 종류의 기체를 1:1로 혼합하여 주입한 경우, 2번 기체가 우선적 으로 흡착되는 경우의 일반적인 파과 곡선을 나타낸 다. 여기서 C0는 총 주입 농도이며, 각 성분은 0.5 C0 의 농도를 가진다. 각 기체의 초기 파과 시간(ts1, ts2)의 차이와 1번 기체의 오버슈트(overshoot: C/C0가 0.5를 넘 는 구간)는 우선 흡착 현상이 일어나는 증거라고 할 수 있다. 오버슈트 효과는 1번 기체가 2번 기체로 대체되 어 발생하는 현상이며, 물질 전달 구역(2단계)의 시작부 분에서 C/C0 값이 0.5를 넘는 현상을 보인다. 일반적으 로, 물질 전달 구역(시간에 대한)에서 분리 가능한 혼합 기체들 간의 초기 파과 시간 차이를 최대화하는 것이 중 요하며, 이는 분리 이후 흡착제가 자주 재생될 필요가 없다는 것을 의미하는 것이다. 참고로 물질 전달 구역 의 시간은 온도, 유량, 초기 농도, 흡착제의 종류에 따 라서 변한다.
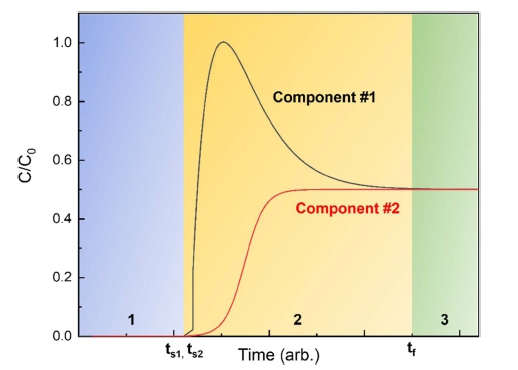
Fig. 3
Phases of typical two-component breakthrough curve where component 2 is preferentially adsorbed (composition of feed mixture is 1:1).
두 종류 혼합기체의 파과 곡선은 흡착제 컬럼의 선택 도를 계산하는 데 사용될 수 있다. 선택도는 일반적으 로 흡착된 2번 기체의 몰(n2ads)과 기체 상태에 대한 몰 (n2gas)의 비율을 1번 기체에 대해서 같이 나눠주는 것으 로 아래 식과 같이 정의할 수 있다.
본 논문에서는, n1gas와 n2gas의 값은 같아서, 실제 선택 도의 값은 n2ads와 n1ads의 비로 계산된다. 2번 기체의 파 과 실험에서 nads 값은 아래 식과 같으며,
여기서 C0는 총 주입한 기체의 농도이며, 그 외의 다른 변수의 값은 식 (1)과 동일하다. 식 (3)과 Fig. 4를 조합 하게 되면, 선택도는 아래 식과 같이 변경할 수 있다.
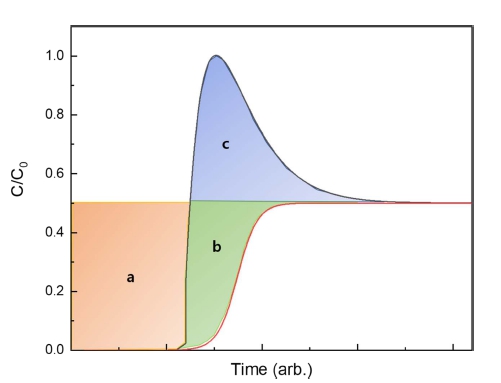
Fig. 4
Selectivity can be calculated as a molar ratio of adsorbed Component 2 (Area(a+b)) to adsorbed Component 1 (Area(a-c)).
위 식은 두 기체의 유량과 초기 농도가 같고, 1:1의 비율로 주입한 혼합기체에 대해서 간략화 된 식이다. 이 렇게 계산된 기체의 선택도는 흡착제의 입자간 공극과 비선택적 기공(비선택적 부피) 뿐만 아니라 흡착 부의( 선택적 부피)에 흡착되어 있는 가스 전체의 선택도를 의 미한다.11)
분리의 용이성 측면에서, 파과 실험은 수소 동위원소 혼합 기체 중에서 우선적으로 덜 흡착되는 기체를 분리 하여 회수하는 간단한 메커니즘을 제공한다. 흡착이 덜 되는 수소가 먼저 흘러나오기 때문이다. 우선적으로 흡 착이 잘 되는 기체를 분리하기 위해서, 일반적인 파과 실험의 조건을 조절하는 것이 필요하다. 다공성 물질을 이용하여 중수소를 분리해내는 것이 목적인 경우, 더 강 력하게 중수소를 흡착하는 물질을 사용하는 것이 파과 실험에서는 적합하다고 할 수 있다. 파과 실험은 수소 동위원소 분리에 있어서 중수소를 분리해내는 첫 번째 단계의 실험 방법일 뿐이며, 실제로는 압력 및 온도 변 동 흡착(PSA 혹은 TSA)와 같은 공정을 이용하여 전략 적으로 중수소를 분리하는 것이 가능하다.
3. 실험 방법
3.1. 실험 설정
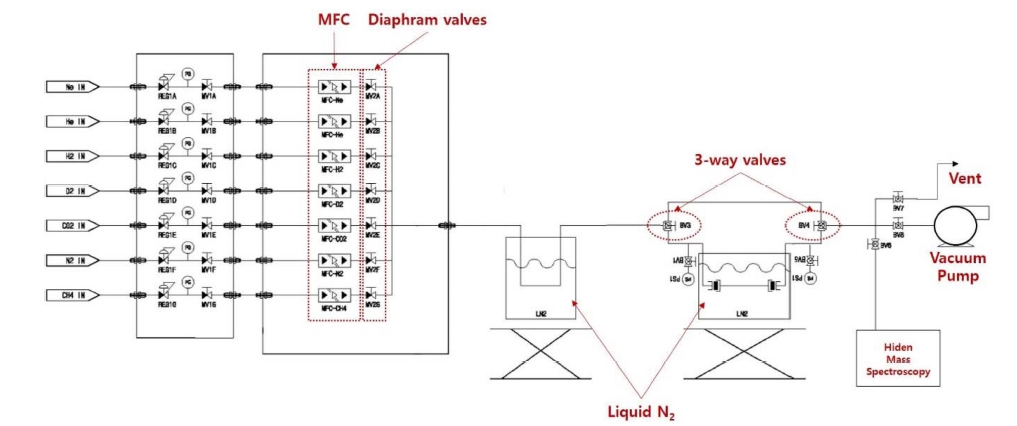
Fig. 5은 본 논문에서 구성한 파과 실험의 구성도를 나타낸다. 기체를 공급하기 위해서 8개의 기체를 각각의 유량 제어기(mass flow controller: MFC)에 연결하여 시 스템을 구성하였으며, hiden quantitative gas analysis (QGA, HAL 201RC)를 질량 분석기로 사용하였다. 파과 실험 동안, 교정된 유량 제어기를 통해서 정해진 유량 의 고순도 기체들을 공급하였으며, 유량 제어기 앞단에 는 다이어프램(diaphragm) 밸브를 사용하여 기체 공급을 제어하였다. 또한 3-way 볼 밸브를 사용하여, 시료 컬 럼과 우회(bypass) 라인의 흐름을 직접적으로 제어하였 다. 시료 컬럼의 온도는 제어기에 연결된 가열 재킷과 액체 질소를 이용하여 제어하였고, 주입 가스의 압력과 조성비는 압력 게이지와 질량 분석기를 사용하여 측정 하였다. 과잉 기체는 진공펌프 및 다른 경로를 통해서 외부로 배출된다.
실험에 사용된 시료 컬럼은 Fig. 6에 나타낸 것과 같 이 디자인되었다. 1/2인치 SUS 관을 12 cm 길이로 잘 라서 양쪽을 기체 라인에 연결할 수 있도록 너트로 마 감하였다. 길이 대비 직경의 비는 약 30:1 였다. 제작된 시료 컬럼은 가열 재킷을 이용하여 내부의 시료를 재생 하거나, 상온 실험을 진행할 때 온도를 유지할 수 있도 록 하였다. 77 K의 환경을 조성하기 위해서는 제작한 시 료 컬럼 전체를 액체 질소에 담궈서 온도를 제어하였다.
본 논문에서는 제올라이트 13X를 수소 동위원소 분리 소재로 사용하여 실험을 진행하였다. Sigma Aldrich에서 판매하는 파우더 형태를 구매하였으며, 시료 컬럼의 직 경을 고려하여 직경 4mm 펠릿을 다수 제작하여 시료 컬럼에 채워 넣었다. 펠릿을 제작하기 위해서 (1) 질량 을 측정한 후 바닥 부분과 금형 본체를 조립한 후, (2) 금형 본체에 시료를 주입한 다음 (3) 기둥과 유압 프레 스를 이용하여 0.25 ton 이하의 압력으로, 시료를 눌러 서 펠릿 형태로 제작하였다. 시료 컬럼 내에 펠릿을 넣 은 후, 남는 공간은 유리 섬유(KANTO Chemical)로 막 아 주었다.
3.2. Breakthrough 실험 절차
본 논문의 목적은 파과 실험의 기초에 대해서 연구하 고, 다공성 물질을 이용한 극저온 수소 동위원소 분리 성능을 측정할 수 있는 시스템을 제작하는 것이다. Fig. 7는 두 종류의 혼합 기체에 대해서, 일반적인 질량 분 석기를 사용하는 파과 실험 절차를 단계별로 나타내는 그림이다.
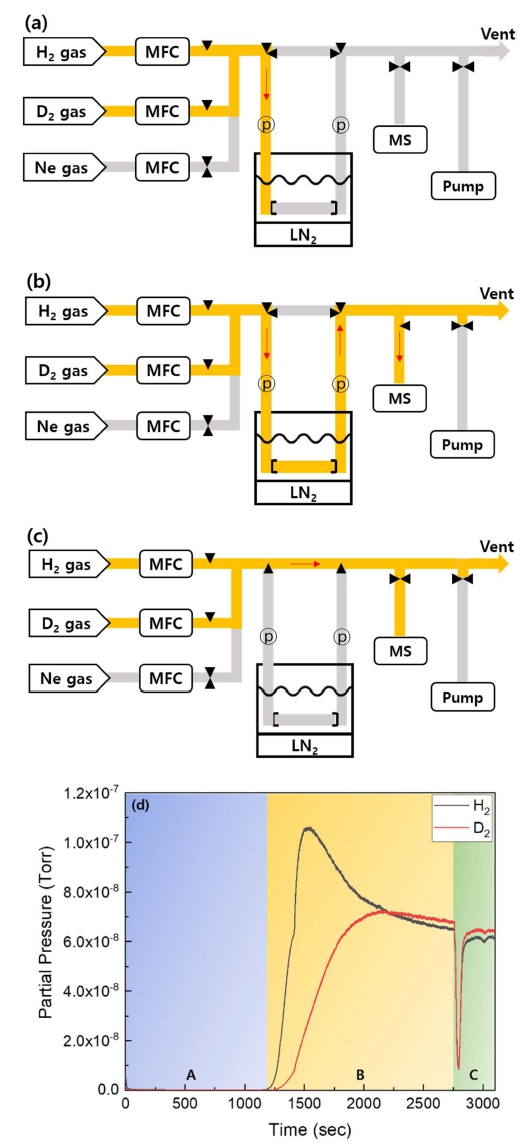
Fig. 7
(a) Removal of residual gas in the breakthrough system by flowing Ne. (b) The feed gas is adsorbed on the sample column. (c) Breakthrough occurs and gas flowing through the sample is measured by the mass spectrometer or vented. (d) Raw data from typical breakthrough experiments measured on mass spectrometer. (H2 signal is black, D2 signal is red). Zone A corresponds to step (a), zone B corresponds to step (b), and zone C corresponds to step (c).
여러 개의 펠릿으로 채워진 시료 컬럼에 가열 재킷을 감아서, 다공성 물질의 흡착되어 있는 기체들을 완전히 탈착 시킨다. 본 실험에서는 제올라이트 13X로 파과 실 험을 하기에 앞서 가열 자켓을 이용하여 150도에서 12 시간 이상 동안 시료 컬럼을 가열하고 진공 펌프를 이 용하여 진공 탈기(vacuum degassing) 공정을 진행하였 다. 다공성 물질의 경우 흡착 사이트가 물 또는 다른 기 체 분자로 인해서 막혀 있을 수 있기 때문에, 이러한 탈 기 공정을 통해서 흡착 가능한 사이트의 수를 증가시킬 수 있다.
전처리를 거친 시료 컬럼을 충분한 양의 액체 질소에 1시간 이상 담궈 77K의 극저온 환경을 조성한다.
진공 탈기 공정과 온도 조절이 끝난 후, 시료 컬럼의 양쪽에 있는 두 개의 3-way 밸브를 우회 라인 쪽으로 조절, He을 20 sccm의 유량으로 5분 이상 주입하여 시 스템의 라인 상에 남아있는 다른 기체를 최대한 제거한 다. 질량 분석기의 성능에 따라서, D2와 He을 구분할 수 없는 장비일 경우, He 대신 Ne을 주입한다.
시료 컬럼 쪽으로도 동일한 작업을 진행하되, 상압(1 bar)에 도달할 때까지 He 혹은 Ne을 주입한다. 만일 He 혹은 Ne을 캐리어 가스로 사용할 경우에는 실험이 끝 날 때까지 계속 주입한다.
시료 컬럼의 양쪽에 있는 두 개의 3-way 밸브를 시 료 컬럼 쪽으로 조절, 측정할 기체(H2/D2)를 3 sccm의 유량으로 동시에 주입하면서, 질량 분석기 소프트웨어에 서 유량에 따른 부분압을 측정하기 시작한다[Fig. 7(a)].
측정 소프트웨어 상에서 시스템이 평형 상태에 이르게 되는 것이 확인되면[Fig. 7(b)], 다시 두 개의 3-way 밸 브를 우회 라인 쪽으로 조절하여, 최종적인 부분압이 평 형 상태에서의 부분압과 동일한 지를 확인한다[Fig. 7(c)]. 각 단계별로 질량 분석기에서 측정된 미가공 데이터를 Fig. 7(d)에 나타내었다.
3.3. 데이터 획득 및 처리
모든 데이터는 Hiden QGA 질량 분석기 및 MASoft 10 소프트웨어를 이용해 측정되었다. 주입되는 기체의 신 호에 대한 기준선을 정하기 위해서는, 실제 파과 실험 을 시작하기 전부터 질량 분석기로 데이터를 수집한다. t = 0인 지점은 3-way 밸브 조절 이후, 시료 컬럼이 혼 합 기체에 처음으로 노출되는 지점에서, 잔여 기체들이 질량 분석기에 흘러 들어간 다음 가장 낮은 부분압을 기 록하는 시간으로 정의한다.
수소 동위원소 분리를 진행한 본 실험에서는, 1:1 H2/ D2 혼합 기체가 항상 공급되었으며, 각 파과 실험에서 평형에 도달할 때까지 데이터가 수집되었다. 평형 상태 의 H2 및 D2 신호(부분압)는 이상적으로는 동일해야 하 는데, 질량 분석기의 특성 및 시료 컬럼의 상태에 따라 서 조금 다를 수 있다. 이럴 경우에는 두 동위원소 중 에서 상대적으로 신호가 큰 기체가 흡착되는 구간(Fig. 7(d)의 A 구간)의 신호를 배경 신호(background signal) 로 지정하여, 원래 데이터에서 제거하여 두 기체 신호 의 최저 레벨 구간을 맞추어 주는 작업이 필요하다. 다 음으로 평형상태의 도달한 구간에서의 신호가 동일하도 록, 더 낮은 신호가 측정된 기체에 스케일 팩터(scale factor)를 곱하여, 평형상태의 신호 또한 C = 0.5가 되도 록 조정한다.
4. 결과 및 고찰
다음 데이터는 Fig. 8에 나타낸 시료 컬럼에서 제올라 이트 13X 1 g의 시료를 사용하여 얻은 것이다. 시료의 길이는 약 10 cm이며, 직경은 1/4인치 SUS 튜브의 내 경인 4 mm이다. 파과 실험은 상온[Fig. 8(a)]과 77 K [Fig. 8(b)]에서 진행되었다. 상온 측정 결과의 경우, 두 동위원소의 파과 시간은 즉각적이었으며, 거동에 있어서 관찰 가능한 차이가 없었다[Fig. 8(a)]. 이는 제올라이트 13X가 수소를 많이 흡착하지 않아서 상온에서 KQS 효 과를 나타내지 않기 때문으로 보인다.
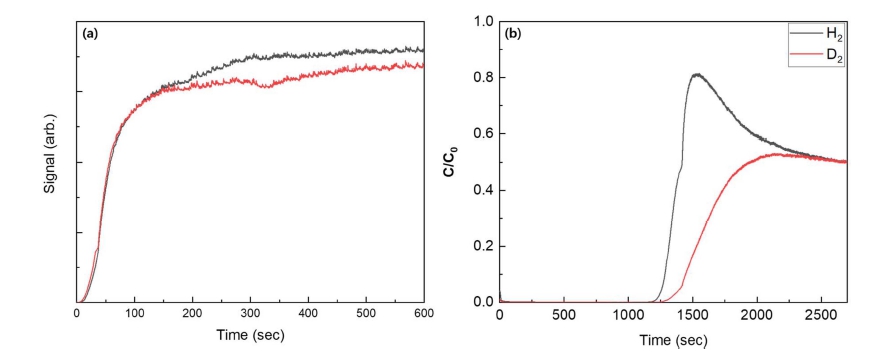
Fig. 8
Zeolite 13X breakthrough experiment results at (a) room temperature and (b) 77 K, each with a flow rate of 3 sccm and 1:1 H2/ D2 mixed gas conditions.
상온의 결과와 비교해서, 액체 질소에 담근 시료 컬럼 을 사용하여 파과 실험을 수행한 경우, 동위원소 간 흡 착 차이가 일부 관측되었다. Fig. 8(b)에 나타낸 초기 파 과 시간은 약 20분이었으며, 이는 77K에서 두 동위원 소가 모두 흡착된다는 것을 의미한다. H2와 D2의 파과 시간 차이와 H2의 오버슈트가 존재하는 것은 제올라이 트 13X에 H2보다 D2를 우선척으로 흡착된다는 것을 의 미한다. 초기 파과 시간의 경우 약 1,200 sec로, 다른 다 공성 물질인 Cu(I)-MFU-4l MOFs와 제올라이트 5A를 이용한 유사한 조건의 실험 결과와 비교하여 각각 약 4 배, 1/5배의 결과를 보였다.16-17) 이러한 초기 파과 시간 의 차이는, 시료 컬럼에 주입되는 기체의 유량, 펠릿의 모양, 펠릿 제작 조건 등의 차이에서 기인한 것으로 보 인다.
측정된 파과 곡선을 바탕으로, 식 (4)를 이용하여 계 산된 선택도의 값은 약 1.54 였다. 이 선택도 값은 다 른 제올라이트 종류인 5A, Y를 사용한 비슷한 조건의 파과 실험 결과인 1.6과 유사한 수치였으며,18) 100 K의 온도에서 Cu(I)-MFU-4l은 강력한 Cu open metal site로 인한 CAQS 효과로 인해, 약 8의 높은 선택도를 보였다.
5.결 론
본 논문의 목적은 극저온에서 다공성 소재를 이용한 수 소 동위원소의 분리를 실험하기 위한 파과 곡선 측정 장 치를 설계하고, 제작하여 실험하는 것이었다. 다공성 물 질인 분자 체 제올라이트 13X를 이용하여 파과 실험을 진행하였으며, 77 K의 온도에서 H2 보다 D2가 우선적으 로 흡착이 되는 결과를 관측하였다. 측정된 77K 선택 도는 약 1.54였으며, 이는 유사한 환경에서 다른 제올라 이트를 이용한 파과 실험 결과와 비슷한 선택도 수준이 었음을 확인하였다. 측정된 선택도는 산업용(기상) 수소 동위원소 분리 공정인 20 K 극저온 증류법(1.5@24K)과 유사한 결과를 보여주었다. 이번 결과는 향후 M O F 등 결정성 소재의 특성 분석에 많이 활용될 수 있을 것이 라 기대하고 있다.