1. 서 론
온도의 함수로 이종 재료와 접촉하는 유리 계면에서 고상-액상 상태 사이의 부피 자유에너지 차이가 결정상 형성을 촉진한다고 알려져 있다.1) 이로 인해 유리 계면에서 형성되는 불균일 핵생성 2차상에 관한 다양한 연구가 보고되고 있다. 기존의 연구에서 유리 계면에서 형성되는 불균일 핵생성인자로 재분해, 핵생성제, 그리고 산화환원 반응 등이 제시되고 있다.
불균일 핵생성 가성성 인자로서 규산알루미노유리/포스테라이트(Mg2SiO4) 계면에서의 Mg2SiO4 재분해에 의한 MgO-Al2O3-SiO2 액상 공융점은 고삼중석(SiO2), 프로토엔스테타이트(MgSiO3), 그리고 코디어라이트(2MgO・2Al2O3・5SiO2)와 같은 불균일 결정상 형성이 있다. 또한 지르코니아와 AZS(Al2O3- ZrO2-SiO2계)유리 계면에서 ZrO2가 핵 형성제로 작용하여 클리노엔스타이트(clinoenstatite)를 형성한다.2)
산화환원 반응은 포스테라이트/창연산화납유리/SUS 304로 구성되는 샌드위치 계면에서의 용질형성과 레독스(redox) 반응이 있다.3) 이 과정에서 PbO용질 형성과 Pb와 Bi원소 확산에 의한 급격한 표면장력 감소, 그리고 금속 측은 전자를 내어놓고 유리의 산소이온을 금속이온이 공유하는 산화환원 반응에 의해 불균질 핵생성이 일어난다고 보았다.2) 이 경향은 인코넬(inconel)/비스메이트(bismate)유리 계면에서 금속의 산화층 산소가 고갈되면 유리에서 이동한 산소와 금속이온에 의한 반응과 물질 확산 모델과 유사하다. 이 모델은 금속의 산화환원 반응과 농도 구배에 의한 원소 확산이 동시에 진행되어 금속/유리 계면에서 2차 상이 형성된다고 보았다.
이종 접합 유리 계면에서 형성되는 2차상은 유리 양이온 확산, 금속이온의 산화환원 반응에 의한 계면에너지 감소로 젖음성, 경도, 영율, 그리고 미세구조 변화가 나타난다. 이 불균질 2차상의 원인을 액상공융점, 산소공유에 의한 원자이동 또는 표면배열에 의한 자유에너지 변화와 관련이 있다고 볼 수 있다.4,5) 이에 반해 과냉각액체의 융액 냉각 과정에서 발생하는 결정화와 분상은 이종재료 계면에서 2차상을 형성하는 가성성 인자와 구별된다.6,7) 또한 유리전이온도(Tg) 이상에서 상이한 이력곡선, 결정화와 분상은 구조변화에 의한 연속적인 엔탈피와 비열 변화를 수반한다.8) 따라서 유리와 금속 접합 계면에서의 화학반응, 그리고 이동 물질 종에 따른 결정상 형성에 미치는 요인에 관한 사례별 연구가 필요하다. 이는 재분해, 핵생성제, 그리고 산화환원 반응에 의해 형성된 결정상은 유리의 분상, 그리고 유리조성을 제형한 결정화 유리기구와는 구별됨을 의미한다.
이런 관점에서 본 연구에서는 온도의 함수로 쾌삭강/창유리 계면에서 물질 확산, 금속표면화학, 미세구조, 밀도, 그리고 레독스 반응 분석으로 2차상 형성 가성성 인자와 유리 분상을 비교 고찰하고자 하였다.
2. 실험 방법
금속과 유리 계면 반응에 사용된 창유리와 납쾌삭강 시편 조성과 물성은 Table 1과 같다. 유리와 금속 하우징 가공형상은 Fig. 1과 같다. 제조 과정에서 시편들에 부착된 기름 성분을 제거하기 위하여 0.2 % NaOH용액에 5 min 동안 함침 시켰다. 함침 시편은 증류수와 에탄올을 이용하여 순차적으로 세척한 후 150 °C에서 2 h 동안 건조하였다. 금속 하우징에 유리를 결합한 시편을 전기로에서 900 °C~1,050 °C, 50 °C 간격으로 접합반응 시킨 4종의 시편을 얻었다. 시편의 열처리 조건은 공통적으로 승온속도와 냉각속도는 5 °C/min, 그리고 접합 유지 시간은 20 min이었다. 대조군은 창유리 그 자체이다. 온도의 함수로 열처리한 금속-유리 시편의 유리 곡면 변화는 금속 하우징에 파라핀을 주입하여 접촉각 변화를 간접적으로 관찰하였다(Fig. 2). 접합계면의 미세구조와 확산 물질의 종류를 포함한 정성 및 정량분석은 다이야몬드 톱으로 접합 시편을 절단한 파단면을 주사전자현미경(scanning electron microscope, SEM)/에너지분산형분광기(energy dispersive spectroscopy, EDS)(JSM-6380V, Jeol, Japan)로 관찰하였다. 또한 유리 시편의 밀도는 아르키메데스법으로 5회 이상 측정 후 평균값()과 표준편차()를 구하였다. 여기서 은 측정횟수, -1은 자유도를 각각 나타낸다. 한편 온도의 함수로 금속과 접합한 소다라임 유리의 비대칭 신축, 네트워크 중합도, 그리고 비가교산소(non-bridging oxygen, NBO) 신축 등을 분석하기 위하여 금속면에 부착된 온도별 유리 시편을 KBr (1:200)과 혼합・분쇄 후 가압한 윈도우를 푸리에 변환 적외선 분광기(fourier transform infrared, FTIR, VERTEX 80v, Bruker, USA)로 화학결합을 분석하였다. 이때 측정 파수대 범위는 4,000-400 cm-1이었다.
Table 1.
Characteristics of the used free-cutting steel (SUM24L) and soda-lime glass specimens.
3. 결과 및 고찰
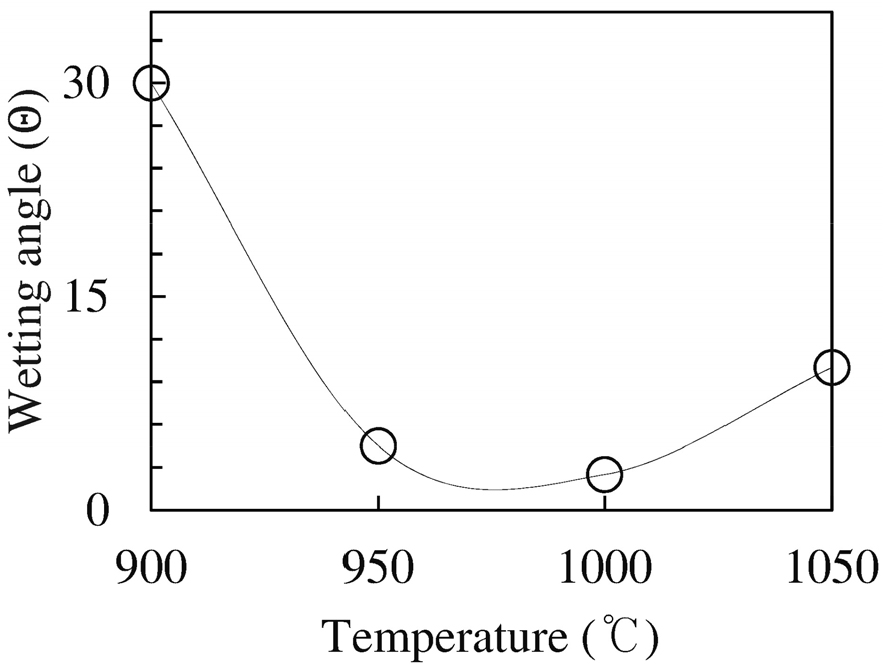
Fig. 3은 온도에 따른 창유리 시편의 접촉각(θ) 측정 결과를 나타낸 것이다. 900 °C에서 열처리된 시편은 θ = 30°에서 온도가 증가할수록 θ는 점차 감소하여 0 °에 가까워지는 경향을 보이고 있다. 이 경향은 창유리의 유리전이온도(Tg, ≈ 570 °C)와 연화점(≈ 715 °C)보다 높은 열처리 온도에 의한 유리 구조의 이완(relaxation)인 풀림, 금속이온, 그리고 용질에 의한 계면에너지 변화와 직접적 연관성을 가지는 것으로 판단된다.9) 체적변화는 900 °C 시편에서 가장 크게 나타나지만 복귀하는 에너지와 시간이 상대적으로 지연되는 반면에 온도가 증가하면 체적변화의 복귀가 빠르게 이루어져 접촉각 감소에 기여한다. 즉, 900 °C 시편은 유리 구조가 열적 평형 상태로 완전히 복귀하기 위한 에너지와 시간이 충분하지 않아 구조 이완이 상대적으로 지연된다. 그러나 온도가 더욱 증가하면 체적 변화가 더 빠르게 복귀하여 접촉각은 지속적으로 감소한다.
포스테라이트는 MgO 표면 에너지와 산화납유리의 표면장력이 1,000 erg/cm2와 150 dyne/cm로 6.7배 차이가 난다. 또한 PbO-Bi2O3-B2O3-ZnO계 유리 내 PbO 성분이 MgO 표면에 용질로 도입되면 급격한 표면장력 감소가 나타난다.3) 온도의 함수로 관찰된 젖음각, 은 90° 이하로, 관계가 성립함을 확인할 수 있었다. 여기서 는 고체-기체, 는 고체-액체, 그리고 는 액체-기체의 표면 에너지를 각각 의미한다. 그러나 쾌삭강의 열팽창계수, 14.4 × 10-6 /°C와 창유리의 열팽창계수 9.5 × 10-6 /°C의 34 % 차이는 θ거동에 유의미한 영향을 미치지 않는 것으로 나타났다.
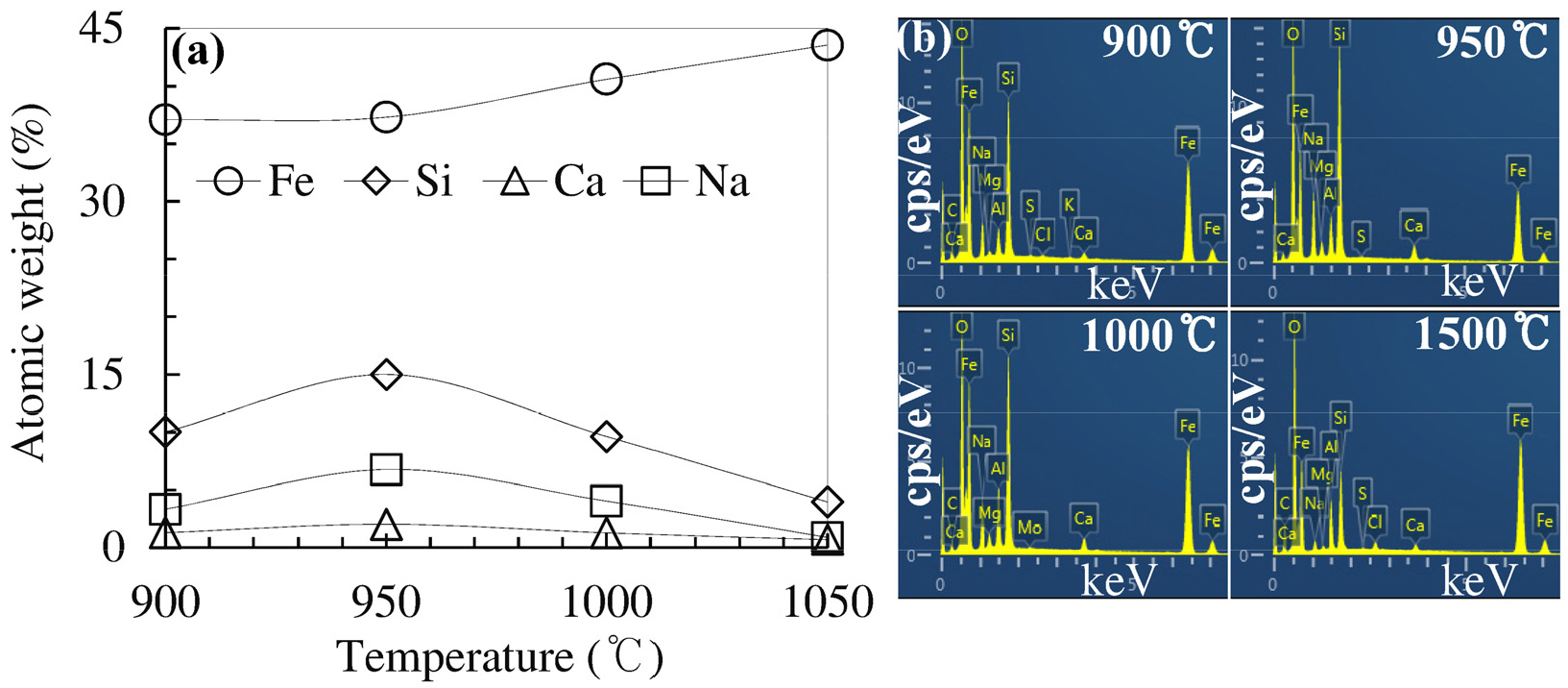
Fig. 4는 시편의 계면 미세구조와 물질이동을 SEM/EDS로 정성 분석한 디지털 맵핑 결과이다. Fig. 4(a)의 900 °C 시편은 경계면을 중심으로 균열, 공극, 그리고 2차 상이 형성된 미세구조를 보여주고 있다. 포러스한 경계면을 중심으로 50~120 µm 크기의 침상, 반응 중심에는 역삼각형 영역, 그리고 ~5 µm 크기 구형이 발달된 형상을 보이고 있다. 공극이 형성된 계면 미세구조는 Fe산화에 의한 과잉 산소 발생에 기인하는 것으로 판단된다. 유리 내에 존재하는 물리적으로 불활성인 산소는 금속이온의 이동에 따른 산화환원 반응 조건 변화에 의해 화학적 결합을 형성한다. 유리 망목의 [SiO4]n- 구조에서 Si원자 주위의 4개 O원자는 각각 2개의 Si원자가 연결되어있으며, 이온들은 8배위 산소와 4개의 최외각전자를 공유한다. 또한 SiO2의 이온은 산소와의 공유결합(Si-O)으로 전하 균형에 영향을 받지 않아 식 (1)과 (2)와 같이 표면 산소층 배열이 급격히 형성된다.9,10)
이후 Fe 이온이 과잉으로 존재하는 산소 이온을 흡착하면서 금속 표면의 계면에너지가 감소하는 현상이 발생한다. 이는 금속/유리 계면에 과잉 산소 이온에 의한 레독스 반응이 촉진되어 계면에 과잉의 산소 발생에 기인하기 때문이다. 이 모델은 MgO 내 Al2O3 100~150 ppm 용질이 입계 편석을 일으켜 표면 에너지를 감소시키고, 금속/유리 계면에서 금속 측의 레독스 반응 생성물이 온도상승에 따라 증가 및 확산하는 기존의 연구결과와 일치한다.11)Fig. 4(a)의 EDS분석에서 포러스한 영역 성분은 Si, Na, Fe 풍부상으로 나타났으며, Fe는 특정 경계면에 국한되어 확산되는 경향을 보이고 있다. 이 Fe 이동은 유리 내 산화환원 반응 가설을 지지한다. 미세구조 분석에서 침상상은 Fe, Ca, Na 풍부상으로 확인되었으나, 매트릭스 내 Ca 분포는 제한적이었다. 미세구조 분석에서 침상은 Fe, Ca, Na로 유리 내 Ca와 Fe 간 반응성에 대한 추가 검토 필요성을 시사한다. 한편 역삼각형 영역은 Si, Ca, Na 풍부상으로 분석되어 확산 영역에 따라 이온종 분포 차이를 보이고 있다. Fig. 4(a)의 미세구조 분석에서 관측된 침상과 구상 결정은 이종재료 계면에서 쉽게 일어나는 불균일 핵생성에 기인한 것으로 해석된다. 불균일 핵생성은 액상과 고상 사이의 부피 자유에너지() 차이가 작고, 핵생성에 필요한 과냉각 정도도 감소하여, 결정핵의 형성이 균일 핵생성보다 더욱 용이하게 이루어진다.
불균질 핵생성에 영향을 미치는 임계반경, 와 에너지 장벽, 는12)
여기서 𝛾는 표면장력, 그리고 은 과냉각액체 핵의 표면에너지를 각각 나타낸다. 식 (3)에서 제시된 바와 같이, 새로운 상이 기존 고상에 충분히 젖어서 접촉각(𝜃)이 작아지고, 식 (4)의 에너지 장벽값이 매우 낮아져 핵이 쉽게 형성되는 현상론적인 결과와 일치한다.
Fig. 4(b)의 950 °C 시편은 포러스한 영역은 소멸하고 계면 층 형성을 나타내고 있다. 1,000 °C 시편인 Fig. 4(c)의 유리계면에 약 74 µm의 2차상이 발달한 반응 영역과 상호간 계면이 치밀하게 부착된 미세구조를 보이고 있다. 그러나 1,050 °C 시편인 Fig. 4(d)에서 유리 측뿐만 아니라 금속에서도 100 µm 폭의 반응계면이 형성된 특징적인 미세구조 형상을 보이고 있다. 계면을 중심으로 100 µm 대칭 형성된 1,050 °C 시편의 미세구조는 온도의 함수로 금속이온의 이동에 의해서 구성되어 새로운 결정상으로 진화하는 과정을 보여주었다.
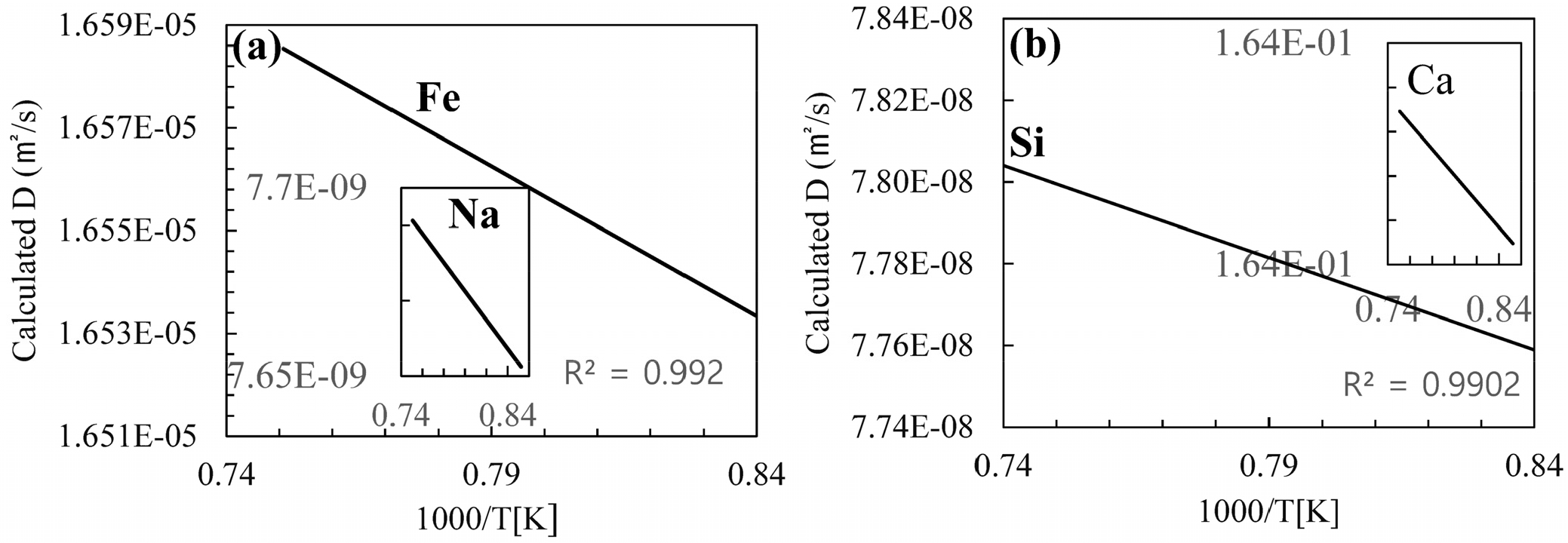
이 거동은 금속/유리 계면에서 형성된 반응층의 EDS 분석을 나타낸 Fig. 5에서 공통적으로 Na이온과 Ca이온이 금속 계면에 분포한다. 이는 양이온의 확산 계수는 Ca2+ > Na+ > K+ >> Mg2+로 이온 크기가 클수록 빠르게 이동하는 경향과 일치한다.13) 이동 성분은 공통적으로 Ca2+ > Na+ 이며 900 °C와 950 °C를 나타낸 Fig. 4(a)와 (b)에서 Ca-Na 풍부상을 형성한다. 그러나 1,000 °C와 1,050 °C 시편을 분석한 Fig. 4(c)와 (d)에서 Na, Ca, K, Pb, Cr, Ni 등 알칼리 성분과 금속원소가 비교적 접합계면 전체에 걸쳐 균일함을 보이고 있다. 따라서 미세구조 변화에 영향을 미치는 확산원소의 선지수에 따른 확산계수, 는14)
여기서 D는 확산계수, Do는 선지수, Qd는 활성화 에너지, R은 기체상수, 그리고 T는 절대온도(K)를 각각 의미한다. 유리 내의 Fen+, Si4+, Na+, Ca2+ 등의 모든 이온 수가 동일하지 않기 때문에 아레니우스 상수를 활용하여 확산계수, D를 계산하였다. D 계산에 사용된 아레니우스 상수, Do와 활성화 에너지, Qd는 다음과 같다. Fe는 1.7 × 10-5 m2/s와 273 kJ/mol, Na는 0.84 × 10-8 m2/s과 433 kJ/mol, Ca는 1.65 × 10-1 m2/s와 45 kJ/mol, 그리고 Si는 8.0 × 10-8 m2/s와 301 kJ/mol를 각각 이용하였다.15,16,17,18) 그러나 금속 산화층 계면에서 산소의 확산계수는 양이온, 음이온의 확산계수와 평형농도로 부터 확산속도는 고려하지 않았다.19) 계산된 결과는 Fig. 6과 같이 전형적인 아레니우스 거동을 보이며, Ca이온의 이동속도가 가장 빠른 것으로 나타나 성분이동 결과와 비교적 잘 일치함을 알 수 있었다.
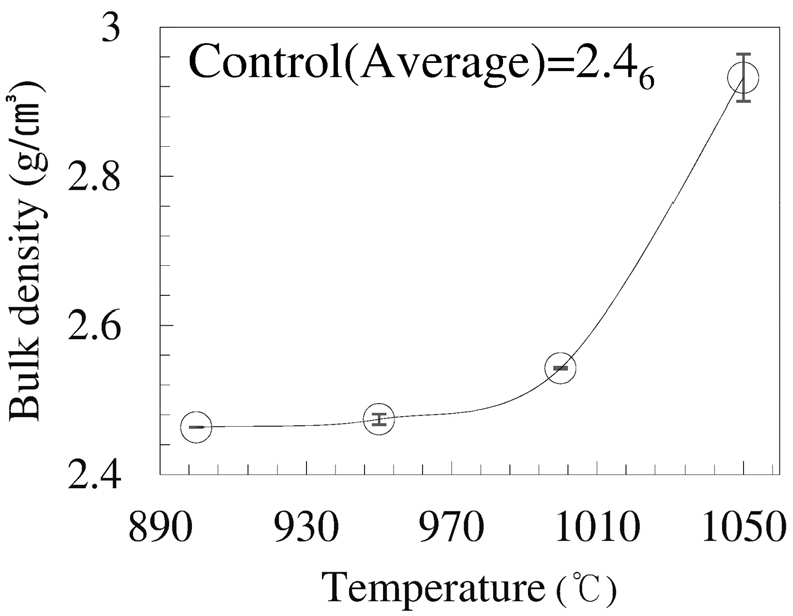
Fig. 7에서 대조군과 열처리 시편의 유리밀도는 온도에 비례하는 경향을 나타내고 있다. 900 °C 열처리 온도는 대조군의 Tg, ≈570 °C와 연화온도, ≈715 °C보다 높아 유리 구조 변화로 밀도가 감소하는 일반적인 경향과 다른 거동을 보이고 있다. 이는 원자재배열로 인한 중합 무질서 정도에 의한 부피팽창 영향보다는 외부 금속이온 확산에 의한 원자 수 증가 영향과 금속확산 이온에 의한 유리 조성변화가 더 크게 작용하기 때문으로 판단된다.18) 즉 Fe의 산화반응과 유리 내의 산소와 환원의 레독스 반응, 그리고 유리내에서 전기적 중성을 형성하여 비가교산소는 감소시키지만, 전체 이온수는 증가하기 때문이다. 이 거동은 온도에 비례하기 때문에 1,050 °C 시편은 대조군 시편보다 약 20 % 정도의 밀도 증가를 나타내는 경향과 일치한다.3,10) 이 경향은 규산알루미노유리를 금속 산화분위기에 노출 시키면 Fe 산화반응에 의해 산소원자가 유리 내에 침입하여 Fe-Si-Al-O계 비율변화로 원자수가 증가하여 나타난다.20) 유리 밀도의 2.4~2.9 g/cm3 변화는 Fe이동 농도에 의해 결정될 수 있음을 확인하였다. 또 다른 요인은 Fe2+, Fe3+ 등 다가이온 존재에 의해 불활성 기체인 수증기, 수소, CO2의 물리적 용해 특성에 의한 영향도 있다.21) 따라서 금속이온이 유리내로 확산이 증가하는 1,050 °C 시편에서 가장 많은 기체용해가 일어나기 때문에 상대적으로 높은 밀도를 나타내는 것으로 판단된다.
유리의 밀도, 𝜌 변화를 몰체적의 역수로 고려하면22)
여기서 , 은 각 산화물 의 부분 몰체적과 중량백분율을 나타낸다.
따라서 온도에 따른 몰부피는 밀도와 반비례하며, 밀도가 증가하면 감소하는 비율은 분자량에 좌우됨을 의미한다. 온도에 따른 몰부피 변화량범위, 34.1~40.5 cm3/mol는 대조군과 열처리 시편으로 나누어 설명이 가능하다. 대조군의 소다라임 알칼리 함유량은 27 wt%로 일정하기 때문에 몰부피는 40.5 cm3/mol 정도이다.23) 이때 밀도는 2.47 g/cm3로 △ρ ≤ 0.03 범위 내에서 NBO수를 가진다.24) 소다유리의 경우, Tg (≈550 °C)에서 Si-O-Si 결합의 각도의 변화와 Na+ 이온의 재배치가 일어나며, 이로 인해 몰부피의 급격한 비선형적 변화가 보고되고 있다.25) 그러나 온도의 함수로 반응하여 Fe는 레독스 반응으로 유리내에 지속적으로 Fe2O3로 용해됨으로서 몰부피가 감소한다. 이는 밀도가 2.4 g/cm3에서 2.9 g/cm3으로 증가(△ρ ≥ 16.1 %)한 것은, 유리 내 Fe 이온농도 증가에 따른 전기적 중화 작용으로 인해 NBO 수가 감소하였기 때문으로 판단된다.8,20) 한편 구조 안정성은 BaO-V2O5-Fe2O3 유리계에서 V-O-Fe 브릿지 형성으로 BaO-V2O5 유리의 불안정한 판 및 사슬 구조가 변화하여 구조안정성 증가하는 연구결과도 있다.26)
알칼리 함유량을 변화시킨 2성분계 유리에서 알칼리 함량이 높아질수록 유리 구조내 비가교 산소를 많이 형성하기 때문에 밀도 증가 거동을 나타낸다. 즉 유리 내 Si원자는 모두 4배위 상태로 Si원자를 둘러싸는 4개의 산소원자를 사이로 인접한 4개의 Si-O-Si결합을 형성한다. 이 Si 원자에 결합된 산소원자는 모두 Si-O-Si 결합 형성에 관여하는 가교산소는 알칼리 이온에 의해서 비가교산소 형성에 따른 것이다. [SiO4]n-유리 망목구조에 Li, Na, K, Be, Mg, Ca 등 중간재 또는 망목수식제가 도입되면 NBO생성이 증가한다는 일반적인 이론과 일치한다.27) 따라서 중합도와 연관지어 NBO원자수에 연관된 NBO원자질량의 이온 배수와 네트워크 형성제 전체 질량의 이온 비율로 설명 가능하다.
여기서 는 네트워크 형성 전체 질량의 이온 수, 는 유리 산소 질량의 이온 수를 각각 나타낸다. 식 (7)과 같이 NBO 증가는 밀도 증가와 직접적인 연관성을 나타낸다.20,21)
이와 반대로 결정질 α-쿼츠 밀도는 2.6 g/cm3인 반면에 붕규산 유리 밀도는 2.2 g/cm3이다. 이는 사면체 형성에 따른 체적변화가 밀도에 강한 영향을 미침을 의미한다.28) 따라서 유리의 밀도는 실리카 체적변화, 알칼리 함량, 실리카 네트워크의 중합도, 그리고 외부이온 확산에 의해 결정되는 것을 확인할 수 있다. 이러한 경향은 소다유리가 Tg ≈ 550 °C 이상에서 점탄성(viscoelastic)에 의한 부분적인 유동성 발생, 부피 팽창, 그리고 밀도 감소가 상대적으로 크게 나타나는 기존의 연구 결과와 일치한다.29)
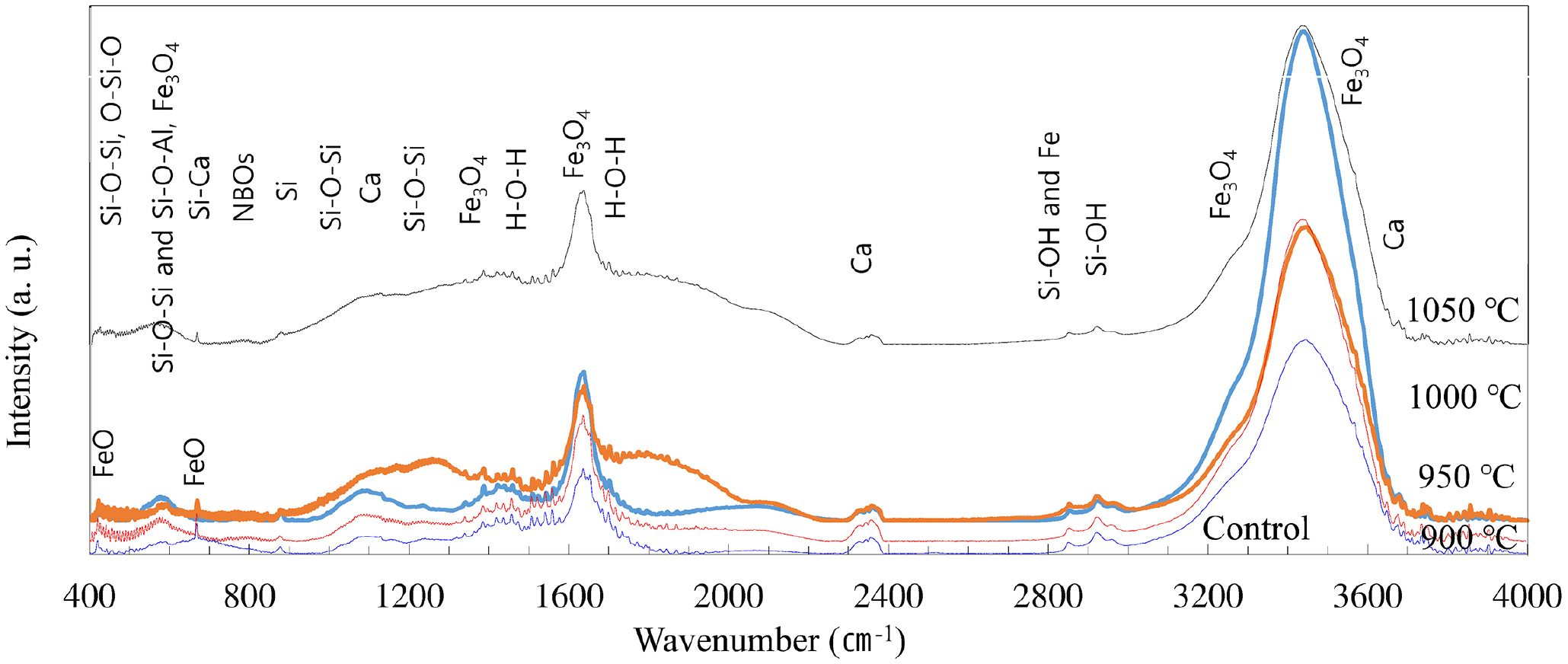
Fig. 8은 FTIR 흡수 스펙트럼으로 유리의 구조적 특징과 결합을 Si-O-Si 신축 진동, 결합, 알칼리 원소에 의한 NBO 결합 분석 결과를 나타낸 것이다. 700~800 cm-1 파수대의 흡수 대역은 일정하며, 400 cm-1 파수대와 1,200~1,300 cm-1 파수대에서 뚜렷한 변화가 관찰되었으나, 전체적으로 유사한 스펙트럼 패턴을 가지는 것으로 분석되었다. 진동 대역의 공통적인 주요 피크는 다음과 같다. 1,014~986 cm-1, 1,200 cm-1, 그리고 900 cm-1 부근에서 숄더를 가지는 3개의 비대칭 Si-O 신축 진동 피크가 나타났다. 454 cm-1의 Si-O-Si와 O-Si-O 굽힘 모드, 580-604 cm-1의 Si-O-Si의 굽힘 진동 및 Si-O-Al 결합, 670 cm-1의 Si-Ca 굽힘 모드, 775 cm-1에서의 Si-Ca의 불안정한 결합 진동, 그리고 1,049 cm-1을 중심으로 한 넓은 대역의 Si 피크가 나타나고 있다. 특히 1,200~850 cm-1 대역은 SiO4 사면체의 비대칭 신축 진동에 해당하며, 이 대역의 위치는 규산염 네트워크인 가교산소수 연결 정도에 따라 달라진다. 이 대역의 위치는 규산염 네트워크의 연결 정도, 그리고 SiO4 사면체 고립정도와 SiO4가 다른 SiO4 사면체의 4개 산소 이온 공유여부에 의해 결정된다. 770 cm-1은 Si-O-Si 브릿지의 대칭 굽힘 모드, 그리고 463~454 cm-1은 Si-O-Si 브릿지의 굽힘 진동에 기인한다.30) 대조군과 저온열처리 시편은 1,080 cm-1에서 Si-O-Si에 연관된 피크가 나타나는 반면에 고온시편은 1,200~1,300 cm-1 파수대의 숄더 스펙트럼은 4배위된 Fe 이온의 Fe-O 신축 진동에 기인하는 것으로 해석된다.31) 또한 밴드 위치가 1,080 cm-1에서 1,200 cm-1로의 피크 이동은 유리의 조성 내 Fe2O3 함량증가에 따른 유리망목의 탈중합(depolymerization)의 결과로 판단된다.
열처리 온도에 따른 FTIR 스펙트럼 변화는 고온시편에서 비교적 분명한 차이를 보인다. 이는 논의된 주요 흡수 대역인 1,180 cm-1, 1,200~1,300 cm-1 영역, 그리고 1,700 cm-1 부근에서 흡수피크의 이동 및 흡수강도가 관찰되었다. 또한 2,400 cm-1와 2,800~2,950 cm-1 영역에서는 Ca-O, Si-OH, Fe-O 결합 피크가, 3,450 cm-1에서는 C-S-H 구조에 기인한 넓은 흡수대가 나타났다. 위의 결과로부터 열처리에 따른 파수 이동 및 강도 변화는 금속 이온의 확산・이동이 유리 네트워크 결합 구조에 직접적인 영향을 미침을 확인할 수 있었다. 유리 내부에서의 금속 이온 확산은 온도 상승에 따라 가속화되며, 이는 네트워크 구조의 재배열과 결합 상태 변화로 이어진다. 특히, 알칼리 및 알칼리토금속 이온은 NBO 형성을 유도하여 Si-O-Si 또는 B-O-B와 같은 기본 네트워크 결합을 변화시키며, 전이금속 이온은 네트워크 형성자 혹은 변조자로 작용하여 구조적 안정성에 영향을 미칠 수 있다. 이 구조적 변화는 유리의 밀도, 계면 반응성, 이차상 형성 거동을 결정하는 중요한 요인이 된다.
4. 결 론
온도의 함수로 금속과 접촉하는 유리 계면에서 형성되는 불균일 2차상의 가성성 인자 연구를 통해 다음과 같은 모델을 설립하였다. 창유리 시편의 젖음각은 연화점보다 높은 열처리 온도로 풀림에 의한 체적변화에 의존하며 젖음각, θ는 30° 이하로 나타났다. 금속산화에 의한 레독스 반응으로 과잉의 산소를 형성하여 계면을 중심으로 2차상을 형성하는 주요 요인으로 규명되었다. 계면에서 확산이동의 현상론적인 물질이동은 아레니우스 거동을 나타내었으며, 양이온 확산 계수는 Ca2+ > Na+ > K+ >> Mg2+ 순이였다. 유리 밀도는 외부 금속 이온이 확산・이동하면서 원자 수가 증가한 효과에 의해 주로 결정되는 것으로 나타났다. 또한 유리의 중합도는 고온 시편은 4배위된 Fe 이온의 Fe-O 신축 진동과 유리 내 Fe2O3로 인해 유리 네트워크의 탈중합 증가가 나타났다. 또한 유리 네트워크의 탈중합도는 고온에서 4배위된 Fe 이온의 Fe-O 신축 진동과 유리 내 Fe2O3로 증가에 기인하였다. 따라서 금속/유리 계면에서 형성되는 불균질 결정상은 Tg 온도 이상에서 유리 내 이온 이동과 금속이온 도입에 따른 화학결합, 풀림에 의한 체적 변화에 따른 젖음각, 금속이온 확산에 따른 유리의 미세구조 변화, 금속원소의 표면 산소층 배열에 의한 레독스반응, 그리고 물질이동 속도가 불균일 2차상 형성에 영향을 미치는 가성성 인자임을 확인하였다.