1. 서 론
인산 지르코늄(zirconium phosphate)계 화합물의 열팽 창 특성은 특이한 결정구조에 의한 현상으로 열을 가할 때 특정 방향으로 결정구조가 수축하는 현상을 보인다.1) 2ZrO2·P2O5 세라믹스는 ZrO6 팔면체와 PO4 사면체의 모 서리를 서로 공유하고 있으며, 망목구조와 같이 결정구 조 속에 열린 공간을 가지는 결정은 모서리를 공유하는 배위다면체로 쉽게 회전하고, 이 움직임에 의하여 열진 동에 의한 원자간 거리의 변화에 의하여 열팽창 정도가 영향을 받게 된다.2) 특히 이 같은 열팽창 거동은 결정 축 a축 방향으로 수축이 발생하게 되어 이방성 열팽창 에 의하여 매우 낮은 열팽창 거동을 보이게 된다.3,4) 일 반적으로 안정한 상을 보이는 α상의 2ZrO2·P2O5는 합성 시 불안정한 형태의 β상을 거쳐 합성되고, 비가역적인 상 변환을 갖는다. 2ZrO2·P2O5의 소결거동에서는 소결조제로 첨가되는 물질의 종류에 따라 또는 결정립 크기에 따라 각각의 축 방향으로의 열팽창 거동이 달라지게 되어, 서 로 상이한 열팽창 거동을 보이는 것이 특징이다.5)
균질하고 미세한 세라믹 분말의 합성 방법중에서 폴리 머 용액합성법은 물에 쉽게 용해되는 폴리머인 PVA (polyvinyl alcohol), PEG (polyethylene glycol), EG (ehtylene glycol)를 이용하여 용액내의 금속 양이온들의 분산을 극대화하여 균질하고 안정된 전구체를 얻을 수 있으며, 하소온도를 낮출 수 있는 장점이 있다. 또한 PVA 폴리머를 이용함으로써 Pechini resin 방법과는 달 리 chelation 공정이 생략되고, 단지 물리적 작용인 고 착공정(steric-entrapment)만이 양이온의 분산에 이용 되어 진다. PVA만의 특수한 작용에 의하여 이루어지는 이 같 은 공정은 물에 용해된 PVA의 hydroxyl group이 금속 양이온을 강하게 고착시켜 줌으로서 균일한 분산을 가 능하게 하여 매우 안정된 전구체를 제조할 수 있는 장 점이 있다. 따라서 하소된 분말도 매우 미세하고 좁은 입도분포를 보이게 된다.6-8) 또 다른 특징은 전구체 제 조를 위한 고온 건조 과정에서 PVA 폴리머와 nitrate 형 태의 금속 양이온에서 발생하는 CO, CO2 및 NOx 가스 의 상호 작용에 의하여 다공성의 전구체를 제조할 수 있 고, 하소 과정 시 PVA의 뛰어난 열분해 성질에 의하여 낮은 온도에서 폴리머의 탈지가 가능함으로 하소 후 다 공성의 분말을 얻을 수 있다는 장점이 있다. 이 경우 적 절한 밀링과정을 거쳐 나노크기의 미세한 분말을 얻을 수 있다. 또한 PVA 공정에서 발현되는 carbonaceous 반 응은 폴리머 분해에 따른 산화반응에 의해 발열반응을 동반하여, 양이온의 산화가 촉진되어 미세하고 단일상의 산화물 분말 합성이 상대적으로 낮은 온도에서 얻어지 게 된다.9-11)
본 연구에서는 일반 고상법을 통한 상압 열처리를 통 하여 잘 합성되지 않는 α상의 2ZrO2·P2O5 분말을 PVA 폴리머 용액법을 이용하여 분말의 합성조건을 고찰하였 다. 특히 나노에 접근하는 입자크기 제어가 요구되는 분 말 합성을 위해 PVA 폴리머 첨가량과 열처리온도 조절 에 따른 합성거동을 고찰하였으며, 소결조제를 첨가하지 않은 α상의 2ZrO2·P2O5의 열팽창 거동을 고찰하였다.
2. 실험 방법
2.1 전구체 준비 및 합성
본 실험에서는 출발원료로 ZrO(NO3)2·xH2O (technical grade, Sigma-Aldrich Co., USA), P2O5 (98.0 %, Kanto Chemical Co., Inc, Japan)를 사용하여 증류수에 2:1의 몰 비율로 각각 용해시킨 후 5 wt%의 PVA (molecular weight - 146,000~186,000, Sigma-Aldrich Co., USA) 용 액을 함께 혼합하였다. 예비 실험 결과, 인산(H3PO4)을 사용하였을 경우는 합성이 원활히 이루어지지 않았다. 5 wt%의 PVA 용액은 증류수 95 cc당 5 g의 PVA 분말 을 용해시켜 제조하였다. 폴리머의 긴 사슬은 용액에서 hydroxyl groups를 가진다. 한 개의 -(OH) functional group 을 갖는 PVA 모노머(monomer)는 용액내의 양이온에 대 한 상대적인 양이 분산에 영향을 미치게 된다. 본 실험 에서는 PVA의 첨가량을 첨가한 금속 양이온들의 비에 대해 4:1, 8:1, 12:1, 16:1의 비율로 혼합하였다. 즉, 첨 가된 금속 양이온의 원자가를 기준하여 1개의 -(OH) functional group을 갖는 PVA 모노머에 대한 금속 양이 온의 원자가 비로써 PVA의 첨가량을 정하였다. 제조된 졸(sol) 상태의 용액은 핫 플레이트에서 교반하면서 열 을 가해 건조시켰다. 건조 후 얻어진 겔(gel) 형의 전구 체를 100 °C에서 24시간 동안 완전 건조시켰다. 완전히 건조된 2ZrO2·P2O5 전구체의 유기물 제거를 위하여 500 °C에서 한 시간 동안 공기분위기 박스로에서 하소한 다 음 노냉 하였으며, 이때의 승온속도는 분당 4 °C로 하였 다. 하소된 분말은 합성을 위하여 공기분위기 박스로에 서 1100 °C, 1150 °C, 1200 °C의 각 온도에서 열처리 한 다음 노냉 하였으며, 승온속도는 분당 5 °C로 하였다.
2.2 특성 분석
분말 합성 시 발현되는 온도변화에 따른 열분석 특성 을 고찰하기 위하여 열분석기(STA 1500, Santon Redcroft, U.K.)를 이용하였고, 상온에서 1300 °C까지 대기 분위기 에서 10 °C/min의 승온속도 조건 하에서 분석하였다. 폴 리머의 첨가량, 열처리 온도에 따른 상변화 및 결정상을 분석하기 위해 X-ray diffractometer (Rigaku D/MAX 2200, Japan)를 사용하여 고찰하였다. 합성된 분말 소결 체의 승온 시 열팽창거동을 알아보기 위해 열팽창계수 측정기(Dilatometer DIL402C, Netzsch, Germany)를 이 용하여 측정하였으며, 승온속도는 분당 10 °C로 하였 다. 소결시편은 합성된 분말을 원통형 모양으로 일축가압 성형하여 합성온도와 같은 1200 °C에서 1시간 열처리하 여 제조하였다. 합성된 분말의 미세구조를 관찰하기 위 하여 전계방출주사전자현미경(FE SEM, JSM-7100F, JEOL, Japan)을 사용하였다.
3. 결과 및 고찰
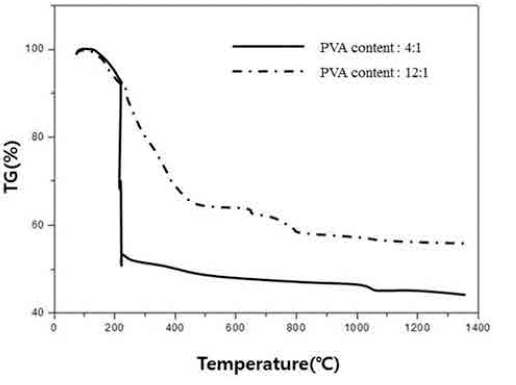
합성된 전구체에 대한 열분해 결과를 Fig. 1에 나타내 었다. PVA의 첨가량이 상대적으로 많은 4:1의 경우, 많 은 양의 PVA 열분해에 의하여 낮은 온도에서 급격한 무 게감소가 관찰되었다. 이후에 약 10 %에 해당되는 무게 감소는 잔유탄소와 zirconium nitrate hydrate의 열분해에 의한 무게감소로 예측된다.12) 이에 비하여 상대적으로 PVA 첨가량이 적은 12:1의 경우는, PVA 양에 비하여 상대적으로 zirconium nitrate hydrate의 양이 많은 분률을 차지하여, 무게감소 거동이 4:1의 경우와 다른 결과를 보 이고 있다. 전체 무게감량이 4:1에 비하여 감소함과 동 시에 지속적인 무게감량을 보이고 있다. 두 경우 모두 800 °C 이후에는 미미한 무게감소가 관찰되었다.
Fig. 2에는 PVA 함량 12:1의 분말을 열처리 온도를 달 리하여 합성한 후 각 온도에 따른 결정상 고찰 결과를 나타내었다. 모든 분말시편은 분당 승온속도는 5 °C, 유 지시간은 4시간으로 동일하게 열처리 하였다. 1200 °C에 서 잘 발달된 α상의 2ZrO2·P2O5 분말 합성이 가능하였 다. 50 °C 낮은 1150 °C에서는 β상의 2ZrO2·P2O5와 α상 이 공존하였으며, 1100 °C에서는 β상과 미 반응 된 ZrO2 가 관찰되었다. I. Yamai1) 등은 zirconium oxychloride와 phosphoric acid를 출발물질로 사용한 액상법에 의하여 안 정된 α상의 2ZrO2·P2O5을 1350 °C에서 합성하였다. 이 보다 150 °C 낮은 온도에서 합성이 이루어진 본 논문의 실험과 비교해 볼 때, 합성을 위한 출발물질이 다른 영 향도 있지만, 폴리머 첨가에 의한 용액 내 양이온들의 분산효과가 이 같은 낮은 온도 합성에 영향을 미쳤다고 생각된다. 또한 폴리머의 분해 및 산화 반응으로 발열 반응이 동반되고 이것은 양이온 산화를 촉진하여 합성 온도가 낮아지게 원인도 생각해 볼 수 있다.11)
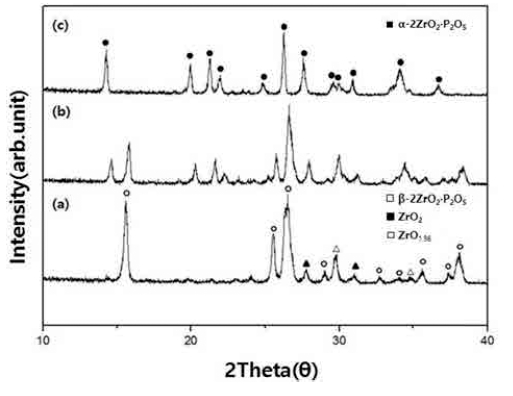
Fig. 2
XRD patterns of 2ZrO2·P2O5 precursor powders fired at different temperature at (a) 1100 °C, (b) 1150 °C and (c) 1200 °C for 4h.
Fig. 3에 PVA 함량을 달리하여 1200 °C에서 분당 5 °C 로 4시간 동안 열처리한 결과를 나타내었다. PVA 함량 이 12:1의 경우, Fig. 2의 결과와 같이 α상이 관찰되었 으며, 이 보다 첨가량이 적을 때(16:1)도 α상의 결정상 이 관찰되었으나, 피크의 폭이 넓고 낮은 피크 강도를 보이는 것으로 보아, 결정도가 낮고 결정립 크기가 작 은 분말이 합성되었음을 알 수 있다. 12:1 보다 PVA 함 량이 많은 8:1의 경우, α상과 함께 β상이 관찰되었으며, 4:1의 경우는 α상은 관찰되지 않았다. PVA 첨가량이 양 이온의 분산 및 산화반응에 영향을 미쳐, 분말의 합성 거동에 영향을 끼침을 알 수 있었으며, PVA 12:1의 첨 가 조건에서 결정입자의 크기 증가와 결정도 증가가 발 현됨을 확인 할 수 있었다.
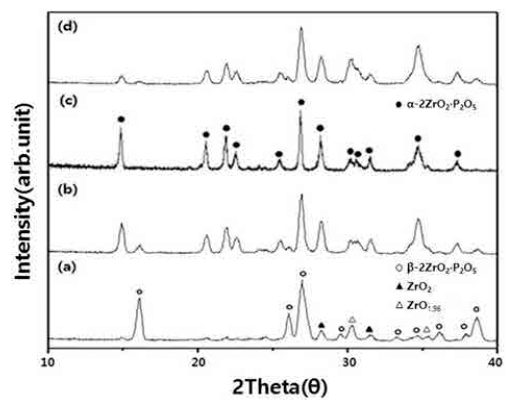
Fig. 3
XRD patterns of 2ZrO2·P2O5 precursor powders prepared from different PVA content of (a) PVA 4:1, (b) PVA 8:1, (c) PVA 12:1 and (d) PVA 16:1.
Fig. 4에는 PVA 함량 4:1, 12:1의 분말을 1200 °C에서 분당 5 °C로 유지시간을 1시간, 3시간으로 열처리한 결 과를 나타내었다. PVA 함량 4:1의 경우는 유지시간과 상 관없이 β상이 주 결정상으로 관찰되었고, PVA 함량 12:1 의 경우에는 α상이 관찰되었으나, β상도 함께 관찰되었 다. 유지시간이 짧은 경우는 β상의 분율이 증가하였다. 이와 같은 결과로 볼 때, 안정한 α상의 2ZrO2·P2O5 분 말합성을 위해서는 PVA 함량의 조절과 함께 1200 °C 이 상에서 4시간 이상 열처리 하는 것이 필요하다는 것을 알 수 있다.
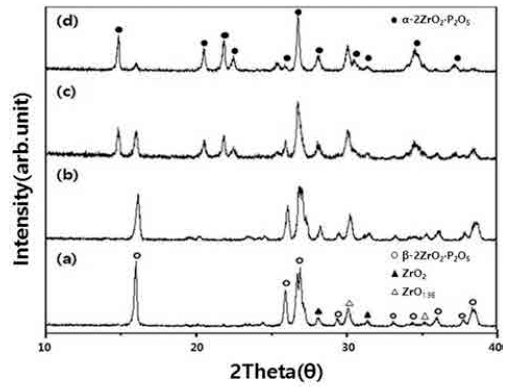
Fig. 4
XRD patterns of 2ZrO2·P2O5 precursor powders fired at 1200 °C with different PVA content and holding time (a) PVA 4:1, 1h, (b) PVA 4:1, 3h, (c) PVA 12:1, 1h and (d) PVA 12:1, 3h.
Fig. 5에는 1200 °C에서 4시간 열처리하여 합성된 2ZrO2· P2O5 분말의 미세구조를 PVA 함량을 변수로 관찰한 결 과를 나타내었다. PVA 함량이 적어질수록(4:1에서 16:1 로 갈수록) 입자의 크기가 작아짐을 확인할 수 있었다. 분말의 응집 정도는 큰 차이는 없었으며, 일부 입자의 경우는 pre-sintering 현상이 발현되어 서로 붙어 치밀화 된 형상을 나타내었다. 16:1의 경우, XRD 피크 폭이 상 대적으로 넓은 것과 일치하며(Fig. 3), 12:1의 경우, 분 말의 평균입자 크기는 100~200 nm로 매우 미세한 입자 로 이루어져 있음을 알 수 있었다.

Fig. 5
FE SEM micrographs of 2ZrO2·P2O5 powders synthesized at 1200 °C for 4h (a) PVA 4:1, (b) PVA 8:1, (c) PVA 12:1 and (d) PVA 16:1.
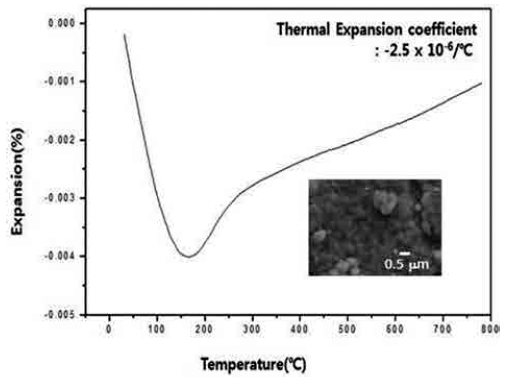
Fig. 6에는 합성된 α상의 2ZrO2·P2O5 분말을 가압성 형 후 열처리하여 소결된 시편의 열팽창 거동 결과를 나 타내었다. 200 °C까지는 급격한 음의 열수축을 보이고 이 후에는 다시 완만히 팽창하는 결과를 보였다. 소결조제 를 첨가한 2ZrO2·P2O5의 경우는 약 400 °C~500 °C부터 음의 열수축이 팽창으로 변하지만,1) 본 연구결과에서 보 듯이 순수한 2ZrO2·P2O5의 경우는 훨씬 낮은 온도에서 열팽창 변곡점이 관찰되었다. 2ZrO2·P2O5의 열팽창 변곡 점은 첨가해준 소결조제의 영향을 받게 되는데,1,2) 본 실 험 결과와 같이 200 °C로 낮게 관찰된 경우는 매우 특 이한 경우이며, 그 이유는 소결조제를 사용하지 않은 이 유도 있겠으나, 나노크기의 결정립에 의한 영향을 추론 해 볼 수 있다.1) 400 °C~500 °C에서 열팽창 변곡점을 보 인 소결조제가 첨가된 2ZrO2·P2O5 소결체는 약 10 μm 입 자크기를 보였다.1,2) 그러나 PVA 용액법에 의해 제조된 분말 가압체를 1200 °C에서 소결한 경우, 약 0.5~1.0 μm 의 입자크기를 보였다(Fig. 6). 800 °C까지의 열팽창을 분 석하여 평균 열팽창계수를 계산한 결과 −2.5 × 10−6/°C의 음의 열팽창계수 값이 얻어졌다. 소결조제가 첨가되지 않 은 순수한 2ZrO2·P2O5는 수축과 팽창을 거치며 음의 열 팽창거동을 보임을 알 수 있었다.
4. 결 론
PVA 용액 합성법을 이용하여 2ZrO2·P2O5 분말을 합 성하고 합성된 분말의 특성을 분석하여 다음과 같은 결 론을 얻었다.
1) 고상합성법으로는 합성이 이루어지지 않는 α상의 2ZrO2·P2O5 분말을 PVA 합성법에 의하여 비교적 간단 히 제조할 수 있었으며, PVA 첨가량이 12:1의 경우에 합성된 분말은 100~200 nm 크기의 비교적 균질하며 미 세한 입자크기를 보였다.
2) 결정화 거동 및 분말의 미세구조는 PVA 함량과 온 도에 따라 크게 영향을 받았으며, 12:1의 PVA 함량과 1200 °C에서 4시간 열처리 시, 잘 발달된 α상의 2ZrO2· P2O5 분말을 제조할 수 있었다.
3) 합성된 α상의 2ZrO2·P2O5 분말로 소결조제 없이 제 조된 소결체는 200 °C까지는 급격한 음의 열수축을 보 이고 이후에는 다시 완만히 팽창하는 결과를 보이며 800 °C까지 수축과 팽창거동을 보이며 −2.5 × 10−6/°C의 음의 열팽창계수를 보였다.