1. 서 론
텅스텐(W)은 높은 융점과 낮은 열팽창계수 및 높은 밀 도에 의한 우수한 방사선 차폐능 등을 나타내어 고온· 고강도 구조재, 접점재 및 방사능 차폐재 등 다양한 분 야로 응용되고 있다.1,2) 일반적으로 W은 열간가압성형(hot pressing) 또는 열간정수압성형(hot isostatic pressing) 등 의 가압소결 방법을 이용하나, 높은 융점 때문에 완전 한 완전 치밀체의 제조에는 어려움이 있고 또한 열간 압 연 등 추가적인 공정을 도입할 경우에는 다양한 형상을 갖는 시편의 제조에 어려움이 있다.3,4) 따라서 상압소결 에 의한 조밀화 공정이 요구되나, 기존의 마이크로 크 기 분말로는 고밀도의 W 소결체 제조에 한계가 있다.
상압소결 공정에 의한 고밀도 W의 제조에는 2가지 방 법이 제안되었다.5) 첫 번째는 Ni 등의 소결 활성제를 사 용하는 것이나 제조된 W-Ni 소결체는 높은 입계취성을 갖는 문제가 있다.6) 두 번째 방법으로는 높은 소결 구 동력을 갖는 나노크기의 W 분말을 사용하는 것이나 분 말제조에 복잡한 공정단계가 요구되는 단점이 있다.7) 이 러한 방법 이외에 상이한 크기를 갖는 분말이 혼합된 성 형체를 이용하여 상압 소결하는 공정이 최근에 많은 주 목을 받고 있다.8,9) 일반적으로 2개 이상의 크기를 갖는 분말이 적정한 비율로 혼합될 경우에는 큰 분말사이에 작은 분말들이 위치하여 성형체 밀도가 증가하며, 또한 소결과정 중에 작은 크기의 분말들이 빠른 목 성장과 입 계확산에 의한 물질이동 속도의 증가에 기여하여 소결 성을 향상시킬 수 있다.
따라서 본 연구에서는 W 분말의 소결성 향상을 위해 나노와 마이크로 크기가 균일하게 혼합된 W 분말을 제 조하고 합성거동을 분석하고자 하였다. 나노/마이크로 크 기의 W 혼합분말은 볼 밀링 한 WO3 분말을 마이크로 크기의 W 분말과 균일하게 혼합한 후 수소환원하여 제 조하였다. 또한 WO3 분말의 환원거동과 공정단계 별 미 세조직 특성을 분석하여 나노/마이크로 구조를 갖는 W 혼합분말의 제조를 위한 최적의 공정조건을 제시하고자 하였다.
2. 실험 방법
본 연구에서는 순도 99.9 %, 평균 입자크기 1 μm의 WO3(Kojundo Chemical Lab. Co., Japan)와 순도 99.9%, 평균 입자크기 12 μm의 W(Sigma Aldrich, USA)을 원 료분말로 사용하였으며, Fig. 1에 분말의 형상을 나타내 었다. WO3 분말의 볼 밀링과 수소환원으로 나노크기의 W 분말을 제조하기 위해, 우선 WO3 분말과 직경 3 mm 의 ZrO2 볼을 섞고 에탄올 용액 내에서 10시간 동안 밀 링하였다. 이때 볼과 분말은 15:1의 무게비로 하였다. 계 속해서 12 μm 크기의 W 분말을 추가한 후 동일한 조 건으로 10시간 동안 습식밀링 하였다. 이때 WO3 분말 은 수소 환원 후의 W 분말이 5 wt%가 혼합되도록 계 산하여 첨가하였다. 밀링한 혼합분말은 60 °C에서 10시 간 동안 건조하여 에탄올을 제거하였다.
WO3 분말의 환원거동은 TPR(temperature programmed reduction)를 이용하여 평가하였으며, 이 장비는 Ar-10% H2 혼합가스를 흘려주며 시편을 가열하는 장치와 배출 되는 가스의 열전도도를 측정하는 TCD(thermal conductivity detector)로 구성되어 있다.10) 본 연구에서는 50 mg 의 WO3 분말을 TPR에 장입한 후 0.05 l/min의 유속으 로 혼합가스를 흘려주고 2-20 °C/min의 승온속도로 900 °C까지 가열하며 TCD 값의 변화를 측정하여 환원거동 을 해석하였다. 복합분말 제조 및 수소환원 등 각 공정 단계에서의 상 및 미세조직은 XRD(D/Max-IIIC, Rigaku Denki Co.)와 SEM(JSM-6700F, JEOL Co.)을 이용하여 분석하였다. 분말크기는 레이저입도분석기(LPA, Beckman Counter Co., Model: Ls I3 320)를 이용하여 측정하였다.
3. 결과 및 고찰
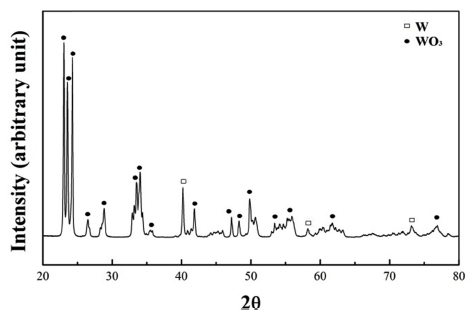
나노와 마이크로 크기가 혼합된 W 분말을 제조하기 위해, 우선 10시간 동안 볼 밀링한 WO3 분말을 12 μm 크기의 W 분말에 혼합하여 밀링하였다. Fig. 2(a)는 밀 링한 WO3/W 혼합분말의 미세구조 사진을 나타낸 것으 로 마이크로 크기의 W 분말 표면에 미세한 WO3 분말 들이 국부적으로 분포함을 확인할 수 있다. Fig. 2(b)는 혼합분말에 대한 입도분포 분석결과로서 전체적으로 조 대한 분말과 미세한 분말이 혼합된 전형적인 bimodal 형 태를 보여준다. 조대한 분말의 경우 평균크기가 약 12 μm이며, 미세한 분말의 경우는 약 0.7 μm으로 볼 밀링 을 통해 WO3 분말의 평균크기가 감소했음을 알 수 있 다. 한편 혼합분말은 Fig. 3의 XRD결과와 같이 순수한 WO3와 W 상으로만 이루어져 있음을 알 수 있다.
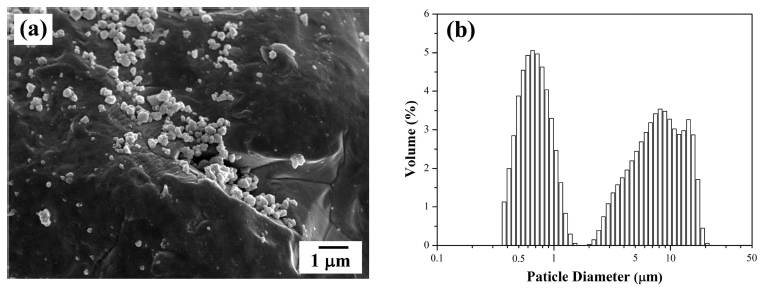
Fig. 2
Characteristics of WO3 and W powder mixture prepared by ball milling; (a) SEM image and (b) particle size distribution.
WO3 분말의 환원거동을 정량적으로 해석하기 위해 TPR 기기를 이용하여 Ar-10% H2 혼합가스를 흘려주며 승온속도에 따른 TCD 값의 변화를 측정하였다. Fig. 4 는 온도에 따른 TPR 분석결과로서 각각의 곡선에는 Tm1 과 Tm2로 표시된 2개의 반응피크가 존재한다. 기존의 논 문에서 보고된 바와 같이,11) WO3 분말은 중간 생성물 을 동반하는 몇 단계의 환원 과정을 거쳐 최종적으로 W 으로 변환된다. 우선 WO2.9와 WO2.72 형성의 2단계 환 원 과정을 통하여 WO2의 조성을 갖는 중간 생성물로 환 원되며, 계속해서 고상 산소이동 기구와 화학기상이동 기 구에 의해 WO2가 금속 W으로 환원된다. 따라서 첫 번 째 피크인 Tm1은 WO3가 WO2로 환원되는 반응에 의한 것이고 두 번째 피크(Tm2)는 WO2가 W으로 환원되는 반 응에 기인한 것임을 알 수 있다.
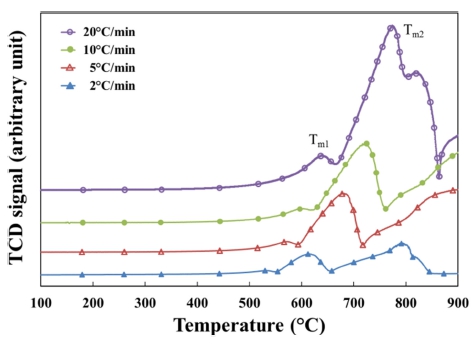
Fig. 4
TCD signal curves for the reduction process of WO3, scanned at different heating rates in Ar-10% H2 atmosphere.
한편 Fig. 4와 같이 승온속도가 증가함에서 반응피크 의 위치가 고온부위로 이동하며, 이는 WO3 환원이 열 활성화 과정임을 고려할 때 빠른 승온속도에서는 충분 한 열활성화를 위한 시간이 상대적으로 적기 때문으로 해석된다. 따라서 승온속도에 따른 반응피크의 변화는 직 접적으로 WO3 환원의 활성화 에너지와 관련되며, 이는 Kissinger method를 이용하여 다음 식과 같이 반응에 관 련된 활성화 에너지를 구할 수 있다.12)
여기서 ϕ는 승온속도, Tm은 최대 반응속도의 온도, R 은 기체상수, Q는 활성화 에너지를 나타낸다.
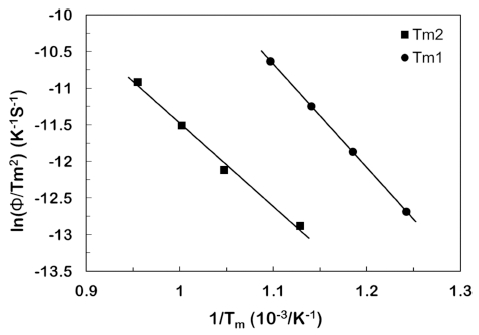
Fig. 5는 식 (1)을 이용하여, 본 실험에서 적용한 승 온속도 2, 5, 10, 20 °C/min 및 Fig. 4에서 구한 최대 반응온도(Tm) 값으로부터 ln(ϕ/Tm2)을 계산하여 y축으로 하고 1/Tm을 x축으로 도시하여 나타낸 그림이다. 도시된 직선의 기울기로부터 Tm1과 Tm2 반응에 대한 활성화 에 너지를 계산하면 각각 117.4 kJ/mol 및 94.6 kJ/mol의 값 을 나타내었다. 본 연구에서 얻은 값과 기존 논문에서 보고된 활성화 에너지 값의 비교를 위해 Table 1에 반 응단계 및 측정 분위기에 따른 활성화 에너지 값을 나 타내었다.13-15) 기존의 연구는 본 실험조건과 정확하게 일 치하지 않으나 N2-25% H2를 환원분위기로 사용한 경우 에서는 유사한 활성화 에너지 값을 나타내었으며, 본 연 구에서 얻은 활성화 에너지 값은 환원거동의 해석에 중 요한 기초자료를 제공한다는 점에서 유익한 결과로 판 단한다.
Table 1
Comparison of apparent activation energy for reduction of WO3.
| WO3→ WO2 | WO2→ W | Atmosphere | Reference | |
|---|---|---|---|---|
| Reported activation energy (kJ/mol) | 91.8 | 147.2 | Ar-25% H2 | (13) |
| 104.0 | 83.0 | N2 -25% H2 | (14) | |
| - | 83.6 | H2 | (15) | |
| This work (kJ/mol) | 117.4 | 94.6 | Ar-10% H2 | - |
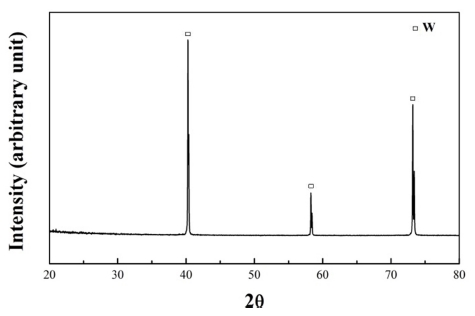
Fig. 6은 볼 밀링한 WO3와 W의 혼합분말을 750 °C에 서 1시간 동안 환원한 후 분석한 XRD 결과이다. 환원 후에는 다른 반응상 등의 형성 없이 WO3 상이 모두 W 상으로 환원되었음을 알 수 있다. Fig. 7은 환원분말을 SEM으로 관찰한 미세조직 사진으로, 평균크기 약 100 nm의 W입자들이 조대한 W 분말 표면에 균일하게 분 포함을 알 수 있다. 따라서 나노와 마이크로 크기가 균 일하게 혼합된 W 분말은 WO3와 W 혼합분말의 볼 밀 링과 수소환원 공정으로 제조가 가능함을 나타낸다.
4. 결 론
W 분말의 소결성 향상을 위해 나노와 마이크로 크기 가 균일하게 혼합된 W 분말을 제조하고 합성거동을 분 석하였다. 볼 밀링한 WO3/W 혼합분말은 마이크로 크기 의 W 분말표면에 약 0.7 μm크기의 WO3들이 존재하며 전형적인 bimodal형태의 입도분포를 나타내었다. Ar-10% H2 혼합가스 분위기에서 TPR을 이용한 WO3 분말의 환 원거동 분석결과 2개의 반응피크가 존재함을 확인하였으 며 이는 WO2로의 환원과 계속해서 WO2가 W으로 환 원되는 반응에 기인한 것으로 해석하였다. 승온속도에 따 른 반응피크 온도의 변화로부터 활성화 에너지를 계산 하였으며, WO3로부터 WO2로의 환원과 WO2로부터 W 으로 환원에 대한 활성화 에너지는 각각 117.4 kJ/mol 및 94.6 kJ/mol로 측정되었다. 볼 밀링한 WO3/W 분말을 750 °C에서 1시간 동안 환원한 혼합분말은 다른 반응상 등의 형성 없이 모두 W상으로 존재하며 평균크기 약 100 nm의 W입자들이 조대한 W 분말 표면에 균일하게 분포함을 확인하였다. 따라서 나노/마이크로 크기의 W이 균일하게 혼합된 분말은 볼 밀링 한 WO3 분말을 마이 크로 크기의 W 분말과 혼합한 후 수소환원하는 공정으 로 제조가 가능함을 제시한다.